羅非魚鱗膠原肽亞鐵螯合物制備工藝優(yōu)化及結(jié)構(gòu)表征
唐順博 涂宗財(cái),3 沙小梅 張 耀 張 露
(1. 江西師范大學(xué)國(guó)家淡水魚加工技術(shù)研發(fā)專業(yè)中心,江西 南昌 330022; 2. 江西師范大學(xué)江西省淡水魚高值化利用工程技術(shù)研究中心,江西 南昌 330022; 3. 南昌大學(xué)食品科學(xué)與技術(shù)國(guó)家重點(diǎn)實(shí)驗(yàn)室,江西 南昌 330047)
鐵為人體必需元素,在維持正常造血功能和增強(qiáng)免疫功能等方面起到巨大作用[1]。世界上約有25%的人患有貧血,其中一半是缺鐵造成的,口服補(bǔ)鐵劑是治療缺鐵性貧血的重要方法之一,但傳統(tǒng)硫酸亞鐵復(fù)合劑可能會(huì)導(dǎo)致患者腸胃不適[2]。研究發(fā)現(xiàn),氨基酸鐵螯合物比傳統(tǒng)硫酸亞鐵復(fù)合劑具有更好的補(bǔ)血效果[3],多肽亞鐵螯合物作為一種新型補(bǔ)鐵劑,可通過(guò)肽的轉(zhuǎn)運(yùn)系統(tǒng)直接被人體吸收,并且對(duì)人體刺激較小,有希望用于一些特殊人群[4-5]。
明膠是一種多功能性的生物大分子,普遍用于食品、醫(yī)藥及化工領(lǐng)域[6-8]。與傳統(tǒng)明膠相比,魚明膠具有來(lái)源廣,價(jià)格低,營(yíng)養(yǎng)價(jià)值高等特點(diǎn)。隨著近年水產(chǎn)養(yǎng)殖的發(fā)展,魚類加工副產(chǎn)物如魚鱗、魚頭、魚內(nèi)臟等資源被大量浪費(fèi),充分利用加工副產(chǎn)物能大大提高魚類的綜合價(jià)值[9]。沙小梅等[10]從鳙魚魚鱗中提取魚鱗明膠并研究了提取過(guò)程中pH值對(duì)鳙魚魚鱗明膠性質(zhì)的影響;Sinthusamran等[11]研究了不同提取溫度對(duì)鱸魚魚皮明膠性質(zhì)的影響。羅非魚別稱非洲鯽魚,肉質(zhì)鮮嫩,富含多種營(yíng)養(yǎng)物質(zhì),是中國(guó)魚類養(yǎng)殖中的重要品種[12],賈杏歌等[13]研究了不同濃度戊二醛對(duì)羅非魚鱗膠原蛋白膜機(jī)械性和抗水性的影響;李瑞杰等[14]比較了不同酶解物的鈣離子螯合能力和螯合物的抗氧化活性。劉永等[15]曾對(duì)羅非魚鱗膠原蛋白肽鐵螯合物的制備工藝進(jìn)行了優(yōu)化,但未對(duì)螯合物結(jié)構(gòu)進(jìn)行探究。
研究擬以羅非魚鱗膠原肽為原料制備多肽亞鐵螯合物,并對(duì)多肽亞鐵螯合物的最佳制備工藝及其結(jié)構(gòu)進(jìn)行探索,以期為羅非魚魚鱗的精深加工及高值化利用提供技術(shù)參考。
1 材料與方法
1.1 材料與試劑
羅非魚鱗明膠:蘇州吉利鼎海洋生物科技有限公司;
堿性蛋白酶:酶活力為8.68×107U/g,諾維信酶制劑公司;
乙腈、三氟乙酸:色譜純,上海阿拉丁生化科技有限公司;
細(xì)胞色素C、抑肽酶、L-氧化型谷胱甘肽、羥脯氨酸:色譜純,北京索萊寶科技有限公司;
其余試劑均為分析純。
1.2 儀器與設(shè)備
SevenCompact臺(tái)式pH計(jì):S220型,梅特勒—托利多儀器(上海)有限公司;
冷凍干燥機(jī):SR-AON-50型,上海舍巖儀器有限公司;
HSM高效液相色譜:D-2000型,日本Hitachi公司;
酶標(biāo)儀:Synergy H1型,美國(guó)Bio Tek公司;
氨基酸分析儀:L-8900型,日本Hitachi公司;
智能型傅立葉變換紅外光譜儀:Nicolet5700型,美國(guó)熱電尼高力公司;
掃描電鏡:S-3400N型,日本Hitachi公司;
X射線衍射儀:D8 ADVANCE型,德國(guó)BRUKER公司。
1.3 試驗(yàn)方法
1.3.1 魚鱗多肽的制備 酶解方法參考文獻(xiàn)[16]修改如下:取魚鱗明膠加蒸餾水配成濃度為5%的明膠溶液,置于50 ℃恒溫水浴鍋中保溫15 min,用0.1 mol/L NaOH調(diào)節(jié)pH至8,加入明膠質(zhì)量比為1%的堿性蛋白酶水浴30 min,再次調(diào)節(jié)pH至8,水解4.5 h,水解結(jié)束后立即沸水浴10 min滅活,冷卻,4 000 r/min離心15 min,取上清液,經(jīng)冷凍干燥后存于4 ℃冰箱備用。
1.3.2 多肽分子量測(cè)定 按照GB 31645—2018《食品安全國(guó)家標(biāo)準(zhǔn) 膠原蛋白肽》對(duì)多肽分子量進(jìn)行測(cè)定。取1.3.1中多肽粉配制成1 mg/mL的溶液,過(guò)0.22 μm水系濾膜后,使用高效液相色譜儀進(jìn)行分析。以細(xì)胞色素C(12 384 Da)、抑肽酶(6 511.51 Da)、L-氧化型谷胱甘肽(612.63 Da)和羥脯氨酸(131.13 Da)為標(biāo)準(zhǔn)品繪制相對(duì)分子質(zhì)量校正曲線。色譜條件:色譜柱型號(hào)為XBridge BEH 125? SEC(3.5 μm,7.8 mm×300 mm);流動(dòng)相比例為V乙腈∶V水∶V三氟乙酸=40∶60∶0.05;流速0.5 mL/min;柱溫30 ℃;進(jìn)樣量10 μL。
1.3.3 多肽亞鐵螯合物制備工藝優(yōu)化
(1) 亞鐵螯合物的制備流程:
多肽→加入一定比例水→加入抗氧化劑(抗壞血酸)→調(diào)節(jié)pH值→按比例加入鐵鹽→進(jìn)行螯合反應(yīng)→加入無(wú)水乙醇沉淀→離心得到沉淀→冷凍干燥[17]
(2) 單因素試驗(yàn):由于亞鐵螯合受pH、多肽濃度及多肽與亞鐵鹽質(zhì)量比影響較大[18],因此試驗(yàn)固定反應(yīng)溫度為25 ℃,反應(yīng)時(shí)間為40 min,pH為5.0,多肽濃度為3%,多肽與亞鐵鹽質(zhì)量比為3∶1,依次對(duì)pH值(3.0,4.0,5.0,6.0,7.0),多肽濃度(1%,2%,3%,4%,5%),多肽與亞鐵鹽質(zhì)量比(1∶1,2∶1,3∶1,4∶1,5∶1)進(jìn)行單因素試驗(yàn),以螯合率和螯合物得率為指標(biāo),探討單因素對(duì)螯合反應(yīng)的影響。
(3) 響應(yīng)面試驗(yàn)設(shè)計(jì):根據(jù)單因素試驗(yàn)結(jié)果,以pH值、多肽與鐵鹽質(zhì)量比和多肽液濃度為影響因素,設(shè)計(jì)三因素三水平響應(yīng)面試驗(yàn),以多肽螯合物得率為評(píng)價(jià)指標(biāo),探索螯合物的最佳制備工藝。
1.3.4 評(píng)價(jià)指標(biāo)的測(cè)定 采用鄰菲羅啉比色法[17]評(píng)價(jià)肽—鐵螯合體系中亞鐵離子的含量、鐵螯合率和螯合物得率。
(1) 鐵離子含量:
(1)
式中:
F——體系鐵離子含量,mg/kg;
C——從標(biāo)準(zhǔn)曲線獲得溶液相應(yīng)的鐵含量,μg;
M——稱取樣品的質(zhì)量,g;
V1——測(cè)定所取的溶液體積,mL;
V2——樣品處理后的定容體積,mL。
(2) 鐵螯合率:
(2)
式中:
D——鐵螯合率,%;
m1——螯合物中鐵的含量,mg;
m2——加入鐵的含量,mg。
(3) 螯合物得率:
(3)
式中:
Y——螯合物得率,%;
M1——生成物總質(zhì)量,g;
M2——加入反應(yīng)體系的總質(zhì)量,g。
1.3.5 氨基酸組成分析 參照GB 5009.124—2016《食品安全國(guó)家標(biāo)準(zhǔn) 食品中氨基酸的測(cè)定》,采用氨基酸自動(dòng)分析儀對(duì)樣品中氨基酸的含量進(jìn)行測(cè)定。
1.3.6 多肽亞鐵螯合物的結(jié)構(gòu)表征
(1) 掃描電鏡分析:取少量樣品,均勻涂在樣品盤的導(dǎo)電膠上進(jìn)行噴金處理,之后采用S-3400N型掃描電子顯微鏡進(jìn)行掃描,對(duì)其表觀形貌進(jìn)行分析。
(2) 紅外光譜分析:采用Nicolet 5700型紅外光譜儀測(cè)定多肽與多肽亞鐵螯合物的紅外光譜,掃描范圍為400~4 000 cm-1。
(3) X衍射分析:將樣品研磨均勻后,采用Bruker D8 X-射線衍射儀進(jìn)行分析測(cè)定,分析條件為:Cu靶,管電流40 mA,掃描速度10°/min,掃描角度為5°~80°。
1.4 數(shù)據(jù)處理
2 結(jié)果與分析
2.1 多肽分子量分布
通過(guò)對(duì)標(biāo)品出峰時(shí)間與標(biāo)品分子量進(jìn)行線性擬合,得到分子量標(biāo)品標(biāo)準(zhǔn)方程為Y=6.855 16-0.249 9X(R2=0.997),由圖1可知,膠原多肽中主要含有4個(gè)組分,經(jīng)計(jì)算各組分平均分子量分別為7 479,5 450,3 030,889 Da,符合GB 31645—2018標(biāo)準(zhǔn)對(duì)多肽的定義。
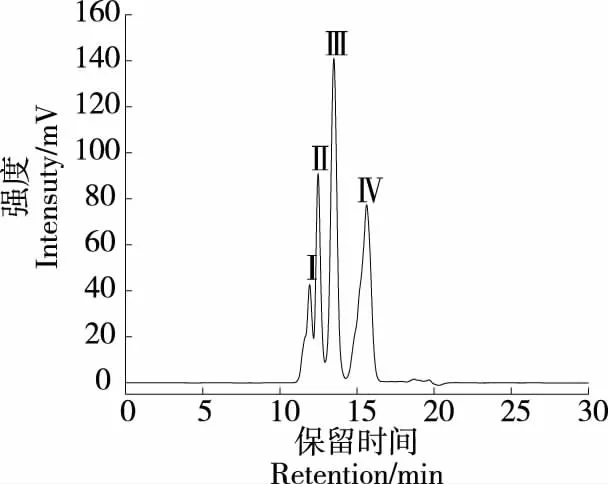
圖1 膠原多肽分子量分布
2.2 單因素試驗(yàn)結(jié)果
由圖2(a)可知,當(dāng)固定多肽液濃度為3%,多肽與亞鐵鹽質(zhì)量比為3∶1時(shí),螯合率和螯合物得率先升高,在pH為5時(shí)達(dá)到最大值,隨后又減小,表明反應(yīng)體系在弱酸或中性時(shí),溶液中的OH-會(huì)參與Fe2+的反應(yīng),不利于螯合反應(yīng)的進(jìn)行[19];由圖2(b)可知,固定pH為5,多肽與亞鐵鹽質(zhì)量比為3∶1時(shí),螯合率先增大后減小,在多肽液濃度為3%時(shí),螯合率和螯合物得率最高,這是因?yàn)槎嚯臐舛仍龃螅谒腥芙庑宰冃。瑓⑴c反應(yīng)的多肽更少;由圖2(c)可知,當(dāng)固定多肽濃度為3%,pH為5時(shí),螯合率隨亞鐵鹽質(zhì)量比的增大而減小,螯合物得率先增大后減小,當(dāng)質(zhì)量比為3∶1時(shí)達(dá)到最大,可能是由于多肽與亞鐵離子的結(jié)合位點(diǎn)有限,當(dāng)結(jié)合數(shù)目達(dá)到最大時(shí),不再發(fā)生反應(yīng),不能生成螯合物[20]。

圖2 pH、多肽濃度和多肽與鐵鹽質(zhì)量比對(duì)螯合反應(yīng)的影響
2.3 響應(yīng)面優(yōu)化分析
2.3.1 響應(yīng)面試驗(yàn)設(shè)計(jì)及結(jié)果分析 根據(jù)單因素試驗(yàn)結(jié)果,選取pH、多肽濃度、肽鐵鹽質(zhì)量比三因素(見(jiàn)表1),利用Box-Behnken中心組合原理設(shè)計(jì)三因素三水平的響應(yīng)面試驗(yàn),試驗(yàn)方案與結(jié)果見(jiàn)表2。

表1 響應(yīng)面因素及水平表
用Desgin-Exper 8.0軟件對(duì)表2的試驗(yàn)結(jié)果進(jìn)行分析,建立螯合物得率(Y)的二次響應(yīng)面回歸模型為:

表2 響應(yīng)面試驗(yàn)方案與結(jié)果
Y=1.15A+0.75B+0.80C-0.05AB+0.28AC-0.89BC-2.00A2-3.44B2-2.12C2+65.83。
(4)
根據(jù)表3中方差結(jié)果分析,該二次模型P值<0.000 1表明極顯著,相關(guān)系數(shù)R2為0.979 9,表明預(yù)測(cè)值和實(shí)測(cè)值之間有很高的相關(guān)性,RAdj2為0.954 1,表明此模型能解釋95.41%的響應(yīng)值變化,因此該模型可以較好地描述pH值、多肽液濃度和多肽與鐵鹽質(zhì)量比對(duì)螯合反應(yīng)影響的變化規(guī)律。
回歸方程的各項(xiàng)方差分析結(jié)果表明,A、B、C、A2、B2和C2對(duì)螯合物得率的影響極顯著(P<0.01),BC相互作用對(duì)螯合物得率的影響顯著(P<0.05),而AB、AC的相互作用對(duì)螯合物得率的影響不顯著(P>0.05)。由F值可知,各因素對(duì)螯合物得率的影響次序:pH>肽鐵質(zhì)量比>多肽濃度。剔除不顯著項(xiàng)AB、AC后對(duì)方程進(jìn)行優(yōu)化,得優(yōu)化后的方程為:
Y=1.15A+0.75B+0.80C-0.89BC-2.00A2-3.44B2-2.12C2+65.83。
(5)
由圖3可知,因素B和C之間的相互作用等高線圖呈橢圓形,表明多肽濃度與肽鐵質(zhì)量比之間具有顯著的相互作用[21],與表3結(jié)果一致。

圖3 多肽濃度與肽鐵鹽質(zhì)量比的交互作用對(duì)螯合物得率影響的響應(yīng)面圖
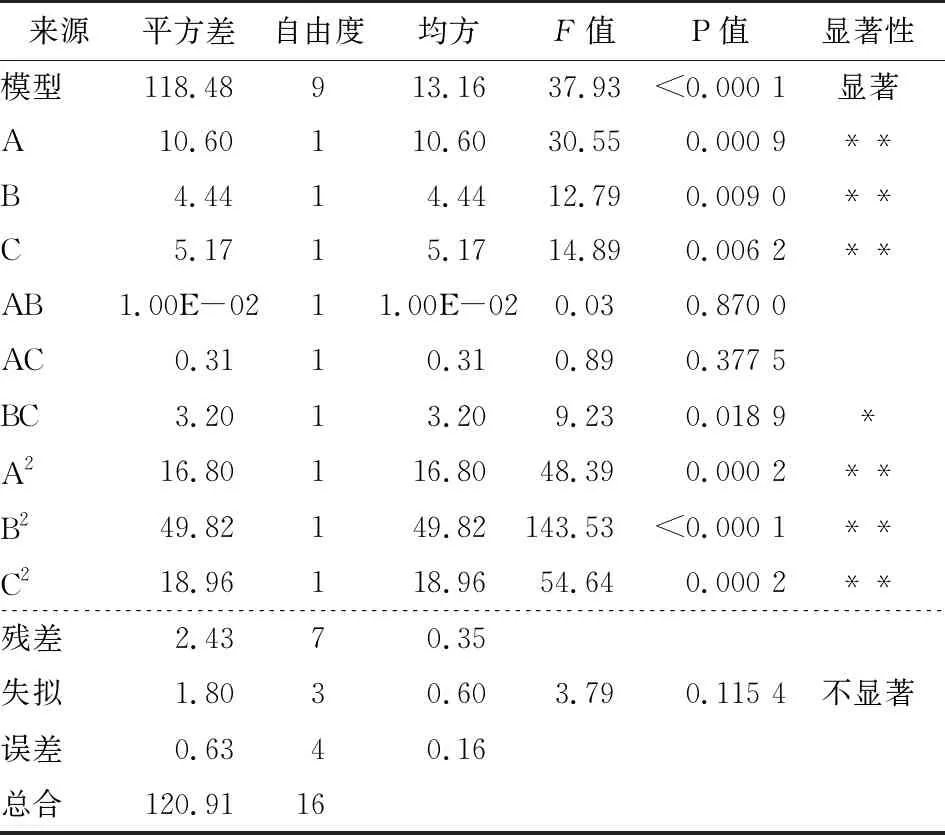
表3 響應(yīng)面二次模型方差分析?
2.3.2 最優(yōu)解的驗(yàn)證 利用Design-Expert 8.0軟件計(jì)算得到肽鐵螯合物最佳工藝條件為pH 5.29,多肽濃度3.09%,多肽與鐵質(zhì)量比3.17∶1.00,預(yù)測(cè)螯合物得率為66.10%。考慮到實(shí)際操作,最佳制備工藝確定為pH 5.30,多肽濃度3.00%,多肽與鐵質(zhì)量比為3.20∶1.00,在此條件下進(jìn)行3次重復(fù)驗(yàn)證實(shí)驗(yàn),螯合率平均值為82%,肽鐵螯合物得率平均值為65.43%,與最佳工藝條件螯合物得率66.10%無(wú)顯著性差異(P>0.05),說(shuō)明此模型可用于反應(yīng)多肽螯合鐵的變化規(guī)律。
2.4 氨基酸組成成分分析
由表4可知,膠原多肽中Gly含量最高,Glu、Pro、Ala和Asp的含量也相對(duì)較高,符合膠原蛋白氨基酸組成特征[22],結(jié)合圖1,多肽分子量分布在800~8 000 Da,因此可認(rèn)為經(jīng)酶解后凍干所得粉末為膠原多肽。Glu、Gly、Lys、His和Arg等氨基酸被認(rèn)為與金屬離子螯合活性密切相關(guān)[23-24],從表4可知,該5種氨基酸在多肽中大量存在,經(jīng)螯合后,其在螯合物中的含量大量增加,與Lee等[25]的研究結(jié)果相符。
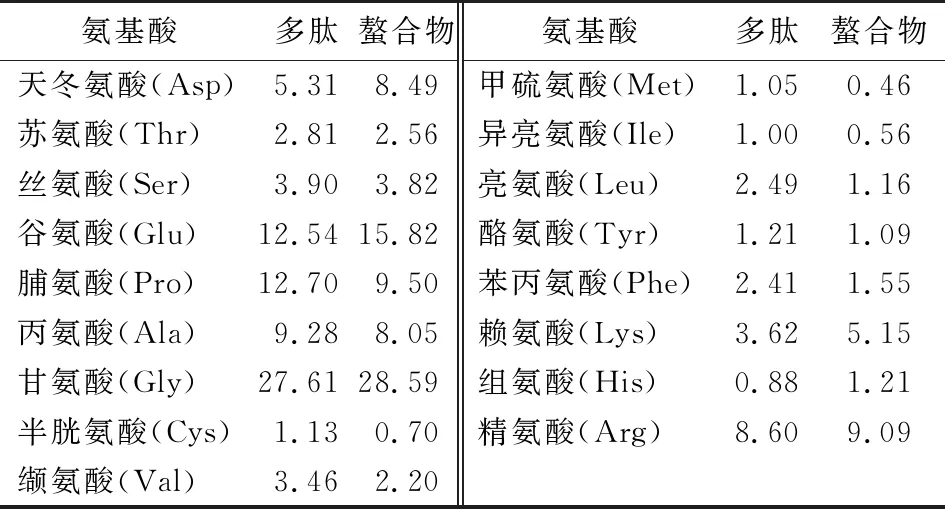
表4 多肽與螯合物的氨基酸組成
2.5 螯合物的結(jié)構(gòu)表征
2.5.1 掃描電鏡分析 由圖4可知,多肽表面光滑并有裂紋,可能是在真空干燥過(guò)程中失水導(dǎo)致,而螯合物是主體成球狀的團(tuán)狀交織結(jié)構(gòu),表面有顆粒附著于球體上,與汪婧瑜等[17]結(jié)果類似。

圖4 多肽與螯合物的掃描電鏡圖
2.5.2 紅外光譜分析 由圖5可知,發(fā)生螯合反應(yīng)后,多肽和肽鐵螯合物的特征吸收峰發(fā)生了明顯的變化。螯合后,多肽的—NH2吸收峰由3 380.60 cm-1移動(dòng)到3 370.97 cm-1,在1 542.77 cm-1處—NH2的吸收峰移動(dòng)到1 546.63 cm-1,多肽的—COO—吸收峰由1 400.67 cm-1移動(dòng)到1 409.71 cm-1,另外多肽的C—H吸收峰由于伸縮振動(dòng)由1 455.99 cm-1移動(dòng)到1 468.64 cm-1,以上結(jié)果表明多肽中—NH2、—COO—與C—H與亞鐵鹽發(fā)生反應(yīng)生成了多肽亞鐵螯合物。

圖5 多肽與螯合物的紅外光譜圖
2.5.3 亞鐵螯合物的X衍射分析 由圖6可知,魚鱗膠原肽在2θ=20°左右處出現(xiàn)強(qiáng)衍射峰,與劉靜[26]所測(cè)圖譜類似,在與亞鐵離子螯合后,多肽螯合物在20°左右的衍射峰減弱,并且向大掠射角偏移,其他地方未出現(xiàn)衍射峰,屬于無(wú)規(guī)則的非晶體結(jié)構(gòu),表明亞鐵離子與多肽以配位鍵形式結(jié)合。

圖6 多肽和螯合物的X衍射圖譜
3 結(jié)論
以魚鱗膠原肽為原料,以螯合物得率和螯合率為指標(biāo),采用單因素試驗(yàn)及響應(yīng)面法優(yōu)化得出了多肽亞鐵螯合物的最佳制備工藝為pH 5.30,多肽濃度3.00%,多肽與亞鐵鹽質(zhì)量比3.2∶1.0,在此條件下螯合率為82%,螯合物得率為65.43%。氨基酸分析表明Glu、Gly、Lys、His和Arg等氨基酸在螯合反應(yīng)中起到重要作用。通過(guò)掃描電鏡發(fā)現(xiàn)多肽與螯合物表觀結(jié)構(gòu)發(fā)生明顯改變,由表面光滑變?yōu)榍蛐蛨F(tuán)狀結(jié)構(gòu);紅外光譜表明膠原多肽中的—NH2、—COO—以及C—H與亞鐵鹽發(fā)生了反應(yīng);X衍射圖譜分析發(fā)現(xiàn)亞鐵離子與多肽以配位鍵的形式結(jié)合,證實(shí)多肽與亞鐵鹽發(fā)生反應(yīng)生成了螯合物。以上研究結(jié)果表明,魚鱗膠原肽可作為新型補(bǔ)鐵劑載體材料,擴(kuò)寬了補(bǔ)鐵劑材料的來(lái)源,同時(shí)為魚類副產(chǎn)物中魚鱗的精加工提供了思路,有利于促進(jìn)魚鱗的高值化利用。后續(xù)將采用體外和體內(nèi)模型研究羅非魚鱗膠原肽亞鐵螯合物的消化穩(wěn)定性和貯存穩(wěn)定性,以及促進(jìn)鐵吸收的效果。

