氮摻雜碳量子點的制備及其在細胞成像與鄰硝基苯酚檢測中的應用
姜 麗,梁峻毅,王玉彤,鮑林春,吳 韻,鄭玉國,夏光平,張小蘭,張仟春*
(1.興義民族師范學院 生物與化學學院,貴州 興義 562400;2.貴州省化學合成及環境污染控制和修復技術特色重點實驗室,貴州 興義 562400;3.黔西南州人民醫院 檢驗科,貴州 興義 562400)
碳量子點(Carbon quantum dots,CQDs)因具有良好的水溶性、光學穩定性、出色的生物相容性、生物低毒性以及強熒光性能[1-4],已在生物醫學成像、分析物檢測、熒光標記、催化劑、探針和光學元件等領域展現出良好的應用前景[5-7]。目前,大量學者研究了多種制備CQDs的方法,主要有水熱法、化學氧化法、微波輔助法、電化學氧化法、激光刻蝕法和超聲法等[4,6]。在眾多的制備方法中,使用廉價和生態友好型生物質的水熱法受到了廣大研究者的青睞,該法合成簡單、綠色環保、經濟。前驅體的選擇是制備CQDs的關鍵,直接影響量子產率、熒光強度及穩定性,是實際應用中提高選擇性和靈敏度的重要因素。在CQDs的制備過程中通過原子摻雜(例如氮、磷、硼等)不僅可以提高CQDs的量子產率及熒光強度,還可在CQDs中提供活性位點,從而拓寬其在分析檢測等領域的潛在應用[1,4,8]。氮外層有5個價電子且存在孤電子對,可提供多余的n電子,使費米能級上移從而改變光學性質,同時氮原子與碳原子大小相當,使得氮成為CQDs中的理想摻雜元素,拓寬了CQDs的應用范圍[4]。因此,高含氮量的物質常作為CQDs前驅體進行研究。
鄰硝基苯酚(o-Nitrophenol,o-NP)是酚類家族中的高劇毒物質,是環境分析優先監測的污染物,美國環境保護署已將其列為優先治理的對象[9]。因此,建立環境樣品中o-NP的分析方法具有重要意義。目前,硝基苯酚的常用分析方法有光譜分析法[9]、毛細管電泳法[10]、流動注射分析法[11]、高效液相色譜法[12]、氣相色譜-質譜法[13]和電化學分析法[14]等。這些方法大多操作繁瑣、儀器價格昂貴、分析檢測成本高。而熒光分光光度法由于操作簡單,且具有良好的選擇性、靈敏性以及使用成本低等優點,廣泛用于物質的分析檢測[15-16]。
L-瓜氨酸和尿素的含氮量分別為24%和47%,是理想的氮摻雜前驅體。本文首次以L-瓜氨酸和尿素為混合前驅體,采用水熱法一步合成了氮摻雜碳量子點(N-CQDs)。對制備的N-CQDs進行表征,研究其發光特性和細胞毒性,并進一步用于細胞成像實驗,證實該N-CQDs具有水溶性好、穩定性高、細胞毒性小、生物相容性好、熒光強度大和量子產率高的優點,具有潛在的應用價值。此外,基于o-NP對探針N-CQDs的選擇性猝滅效應,以及o-NP濃度與N-CQDs熒光強度之間良好的線性關系,發展了一種簡單、快速、靈敏的實際水樣中o-NP的檢測方法。
1 實驗部分
1.1 試劑與儀器
L-瓜氨酸、尿素、硫酸奎寧、磷酸鹽緩沖液(PBS)、對硝基苯酚(p-NP)、鹽酸多巴胺(DA)、Zn(NO3)2·6H2O、AlCl3、Cu(NO3)2·3H2O、MgCl2·6H2O、Fe(NO3)3·9H2O、CaCl2和1 000 μg/mL鄰硝基苯酚(o-NP)標準溶液購自上海阿拉丁生化科技股份有限公司;異丙醇、鄰苯二酚(CC)和對苯二酚(HQ)購于百靈威科技有限公司;NaCl、KCl和Hg(NO3)2·H2O購于國藥集團化學試劑有限公司;3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴鹽(MTT)和DMEM培養基購自北京索萊寶科技有限公司;實驗所用試劑均為分析純;HepG2細胞由黔西南州人民醫院提供;實驗用水為超純水(18.2 MΩ·cm)。
Hitachi-F20高分辨透射電子顯微鏡(HRTEM);Bruker multimode 8原子力顯微鏡(AMF);Leica SP8激光共聚焦掃描顯微鏡(德國韋茨拉爾徠卡);Nicolet 6700傅立葉變換紅外光譜儀(FT-IR)、ESCALAB 250Xi型光電子能譜儀(XPS)、Multiskan FC酶聯免疫檢測儀(美國賽默飛世爾);D8 X射線粉末衍射儀(XRD,德國Bruker公司);RF-6000熒光分光光度計(日本島津公司);4501S紫外-可見光分光光度計(UV-Vis,天津港東科技發展股份有限公司);KT7-900-434高速離心機(德國克恩達);KQ5200DE數控超聲波清洗器(中國昆山超聲儀器有限公司);AL104電子天平(梅特勒-托利多公司)。
1.2 碳量子點的制備
稱取一定質量比的L-瓜氨酸和尿素,加入20 mL超純水,超聲振蕩20 min使其分散完全,將所配溶液轉移至50 mL高壓反應釜中,于180~240 ℃烘箱中反應6~14 h。反應結束后,取出反應釜,待其冷卻至室溫,將反應液超聲分散30 min,于12 000 r/min超速離心20 min,以0.22 μm濾膜過濾后得到N-CQDs溶液,置于4 ℃冰箱中備用。
1.3 氮摻雜碳量子點的細胞毒性及生物成像
通過標準MTT法進行HepG2細胞的毒性檢測實驗,具體操作如下:首先,在37 ℃,5% CO2條件下將HepG2細胞加入到96孔平地板中培養24 h,細胞密度為4×103/孔。然后將細胞培養基取出,每孔加入100 μL含有不同質量濃度N-CQDs(0~1 000 μg/mL)的DMEM培養基培養24 h,清洗細胞,向平地板中每孔加入20 μL 5 mg/mL的MTT繼續培養4 h。隨后吸去細胞培養基和MTT并用磷酸鹽緩沖液(PBS)清洗,加入異丙醇,于100 r/min振蕩10 min,在450 nm波長的酶聯免疫檢測儀上測量每孔的光密度,計算細胞活性。
將100 μL含有10% PBS的新鮮DMEM和HepG2細胞(1×105/皿)加入培養皿中,于37 ℃,5% CO2條件下培養24 h后,加入N-CQDs溶液,繼續培養2 h。用PBS溶液(0.01 mol/L,pH 7.4)沖洗3次后,分別在488 nm和610 nm檢測波長下成像。
1.4 鄰硝基苯酚的檢測
取20.0 μL N-CQDs溶液(25 mg/mL)于5 mL比色管中,以PBS(0.1 mol/L,pH 7.4)緩沖液定容,加入5.0 μL不同濃度的o-NP溶液,室溫下反應30 min,于380 nm激發波長下掃描其熒光發射光譜。N-CQDs的熒光猝滅率為IF/IF0,IF0為無o-NP的N-CQDs溶液的熒光強度,IF為加入o-NP后的熒光強度。
2 結果與討論
2.1 氮摻雜碳量子點的制備
為了獲得最佳熒光強度的N-CQDs,考察了L-瓜氨酸和尿素兩種前驅體的質量比及兩者的質量濃度、制備溫度和制備時間對N-CQDs熒光強度的影響。結果顯示,當L-瓜氨酸與尿素質量比為3∶2時N-CQDs的熒光強度最佳(圖1A)。且當L-瓜氨酸和尿素的質量濃度在6.25~25 mg/mL范圍時,N-CQDs的熒光強度隨質量濃度的增加而增大,并在25 mg/mL時達到最大值,此后隨著前驅體質量濃度繼續增大,N-CQDs的熒光強度反而降低(圖1B),這可能是由于較高濃度易引起N-CQDs聚集而導致熒光猝滅[17-18]所致。因此,選擇兩種前驅體的最佳質量濃度均為25 mg/mL。實驗發現,N-CQDs的熒光強度隨制備溫度的升高而增強,并在240 ℃時達到最大值(圖1C),考慮到對位聚苯內膽反應釜的安全性,選擇240 ℃作為制備的最佳溫度;制備時間對N-CQDs熒光強度也有明顯影響,制備時間為10 h時,熒光強度達到最大值(圖1D),因此選擇10 h作為水熱制備的最佳時間。故N-CQDs的最佳制備條件為:L-瓜氨酸與尿素的質量比與質量濃度分別為3∶2和25、25 mg/mL,制備溫度為240 ℃,制備時間為10 h。

2.2 氮摻雜碳量子點的表征
通過HRTEM及AFM觀察制備的N-CQDs的形貌。圖2A顯示,N-CQDs為近圓形且單分散性良好的納米顆粒;其平均粒徑在2.8 nm左右(圖2A插圖)。從圖2B和圖2C可以看出,該N-CQDs的平均高度約2.7 nm。以上結果表明,所制備的N-CQDs是一種近乎微觀準球形的碳納米顆粒[19]。圖2D為N-CQDs的HRTEM圖,圖中顯示該N-CQDs晶格條紋的晶面間距為0.25 nm,與石墨碳相符;N-CQDs在2θ=22°處的較寬的平緩衍射峰(圖3A)對應于石墨碳的(002)晶面[20],證實其為無定形碳結構。



2.3 氮摻雜碳量子點的光致發光特性
通過三維熒光光譜測試了N-CQDs激發、發射吸收特征峰的大概范圍,結果如圖4A所示,其激發范圍為300~450 nm,發射范圍為350~550 nm。在350~390 nm波長激發下,其主要發射帶集中在415~478 nm,對激發波長具有一定的依賴性,這可能是由共軛π域的發射以及表面缺陷所致[29]。采用UV-Vis和熒光分光光度計考察了N-CQDs的光學吸收特征(圖4B),該N-CQDs在290~600 nm范圍內有較寬的紫外吸收峰(黑線),可能是n-π*躍遷的結果[30]。該N-CQDs最佳的激發(藍線)和發射(紅線)波長分別為380 nm和453 nm。制備的N-CQDs溶液在日光下呈淡黃色,在365 nm紫外燈下,該N-CQDs發射出強烈的藍色熒光(圖4B插圖),當激發波長為380 nm時,在453 nm處出現最強熒光。以硫酸奎寧(0.1 mol/L H2SO4,QY=54%)為熒光標準物,測得N-CQDs的量子產率為39.2%。

2.4 氮摻雜碳量子點的穩定性
實驗發現,采用尿素和L-瓜氨酸為前驅體制備的N-CQDs熒光強度比僅采用L-瓜氨酸制備的CQDs熒光強度高、穩定性好。且N-CQDs可在12 h內保持熒光強度基本不變,17 h后熒光僅減弱13.1%,不影響應用。

圖5 pH值對N-CQDs熒光強度的影響Fig.5 Effect of pH value on the fluorescence intensity of N-CQDs
高酸堿性對N-CQDs具有明顯影響,為了獲得穩定的實際樣品分析條件,考察了pH值對N-CQDs熒光強度的影響。發現在pH 4.0~8.0范圍內,N-CQDs熒光強度變化較小,而在pH 1.0~4.0和pH>8.0時,熒光強度明顯減小(圖5)。因此,進行水樣中o-NP的含量分析時,在pH 7.4條件下進行檢測。
2.5 氮摻雜碳量子點的細胞毒性及生物成像
為了評估N-CQDs的細胞毒性,采用標準MTT法測定了用N-CQDs處理后HepG2細胞的活性。將HepG2細胞分別與不同劑量的N-CQDs培育24 h,當N-CQDs的質量濃度小于100 μg/mL時,細胞活性大于95%;N-CQDs質量濃度達1 000 μg/mL時,其細胞活性仍可達到85%。該結果表明所制備的N-CQDs具有較低的細胞毒性,可用于生物標記。為了進一步證實N-CQDs在細胞成像中應用的可行性,在37 ℃,5% CO2條件下,將HepG2細胞與質量濃度分別為50 μg/mL和250 μg/mL的N-CQDs共培育24 h,并使用熒光顯微鏡在488 nm和610 nm檢測波長下進行觀察。結果顯示,在上述條件下細胞分別發出綠色(488 nm)和紅色(610 nm)的熒光,且綠色熒光的成像效果最佳(圖6),同時經250 μg/mL N-CQDs培育后的HepG2細胞成像效果優于50 μg/mL N-CQDs培育后的成像效果。該結果表明N-CQDs具有良好的滲透性能和生物相容性,可作為生物體成像的探針使用。

圖6 HepG2細胞和N-CQDs(0、50、 250 μg/mL)培育24 h的共聚焦熒光圖像Fig.6 Confocal fluorescence images of HepG2 cells incubated with N-CQDs(0,50,250 μg/mL) for 24 h at two different excitation wavelengths including 488 nm(green) and 610 nm(red)
2.6 選擇性
考察了水中常見的Fe3+、Zn2+、K+、Hg2+、Al3+、Mg2+、Ca2+、Na+、Cu2+、HQ、DA、p-NP、CC等干擾物對測定的影響。如圖7所示,當上述金屬離子及小分子與o-NP的濃度均為10 μmol/L時,各干擾物基本不影響o-NP的測定,說明N-CQDs熒光體系對o-NP具有良好的選擇性。
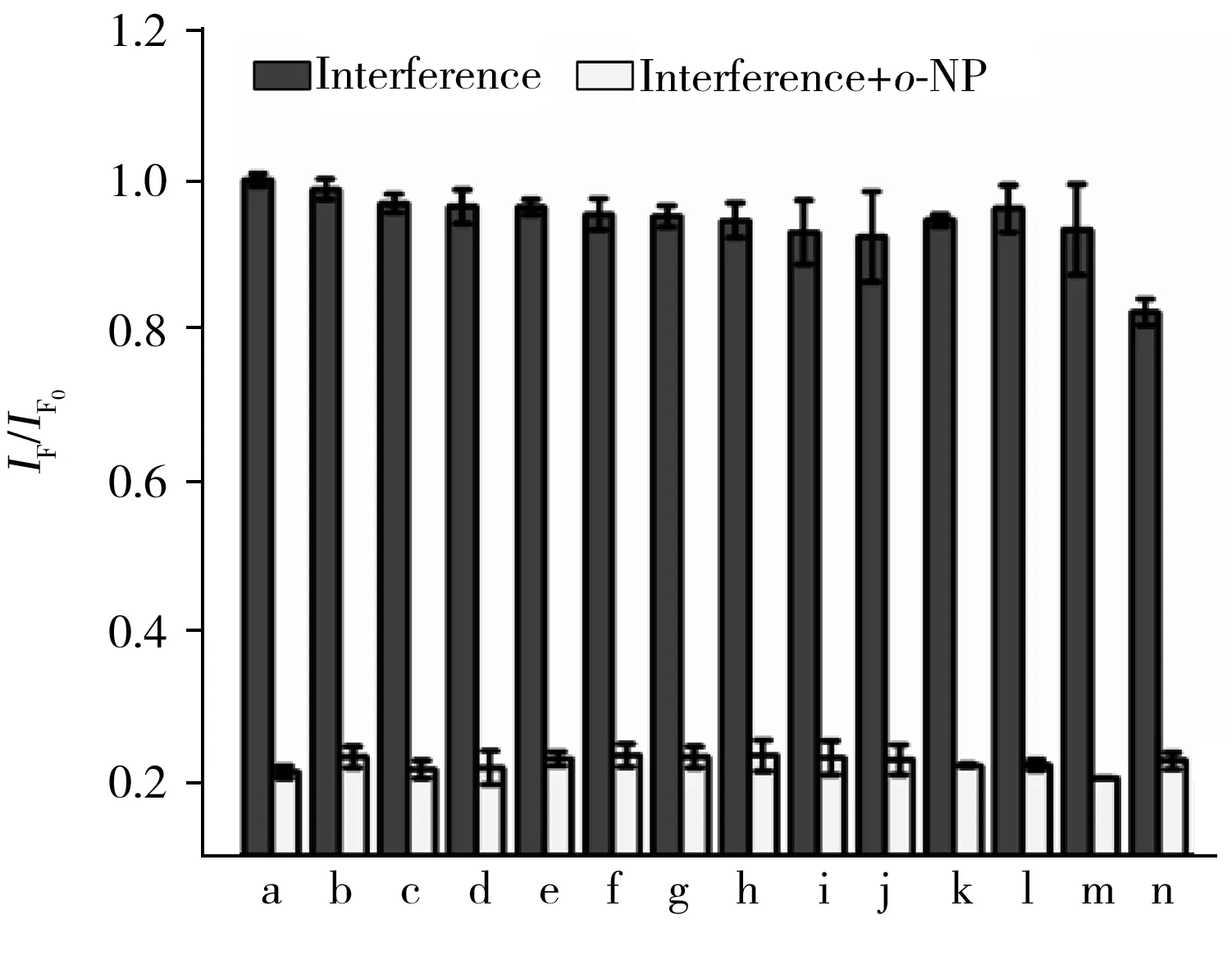
圖7 N-CQDs探針對o-NP的選擇性Fig.7 Selectivity of N-CQDs sensing system to o-NPa-n:blank,Fe3+,Zn2+,K+,Hg2+,Al3+,Mg2+,Ca2+,Na+,Cu2+,HQ,DA,p-NP,CC
2.7 線性關系及檢出限
考察了不同濃度o-NP對N-CQDs體系熒光強度的影響,結果顯示,當o-NP濃度為0.083 3、0.333、0.666、1.00、2.00、4.00、5.00、6.00、8.00、10.0、12.0、30.0、60.0、90.0、 120、150 μmol/L時,體系的熒光強度隨o-NP濃度的增加逐漸降低,體系發生不同程度的熒光猝滅,且N-CQDs熒光猝滅程度與o-NP濃度(c)在0.083 3~12.0 μmol/L范圍內呈良好線性關系,線性方程為IF/IF0=0.0128 8c+1.027 16,r2=0.998,檢出限(S/N=3)為25.2 nmol/L,低于美國國家環境保護署的標準19.4 μmol/L[31],且低于先前一些關于o-NP檢測文獻的報道(表1),表明該N-CQDs可用于地表水樣中o-NP的檢測。
2.8 實際樣品測定
采集貴州省興義市萬峰湖景區湖水和頂效河河水樣品,經12 000 r/min轉速離心后,以0.22 μm濾膜濾除雜質,采用本方法測定,結果如表2所示。本方法測定o-NP的回收率為85.2%~112%,相對標準偏差為2.8%~3.7%。結果表明,本方法具有較好的準確性,可用于實際樣品中o-NP含量的檢測。

表1 本方法與其他o-NP測定方法的比較Table 1 Comparison of the proposed method with other reports for o-NP determination

表2 實際樣品中鄰硝基苯酚的測定(n=3)Table 2 Detection of o-nitrophenol in real samples(n=3)
3 結 論
本研究以L-瓜氨酸和尿素為前驅體,通過水熱法一步合成了分散性良好、球形規則、尺寸均一、平均粒徑為2.8 nm的N-CQDs,該N-CQDs顯示了良好的生物相容性和低細胞毒性,可用于體外HepG2細胞成像。此外,鄰硝基苯酚可與N-CQDs的表面親水性基團(—COOH、—OH和—NH2)進行選擇性絡合導致量子點的熒光猝滅,熒光猝滅程度與鄰硝基苯酚濃度在0.083 3~12.0 μmol/L范圍內具有良好線性關系,檢出限為25.2 nmol/L。所建立的方法簡單、快速,應用于環境水樣中鄰硝基苯酚的測定,結果滿意。

