南極大磷蝦腸道曲霉菌Aspergillus sydowii NJF7的分離與代謝產物的研究
常俊男,李靈智,樊成奇,韓清華,黃洪亮,馬麗艷,陸亞男,李月月,田曉清,3
(1.中國水產科學研究院東海水產研究所,上海 200090;2.農業農村部遠洋與極地漁業創新重點實驗室,上海200090;3.農業農村部東海漁業資源開發利用重點實驗室,上海 200090;4.上海海洋大學,上海 201306)
南極大磷蝦(Euphausiasuperba)因其區域特色、資源保有量優勢以及廣泛應用價值為世界主要發達國家所青睞,國際上已形成磷蝦捕撈技術支撐、高附加值產品驅動為一體的產業鏈[1-3]。我國更將南極大磷蝦商業化開發納入國家海洋發展戰略,積極培育這一海洋生物精深利用新興產業。南極大磷蝦自身富含多種活性物質,包括DHA/EPA等不飽和脂肪酸、磷脂、多種活性低溫酶等[4-8]。而腸道作為磷蝦等動物體內重要的消化吸收器官,其中棲息著數量龐大、結構復雜的腸道微生物組(intestinalmicrobiota),與宿主的營養代謝、遺傳、發育及進化、免疫防御等重要生命過程休戚相關[9-11]。有學者研究發現南極大磷蝦腸道菌群包含大量未知微生物新種屬,隨后通過菌株代謝產物及其生物活性篩選,從南極大磷蝦可培養菌株代謝產物中鑒定化合物48個,具有抗海洋病毒、抗海洋病原菌及抗污損等多種生態學活性[12-16]。因此,我國亟需繼續大力加強南極大磷蝦基礎生物學研究,積極拓展其資源綜合利用新途徑。本研究小組成員在參與第29次極地科學考察時,分離出南極大磷蝦共附生微生物133株,其中7%為未知種[17],并且全部為細菌。丁壯等[18]總結了極地真菌的代謝產物,發現其代謝產物多樣性較好,且具有抗菌、增強抗癌藥物活性、核苷轉移抑制劑等活性。
因此,本文在前人研究的基礎上對第34次“雪龍號”南極考察采集到的南極大磷蝦共附生菌進行真菌菌株分離鑒定,并對其次級代謝產物進行初步研究,以期為極地真菌以及南極大磷蝦綜合利用提供參考。
1 材料與方法
1.1 材料
南極大磷蝦由2017年第34次“雪龍號”南極考察船采用框架拖網采獲。
培養基:孟加拉紅固體培養基[19];PDA固體培養基;YPD固體培養基;YPD液體培養基。用于分離真菌菌株時每種培養基添加抗生素:青霉素、鏈霉素、氯霉素各30μg·mL-1。
色譜材料:柱層析硅膠(200 300目)及預制GF254 TLC硅膠板:青島海洋化學公司;MCI gel(CHP 20P,75 150μm);C18反相硅膠(150 200目):Merck公司;凝膠Sephadex LH 20:Pharmacia Biotech,Sweden。
試劑:乙腈、甲醇(色譜級,Merck公司);其他試劑,如乙酸乙酯、甲醇、丙酮、正丁醇、石油醚、三氯甲烷等(AR,上海國藥集團);標準品尿嘧啶(5 g·瓶-1)(上海國藥集團)。
1.2 實驗儀器
微生物恒溫培養箱(上海一恒科學有限公司,DHP9162A);大型恒溫搖床培養箱(上海天星實驗儀器制造有限公司,TS 211C);超聲波清洗器(上海漢克科學儀器有限公司,SK250LH);光學顯微鏡(上海光學儀器一廠,XSP 44X.9);半制備HPLC儀器(Shimadazu,SPD M20A PDA);半制備HPLC儀器(Waters,2545);液質聯用儀(HR ESI MS,Agilent,1290 HPLC 6224 TOF MS,分辨率≥20 000);旋轉蒸發儀(上海亞榮生化儀器廠,RE3000A);反相半制備色譜柱:YMC Pack ODS AQ column(250×10 mm,S 5μm,12 nm,分離流速2.5 mL·min-1);正相半制備色譜柱:YMC Pack SIL 06 column(250×10 mm,S 5μm,6 nm,分離流速4.0 mL·min-1);核磁共振波譜儀(Bruker AM 400 spectrometer)。
1.3 菌株的分離鑒定
將南極大磷蝦樣品在超凈工作臺內用無菌海水沖洗表面,用研缽研碎,將處理好的樣品加入裝有10 mL無菌海水的50 mL無菌管中,樣品震蕩混勻后梯度稀釋10-1、10-2、10-3,不同梯度分別取300μL菌液涂布于孟加拉紅、PDA和YPD 3種固體培養基上,每個梯度樣品做3個平行。涂布好的平板倒置于15℃培養箱中培養;培養約3~4周后長出菌落,依據菌落特征進行分離,挑取菌落接種至相應培養基上劃線分離純化培養,直至得到純菌落。分離得一株真菌NJF7,菌株保存于YPD或孟加拉紅斜面固體培養基,置于4℃冰箱進行保種;另用30%的甘油保種于-80℃的冰箱進行長期保存。然后轉移到液體培養基送至上海美吉生物醫藥科技有限公司進行一代測序。
同時將滅菌的載玻片45°傾斜插入涂布真菌菌種的固體培養皿中,28℃培養箱中培養3~5 d,用光學顯微鏡觀察菌絲形態特征,如菌落形狀、大小、色澤、質地、有沒有產生孢子等特點,并作記錄。再參考張新軍[20]和孫晶晶等[21]的研究對真菌進行初步的分類、鑒定。
1.4 菌株的次級代謝產物分離純化
1.4.1 發酵液的獲取
NJF7菌株接種在2只50 mL試管中(內有5 mL的YPD液體培養基),搖床恒溫27℃培養活化5~7 d。將活化的NJF7菌株接種至2只1 000 mL三角瓶(內含500 mL YPD液體培養基)中,置于20℃160 r·min-1恒溫搖床培養箱中,發酵培養5 d后得到種子發酵液。將發酵的種子液按一定比例接到裝有YPD液體培養基的2 L三角瓶中,在20℃160 r·min-1恒溫搖床培養箱中發酵培養,共得到培養發酵液約35.5 L。
1.4.2 次級代謝產物的提取分離
NJF7菌株發酵液35.5 L用布氏漏斗及定性中速(直徑18 cm)的濾紙真空抽濾分為菌絲體和胞外濾液兩部分。菌絲體置于-80℃冰箱中冷凍,48 h后取出放在室溫解凍,解凍后依次加入3 L的丙酮和甲醇,用超聲清洗器超聲提取,各提取2次,得到菌絲體部分浸膏。胞外濾液約35.5 L,每1.6 L菌液分別用200 mL的乙酸乙酯和正丁醇萃取各2次,旋轉濃縮得乙酸乙酯部分浸膏157.3 g,正丁醇部分浸膏19.0 g。乙酸乙酯部分與菌絲體提取濃縮的浸膏合并,質量為163.2 g,用650 mL的純水溶解充分,再用325 mL的石油醚、乙酸乙酯、正丁醇3種試劑各萃取3次。萃取液真空低溫旋蒸,除去有機溶劑,得到石油醚部分浸膏10.5 g;乙酸乙酯部分浸膏0.32 g;正丁醇部分浸膏與第一次正丁醇部分合并共31.3 g。
乙酸乙酯部分經Sephadex LH 20凝膠柱分離,通過TLC硅膠板點樣分析得到NJF7I~VII 7部分。NJF7I部分經Waters正向柱制備,流動相為乙酸乙酯 石油醚。NJF7III部分過硅膠分為IIIa和IIIb,然后再用HPLC制備,各部分HPLC梯度洗脫程序以及化合物見表1。
用MCI柱分離正丁醇部分:用1 000mL水洗脫MCI柱4個柱體積,后用400mL甲醇∶水(V∶V=10∶90)淋洗,除去鹽、糖、蛋白等雜質;依次用甲醇∶水(20∶80→50∶50→80∶20→100∶0)洗脫,每梯度洗脫液的用量為1 000 mL。洗脫下來的液體用旋轉蒸發儀依次濃縮得到20%甲醇、50%甲醇、80%甲醇和100%甲醇4個部分。50%和80%甲醇部分經過硅膠分離后再通過HPLC制備,流動相為乙腈 水(水含0.1%三氟乙酸),各部分梯度洗脫程序以及化合物見表2。
2 結果與分析
2.1 菌種鑒定結果
曲霉屬菌種NJF7在孟加拉紅培養基培養,其培養特征(A)和在光學顯微鏡目鏡10倍、物鏡40倍條件下形態(B)見圖1。
真菌NJF7菌落特點:菌落的顏色為黃綠色;質地絲絨狀,形成放射狀溝紋;沒有滲出液;分生出來的孢子頭形成疏松放射狀;頂囊近球形;分生的孢子形狀為球形、近球形。根據姚栗等[22]的研究結果,對照實驗菌種的培養特征和顯微形態,其與黃曲霉菌顏色形態一致。
菌株序列與生物信息學數據庫GenBank(https://www.ncbi.nlm.nih.gov)進行序列的相似性比較分析,尋找最高相似性在98%左右的菌株,選取比對結果中與其相似性較高的模式株,然后對菌株構建系統發育樹(圖2)。
基因序列同源性比對分析發現,菌株NJF7與Aspergillus屬模式種A.sydowii(KX958084.1)相似性最高,為99%,與A.sydowii(JN851025.1)在同一枝節。根據真菌的形態學特點,鑒定NJF7為曲霉Aspergillussydowii。
2.2 次級代謝產物鑒定結果
從菌株NJF7的代謝產物中分離出化合物,分別經HR ESI MS、1H NMR波譜學方法,鑒定了其中13個化合物。結構見圖3。
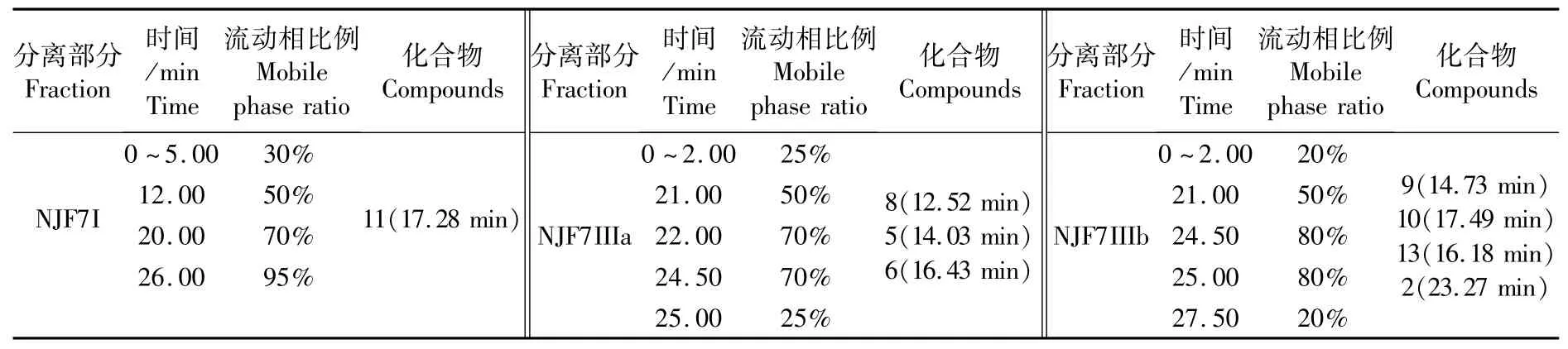
表1 乙酸乙酯各部分梯度洗脫程序表及化合物Tab.1 Gradient elution procedures and compounds of EA

表2 正丁醇部分梯度洗脫程序表及化合物Tab.2 Gradient elution procedures and compounds of n butyl alcohol
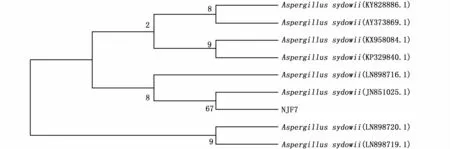
圖2 基于菌株NJF7及其相應模式菌株的18S rDNA構建的系統發育樹Fig.2 Neighbour joining phylogenetic tree based on 18S rDNA gene sequence for the position of strain NJF7
化合物1:淺黃色粉末,HR ESI MS譜得出準分子離子峰m/z261.117 7([M+H]+,計算值為261.116 1),提示其分子式為C14H16N2O3。1H NMR(pyr,600 MHz)數據如下:δH1.53(m,2H),1.81(m,1H),2.13(m,1H),3.29(dd,J=14.7,6.3 Hz,1H),3.36(m,1H),3.58(m,3H),4.09(t,J=8.0,8.5 Hz,1H),4.52(t,J=5.2,5.5 Hz,1H),7.08(d,J=8.4 Hz,2H),7.39(d,J=8.1 Hz,2H),8.58(s,1H)。該化合物數據與文獻[23]報道一致,因此化合物1結構鑒定為環(脯氨酸 酪氨酸)。
化合物2:淺黃色粉末,HR ESI MS譜得出準分子離子峰m/z350.149 9([M+H]+,計算值為350.146 0),提示其分子式為C20H19N3O3。1H NMR(CD3OD,600 MHz)數據如下:δH2.61(dd,J=13.4,6.3 Hz,1H),2.83(dd,J=14.5,5.7 Hz,1H),3.03(dd,J=14.7,4.1 Hz,1H),3.51(dd,J=11.4,6.6 Hz,1H),3.58(m,1H),3.65(m,3H),3.90(m,1H),4.18(m,1H),6.60(m,2H),7.04(s,1H),7.07(m,1H),7.13(m,1H),7.17(m,3H),7.35(d,J=7.9 Hz,1H),7.60(d,J=8.0 Hz,1H)。該化合物數據與文獻[24]報道一致,因此化合物2結構鑒定為環(色氨酸 酪氨酸)。
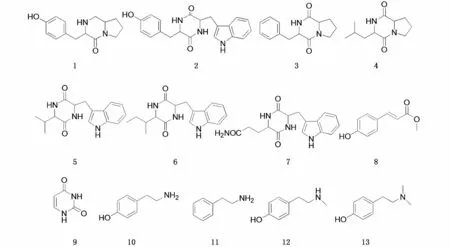
圖3 從NJF7中分離得到的化合物結構式Fig.3 Structure formulas of com pounds isolated from NJF7
化合物3:黃色油狀物,HR ESI MS譜得出準分子離子峰m/z245.127 9([M+H]+,計算值為245.121 2),提示其分子式為C14H16N2O2。1H NMR(CD3OD,600 MHz)數據如下:δH1.25(m,1H),1.82(m,2H),2.11(m,1H),3.18(m,2H),3.38(m,1H),3.55(m,1H),4.08(m,1H),4.46(m,1H),7.46(m,5H)。該化合物數據與文獻[25]報道一致,因此化合物3結構鑒定為環(脯氨酸 苯丙氨酸)。
化合物4:黃色膠狀物,HR ESI MS譜得出準分子離子峰m/z211.141 9([M+H]+,計算值為211.140 2),提示其分子式為C11H18N2O2。1H NMR(CD3OD,400 MHz)數據如下:δH0.97(m,6H),1.56(m,1H),1.67(m,1H),1.77(m,1H),1.92(m,2H),2.02(m,1H),2.33(m,2H),3.48(m,1H),3.56(m,1H),3.83(dd,J=9.7,6.0 Hz,1H),4.26(m,1H)。該化合物數據與文獻[26]報道一致,因此化合物4結構鑒定為環(纈氨酸 脯氨酸)。
化合物5:黃褐色無定型粉末,HR ESI MS譜得出準分子離子峰m/z286.155 2([M+H]+,計算值為286.151 1),提示其分子式為C16H19N3O2。1H NMR(D2O,600 MHz)數據如下:δH0.13(d,J=7.3 Hz,2H),0.69(d,J=7.3 Hz,2H),1.33(m,1H),3.34(dd,J=15.1,5.3 Hz,1H),3.43(s,2H),3.54(dd,J=15.0,5.4 Hz,1H),3.77(m,3H),4.56(td,J=4.6,1.7 Hz,1H),7.24(m,1H),7.29(m,2H),7.55(d,J=9.3 Hz,1H),7.74(d,J=6.7 Hz,1H)。該化合物數據與文獻[27]報道一致,因此化合物5結構鑒定為環(纈氨酸 色氨酸)。
化合物6:淺黃色粉末,HR ESI MS譜得出準分子離子峰m/z300.184 1([M+H]+,計算值為300.166 7),提示其分子式為C17H21N3O2。1H NMR(pyr,600 MHz)數據如下:δH0.83(t,J=7.3,7.5 Hz,3H),1.10(d,J=6.8 Hz,3H),1.18(m,1H),1.56(m,1H),2.15(m,1H),3.72(dd,J=14.5,8.1 Hz,1H),3.95(dd,J=14.5,4.6 Hz,1H),4.19(s,1H),4.77(m,1H),7.28(d,J=1.1 Hz,1H),7.33(m,1H),7.53(s,1H),7.60(m,1H),8.11(d,J=8.1 Hz,1H),9.10(d,J=26.0 Hz,2H),11.98(s,1H)。該化合物數據與文獻[27-28]報道一致,因此化合物6結構鑒定為環(異亮氨酸 色氨酸)。
化合物7:淺黃色粉末,HR ESI MS譜得出準分子離子峰m/z315.169 3([M+H]+,計算值 為315.141 2),提 示 其 分 子 式 為C16H18N4O3。1H NMR(CD3OD,600 MHz)數據如下:δH0.98(m,1H),1.50(m,1H),1.70(m,1H),1.99(m,1H),3.29(m,1H),3.48(m,1H),4.02(m,1H),4.43(m,1H),7.03(m,1H),7.11(m,2H),7.35(dt,J=8.2,0.8 Hz,1H),7.59(dt,J=8.0,0.9 Hz,1H)。該化合物數據比文獻[29]報道的環(天門冬酰胺 色氨酸)的數據多一個亞甲基信號,因此化合物7結構鑒定為環(谷氨酰胺 色氨酸)。
化合物8:白色粉末,1H NMR(D2O,600 MHz)數據如下:δH3.43(s,2H),6.48(d,J=17.2 Hz,1H),7.02(m,2H),7.64(m,3H).該化合物數據與文獻[30]報道一致,因此化合物8結構鑒定為對羥基肉桂酸甲酯。
化合物9:淺黃色針狀結晶,與標準品作對照鑒定化合物為尿嘧啶。
化合物10:黃色無定形粉末,HR ESI MS譜得出準分子離子峰m/z138.089 9([M+H]+,計算值為138.087 4),提示其分子式為C8H11NO。1H NMR(CD3OD,600 MHz)數據如下:δH2.53(t,J=7.7,7.6 Hz,1H),2.80(t,J=7.6,7.7 Hz,1H),6.69(m,1H),7.02(m,1H)。該化合物數據與文獻[31]報道一致,因此化合物10結構鑒定為對羥基苯乙胺。
化合物11:黃色油狀物,HR ESI MS譜得出準分子離子峰m/z122.096 6,([M+H]+,計算值為122.096 4),提示其分子式為C8H11N。1H NMR(CDCl3,600 MHz)數據如下:δH2.71(m,1H),2.98(t,J=7.7,8.0 Hz,1H),7.23(m,1H),7.31(m,1H)。該化合物數據與文獻[32]報道一致,因此化合物11結構鑒定為苯乙胺。
化合物12:白色粉末,1H NMR(CD3OD,400 MHz)數據如下:δH2.56(t,J=7.7,7.5 Hz,1H),2.80(t,J=7.7,7.7 Hz,1H),3.62(s,1H),6.67(d,J=8.1 Hz,1H),7.00(d,J=8.6 Hz,1H)。該化合物數據與文獻[33]報道一致,因此化合物12結構鑒定為N 甲基酪胺。
化合物13:無色針狀晶體,1H NMR(pyr,600 MHz)數據如下:δH2.82(t,J=7.9,7.5 Hz,1H),3.08(t,J=7.7,7.7 Hz,1H),3.57(s,3H),7.10(d,J=9.4 Hz,1H),7.26(d,J=5.7 Hz,1H)。該化合物數據與文獻[34]報道一致,因此化合物13結構鑒定為大麥芽堿。
3 討論
曲霉NJF7是本課題組在南極大磷蝦腸道微生物中分離到的第一株真菌,從其發酵液提取物中鑒定了13個代謝產物結構,化合物結構類型包含二酮哌嗪(1~7)、芳香酸(8)、生物堿類(9~13)。化合物7環(谷氨酰胺 色氨酸)(天然成分)首次從曲霉屬真菌中分離。環肽作為天然產物的一類,通常單獨存在或嵌入在更大、更復雜的結構中,在真菌、細菌、海洋海綿和植物中的次級代謝產物中都有獲得[35]。環肽類化合物由于具有抗腫瘤、抗菌、抗真菌等生物活性而備受研究者關注[29]。例如化合物2對L 929、K 562和HeLa細胞系具有較弱的抗增殖和細胞毒作用[23]。目前已發現的上百個環肽類化合物絕大部分來自于海洋生物,其中海洋微生物所產生的一些特殊環肽顯示出很好的抗腫瘤活性。本研究獲得的芳香酸和生物堿類化合物也表現出良好的活性,例如化合物12可以刺激胃泌素的釋放,在低劑量(25μg·kg-1)時就可獲得最大的釋放活性[33]。后期對化合物7的活性將繼續探討。
但是,通過對NJF7次級代謝產物的研究,發現目前鑒定的次級代謝產物種類少、結構單一、新穎性不足,結構比較復雜的化合物未能被獲得,因此未進一步開展化合物的活性篩選。這可能由于本實驗只使用了YPD一種發酵培養基且培養條件比較簡單的緣故。后期將從培養基種類以及培養條件進行優化,以期得到較為新穎、具有較好生物活性的化合物乃至具有新藥開發前景的天然產物。RUI等[27]在海綿中結合宏基因組學的方法分離到11個環肽成分,在以后的研究中可以考慮首先通過宏基因組學對樣品中具有生物活性的小分子進行預估,以節省分離時間,提高分離效率。

