3種總大腸菌群和大腸埃希氏菌酶底物法檢測試劑性能比較
孫 杰
(上海城投水務〈集團〉有限公司,上海 200082)
酶底物法(defined substrate technology,DST)是指在選擇性培養基上能產生β-半乳糖苷酶(β-D-galactosidase)的細菌群組分解色原底物、釋放色原體,使培養基呈現顏色變化,來檢測水中大腸菌群的方法[1]。與傳統多管發酵法相比,該方法具有操作簡便、檢測時間短、無需確認試驗、無菌要求低等優點,且大量文獻證實,Colilert酶底物法試劑與多管發酵法在檢測大腸菌群結果上沒有顯著性差異[2-3]。因此,該方法被廣泛應用于大腸菌群的檢測[4-6]。《生活飲用水標準檢驗方法》(GB/T 5750.12—2006)[1]和《水質 總大腸菌群、糞大腸菌群和大腸埃希氏菌的測定》(HJ 1001—2018)[7]中,均將酶底物法作為總大腸菌群和大腸埃希氏菌的標準檢測方法。隨著酶底物法應用的普及,市面上出現了各種不同品牌的酶底物法試劑,這些產品的質量良莠不齊,性能也不同,影響檢測結果的準確性。為確定酶底物法試劑的性能,保證檢測結果的真實有效,本文對市面上常見的3種酶底物法試劑進行了分析比較,檢測定量質控、原水、二次供水、管網水等多種水樣,并對其性能進行評價。
1 試驗部分
1.1 主要試劑、設備
3種酶底物商品試劑(Colilert、LI、QT),程控定量封口機、無菌取樣瓶、97孔定量盤、51孔定量盤、NSI定量質控菌株。試驗使用國產恒溫培養箱(SPX-250B-Z型),溫控精度為±0.5 ℃,經計量部門校準合格。
1.2 試驗步驟
(1)水樣采集:原水水樣為上海某水廠的進廠原水,二次供水水樣為上海居民的龍頭水,管網水水樣取自上海某地區的管網監測點。參照GB/T 5750.2—2006進行采集和樣品保存[8],采樣容器使用一次性無菌含硫代硫酸鈉采樣瓶。水樣采集后冷藏保存,并在4 h內進行檢測。
(2)定量質控檢測:NSI定量質控菌株從-10 ℃冰箱中取出,平衡溫度10~15 min后,將質控菌株轉移入預先準備好的100 mL無菌磷酸緩沖液中,輕輕振蕩,待全部溶解后在30 min內進行檢測。
(3)樣品檢測:樣品使用酶底物法進行檢測,檢測項目為總大腸菌群、大腸埃希氏菌。檢測步驟參照GB/T 5750.12—2006。
(4)實際水樣陽性結果測序:對于定量盤陽性結果,送由金唯智生物科技有限公司測序,對菌種進行鑒定。
2 結果分析
2.1 混合質控陽性菌:飲用水和環境水定量質控檢測
Colilert、LI、QT總大腸菌群和大腸埃希氏菌質控檢測結果表明:3種試劑的檢測結果均在質控樣品結果可接受范圍內;QT試劑總大腸菌群和大腸埃希氏菌結果相同,表明該試劑對大腸埃希氏菌的顯色反應有誤,未能區分大腸埃希氏菌和其他混合菌種。為進一步評價試劑性能和結果的準確性,計算檢測結果與真值的相對誤差[相對誤差=(測定值-真值)/真值×100%],如表1、圖1所示。結果表明,Colilert試劑檢測結果與真值的相對誤差最小,檢測結果更接近于真值。計算3種試劑檢測結果相對誤差的標準差,可得總大腸菌群標準差:SD(Colilert)=5.54,SD(QT)=19.87,SD(LI)=34.30,大腸埃希氏菌標準差:SD(Colilert)=7.26,SD(QT)=14.27,SD(LI)=25.84。可知,Colilert試劑標準差最小,表明其檢測結果與真值的相對誤差離散程度較小,性能較為穩定;LI試劑的標準差最大,表明其性能不穩定,結果波動性較大。
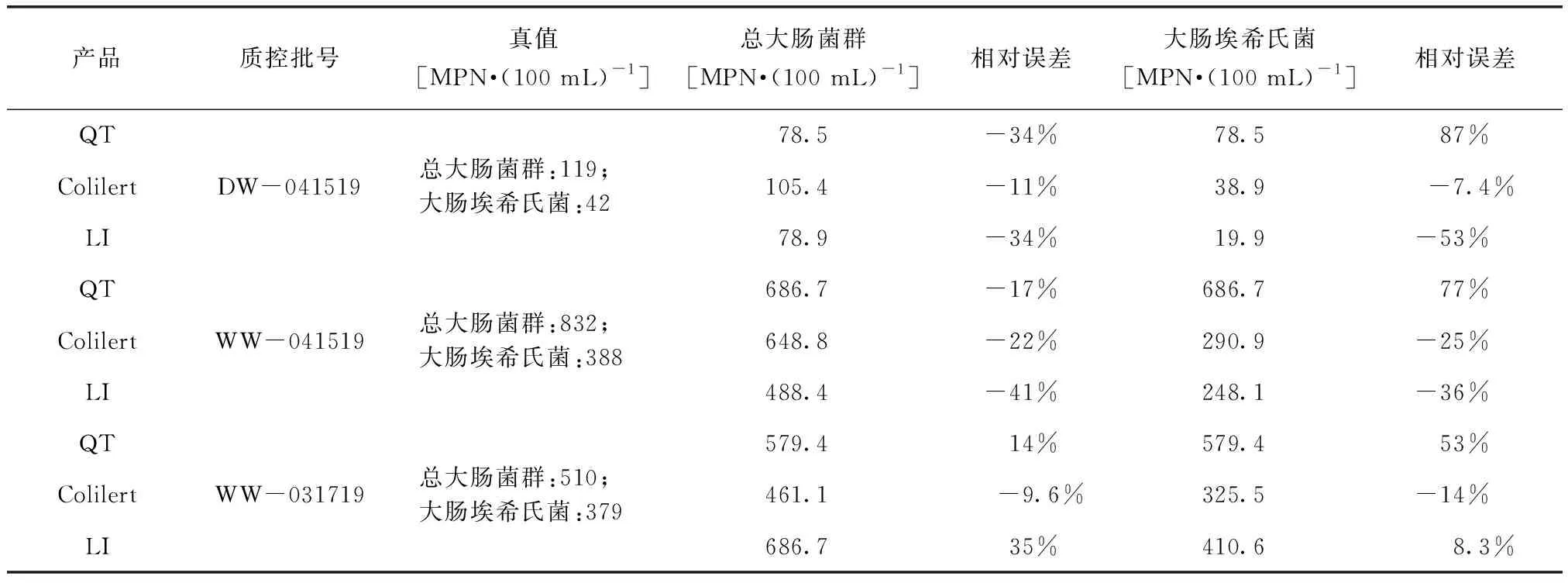
表1 3種試劑檢測NSI定量質控樣品的結果Tab.1 Results of NSI Quantitative Quality Control Samples (QC) Detected by Three Reagents
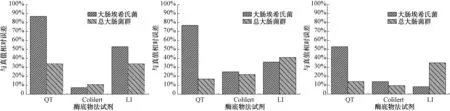
圖1 3種試劑檢測結果真值的相對誤差Fig.1 Relative Error between Test Samples and Trueth-Values
2.2 單一菌種質控及陰性菌:大腸埃希氏菌、銅綠假單胞菌檢測
Colilert、 LI、 QT檢測單一菌種質控及陰性菌。3種試劑的檢測結果均在質控樣品結果可接受范圍內。QT試劑大腸埃希氏菌結果與總大腸菌群結果不一致,證明了2.1節的推斷,即該試劑對大腸埃希氏菌的顯色反應不穩定,不能用于大腸埃希氏菌的檢測,如表2所示。3種試劑對陰性菌銅綠假單胞菌均能有效辨別。計算檢測結果與真值的相對誤差,結果表明, Colilert試劑檢測結果與真值的相對誤差最小,檢測結果更接近于真值。

表2 3種試劑檢測單一菌種質控及陰性菌結果Tab.2 Results of Single Strain QC and Non-Target Bacteria Detected by Three Reagents
2.3 實際水樣
(1)3種試劑檢測二次供水、管網水總大腸菌群,并對陽性結果進行16S rDNA測序,結果如表3所示。Colilert、LI和QT陽性檢出率,二次供水分別為11.43%、5.71%和45.71%,管網水分別為0.00、3.33%、26.67%。提取二次供水和管網水陽性孔菌體的DNA,測定16S rDNA,進行菌種鑒定,確認陽性結果的真實性。測序結果表明,Colilert陽性結果的樣品均含有總大腸菌群,即檢測結果與測序結果吻合。LI陽性結果3組,E-31為真陽性,E-6和G-8兩組結果為假陽性,假陽性率為66.6%,陽性樣本漏檢率為75%。QT檢測陽性結果24組,1組為真陽性,其余23組均為假陽性,假陽性率為95.8%,陽性漏檢率為75%。
(2)對原水總大腸菌群,Colilert、LI和QT的實際檢測結果如表4所示。
運用軟件SPSS Statistics 19,對Colilert、LI和QT檢測結果進行配對t檢驗,為了使數據呈正態分布,對數據進行對數處理后再進行t檢驗,結果如表5所示。
由表3可知:Colilert 與LI、QT的泊松相關系數為0.495和0.319,屬弱相關;P<0.05,具有統計學意義上的顯著性差異。結果表明,LI、QT在檢測原水總大腸菌群時,與Colilert的檢測結果具有差異性。
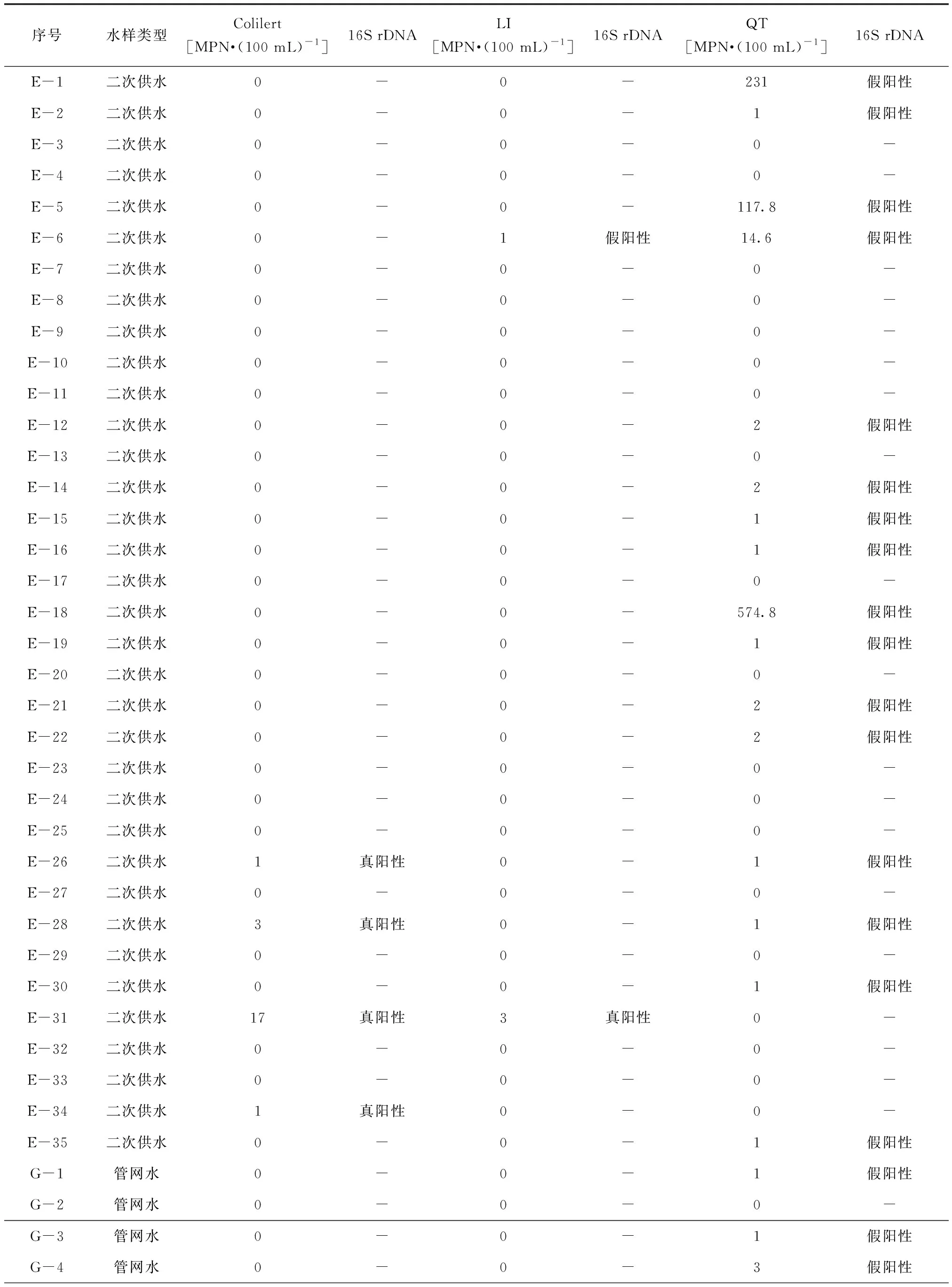
表3 3種試劑對二次供水、管網水的檢測及測序結果Tab.3 Testing and Sequencing Results of Three Reagents for Secondary Water Supply and Pipeline Water
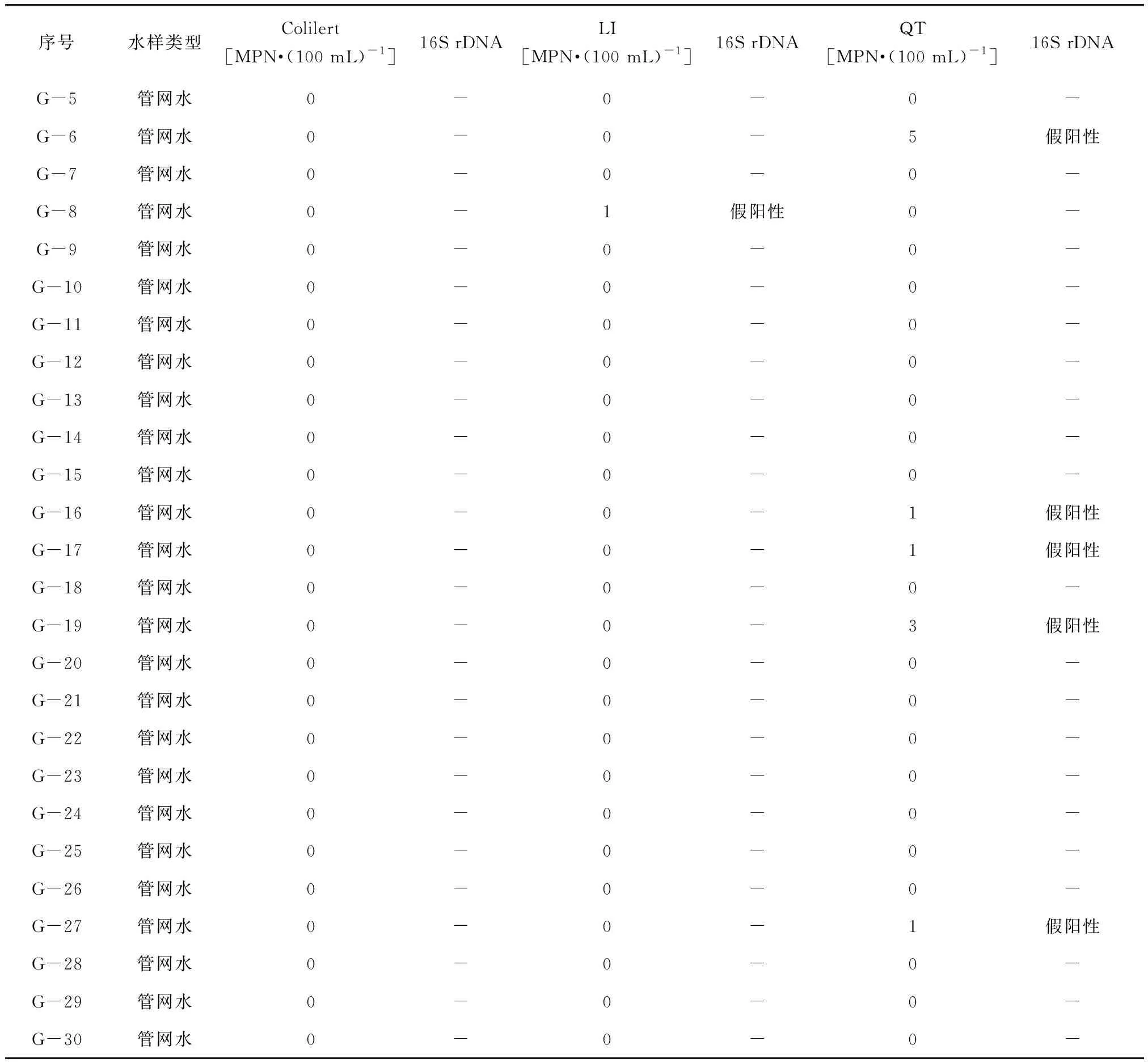
序號水樣類型Colilert[MPN·(100 mL)-1]16S rDNALI[MPN·(100 mL)-1]16S rDNAQT[MPN·(100 mL)-1]16S rDNAG-5管網水0-0-0-G-6管網水0-0-5假陽性G-7管網水0-0-0-G-8管網水0-1假陽性0-G-9管網水0-0-0-G-10管網水0-0-0-G-11管網水0-0-0-G-12管網水0-0-0-G-13管網水0-0-0-G-14管網水0-0-0-G-15管網水0-0-0-G-16管網水0-0-1假陽性G-17管網水0-0-1假陽性G-18管網水0-0-0-G-19管網水0-0-3假陽性G-20管網水0-0-0-G-21管網水0-0-0-G-22管網水0-0-0-G-23管網水0-0-0-G-24管網水0-0-0-G-25管網水0-0-0-G-26管網水0-0-0-G-27管網水0-0-1假陽性G-28管網水0-0-0-G-29管網水0-0-0-G-30管網水0-0-0-
3 討論
3.1 混合質控檢測
Colilert、LI、QT對3組混合質控總大腸菌群和大腸埃希氏菌檢測結果真值相對誤差絕對值的平均值分別為14.35%、36.55%、21.70%和15.51%、32.34%、72.26%。Colilert 檢測定量質控結果真值的相對誤差小,檢測結果準確;LI和QT檢測結果真值的相對偏差較大。標準差結果計算表明,Colilert試劑標準差最小,表明其檢測結果與真值的相對誤差離散程度較小,性能較為穩定;LI試劑的標準差最大,表明其性能不穩定,結果波動性較大。同時,總大腸菌群和大腸埃希氏菌的檢測結果表明,QT不能辨別大腸埃希氏菌與非大腸埃希氏菌,檢測大腸埃希氏菌時存在誤判的可能。
3.2 單一質控及陰性菌檢測
Colilert、LI、QT對3組單一菌種質控總大腸菌群和大腸埃希氏菌檢測結果真值相對誤差絕對值的平均值分別為6.92%、25.6%、20.7%和6.87%、35.02%、6.67%。但是,QT檢測大腸埃希氏菌單一質控時,總大腸菌群和大腸埃希氏菌檢測結果數值不一樣,熒光顏色較弱或呈藍綠色熒光,檢測數值偏低,有假陰性風險。因此,判斷QT不能有效辨別大腸埃希氏菌與非大腸埃希氏菌,檢測大腸埃希氏菌時存在誤判的可能。另外,LI培養基溶解后,顯示淡黃色,增加了結果判讀的難度。
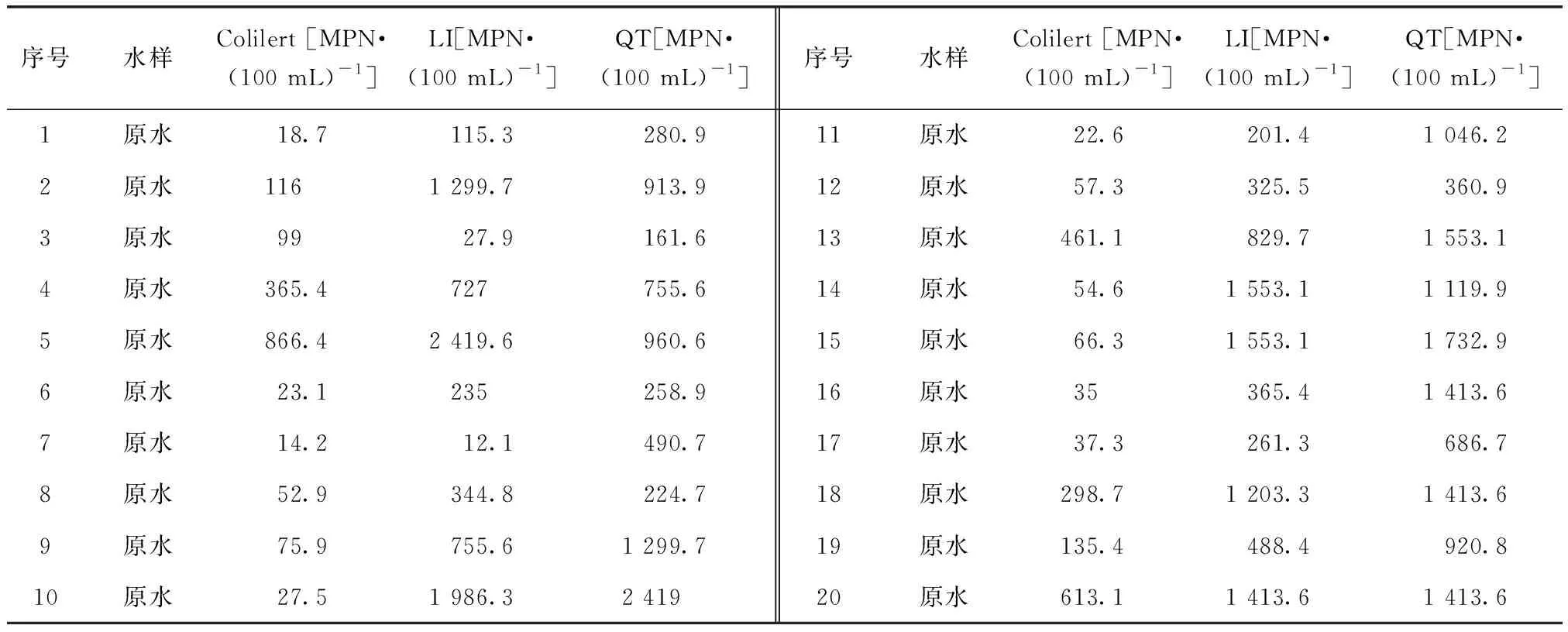
表4 3種試劑檢測原水的結果Tab.4 Testing Results of Raw Water by Three Reagents
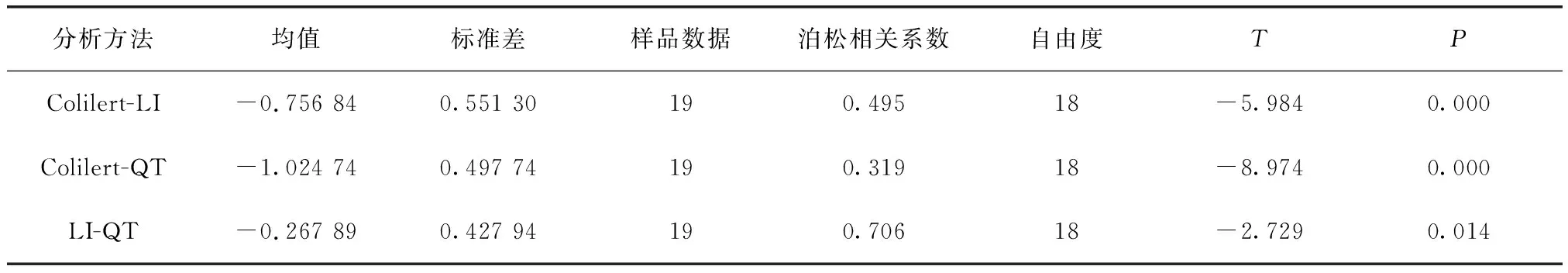
表5 3種試劑對原水檢測結果的t檢驗Tab.5 Results of t-Test of Raw Water by Three Reagents
3.3 實際水樣檢測
對于二次供水和管網水,Colilert 陽性結果與16S rDNA測序結果吻合;LI假陽性率為66.6%,陽性樣本漏檢率為75%;QT檢測假陽性率為95.8%,陽性漏檢率為75%。因此,在檢測實際水樣的過程中,2種酶底物試劑有漏檢陽性水樣的風險,增加了水質實驗室結果的不可信度;假陽性檢測結果的出現,會增加水質實驗室排查水質隱患的工作量。對于原水的檢測,2種酶底物試劑與Colilert 具有弱相關性,具有統計學意義上的顯著性差異,和管網與二次供水的結果可互相驗證。
4 結論
Colilert 試劑質控樣品檢測結果與真值相對誤差較小,實際水樣檢測未出現假陽性,結果真實可靠,性能穩定;LI和QT試劑在檢測質控樣品時,與真值相對誤差較大,檢測實際水樣時,有假陽性和陽性漏檢的風險;QT不能有效辨別大腸埃希氏菌與非大腸埃希氏菌,檢測大腸埃希氏菌時存在誤判的可能。因此,實驗室在選擇酶底物試劑時,應選擇性能優良、口碑較好的品牌,確保檢測結果的準確性。

