阿爾茨海默癥的探索者——張晨教授
張 晨
(首都醫(yī)科大學基礎(chǔ)醫(yī)學院,北京 100069)
1 個人簡介
張晨教授(圖1),現(xiàn)任首都醫(yī)科大學基礎(chǔ)醫(yī)學院院長、博士生導師。1998年畢業(yè)于中國科學技術(shù)大學(學士),2003年畢業(yè)于中國科學院上海神經(jīng)科學研究所(博士,導師周專教授),2004-2010年在Thomas C Südhof教授實驗室從事博士后、助理研究員工作;2010-2018年于北京大學生命科學學院任研究員、博士生導師,2018年調(diào)入首都醫(yī)科大學后任基礎(chǔ)醫(yī)學院院長,帶領(lǐng)首都醫(yī)科大學基礎(chǔ)醫(yī)學院榮獲“2019年全國教育系統(tǒng)先進集體”稱號。現(xiàn)任中國生物物理學會理事、中國實驗動物學會理事、中國神經(jīng)科學學會理事等。共發(fā)表論文60余篇。負責國家級研究課題十余項,包括國家杰出青年科學基金、國家優(yōu)秀青年科學基金,并以首席科學家身份承擔國家重點研發(fā)計劃“基于重大神經(jīng)疾病非人靈長類模型的干細胞治療評價研究”;入選國家百千萬人才工程并被授予“有突出貢獻中青年專家”稱號;獲北京市“長城學者”、青年北京學者、教育部“新世紀優(yōu)秀人才支持計劃”、高等學校科學研究優(yōu)秀成果獎(自然科學獎,一等獎,第二完成人)、全國百篇優(yōu)秀博士論文獎等。

圖1 張晨教授
2 主要學術(shù)貢獻
阿爾茨海默癥(Alzheimer’s disease,AD)是最常見的神經(jīng)退行性疾病,嚴重影響老年人生活質(zhì)量。國際老年癡呆協(xié)會的數(shù)據(jù)顯示,我國當前AD患者超過600萬;同時隨著我國加速步入老齡化社會,預(yù)計到 21 世紀中葉我國AD患者將超過2 000萬;因此AD的診療研究——尤其是AD 精確發(fā)病機制的探索——已經(jīng)成為一個迫在眉睫的事關(guān)社會公共健康的重要科學問題。已有研究[1]結(jié)果顯示,AD大腦中神經(jīng)突觸(腦中神經(jīng)元之間進行信息傳遞和處理的最小單元)的功能障礙是造成認知缺陷的原因,其發(fā)生遠早于腦中神經(jīng)元死亡和臨床癥狀[淀粉蛋白沉積(amyloid plaques)和神經(jīng)纖維纏結(jié)(neurofibrillary tangles)]的出現(xiàn)。淀粉蛋白沉積假說(Aβ假說)的主要提出者Dennis J.Selkoe教授早在2002年就以“Alzheimer’s disease is a synaptic failure”為題在Science撰文提出了“AD的致病主要原因是突觸的損傷”的假說[2],該假說被本領(lǐng)域的大量后續(xù)工作所證實[3-6]。張晨教授團隊長期致力于探索AD病理情況下大腦神經(jīng)突觸功能的早期失常機制,從單細胞分辨率水平的神經(jīng)網(wǎng)絡(luò)視角對AD的病理機制做出了創(chuàng)新性工作,簡述如下:(1)發(fā)現(xiàn)神經(jīng)信號的短時程可塑性失常是AD的早期病理事件,結(jié)合早老素(presenilin)基因修飾動物發(fā)現(xiàn)短時程可塑性的分子機制是細胞內(nèi)鈣庫Ryanodine受體缺失[7-8];(2)為實現(xiàn)單細胞分辨率水平的神經(jīng)網(wǎng)絡(luò)機制研究,開發(fā)了基于雙光子研究AD動物清醒狀態(tài)下短時程記憶的技術(shù)平臺、基于機器學習的自動圖像分析方法和用于在體記錄的新型熒光記錄電極等新技術(shù),發(fā)現(xiàn)前額葉神經(jīng)網(wǎng)絡(luò)無法編碼短時記憶是AD的極早期病理事件,該病變早于可塑性失常[9-14]。(3)通過大規(guī)模篩選發(fā)現(xiàn)了數(shù)個特異性調(diào)控神經(jīng)信號傳遞(突觸數(shù)量和受體)的新分子(ABHD6、PTPRO等),為AD的極早期干預(yù)提供了新靶點[15-21]。主要學術(shù)成績和創(chuàng)新成果詳述如下。
2.1 發(fā)現(xiàn)前額葉神經(jīng)網(wǎng)絡(luò)無法編碼短時記憶是AD的極早期病理事件
當前本領(lǐng)域內(nèi)公認AD致病的主要原因是突觸的損傷,張晨教授前期工作發(fā)現(xiàn) AD 相關(guān)基因PS1的表達產(chǎn)物早老素的作用環(huán)節(jié)是興奮性突觸前的鈣庫 Ryanodine 受體介導的突觸短時程可塑性,暗示AD大腦中的單個突觸的傳遞失衡是早于神經(jīng)元死亡的大腦變化[7-8],這些成果在Faculty of 1000、Science Signaling 等權(quán)威學術(shù)平臺上被眾多科學家多次正面評價。由于 AD 迄今為止并沒有成功的治療和干預(yù)策略,兼之成年后神經(jīng)再生的潛能非常低,因此如何尋找疾病早期大腦變化的特征已經(jīng)成為一個非常重要的基礎(chǔ)和臨床科學問題。運用成像手段對于大腦網(wǎng)絡(luò)進行觀察被認為是尋找AD大腦早期變化的一個重要手段,以往的研究重點集中在幾百微米尺度上的大腦核團之間的相互連接特性,缺少在單細胞分辨率下對AD腦變化的研究工作,這主要是受制于缺乏合適的研究工具。
張晨教授團隊近5年來搭建了基于清醒動物的應(yīng)用雙光子在體成像技術(shù)分析AD大腦神經(jīng)微環(huán)路功能的先進技術(shù)平臺,針對海量的圖像數(shù)據(jù)建立了基于遺傳算法和機器學習的自動圖像分析方法,大幅提高了分析海量雙光子成像數(shù)據(jù)的效率、準確性和可靠性[10](圖2),其中對圖像分析算法中使用的遺傳算法的魯棒性和人工神經(jīng)網(wǎng)絡(luò)的容錯性進行了系統(tǒng)的描述,基于腦神經(jīng)網(wǎng)絡(luò)的特性建立了強容錯性人工神經(jīng)網(wǎng)絡(luò)[12];開發(fā)了可用于在體成像和記錄的熒光玻璃電極,將高分子材料Parylene-C鍍在電生理記錄玻璃電極上,經(jīng)特殊工藝,使其產(chǎn)生足夠的熒光強度,推進了在體電生理記錄的可視化[11](圖3)。應(yīng)用這些工具,張晨教授團隊發(fā)現(xiàn)小鼠mPFC、V1、SSC等神經(jīng)環(huán)路在信息處理過程中存在遠高于隨機模型的高階相關(guān)性,AD動物模型的mPFC神經(jīng)微環(huán)路中神經(jīng)元之間的功能連接強度顯著弱于野生型動物模型,且在AD 動物尚未出現(xiàn)突觸電生理指標異常時發(fā)生短時記憶的原位處理能力障礙[9](圖4),為長期有效改善AD癥狀和防治提供了新的線索。
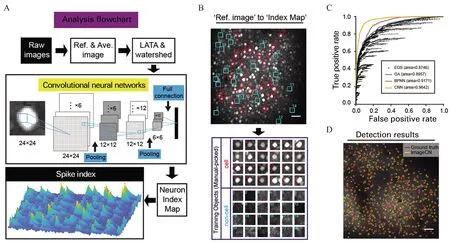
圖2 基于深度學習的雙光子成像數(shù)據(jù)分析方法
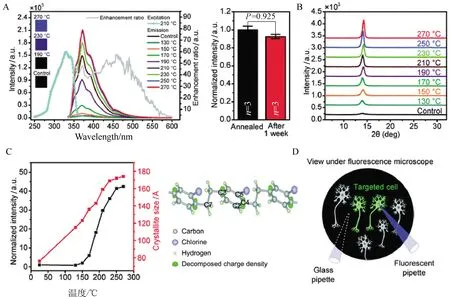
圖3 可用于電生理記錄的熒光玻璃電極的簡單制造工藝
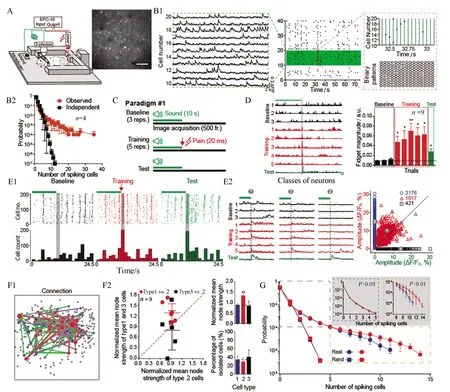
圖4 基于類短時程記憶訓練模式下mPFC神經(jīng)網(wǎng)絡(luò)分析
張晨教授團隊建立的基于遺傳算法的人工神經(jīng)網(wǎng)絡(luò)容錯性分析方法被法國的Bernard Girau教授和IEEE資深成員Cesar torres-huitzil在權(quán)威雜志IEEEAccess的綜述中進行了正面的評價,認為該方法在神經(jīng)網(wǎng)絡(luò)分析上具有泛化能力;關(guān)于熒光電極制造工藝的工作被評為LabonaChip雜志當期的封面文章;研發(fā)的超小型顯微鏡—μScope于2013年獲得北京大學第七屆實驗技術(shù)成果獎(一等獎);2018 年關(guān)于神經(jīng)微環(huán)路失常導致阿爾茨海默癥的研究成果被CellReports作為當期的推薦論文,在其官網(wǎng)首頁滾動展示。
2.2 針對AD的極早期干預(yù),以突觸數(shù)量和突觸受體為指標,篩選出多個調(diào)控突觸功能的新分子,為防治和有效改善AD癥狀提供了新靶點
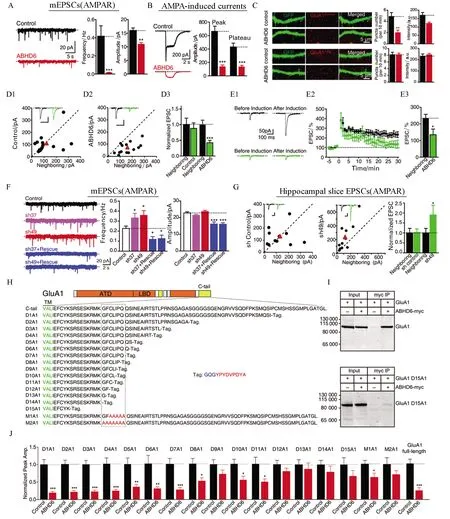
圖5 ABHD6負調(diào)控AMPA受體介導的突觸傳遞
基于領(lǐng)域內(nèi)已有的大量研究,突觸功能失調(diào)被證明是AD早期的主要事件之一,但是以往AD的干預(yù)治療均主要以Aβ假說為基礎(chǔ)(迄今為止基于Aβ假說的藥物研發(fā)均未有成功的案例),因此通過突觸調(diào)控改善AD癥狀的可能性越來越得到領(lǐng)域內(nèi)科學家的重視。張晨教授團隊在調(diào)控突觸數(shù)量和突觸受體領(lǐng)域做出了系統(tǒng)性的工作。在前期工作中發(fā)現(xiàn)了δ-阿片受體(delta opioid receptor, DOR)激活導致的阿片受體上膜過程是與興奮性神經(jīng)肽的釋放過程相偶[21];突觸特異分子neurexin 的表達量與抑制性突觸傳遞效率成反比[19]。張晨教授團隊近年來通過功能篩選發(fā)現(xiàn)了一個新的突觸后AMPA受體相互作用蛋白ABHD6。目前已知的大部分AMPA受體調(diào)節(jié)亞基均是正向調(diào)節(jié)AMPA受體的功能,而張晨教授團隊發(fā)現(xiàn)的ABHD6是一種AMPA受體負向調(diào)控分子,它可以直接與AMPA受體C端相互作用,通過不依賴其水解酶活性的方式降低AMPA受體的膜轉(zhuǎn)運和AMPA受體介導的興奮性的突觸傳遞[22-24];張晨教授團隊通過建立人工突觸形成體系,運用全基因組篩選發(fā)現(xiàn)新的突觸黏附分子PTPRO正向調(diào)控興奮性突觸的數(shù)目,并發(fā)現(xiàn)這種促突觸生成作用是通過其胞外段結(jié)構(gòu)域介導的,從而實現(xiàn)突觸傳遞效率的正向調(diào)控[16](圖6)。張晨教授團隊關(guān)于ABHD6的工作發(fā)表后被國際同行引用并肯定了其對調(diào)節(jié)突觸后AMPA受體轉(zhuǎn)運和功能的重要性,領(lǐng)域內(nèi)的兩位權(quán)威專家瑞士巴塞爾大學Bernhard Bettler教授和德國弗萊堡大學的Bernd Fakler教授在經(jīng)典綜述雜志CurrentOpinioninNeurobiology上對該工作進行了正面的評價,并在整個研究領(lǐng)域已知重要蛋白的模式圖中加上候選人新發(fā)現(xiàn)的蛋白ABHD6。團隊關(guān)于PTPRO的工作發(fā)表于神經(jīng)科學領(lǐng)域權(quán)威雜志美國神經(jīng)科學會會刊JournalofNeuroscience,并被選為當期的 Featured article。
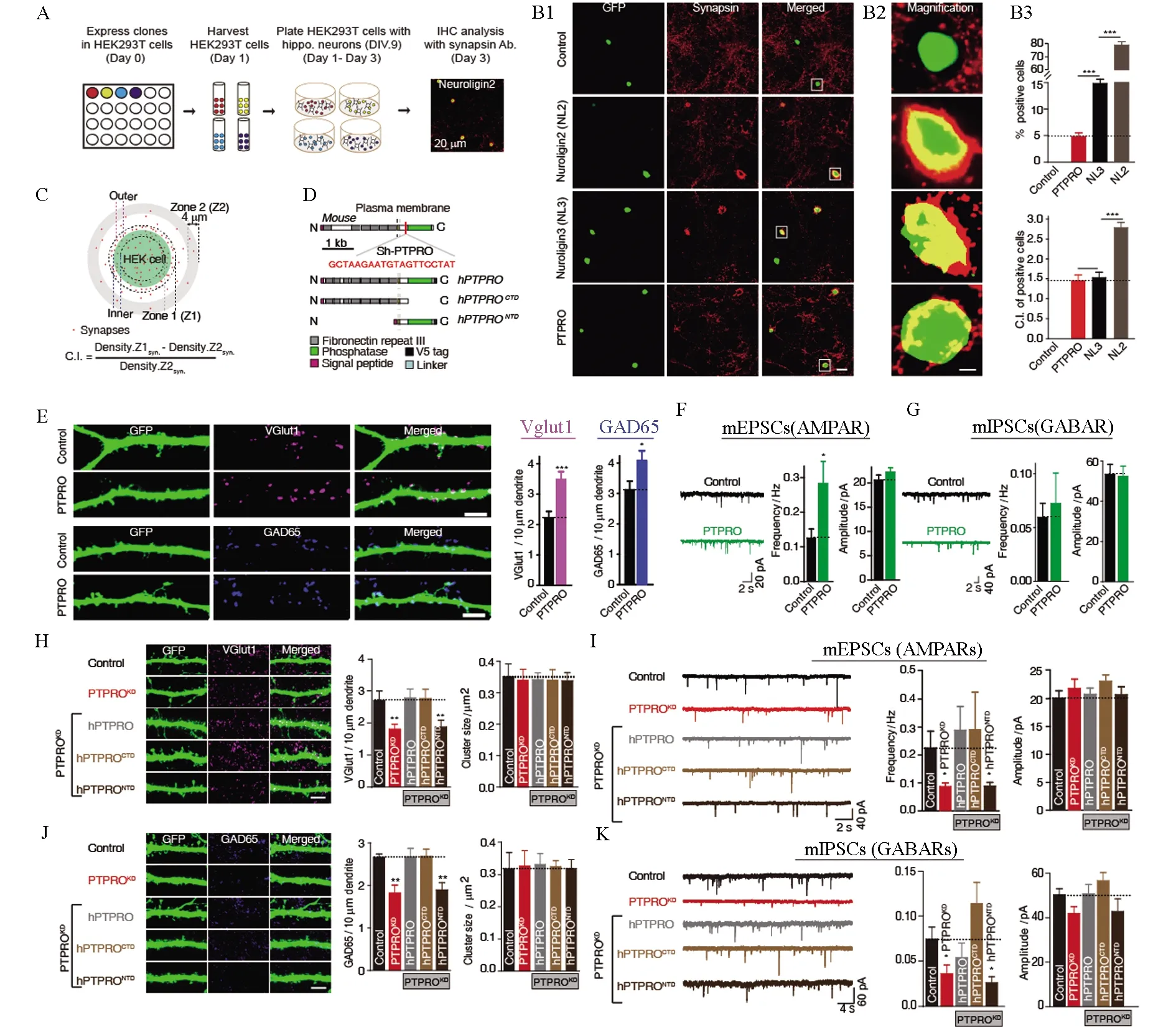
圖6 PTPRO是可以促進突觸形成的突觸黏附分子

