棉花GhPDP基因原核表達條件的優化
劉 東,蘭艷平,張 麗,趙 巖,渠云芳,黃晉玲
(山西農業大學 農學院,山西 太谷 030801)
植物細胞質雄性不育是高等植物中不能產生有功能花粉的一種母性遺傳性狀,是雄蕊退化、花粉敗育或功能不育等原因造成的雄蕊不能正常授粉而雌蕊功能正常的現象。利用雄性不育系育種是作物雜種優勢利用的重要途徑。
Capitani等[1]研究發現,植株的雄性不育系花藥在發育過程中,有氧呼吸途徑相關酶的活性普遍降低,認為植物雄性不育花藥敗育過程與能量代謝異常密切相關。關于能量代謝異常導致作物雄性不育在玉米、水稻、小麥等作物上均有研究報道。大量研究已表明,植物雄性不育的發生與植物體內能量的代謝異常有一定的相關性[2-4]。
在生物體的正常代謝過程中,線粒體通過呼吸作用,為植物體的正常發育提供能量。研究表明,在雄性不育花藥中以呼吸底物降解的糖酵解-三羧酸循環(TCA)途徑為主[5]。線粒體中的糖經過糖酵解途徑形成丙酮酸,丙酮酸再轉化為乙酰輔酶A進入三羧酸循環進行能量代謝,丙酮酸脫氫酶起到關鍵作用,其可以將丙酮酸脫羧氧化成乙酰輔酶A,進而影響三羧酸循環。丙酮酸脫氫酶磷酸酶(Pyruvate dehydrogenase phosphatase,PDP)屬于蛋白磷酸酶M家族(Protein phosphatase M,PPM),是位于線粒體上的絲氨酸/蘇氨酸磷酸酶,是丙酮酸脫氫酶活性的正調控因子,在線粒體中通過水解PDC-E1α亞基絲氨酸上的磷酸基團而恢復PDC活性,以保證代謝的正常進行。通過對棉花雄性不育系的丙酮酸脫氫酶磷酸酶的研究,可以揭示CMS機制,為更好地利用雜種優勢提供可靠的理論依據和實踐意義。
山西農業大學農學院棉花育種實驗室前期已從棉花晉A不育系中克隆出GhPDP基因,并成功將其構建到pMD-19T載體上[6]。本研究以pMD-19T-GhPDP質粒為模板,PCR擴增GhPDP基因的cDNA編碼區,構建原核表達載體pET-22b-GhPDP,誘導重組蛋白表達,并對表達條件進行單因素和正交試驗優化,以提高GhPDP可溶性表達量,為進一步研究GhPDP在棉花雄性不育過程中能量調控方面的功能提供理論基礎。
1 材料和方法
1.1 試驗材料
1.1.1 菌株與質粒 大腸桿菌Trans1-T1、Transetta(DE3)均購自北京全式金生物技術有限公司;原核表達載體pET-22b、pMD-19T-GhPDP重組質粒均由山西農業大學農學院棉花育種實驗室保存。
1.1.2 主要試劑 膠回收試劑盒購自OMEGA公司;質粒提取試劑盒購自北京全式金生物技術有限公司;引物由蘇州金唯智公司合成;甘氨酸、SDS、異丙基硫代半乳糖苷(IPTG)、丙烯酰胺、甲叉丙烯酰胺、TEMED購自美國Amresco公司;2×Pfu PCR MasterMix購自天根生化科技(北京)有限公司;PrimeSTAR GXL DNA Polymerase購自TaKaRa公司;Tris購自北京索萊寶科技有限公司。
1.2 試驗方法
1.2.1 重組表達載體的構建與鑒定 通過Over-lap PCR將目的基因GhPDP連接到pET-22b載體上,引物序列列于表1。使用PDP-F1/R1和PDP-F2/R2分別擴增基因和載體,擴增產物經1%的瓊脂糖凝膠電泳檢測并回收;將回收的基因片段和載體片段按摩爾比1∶1進行PCR擴增,用瓊脂糖凝膠電泳檢測其結果。

表1 PCR擴增引物序列Tab.1 PCR primer sequences
將PCR產物轉化Trans1-T1感受態細胞,篩選陽性克隆送至蘇州金唯智公司進行測序,并提取其質粒轉化大腸桿菌Transetta(DE3)。
1.2.2 GhPDP蛋白表達條件的優化 為獲得較多可溶性目的蛋白,設計單因素試驗和正交試驗對目的蛋白進行優化表達,并采用Bradford方法[7]進行蛋白定量,即不同誘導溫度、時間、IPTG終濃度和菌體密度OD600對目的蛋白表達量的影響。
1.2.2.1 誘導溫度 將轉化菌株接種于含Amp的LB液體培養基中,37 ℃過夜培養,第2天轉接至新的培養基中,繼續培養至OD600為0.8時加入IPTG至終濃度為0.1 mmol/L,分別在16,20,24 ℃誘導5 h后離心收集菌體,超聲波破碎菌體,收集上清與沉淀,加入4×蛋白上樣緩沖液,沸水浴10 min,離心后經13% SDS-PAGE鑒定。
1.2.2.2 誘導時間 細菌培養方法同1.2.2.1,培養至OD600為0.8時加入IPTG至終濃度為0.1 mmol/L,在20 ℃分別培養3,5,7,10 h后收集菌體,超聲波破碎菌體,收集上清與沉淀,經13% SDS-PAGE電泳。
1.2.2.3 IPTG終濃度 細菌培養方法同1.2.2.1,培養至OD600為0.8,分別加入終濃度為0.05,0.10,0.15 mmol/L的IPTG,在20 ℃誘導5 h后收集菌體,超聲波破碎菌體,收集上清與沉淀,經13% SDS-PAGE電泳。
1.2.2.4 菌體密度OD600細菌培養方法同1.2.2.1,繼續培養至OD600分別為0.5,0.8,1.0時,加入IPTG至終濃度為0.10 mmol/L,20 ℃誘導5 h,菌體經超聲波破碎、離心,收集上清與沉淀,經13% SDS-PAGE電泳。
1.2.2.5 正交試驗設計 在單因素試驗的基礎上設計4因素3水平的正交試驗,具體組合列于表2。

表2 正交試驗設計Tab.2 Orthogonal experiment design
1.2.2.6 正交試驗數據分析 按照已設計的正交試驗進行目的蛋白的誘導表達,經13% SDS-PAGE電泳,電泳結果經GeneTools凝膠分析軟件進行目的蛋白定量,得出最佳誘導條件。
2 結果與分析
2.1 重組表達載體的鑒定
GhPDP基因與pET-22b載體擴增后經1%瓊脂糖凝膠電泳檢測,結果如圖1所示,擴增的基因片段和載體片段大小分別約為1 152,5 493 bp,與預期的理論大小相符,沒有非特異擴增存在。將2個片段切膠回收按摩爾比1∶1進行GhPDP基因與pET-22b載體的連接,結果如圖2所示,重組表達載體以多聚體的形式產生,同時因分子量過大而積存于瓊脂糖凝膠的上樣孔中。將多聚體通過熱激轉化Trans1-T1感受態細胞,挑取單克隆進行菌液PCR驗證,結果擴增出與理論基因大小相符合的片段(圖3)。將陽性克隆測序,通過DNAMAN序列比對結果正確,表明pET-22b-GhPDP重組表達載體構建成功。
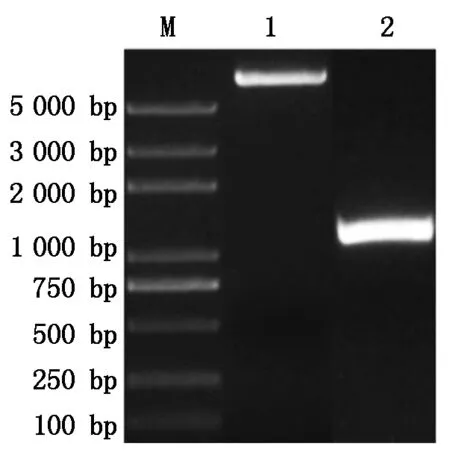
M. Trans2K Plus DNA Marker;1. pET-22b載體 的擴增結果;2. GhPDP基因的擴增結果。 M. Trans2K Plus DNA Marker; 1. Amplification results of pET-22b vector; 2. Amplification results of GhPDP gene.
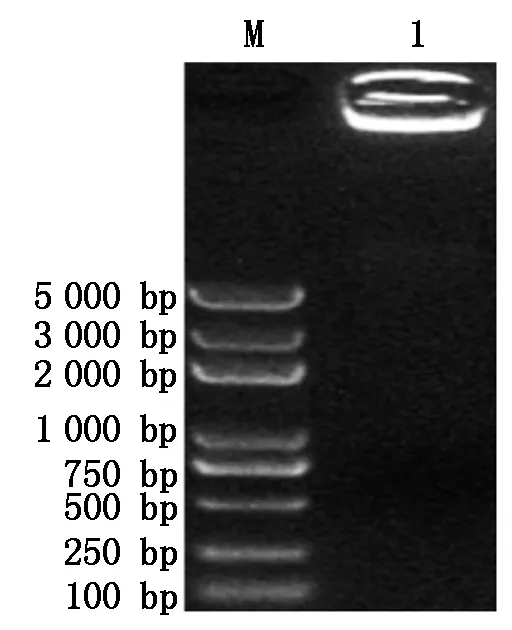
M. Trans2K Plus DNA Marker;1. 多聚體。 M. Trans2K Plus DNA Marker; 1. Multimer.
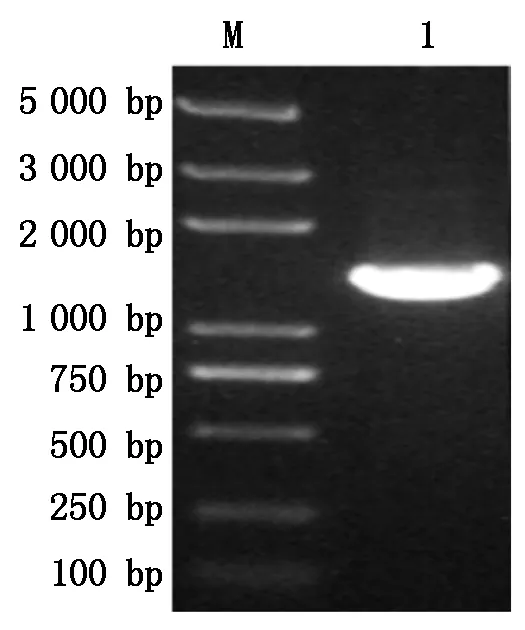
M. Trans2K Plus DNA Marker;1. PCR驗證結果。 M. Trans2K Plus DNA Marker; 1. PCR verification results.
2.2 目的蛋白表達形式的確定
將含重組質粒pET-22b-GhPDP的Transetta(DE3)接種在具有Amp抗性的LB液體培養基中,通過IPTG誘導表達以及13%的SDS-PAGE檢測,結果顯示,與空載轉化菌相比,在48 ku處有一條特異的蛋白表達條帶,分子量與預期目的蛋白大小相當,表明目的蛋白在Transetta(DE3)中表達,其中,大部分以包涵體的形式存在于沉淀中,很少一部分形成可溶性蛋白(圖4)。

M.蛋白質分子量標準;1.空載表達后的上清;2.重組蛋白在Transetta(DE3)中表達后的上清;3.空載表達后的沉淀;4.重組蛋白在Transetta(DE3)中表達后的沉淀。
2.3 重組蛋白表達條件優化
2.3.1 不同誘導溫度對目的蛋白表達量的影響 在OD600為0.8,IPTG終濃度為0.10 mmol/L以及誘導溫度分別為16,20,24 ℃條件下,誘導5 h離心收集菌體進行超聲波破碎,獲得上清與沉淀,經13%的SDS-PAGE檢測,結果顯示,隨著溫度的升高,可溶性目的蛋白的表達量呈先增加后降低的趨勢;在誘導溫度為20 ℃的條件下,GhPDP蛋白的可溶性表達量最高(圖5),通過GeneTools凝膠分析軟件測定,其占上清總蛋白含量的6.98%。

M.蛋白質分子量標準; 1. pET-22b-GhPDP未誘導;2-4. 16,20,24 ℃條件下IPTG誘導5 h后的上清;5-7. 16,20,24 ℃條件下IPTG誘導5 h后的沉淀。
2.3.2 不同誘導時間對目的蛋白表達量的影響 在OD600為0.8、誘導溫度為20 ℃、IPTG終濃度為0.10 mmol/L條件下,分別誘導3,5,7,10 h進行超聲波破碎,經13% SDS-PAGE檢測,結果顯示,誘導5 h時,目的蛋白可溶性表達量最高(圖6),其占上清總蛋白含量的6.65%。
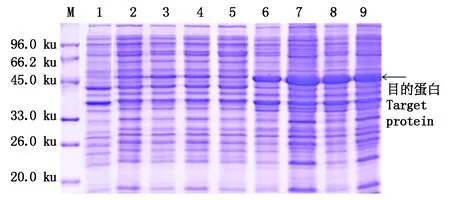
M.蛋白質分子量標準;1. pET-22b-GhPDP未誘導;2-5. 20 ℃條件下IPTG的誘導3,5,7,10 h后的上清;6-9. 20 ℃條件下IPTG分別誘導3,5,7,10 h后的沉淀。
2.3.3 不同IPTG終濃度對目的蛋白表達量的影響 在OD600為0.8、誘導溫度為20 ℃條件下,分別加入IPTG至終濃度為0.05,0.10,0.15 mmol/L,誘導5 h,離心收集菌體沉淀進行超聲波破碎,取上清與沉淀進行13%的SDS-PAGE檢測,結果如圖7所示,在IPTG終濃度為0.10 mmol/L時,可溶性目的蛋白表達量最高,其占上清總蛋白含量的7.30%。
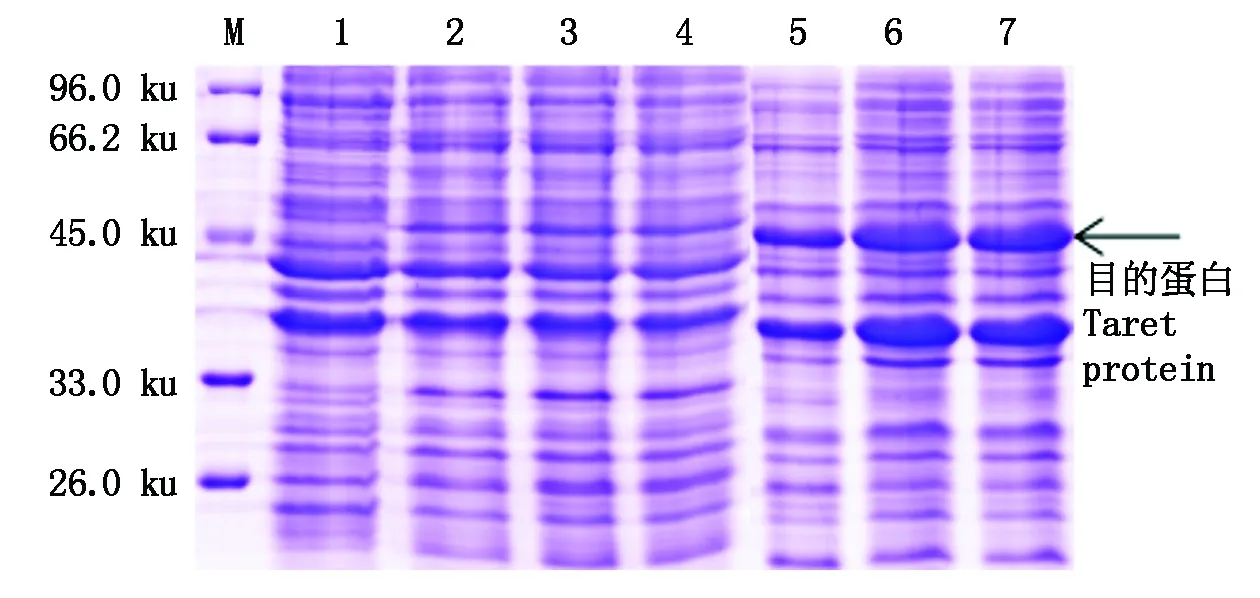
M.蛋白質分子量標準; 1. pET-22b-GhPDP未誘導;2-4. 20 ℃條件下終濃度分別為0.05,0.10,0.15 mmol/L IPTG誘導5 h后的上清;5-7. 20 ℃條件下終濃度分別為0.05,0.10,0.15 mmol/L的IPTG誘導5 h后的沉淀。
2.3.4 不同菌體密度OD600對目的蛋白表達量的影響 分別在菌體密度OD600為0.5,0.8,1.0時,加入0.10 mmol/L的IPTG,20 ℃誘導5 h,取上清與沉淀進行SDS-PAGE檢測,結果顯示,隨著菌體密度逐漸增加,可溶性目的蛋白表達量呈現先增加后降低的趨勢(圖8);當OD600達到0.8時,IPTG誘導產生的可溶性目的蛋白含量最多,其占上清總蛋白含量的8.65%。
綜合以上單因素試驗可知,可溶性目的蛋白表達的最優條件為:在20 ℃條件下,當菌體密度OD600達到0.8時,加入終濃度0.10 mmol/L的IPTG誘導5 h。在此誘導條件下,可溶性目的蛋白表達量最高。
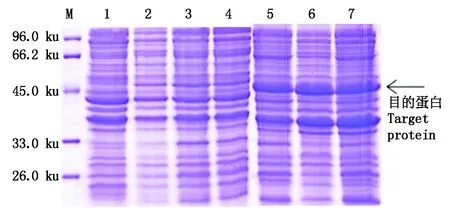
M.蛋白質分子量標準; 1. pET-22b-GhPDP未誘導;2-4. 分別在OD600為0.5,0.8,1.0開始誘導5 h后的上清;5-7. 分別在OD600為0.5,0.8,1.0開始誘導5 h后的沉淀。
2.3.5 GhPDP蛋白誘導優化條件正交試驗 按照已設計的正交試驗(表2)進行目的蛋白誘導表達,經13% SDS-PAGE電泳(圖9),可以清晰地看出,GhPDP基因在不同條件下的表達量有明顯的差異。在上清的SDS-PAGE結果中發現泳道5的目的蛋白表達量最高。
2.3.6 正交試驗數據分析 通過GeneTools凝膠分析軟件定量可溶性目的蛋白濃度,對各因素數據進行極差分析,結果如表3所示,各因素極差大小分別為3.44,2.76,3.21,1.73,通過R值確定誘導條件的各因素影響主次為誘導溫度>IPTG終濃度>誘導時間>OD600,正交試驗最佳組合是,誘導溫度為20 ℃、誘導劑IPTG終濃度為0.15 mmol/L、誘導時間為5 h、菌體密度OD600為0.5,在此誘導條件下,可溶性目的蛋白表達量最大,達到8.96%。為進一步驗證上述結果的可靠性和穩定性,按正交設計優化的最佳條件重復進行了3次誘導,結果發現,目的蛋白表達量均穩定地占上清總蛋白含量的8.96%左右。
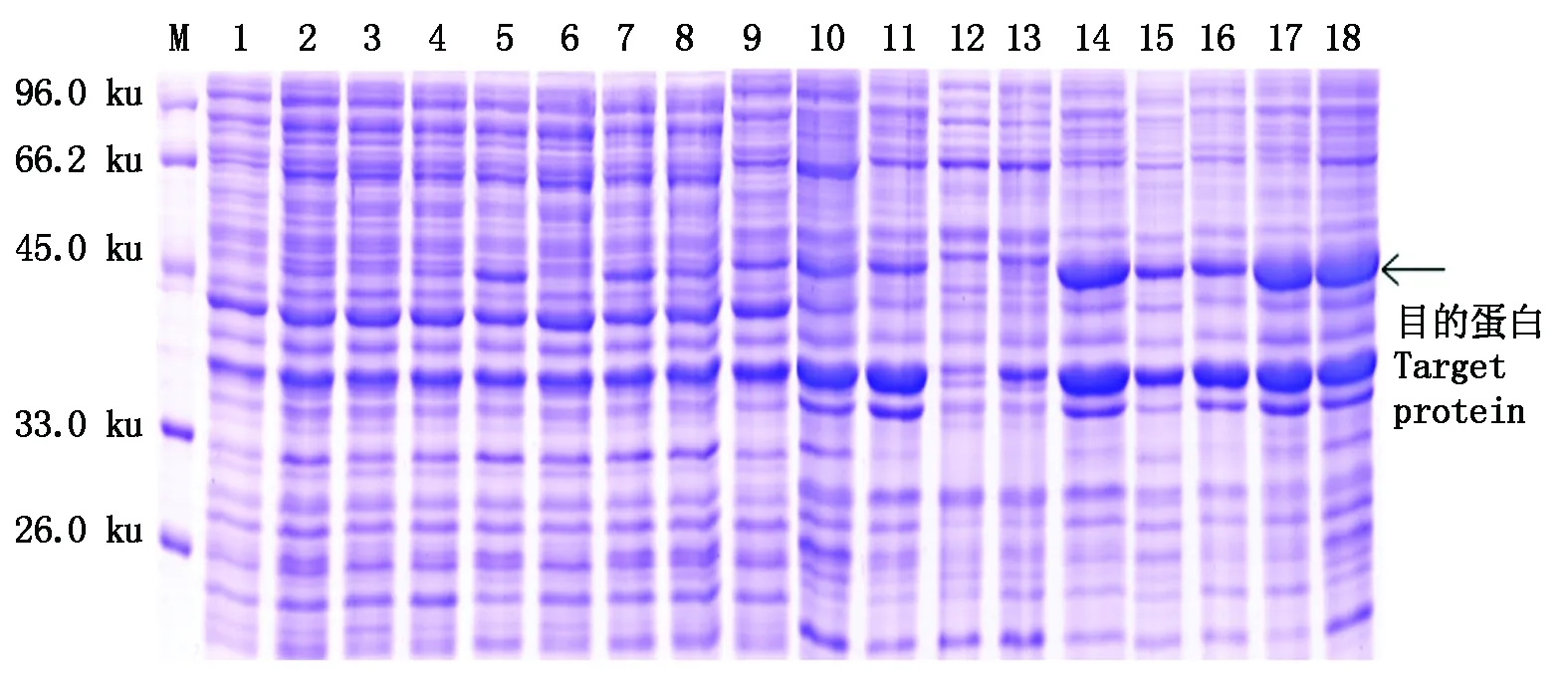
M.蛋白質分子量標準; 1-9. 對應表3各正交試驗組的上清; 10-18. 對應表3各正交試驗組的沉淀。 M. Protein molecular weight standard; 1-9. Corresponding to the supernatant of each orthogonal experimental group of Tab.3; 10-18. Corresponding to the precipitation of each orthogonal experimental group of Tab.3.
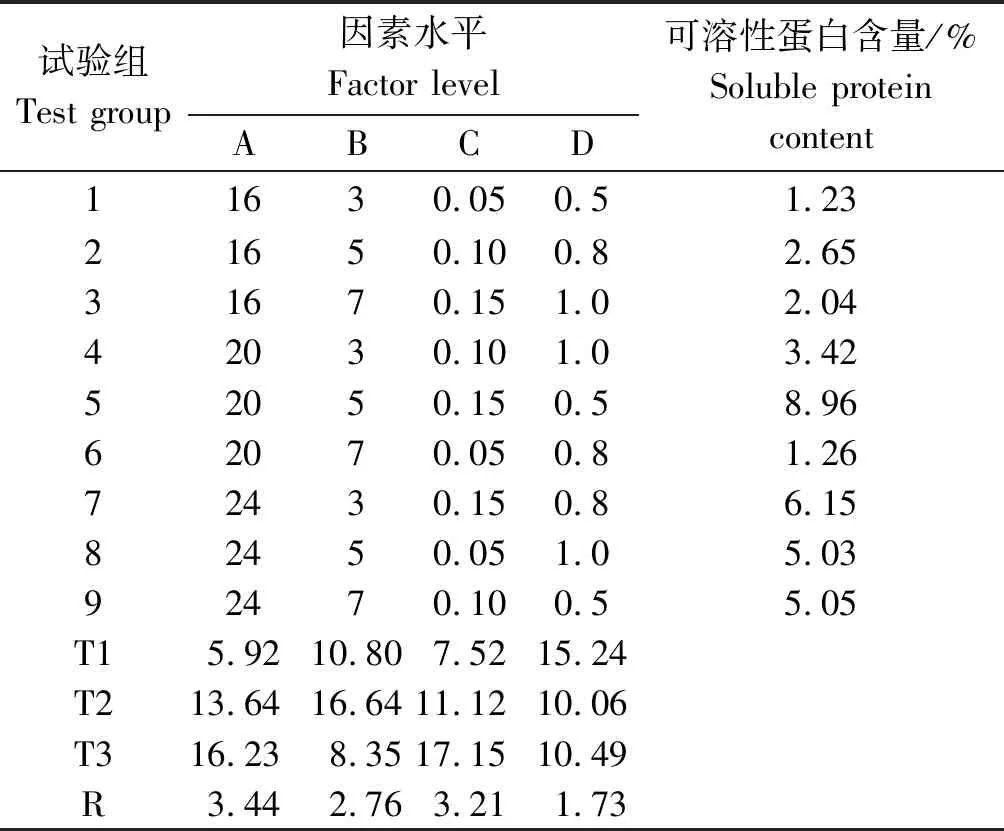
表3 正交試驗設計及其結果Tab.3 Design table and results of orthogonal test
3 結論與討論
植物雄性不育的研究是雜種優勢利用理論研究的重要內容,大量研究證明,能量代謝失衡與植物雄性不育存在一定關系[1],而線粒體是為機體提供能量的動力工廠。細胞存亡與物質能量代謝調節契合于丙酮酸,糖類經過初步酵解后形成丙酮酸,丙酮酸被運輸到線粒體內經過氧化脫羧形成乙酰輔酶A進入三羧酸循環(TCA),最后經過氧化磷酸化形成大量的ATP。線粒體丙酮酸脫氫酶復合體(mtPDC)調控丙酮酸進入TCA循環并且催化的反應不可逆,2種調節酶PDK/PDP通過對PDC-E1a亞基的磷酸化和去磷酸化使PDC失活或復活,PDP作為PDC的調控酶,對能量代謝具有極其重要的作用。
3.1 GhPDP原核表達載體的構建與表達
許多外源蛋白表達主要以無活性、不溶性的包涵體形式產生[8]。其中,包涵體的形成原因很多,外源基因的快速高效表達是其中的原因之一[9]。外源基因在大腸桿菌中能否高效表達受很多因素影響,如大腸桿菌菌株、誘導溫度、誘導劑IPTG的終濃度和誘導時間[10]。潘濱等[11]在大腸桿菌Rosetta(DE3)、BL21(DE3) pLysS和Rs21菌株誘導Rep蛋白表達,研究發現當選用表達菌株BL21(DE3) pLysS和Rs21菌株時,Rep蛋白表達量很低;當選用表達菌株Rosetta(DE3)時,Rep蛋白表達明顯,且在IPTG誘導后表達量顯著增加。
本試驗采用目前廣泛應用的大腸桿菌表達系統表達外源蛋白棉花丙酮酸脫氫酶磷酸酶GhPDP,選用表達載體為pET-22b,其能夠編碼6個組氨酸殘基、并與目的蛋白的C末端形成融合蛋白,可以直接用于后續目的蛋白的純化[12-14],且由于組氨酸標簽非常小,對目的蛋白的結構和性質造成影響較小,因此,不需要將其從目的蛋白中切除;pET-22b表達載體上的T7啟動子在加入誘導劑IPTG時能與大腸桿菌Transetta(DE3)菌株內的T7 RNA聚合酶特異性結合,從而實現下游靶基因的表達。本試驗成功構建pET-22b-GhPDP重組表達載體,并在大腸桿菌Transetta(DE3)內表達,表達形式多為包涵體,少量為可溶性蛋白。
3.2 誘導溫度對目的蛋白表達量的影響
誘導溫度是影響原核蛋白表達的重要因素之一[15]。高溫誘導時,大腸桿菌的生長速度快,表達蛋白的速度也隨之加快,導致表達的目的蛋白沒有足夠的時間進行正確的折疊,從而容易形成包涵體。因此,降低溫度有利于目的蛋白的可溶性表達。本試驗中,目的蛋白在16,20,24 ℃表達時均有包涵體形成,但在20 ℃時目的蛋白可溶性表達量最高。
3.3 IPTG濃度對目的蛋白表達量的影響
IPTG終濃度對大腸桿菌生長和蛋白表達也有一定的影響[16],IPTG 是一種十分有效的乳糖操縱子的誘導劑,合理的濃度可提高表達量,在縮短表達周期的同時可降低成本;而濃度過高會增加原核表達系統的負載,抑制細菌的生長,甚至對細胞具有一定的殺傷作用[17]。因此,本試驗采用低終濃度的IPTG進行誘導,當IPTG終濃度為0.10 mmol/L時,誘導的可溶性目的蛋白相對較多。
3.4 誘導時間對目的蛋白表達量的影響
不同的蛋白誘導時間也不同,有些蛋白對細胞有毒害作用[18-20]。因此,需要對誘導時間進行優化。在本試驗中,隨著誘導時間的增加,目的蛋白的可溶性表達量呈現先增加后降低的趨勢;在5 h時可溶性蛋白表達相對較多,5 h后達重組菌的生長平衡期,此時融合蛋白的表達量已無明顯增加;若繼續培養可則能會由于菌體老化分解導致表達量反而下降。
3.5 菌體密度OD600對目的蛋白表達量的影響
原核表達中誘導時機也很重要,誘導時機過早會導致目的蛋白產量降低;而誘導時機過晚會影響工程菌的穩定性和活性,進而影響目的蛋白的表達量。在本試驗中,隨著菌體密度逐漸增加,可溶性目的蛋白的量呈現先增加后降低的趨勢,在菌體密度OD600為0.8時,可溶性目的蛋白相對較多,重組菌進入對數生長期初期,重組質粒拷貝數大量擴增,細菌濃度較低,加入 IPTG 誘導后外源營養物質將主要用于融合蛋白表達,而外源蛋白合成將和細菌自身的生長繁殖競爭營養物質,從而抑制重組菌的生長。
3.6 原核表達的最佳誘導條件
正交試驗充分考慮交互作用和全面性,選取部分具有代表性的試驗點,對試驗因素及條件進行優化組合,從而使試驗效率提高[21]。本試驗通過對誘導溫度、誘導時間、IPTG終濃度和菌體濃度OD600進行正交試驗,對其結果分析得出,誘導條件的各因素影響主次為誘導溫度>IPTG終濃度>誘導時間>OD600;綜合所有因素得出誘導最佳條件:菌體密度OD600為0.8、誘導溫度為20 ℃、IPTG終濃度為0.10 mmol/L、誘導時間為5 h,此條件下,可溶性目的蛋白可達8.96%。

