艾迪注射液聯合GC方案治療中晚期非小細胞肺癌療效及安全性研究
馬艷華, 王文尖
(三亞中心醫院,海南三亞 572000)
隨著環境污染加劇及現代社會生活方式改變,肺癌發生的概率正呈逐年上升趨勢,近年發病率達61.4/10 萬人,其中非小細胞肺癌占比近80%,5 年生存率僅為14%[1-2]。因發現病情時多數已接近中晚期,臨床上化學治療被作為非小細胞肺癌的常規治療手段[3-4]。以鉑類為基礎的聯合化療方案是目前普遍認同的標準治療方案,GC 方案(吉西他濱+ 鉑類)就是屬于治療該疾病的常用化療方案之一,其療效和安全性與GP 方案(吉西他濱+ 順鉑)基本相當,均可作為中晚期非小細胞肺癌的一線治療方案[5-6]。但化療藥物能抑制患者機體的免疫功能,產生一定的毒副反應并影響患者的生活質量[7]。本研究在GC 方案基礎上聯合中藥復方制劑艾迪注射液對中晚期非小細胞肺癌患者進行治療,獲得了較好的臨床療效,現將研究結果報道如下。
1 對象與方法
1.1研究對象及分組選取2018年6月~2019年12 月在三亞中心醫院腫瘤內科病房或門診接受治療的中晚期非小細胞肺癌患者,共132例。按患者就診先后順序,采用隨機數表將患者隨機分為治療組67例和對照組65例。本研究符合醫學倫理要求并通過醫院倫理委員會的審核批準。
1.2病例選擇標準
1.2.1 納入標準 ①生命體征較好,預計生存時間在3個月以上;②不存在化療禁忌癥且愿意接受化療方案;③存在客觀可測量的瘤實質病灶;④經病理活檢或免疫組化確診為Ⅲb期或Ⅳ期非小細胞肺癌;⑤自愿參加本研究并簽署知情同意書的患者。
1.2.2 排除標準 ①存在嚴重肺系感染等并發癥且需采取其他治療方案干預治療的患者;②合并有嚴重的肝、腎、心、血液系統、神經系統和免疫系統等疾病的患者;③耐受性和依從性較差的患者;④預計生存期短于3個月的患者;⑤因各種原因中途退出研究的患者。
1.3治療方法
1.3.1 對照組 單獨采用GC 方案化療。①卡鉑(齊魯制藥海南有限公司生產,批準文號:國藥準字H20020180),給藥量為15 mg/kg,溶于5%葡萄糖注射液500 mL 中,靜脈滴注,每天1 次,每療程用量不超過35 g。②吉西他濱[南京正大天晴(ZDTQ)有限公司,批準文號:國藥準字H20093403],給藥量為1 000 mg/cm2,溶于0.9%生理鹽水300 mL,靜脈滴注,每周1 次,連續治療3 周后停藥1 周,再繼續按照原劑量治療,28 d為1個療程。
1.3.2 治療組 采用GC 方案聯合艾迪注射液治療。①化療方案與對照組相同。②艾迪注射液(貴州益佰制藥股份有限公司生產,批準文號:國藥準字Z520161521)50 mL,溶于5%葡萄糖注射液250 mL中,靜脈滴注,每日1次。
1.3.3 療程 2 組患者均以28 d 為1 個療程,共治療3個療程。
1.4觀察指標①生活質量評分:采用癌癥患者生命質量測定表(QLQ-C30)評價患者的生活質量,評定項目包括角色功能、身體功能、認知功能、社會功能、情感功能等5項,生活質量與得分成正比[8];②觀察患者的藥物毒副反應情況,包括檢測患者的血常規、肝腎功能和心電圖等;③觀察2組患者治療前后的IgG、IgA、IgM 等免疫球蛋白指標的變化情況。
1.5療效判定標準以實體瘤療效評價標準(RECIST)[9]作為依據,將臨床療效評定為完全緩解(CR)、部分緩解(PR)、穩定(SD)和進展(PD),總有效(RR)= CR + PR,疾病控制(DCR)= CR + PR +SD。
1.6統計方法采用SPSS 21.0統計軟件進行數據的統計處理。計量資料以均數± 標準差(±s)表示,治療前后比較采用配對樣本t檢驗,組間比較采用兩獨立樣本t檢驗;計數資料以率或構成比表示,組間比較采用χ2檢驗。以P<0.05表示差異有統計學意義。
2 結果
2.1 2組患者基線資料比較治療組67 例患者中,男37例,女30例;年齡45~74歲,平均年齡(57.64 ± 5.96)歲;其中Ⅲb 期患者41 例,Ⅳ期患者26 例。 對 照 組65 例 患 者 中, 男35 例, 女31 例;年齡44~73 歲,平均年齡(57.20 ± 6.13)歲;其中Ⅲb期患者38例,Ⅳ期患者17例。2組患者的性別、年齡、腫瘤分期等基線資料比較,差異均無統計學意義(P>0.05),具有可比性。
2.2 2組患者臨床療效比較表1 結果顯示:經3 個療程治療后,治療組的總有效率為40.29%(27/67),對照組為36.92%(24/65),組間比較,差異無統計學意義(χ2= 2.230 8,P>0.05);而治療組的疾病控制率為83.58%(56/67),明顯高于對照組的61.53%(43/65),組間比較,差異有統計學意義(χ2= 6.789 6,P<0.05)。
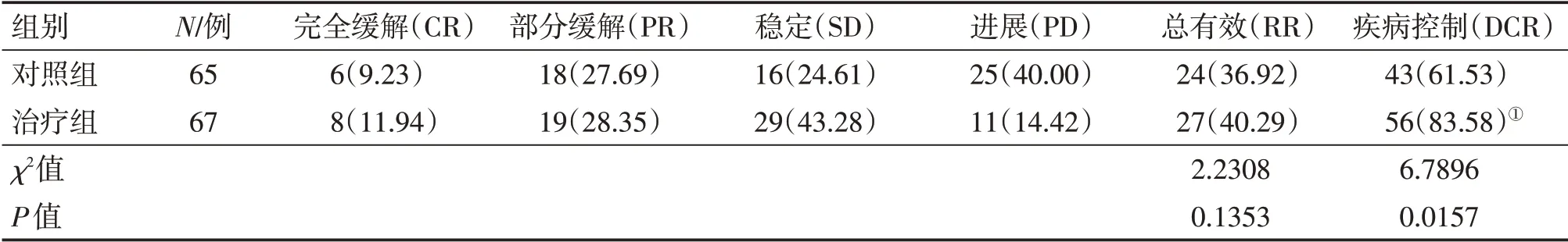
表1 2組中晚期非小細胞肺癌患者臨床療效比較Table 1 Comparison of clinical efficacy of the advanced non-small cell lung cancer patients in the two groups [n/例(p/%)]
2.3 2組患者藥物毒副反應比較表2 結果顯示:治療后,治療組患者的肝功能損害、腎功能損害、惡心嘔吐及白細胞減少發生率均略低于對照組,但組間比較差異均無統計學意義(P>0.05);而血小板減少發生率明顯低于對照組,組間比較,差異有統計學意義(P<0.01)。
2.4 2組患者治療后生活質量評分比較表3結果顯示:治療后,治療組患者的角色功能、身體功能、認知功能、社會功能、情感功能等各項生活質量評分均明顯高于對照組,差異均有統計學意義(P<0.05)。

表2 2組中晚期非小細胞肺癌患者藥物毒副反應發生率比較Table 2 Comparison of the incidence of toxic and side effects in the advanced non-small cell lung cancer patients in the two groups [n/例(p/%)]
表3 2組中晚期非小細胞肺癌患者治療后生活質量評分比較Table 3 Comparison of QOL scores of the advanced non-small cell lung cancer patients in the two groups after treatment ( ± s,s/分)
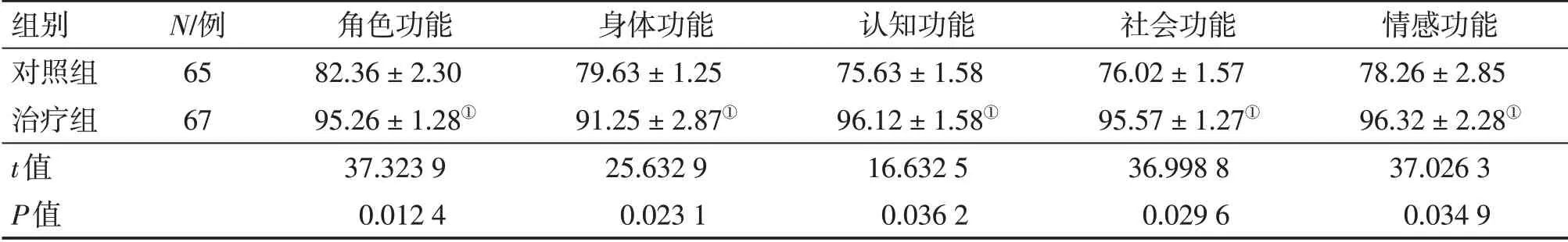
表3 2組中晚期非小細胞肺癌患者治療后生活質量評分比較Table 3 Comparison of QOL scores of the advanced non-small cell lung cancer patients in the two groups after treatment ( ± s,s/分)
①P<0.05,與對照組比較
組別對照組治療組t值P值N/例65 67角色功能82.36 ± 2.30 95.26 ± 1.28①37.323 9 0.012 4身體功能79.63 ± 1.25 91.25 ± 2.87①25.632 9 0.023 1認知功能75.63 ± 1.58 96.12 ± 1.58①16.632 5 0.036 2社會功能76.02 ± 1.57 95.57 ± 1.27①36.998 8 0.029 6情感功能78.26 ± 2.85 96.32 ± 2.28①37.026 3 0.034 9
2.5 2組患者治療前后免疫球蛋白指標比較表4結果顯示:治療前, 2組患者的IgG、IgA、IgM等各項免疫球蛋白指標比較,差異均無統計學意義(P>0.05)。治療后,2組患者的IgG、IgA、IgM 等各項免疫球蛋白指標均較治療前升高(P<0.05),且治療組的升高作用均明顯優于對照組,差異均有統計學意義(P<0.05)。
表4 2組中晚期非小細胞肺癌患者治療前后免疫球蛋白指標比較Table 4 Comparison of immunoglobulin levels of the advanced non-small cell lung cancer patients in the two groups before and after treatment ( ± s)

表4 2組中晚期非小細胞肺癌患者治療前后免疫球蛋白指標比較Table 4 Comparison of immunoglobulin levels of the advanced non-small cell lung cancer patients in the two groups before and after treatment ( ± s)
①P<0.05,與治療前比較;②P <0.05,與對照組治療后比較
組別對照組治療組P值N/例65 67 IgG[ρ/(g·L-1)]治療前11.8 ± 1.0 11.8 ± 0.9>0.05治療后12.3 ± 0.9①14.5 ± 1.0①②<0.05 IgA[ρ/(mg·L-1)]治療前2345 ± 200 2411 ± 230>0.05治療后2600 ± 400①2900 ± 300①②<0.05 IgM[ρ/(mg·L-1)]治療前1210 ± 200 1180 ± 300>0.05治療后1360 ± 200①1550 ± 200①②<0.05
3 討論
近年來,隨著吸煙人群數量的增加以及空氣污染程度的不斷加重,肺癌發病率明顯提高[10-11]。非小細胞肺癌屬于常見肺癌類型的一種,多數患者就診時已處于晚期,通常需要行靶向治療、免疫治療和化療等。GP 方案是臨床實踐當中治療晚期非小細胞肺癌的常用方式,然而不少患者往往難以耐受胃腸道反應等藥物不良反應。而GC方案中卡鉑屬于第2代鉑類廣譜抗癌藥,與順鉑相比具有消化道反應輕而骨髓反應略重的特點[12]。本研究中,治療組的疾病控制率為83.58%,明顯高于對照組的61.53%,差異有統計學意義(P<0.05);且治療組治療后的血小板減少發生率明顯低于對照組,生活質量評分明顯高于對照組,差異均有統計學意義(P<0.05),提示在GC方案基礎上聯合艾迪注射液治療中晚期非小細胞肺癌,有利于進一步提高疾病控制率,減少化療藥毒副反應,改善患者生活質量。
迄今為止,腫瘤化療并輔以其他療法是臨床治療中晚期惡性腫瘤的最常用手段之一,但腫瘤大劑量化療后容易引發骨髓抑制、惡心嘔吐等嚴重不良反應,甚至可能導致化療間隔時間拖延、化療藥用量受限及化療中途停止等情況發生。
艾迪注射液是依據中醫學扶正祛邪的原則進行組方,并采用現代方法制作而成的中藥復方制劑。方中以斑蝥為君藥,黃芪、人參為臣藥,刺五加、甘草為佐藥,諸藥配伍,共奏解毒散結、扶正祛邪之功效。現代藥理研究[13-14]表明,斑蝥的抗癌有效成分為斑蝥素,不僅能抑制腫瘤細胞,而且還能刺激骨髓生成白細胞,對機體有免疫調節作用;而黃芪、人參、刺五加等可提高機體免疫功能,增強機體耐受性,起到扶助正氣之功效。多項研究[15-18]表明,該復方制劑可對腫瘤進行多靶點治療,減少腫瘤細胞DNA 能量代謝與修復,具有毒副作用低、雙向調節免疫功能等優點,因此,在腫瘤防治中發揮著重要作用。
綜上所述,艾迪注射液聯合GC方案協同治療中晚期非小細胞肺癌,能夠提高化療的疾病控制率,提高患者生活質量,用藥的安全性較高,其胃腸道反應和骨髓抑制均較輕,其機制可能與提高機體免疫功能有關,值得臨床進一步深入探究。

