聚氧乙烯基聚合物固態電池的界面研究進展*
劉玉龍 辛明楊 叢麗娜? 謝海明?
(東北師范大學化學學院, 國家地方動力電池聯合工程實驗室, 長春 130024)
聚氧乙烯基聚合物固態電池具有高安全性和高能量密度的特點, 極有可能成為下一代儲能器件. 然而,聚氧乙烯基電解質本身的電化學窗口窄, 極大的限制了其能量密度的進一步提升. 目前適配聚氧乙烯基電解質且長循環穩定的正負極材料較少, 這嚴重阻礙了聚氧乙烯基聚合物固態電池的廣泛應用. 其主要問題在于電極材料與聚氧乙烯聚合物電解質之間的負極界面和正極界面都容易發生副反應, 大大地縮短了電池的循環壽命. 為了抑制這些副反應, 人們采取了相應的策略, 取得了一定的成效. 為充分理解固態電池界面處的變化, 可采用各類先進表征手段對其進行研究, 這將為下一步提高固態電池循環穩定性提供更科學的依據.
1 引 言
聚氧乙烯(polyethylene oxide, PEO)基聚合物固態鋰電池的發展離不開Michel Armand 教授,正是由于他的開拓和長期堅持才使得這個領域取得了長足的進步[1]. 1980 年, 通過使用PEO-LiSO3CF3電解質, 實現了120 ℃高溫下聚合物固態電池的50 次長循環壽命[2]. 隨著鋰鹽、聚合物基體、添加劑和加工工藝的優化, 聚合物固態電池的使用溫度逐漸降低到60 ℃. 然而, 由于PEO 類高分子量聚合物的本征性質(融化溫度大約60 ℃), 聚合物固態電池的使用溫度難以繼續降低[3-4].
PEO 基電解質是眾多聚合物電解質中研究最早和最多的一類材料. 其導電機理是鋰離子與氧化乙烯單元結構上的氧原子不斷發生絡合和解離反應. 由于PEO 的介電常數低, 這就導致PEO 電解質中離子聚集現象嚴重, 鋰離子遷移困難. 為了減少離子聚集現象的發生, 在聚碳酸酯體系聚合物電解質中引進強極性基團從而提高電導率. PEO 基電解質中的離子遷移主要發生在無定型區域, PEO的融化溫度高于60 ℃, 因此其室溫電導率低. 相反, 聚硅氧烷基聚合物的玻璃化溫度低, 室溫下的即可獲得高的離子電導率[5]. 此外, PEO 基電解質的電導率與其分子量密切相關. 1993 年, Shi 和Vincent[6]研究了PEO 電解質電導率隨聚合物分子量的變化, 分子量范圍為0.4 到4000 kg/mol.結果發現PEO 分子量在3200 kg/mol 以下時其離子電導率隨分子量的升高迅速降低, 高于3200 kg/mol 之后變化趨于平穩. Teran 等[7]進一步研究了分子量為0.2 到360 kg/mol 的PEO, 實驗用的聚合物的分散度更低且高分子量的PEO 樣品更多. 結果表明, PEO 電導率隨分子量變化的趨勢曲線與Shi 和Vincent 的研究類似, 電導率呈指數性降低然后穩定在一個平臺.
傳統情況下, 聚合物電解質的電化學窗口一般通過測量線性掃描伏安法來獲得. 最近, Marchiori 等[8]利用第一性原理對聚合物類電解質的電化學穩定窗口進行了理論計算. 先計算聚合物本身的電化學穩定窗口, 然后將聚合物與不同的鋰鹽進行搭配來計算電解質的電化學窗口. 根據他們的計算數據,PEO 本身的最低未占據軌道能量是3.13 eV(相對于標準氫電極, 其氧化電位為3.13 V), 最高占據軌道能量是—5.99 eV(相對于標準氫電極, 其還原電位為5.99 V). 這表明PEO 本身的耐氧化性能較差而對鋰金屬負極的穩定性高(相對于標準氫電極, 鋰還原電位為3.65 V). 當PEO 與不同鋰鹽配合時, 由于氧化過程中聚合物和鋰鹽結構發生重組從而使聚合物提前發生氧化, 這種結果導致電解質的氧化電位進一步降低. 理論計算結果表明, PEO/LiTFSI 體系的氧化電位是3.57 V(相對于鋰金屬),這個結果與大部分的實驗相符. 為了提高PEO 基聚合物電解質的氧化電位, 需要通過引入譬如碳氮三鍵、碳氧雙鍵等基團來提高聚合物本身的氧化電位或者通過添加耐氧化的鋰鹽來抑制其提前分解[8].
目前, PEO 基聚合物電解質的主要挑戰是: 室溫離子電導率低、電化學窗口窄和界面阻抗高[9].為了解決上述難題, 研究者們提出了不同的策略來提高聚合物電解質的性能. 例如, 為了提高聚合物電解質的電導率, 過去數十年中人們采用各種諸如嵌段共聚物、接枝共聚物、交聯共聚物、無機-有機復合、添加劑等策略[10]. 其中, 2005 年報道的納米結構PEO 固態電解質的室溫電導率高達2 × 10—4S/cm, 將其用于LiCoO2/Li 電池中也表現出優異的電化學性能[11]. Tan 等[12]通過在PEO基體中添加多陽離子型離子液體, 增加無定型PEO 比例并促進鋰鹽的解離, 從而提高了電解質的電導率. Liu 等[13]則利用聚間苯二甲酰間苯二胺(PMIA)作為添加劑, 通過PMIA 和PEO/TFSI之間的氫鍵相互作用來增加PEO 的無定型比例并最終提高其離子電導率. 該方法所制備的聚合物可與鋰金屬進行長循環且與LiFePO4正極穩定循環100 圈后保持93%的容量. 為了減少負極界面處鋰枝晶的產生, 人們開發了單離子聚合物電解質和其他高離子遷移數體系的電解質, 從而提高負極界面的穩定性[14,15]. PEO 自身對高電壓氧化的耐受力較差, 在4 V 左右即發生分解, 因此無法匹配高電壓正極材料. 針對該缺點, Zhou 等[16]提出了雙層聚合物電解質的構建, 針對正極和負極分別采用不同特性聚合物, 該思想對今后電解質的開發具有指導意義. Liang 等[17]利用腈類電解質碳氮三鍵的氧化電位高的特點, 將丁二腈與PEO 復合后所制備的固態電解質的電化學窗口提高到4.15 V. 電解質在Li/LiNi0.8Co0.15Al0.05O2(NCA)電池中以1 C倍率循環1000 圈后的容量保持率為66%.
雖然PEO 基聚合物電解質目前存在大量的問題, 但是由于其較高的安全性能仍然受到了廣大電池企業和電動車企業的厚愛[18-20]. 法國Bolloré公司聯合意大利著名汽車設計公司賓尼法利納共同出品的Bluecar, 采用高溫PEO 體系組裝的鋰金屬聚合物電池, 其能量高達30 kWh, 電動車的最高運行速度為120 km/h, 駕駛距離可至250 km,于2011 年正式進入巴黎汽車租賃市場. 隨著人們對高安全性電池的探索, PEO 固態電池的發展也取得了不斷的進步, 尤其是對于高電導率和寬電化學窗口的PEO 基聚合物固態電解質的開發[21]. 對于PEO 基聚合物電解質和正、負極的界面研究,最近也獲得了大量的關注并取得了重要的進展(圖1). 因此, 下面將對PEO 電解質的正負極的界面研究進展展開論述.
2 PEO 基聚合物固態電池的負極界面研究進展
2.1 PEO 基固態電解質與負極界面的反應
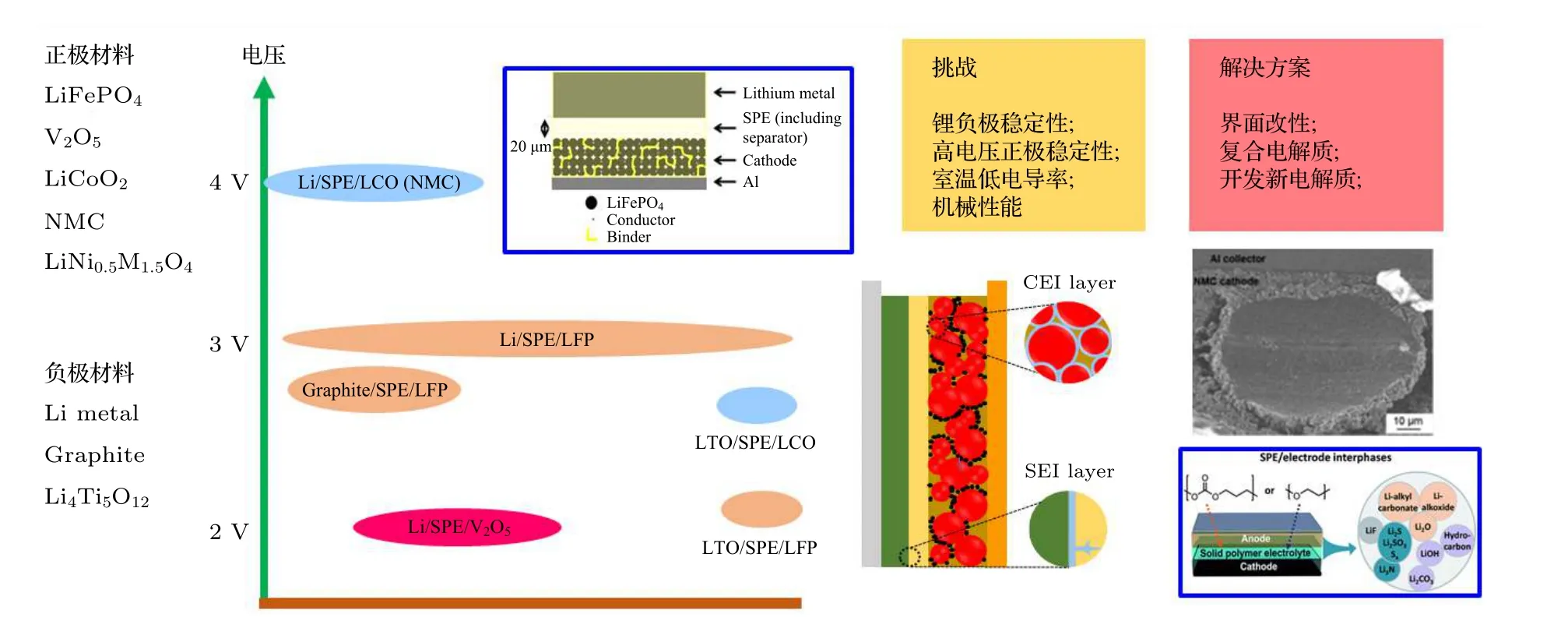
圖1 PEO 基聚合物電解質固態電池發展概況.Fig. 1. Overview of the PEO polymer based solid-state battery.
聚合物固態電解質與鋰金屬的界面反應源于鋰金屬的強還原性和固態電解質成分的分解.Croce 和 Scorati[22]首次報導了PEO 與鋰金屬之間的反應, 通過記錄Li-PEO 之間的界面電阻隨時間的演變, 猜測并證明了鋰金屬表面有一層鈍化膜產生. 然而, 這層鈍化膜的存在對于電池性能起到的作用尚無明確定論. Baudry 等[23]研究發現電池在這層鈍化膜的作用下仍然可以運行300—400 圈.為了進一步證明聚合物與鋰金屬之間的界面反應的狀況, 人們開始組裝鋰/聚合物/鋰對稱電池進行測試. Persi 等[24]利用氧化鋁增強的聚合物電解質,通過對稱電池測試表明界面電阻在隨著時間推移逐漸減少, 60 天以后的界面電阻基本保持穩定, 從而判斷通過復合可以減少界面的反應. Li 等[25]利用鈦酸鋇作為添加劑用于復合聚合物固態電解質中, 結果發現界面電阻隨著時間不斷的增加, 250 h后仍然不能穩定. 這說明了不同組分的聚合物電解質與鋰負極的界面反應不盡相同, 如果對組分進行優化才可以減少界面電阻. Hallinan 等[26]利用X射線光電子能譜(X-ray photon spectroscopy, XPS)研究表明, 產生鋰枝晶的鋰負極表面有鋰鹽的分解產物和有機物的分解產物. 利用原子力顯微鏡(atomic force microscope, AFM)技術和紅外光譜手段(Fourier transform infrared spectrometer,FTIR), Mancini 等[27]發現鋰金屬表面首先形成CF3自由基, 該自由基可奪取聚合物骨架中的氫原子,隨后鋰原子可能會進一步破壞聚合物中的C—O鍵形成Li-O-R 型物質. 目前我們對于鋰金屬和聚合物之間的詳細化學反應知之甚少, 在之后的研究中, 需要人們對其進行重點關注.
此外, 由于鋰沉積的不均勻性, 聚合物中也不可避免會產生鋰枝晶. 聚合物固態電解質中的鋰枝晶生長通常與固態電解質的離子遷移數、機械性能以及鋰金屬雜質有關. 早期的研究表明, 由于聚合物電解質的彈性模量低, 鋰枝晶經常在PEO 基的固態電解質中產生. 此外, 聚合物電解質通常在高溫下運行, 這會使得聚合物變軟, 進一步增加鋰枝晶穿透的風險[28]. Harry 等[29]認為, 鋰枝晶的生長跟固態電解質表面的不均勻性息息相關. 由于表面雜質的存在, 含有雜質的地方會出現鋰的不均勻沉積. 雜質相通常是富氧且絕緣, 這就阻礙了鋰金屬沉積在其表面. 由于局部電流的升高, 鋰的沉積和剝離只能發生在雜質的附近. 此外, 由于不均勻沉積的出現導致雜質上部出現了洞穴. 在兩者的同時作用下, 鋰金屬和固態電解質之間的空隙越來越大, 導致了鋰枝晶生長現象加劇(圖2(a)). 利用同步輻射X 射線三維成像技術(synchrotron X-ray microtomography, XTM), Maslyn 等[30]發現PSPEO-PS 聚合物電解質中的鋰枝晶的生長與電流密度密切相關, 在較低電流密度下, 鋰可以發生均勻沉積和剝離, 隨著電流密度升高, 界面出現了球形的突出物, 進一步加大電流密度, 除了球狀突出物外也出現了鋰枝晶. 基于低電流密度下鋰的均勻沉積現象, 可以首先在低電流下進行鋰的沉積, 得到新鮮的、無雜質的鋰薄層. 通過這種方式減少鋰表面的雜質含量, 遏制了聚合物與鋰金屬間的鋰枝晶生成進度從而延長了鋰金屬電池的壽命[31]. Dollé等[32]利用原位掃描電鏡技術(in situ scanning electron microscopy, in situ-SEM)觀察鋰枝晶在PEO中的生長狀況(圖2(b)). 結果表明隨著電流密度的增大, 鋰沉積形貌從苔蘚狀演變成枝晶狀, 枝晶生長點位于鋰金屬與聚合物之間, 嚴重時枝晶的生長會導致二者剝離進而影響電池的長循環壽命.同時聚合物電解質中鋰鹽的濃度也會影響鋰枝晶的形成. 隨著鋰鹽濃度的增加, 鋰枝晶穿透電解質的時間逐漸縮短. 這種現象出現的原因可能是機械強度的變化、界面接觸性的變化、電解質電化學性質的變化或者是濃度梯度的變化[33].
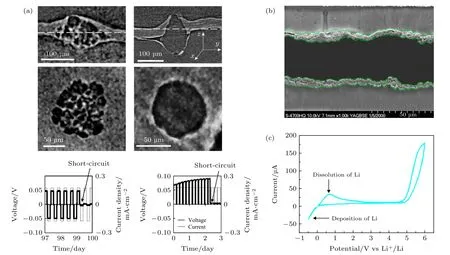
圖2 PEO 基固態電解質與負極的反應 (a) 鋰的不均勻沉積形成的鋰枝晶[29]; (b)鋰金屬沉積的原位電鏡掃描圖片[32]; (c) 鋰金屬沉積的循環伏安曲線[34]Fig. 2. Anode side reaction in PEO based solid state battery: (a) Lithium dendrite formation during deposition[29]; (b) in-situ SEM images of lithium deposition[32]; (c) C-V curves of lithium deposition/dissolution[34].
Golozar 等[35]用掃描電鏡技術(scanning electron microscopy, SEM)分析了PEO 固態電池循環后的鋰金屬形貌和化學成分變化, 結果表明鋰金屬表面形成了苔蘚狀和空心針狀的鋰枝晶. 并且通過化學成分分析發現鋰表面形成了鋰的碳化物、氧化物和碳氧化物等. 為了理解鋰枝晶的生長與聚合物電解質的本征特性的關系, Barai 等[36]通過理論計算獲得了聚合物固態電解質的發展方向. 計算結果表明, 制備的聚合物必須具有足夠高的彈性模量來減少鋰枝晶的形成: 一方面, 通過提高剪切應力來降低尖端處的交換電流密度從而減少鋰枝晶的產生; 另一方面, 當聚合物電解質的剪切模量大于鋰枝晶彈性模量的千分之一時, 鋰枝晶可生長的高度就會由于塑性形變而受到限制. 今后的工作中,人們可以依據該理論指導合成相應的高彈性模量聚合物電解質并對鋰枝晶穿透性能進行驗證.
最近, Galluzzo 等[37]通過高溫下的核磁共振譜(nuclear magnetic resonance , NMR)表征發現鋰原子會大量溶解在純PEO 聚合物當中. 實驗中將鋰金屬/PEO(salt-free)/鋰金屬對稱電池在高溫下進行靜置, 測試發現整體電池電阻值發生變化,這是因為鋰原子溶解在PEO 基體中. 這個現象也能解釋和證明聚合物鋰金屬固態電池中PEO 和鋰金屬之間的強粘附作用, 同時為PEO 基聚合物電解質的發展提供了很好的指導作用.
除了金屬鋰負極, 石墨負極也被用于聚合物固態電池的研究中. Zaghi[38]分別采用石墨和鈦酸鋰用作聚合物固態電池中的負極, 結果發現石墨負極在PEO 基聚合物中的容量衰減很快而鈦酸鋰負極中沒有出現明顯的容量衰減. 為了減少石墨負極表面界面反應, Imanishi 等[39]采用PVC 碳包覆的方法改善石墨表面, 提高了石墨負極的充放電容量.為了進一步提高負極的容量, Kobayashi 等[40]也采用了硅碳復合的策略用于PEO 聚合物固態電池中, 最終獲得了1000 mAh/g 的可逆容量. 最理想的狀況是將高容量的Si 負極用于PEO 電解質中,通過把Si 負極埋伏在碳紙的孔道結構實現與正極材料的匹配, 得到一個高容量的固態電池[41]. 此外,PEO 基聚合物與Na 金屬負極之間也有界面反應,Xu 等[42]通過PEO-Na3PS4復合有效地遏制了界面副反應. 雖然其他負極材料也可適用于PEO 基固態電池測試, 但是目前的研究基礎還很薄弱, 需要后續的研究對其進一步驗證.
2.2 負極界面改善策略
原則上, 可以通過改善鋰金屬表面SEI 膜的組分和構成來緩和鋰金屬與PEO 電解質的反應. 其中Appetecchi 等[43-44]發現通過熱壓無溶劑過程制備PEO 的電解質可以減少負極界面反應.他們認為這樣制備的聚合物雜質含量少, 可減少鋰金屬與鋰鹽的副反應. Bac 等[45]的工作證實了這個策略的科學性, 他們發現隨著鋰鹽濃度的增加, 負極界面的阻抗會相應地發生變化. 進一步工作發現,用LiFSI 部分替代LiTFSI 可以進一步減少界面的阻抗值. 為了減少界面的阻抗, 也有優先對鋰金屬表面進行處理形成穩定的界面層, 從而減少界面的副反應[46]. Zeng 等[47]在鋰金屬表面紫外光原位聚合得到聚醚丙烯酸酯(ipn-PEA)電解質, 電解質的機械強度(12 GPa)高、鋰離子導電率(0.22 mS/cm)高. 利用這種電解質包覆的鋰金屬進行鋰對稱電池測試, 結果發現沉積的鋰形貌十分均勻 (圖3 a).
通過構筑無機-有機復合電解質抑制PEO 基聚合物電解質中鋰枝晶產生. 引入無機物, 一方面可以提高聚合物電解質的離子電導率, 一方面可以提升機械性能. 電解質本征導電率的升高和機械強度的提高可提升其抑制鋰枝晶的能力. 例如, 清華大學Zhao 等[48]將Ta 摻雜的LLZO 顆粒加入到PEO 電解質中, 大大降低了PEO 的結晶溫度, 復合電解質的室溫導電率為1.12 × 10—5S/cm 且具有良好的機械性能. 同時由于陶瓷顆粒和聚合物基質的相互作用, 陰離子的移動被束縛, 鋰沉積的均勻性大大提高. 通過三明治結構的電解質可同時獲得高離子電導率和高機械性能, 同時保留聚合物固態電解質的柔性和可加工性能. 這樣的設計既可以抑制鋰枝晶又能保證鋰金屬和固態電解質的優良接觸. 例如, Huo 等[49]通過設計不同顆粒和體積分數的LLZO-PEO 復合電解質, Li/Li 對稱電池在0.2 mA/cm2下穩定循環400 h, 而未出現電池短路現象. 這種設計充分發揮了三明治結構電解質優異的界面接觸和鋰枝晶抑制的優勢(圖3(b)).
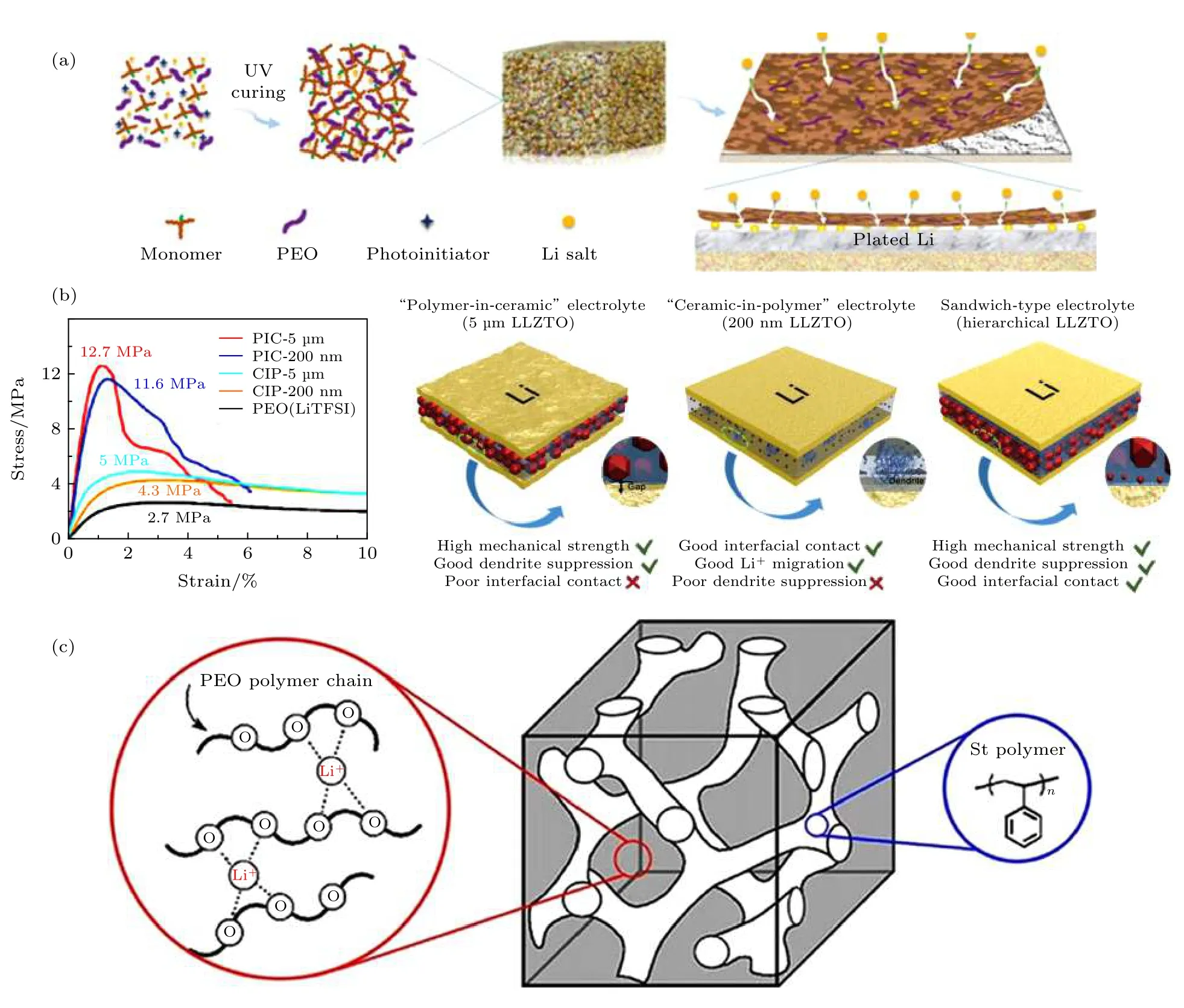
圖3 負極界面改善策略 (a) 鋰金屬表面修飾[47]; (b) 有機-無機復合電解質[49]; (c)嵌段聚合物[54]Fig. 3. Strategies to improve the anode stability[47]: (a) Surface modification of Li metal; (b) organic-inorganic composite electrolyte[49]; (c) triblock co-polymer[54].
理論計算結果表明, 鋰枝晶在高彈性模量的聚合物電解質中生長比較緩慢. 通過合成高彈性模量的嵌段共聚物作為電解質的基材可能是一種有效抑制鋰枝晶生長的策略. Pawlowska 等[50]、Chintapalli等[51]和Yuan 等[52]制備了以LiTFSI 為Li 鹽的PS-PEO SPE 體系, 其結構包含了高模量PS 段及高離子電導的PEO 段. 圖3(c)所示是這類嵌段聚合物的示意圖, 其中PS 部分用于提高聚合物的機械性能, PEO 部分用于提供離子導電通道. 然而,鋰金屬表面的雜質可能會導致負極界面出現鋰鼓包, 最終引發鋰枝晶生長并穿透聚合物電解質. 為了減少這類失效現象, 可以采用先在界面沉積少量鋰的預處理方案, 來減少鋰枝晶穿透的風險. 實驗結果表明, 通過預處理后鋰金屬在PS-PEO 類聚合物電解質中的循環壽命增加了一個數量級(超過4500 h), 鋰鼓包產生的數目也屈指可數[31].
最近, Fu 等[53]提出了其他的策略來抑制鋰枝晶的產生. 他們認為可以設計具有與陶瓷電解質類似的低鋰偏摩爾體積(partial molar volume of Li+)的“軟”離子導體(soft solid-ion conductor )來抑制固態鋰金屬電池中枝晶的生長. 例如, 通過四丁基氟化銨與鋰金屬原位生成納米LiF 并將其限域在剛性聚合物基體(PIM-1)的開放空洞網絡中. 然后將LiF@PIM-1 復合物包覆的鋰金屬用鋰電極分部組裝技術(LESA)裝成扣式電池后進行測試.通過XTM 觀察發現, LiF@PIM-1 復合物包覆的鋰金屬經過160 h 測試后表面依舊平滑而未處理的鋰金屬負極出現明顯鋰枝晶. 將LiF@PIM-1 復合物包覆的鋰金屬組裝成鋰對稱電池后進行長循環、大容量測試, 其壽命長達1000 h.
綜上可知, 為了減少負極界面的副反應以及鋰枝晶的產生, 可能需要進行多種協同策略從而達到最佳效果. 一方面需要對鋰金屬表面的物理和化學特性進行修飾實現鋰金屬的均勻成核, 另一方面通過改善電解質本身的性質來獲得高機械性能從而阻斷鋰枝晶的生長. 或者通過設計低鋰離子偏摩爾體積的“軟”固態離子導體來阻斷鋰枝晶的生成.
2.3 PEO 基固態電解質負極界面的表征
為了能更好地理解鋰枝晶生長機理并提出合理的策略控制鋰枝晶的生長, 對于負極界面的表征是非常重要的. 但是, 直接觀測鋰枝晶的形成和演化過程是具有挑戰性的, 因為鋰金屬對空氣非常敏感且容易被電子輻照破壞. 但經過研究者們幾十年的不斷探索, 人們還是開發了幾種手段對界面進行較為直觀的觀察.
為了探究鋰金屬表面與PEO 固態電解質接觸前后的變化, Ismai 等[55]應用XPS 發現鋰金屬表面有LiF 生成. Sun 等[56]研究了PEO 基固態電解質與鋰金屬界面電化學反應生成的SEI 組分(圖4(a)).結果表明, 界面的組分主要由鋰鹽的分解物如Li2S, Li3N, LiF 組成. 由于PEO 中含有微量的水分, 界面SEI 膜中也探測到了大量的LiOH. Xu 等[57]通過XPS 探究石墨負極表面的SEI 化學組分. 結果發現, 不同于普通的液體電解液, 聚合物固態電解質含有的水分高, 更容易在石墨負極表面產生氫氧化鋰并加速鋰鹽的分解. 這種堿金屬氧化物含量高的界面組分是否有益于固態電池的性能尚無定論, 需要人們今后更詳細的研究.
SEM 通常是最直觀的研究手段, 適用于直接觀測PEO/鋰金屬界面的反應, 特別是鋰枝晶的生長狀況. Rosso 等[58]利用SEM 結合FIB, 發現界面處的不均勻沉積會形成鋰凸起, 這種鼓包最終會導致電池短路. Dollé等[59]利用in-situ SEM 探究了鋰枝晶的原位生長過程. 隨著電流密度的升高,鋰沉積形貌由苔蘚狀逐漸變成針尖狀的鋰枝晶. 并且隨著枝晶進一步長大, 導致部分位點的電極和聚合物電解質剝離. Hovington 等[60]利用原位截面SEM 分析了兩種不同正極的長循環性能并觀測了電解質與電極的界面. 結果表明, 采用納米釩酸鋰的正極材料會在正、負極界面處發生聚合物電解質的分解, 從而導致界面層厚度的不斷增加. 相反,采用納米磷酸鐵鋰正極的界面非常平整, 這可能是因為負極鋰表面形成了穩定的SEI 膜. Golozar 等[35]為了探究聚合物固態電解質與負極界面的鋰枝晶生長狀況, 通過FIB 結合SEM 發現了兩種完全不同的鋰沉積形貌(圖4(b)).
利用XTM, Harry 等[61]分析了聚合物與鋰負極界面處的鋰沉積情況. 由圖4(c)可知, 塊狀的鋰枝晶首先出現在界面之下, 然后逐漸透過聚合物電解質. 通過三維重構技術可以很好的還原鋰枝晶穿透的動態過程. 結果證明鋰枝晶的生長都發端于界面處而不是電解質內部, 這表明了鋰金屬表面的性質對控制鋰枝晶生長的重要性. 利用XTM 技術去追蹤聚合物與鋰負極界面的雜質, 可得知雜質相是導致鋰鼓泡產生的重要原因. 因此, 實際應用中需要對鋰金屬進行除雜或修飾, 從而提高鋰金屬負極的循環壽命[29].
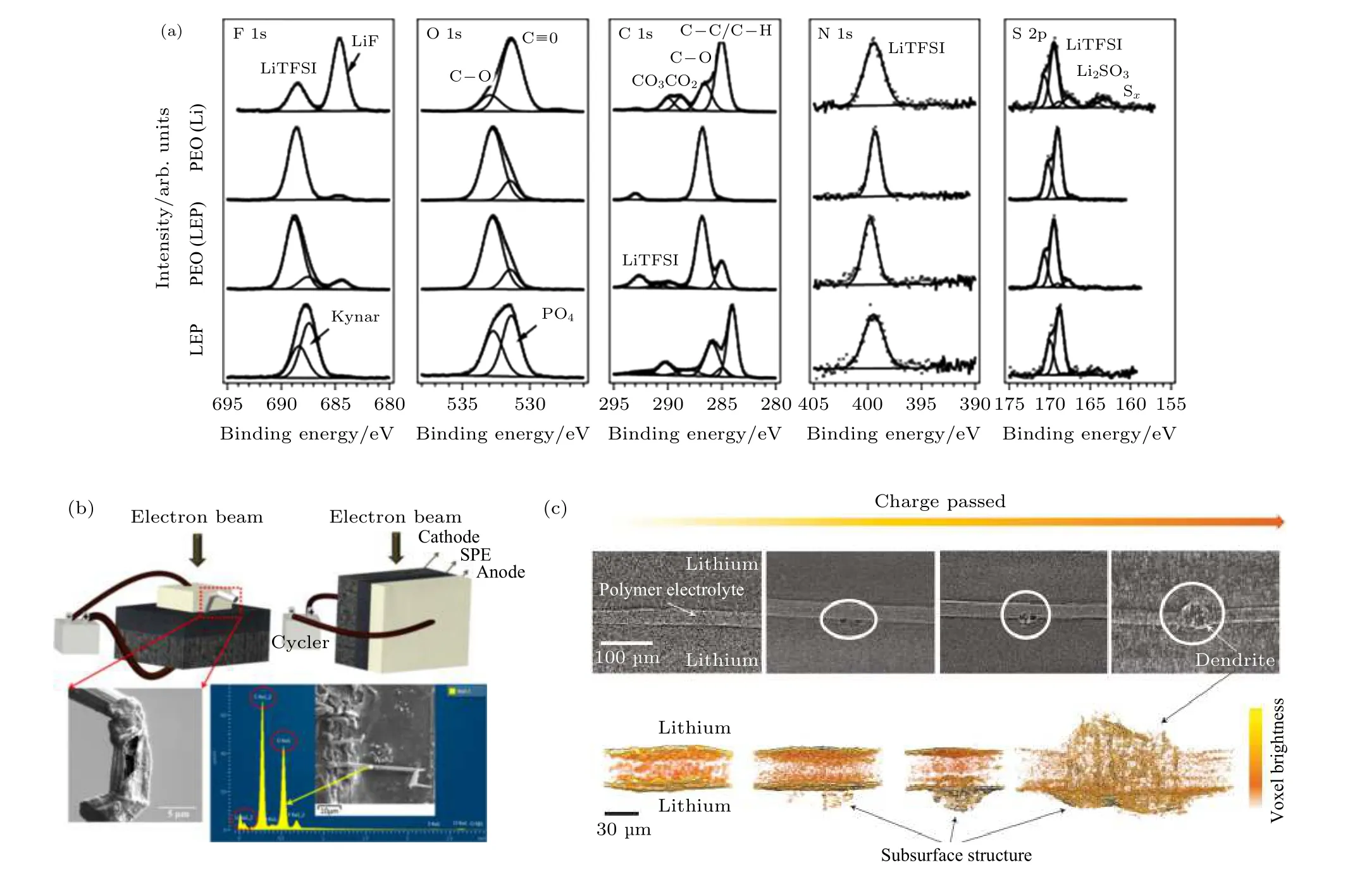
圖4 負極界面表征 (a)常規XPS[56]; (b)原位SEM[35]; (c)同步輻射CT[61]Fig. 4. Advanced characterization of anode interface: (a)Lab-XPS[56]; (b)in-situ SEM[35]; (c) synchrotron X-ray microtomography[61].
綜上可知, 聚合物電解質與鋰金屬界面處的微觀變化具有復雜性的特點, 需要通過綜合研究手段達到科學的結論.
3 PEO 基聚合物固態電池的正極界面研究進展
3.1 PEO 基固態電解質與正極的界面行為
目前PEO 基聚合物固態電解質在提升室溫離子電導率, 鋰離子遷移數, 機械強度及與金屬鋰負極兼容性等方面進行了大量的研究工作, 并且均取得了突破性的進展. 然而, PEO 體系在高電壓下的熱力學和動力學不穩定問題則較少受到關注. 盡管基于PEO 的聚合物電解質與LiFePO4正極具有良好的化學和電化學穩定性, 但有限的理論能量密度限制了固態電池在更高能量密度需求的領域的應用[5,62,63]. 例如, 法國博羅雷研發的以Li|PEO|LiFePO4固態電池組裝的“Bluecar”電動車的能量密度僅為100 W·h·kg-1, 遠低于普通液體電池的能量密度.
層狀過渡金屬氧化物正極, 如LiCoO2和LiNixCoyMnzO2, 具有高充、放電電壓平臺和高的理論比容量(270 mA·h·g—1), 在高能量密度固態鋰電池的應用領域表現出極大的潛力[64-66]. 如圖5 所示, 以高鎳三元材料為正極, 金屬鋰(Li)作為負極的固態鋰電池的能量密度有望突破350 W·h·kg—1, 能夠超越現有商用液態鋰離子電池的能量密度[67]. 此外, 從結構穩定性方面考慮, PEO 基聚合物電解質有可能抑制三元正極材料中過渡金屬離子溶解, 避免層狀結構向尖晶石和巖鹽相結構轉變, 從而緩解高電壓正極材料容量衰減和產氣等問題[68].
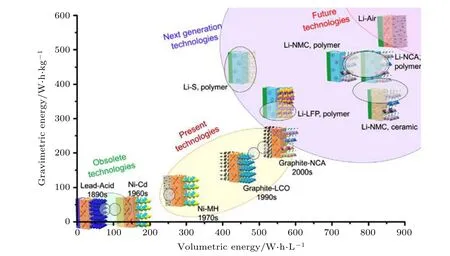
圖5 傳統電池及全固態鋰電池體系質量能量密度和體積能量密度預測與比較圖[67]Fig. 5. Prediction of volumetric and gravimetric energy density for traditional battery and all solid-state battery.
另外, 高比容量正極在循環過程中自身產生的體積變化會使界面的接觸性變差, 最終導致電池內阻急劇增加[67]. 因此, 為實現更高能量密度、高安全性的高電壓聚合物固態鋰電池的研發, 現階段亟需解決高電壓正極與PEO 聚合物固態電解質間的界面問題.
3.2 正極界面改善策略
目前, 已有大量的研究工作報道了提升高電壓正極與PEO 基聚合物電解質的界面穩定性的方法. 目前采取的改性策略主要圍繞兩大方面: 1) 正極表面包覆改性; 2) 高電壓正極/PEO 基電解質的界面層構建.
3.2.1 正極表面改性
表面包覆改性是最早應用在固態鋰電池中解決LiCoO2正極與PEO 聚合物電解質的界面問題的策略[69-77]. Seki 等[74]提出PEO 電解質的氧化分解發生在4.0 V, 連續的氧化分解會增加LiCoO2/PEO 的界面電阻, 導致在4.4 V 截止電壓下的循環性能較差. 此外, LiCoO2在持續充電時, 高度氧化的Co4+離子會加速PEO 電解質的氧化分解[73].Yang 等[75]最早采用金屬氧化物或磷酸鹽作為包覆層材料, 如Al2O3, ZrO2, MgO 和AlPO4, 用于提高LiCoO2的容量保持率和結構穩定性. Miyashiro 等[73]采用噴霧包覆方法將厚度為100 nm 的Al2O3均勻地包覆在正極LiCoO2顆粒表面. Al2O3在鋰化過程中生成了少量的LiAlO2, 能夠支持界面進行氧化還原反應. 實驗結果表明高氧化態的Co4+與PEO 電解質接觸面減少, 正極/電解質界面副反應得到一定程度的控制. 然而, 惰性氧化物通常既是電子絕緣體又是較差的離子導體, 會額外增加鋰離子擴散阻力和界面電荷轉移阻抗. 為了解決這一問題, 大量研究工作采用快離子導體如Li3PO4[74]和Li1+xAlxTi2—x(PO4)3(LATP)[69,70,75-77]作為包覆材料來改善LiCoO2/PEO 的界面穩定性.其 中, NASICON 型Li1+xAlxTi2—x(PO4)3(LATP)固態電解質由于其具有高的離子電導率, 高耐氧化分解電位及低廉的成本而吸引了眾多研究者的關注. Morimoto 等[76]通過簡單的固相混合方法將Li1.3Al0.3Ti1.7(PO4)3(c-LATP)包覆到LiCoO2表面. 電化學性能結果表明, 5 wt.% c-LATP 包覆的LiCoO2在截止電壓為4.5 V 下表現出最佳的循環穩定性. 然而, 固相法制備的c-LATP 顆粒較大,很難保證完全且均勻地覆蓋到材料表面(圖6(a)).隨后, Shim 等[77]采用前驅體包覆方法獲得了粒子尺寸相對較小的Li1.3Al0.3Ti1.7(PO4)3, 并用于改性LiCoO2(圖6(b)), 在4.5 V 截止電壓下, 其循環性能和倍率性能均優于固相法包覆改性的LiCoO2.最近, Li 等[75]采用一種簡單易行的溶液方法將0.5 wt% Li1.4Al0.4Ti1.6(PO4)3(LATP)均勻包覆到LiCoO2表面, 獲得的材料表面較為光滑, 無明顯大顆粒沉積, 包覆層厚度僅為20 nm(圖6(c)). 以改性后LiCoO2作為正極、PEO 聚合物作為電解質及金屬鋰為負極組裝的固態電池表現出較高的可逆比容量和更穩定的循環性能. 在充電截止電壓為4.2 V, 0.2 C 倍率下進行50 次循環后的容量保持率高達93.2%.
除了高電壓LiCoO2正極, LATP 也常作為包覆材料保護高鎳三元LiNixCoyMnzO2正極材料[78,79].Wang 等[79]采用簡單的機械融合制備Li1.4Al0.4Ti1.6(PO4)3(LATP)包覆LiNi0.6Co0.2Mn0.2O2(NCM 622)正極, 并系統探究了不同融合溫度對包覆改性材料電化學性能的影響. 實驗結果表明包覆改性后的NCM622 的電化學性能和熱穩定性均優于未進行包覆改性的材料. 其中, 經過600 ℃下熱處理的 LATP 包覆NCM622, 在4.5 V 充電截止電壓下和1C 倍率下循環100 次的容量保持率為90.9%(圖6(d)). XPS 結果顯示, 隨著融合溫度的升高,正極表面不純相Li2CO3的含量逐漸降低, 同時P-O的含量也有所下降, 這說明在高溫條件下LATP 存在并逐步擴散到NCM622 表面的趨勢(圖6(e)—(f)).P, Ti 和Al 等元素適量摻雜到正極結構表面能夠有效地抑制高鎳材料層狀結構的相轉變. 因此,LATP 包覆NCM622 電極在高電壓下的循環穩定性得到了顯著提升.
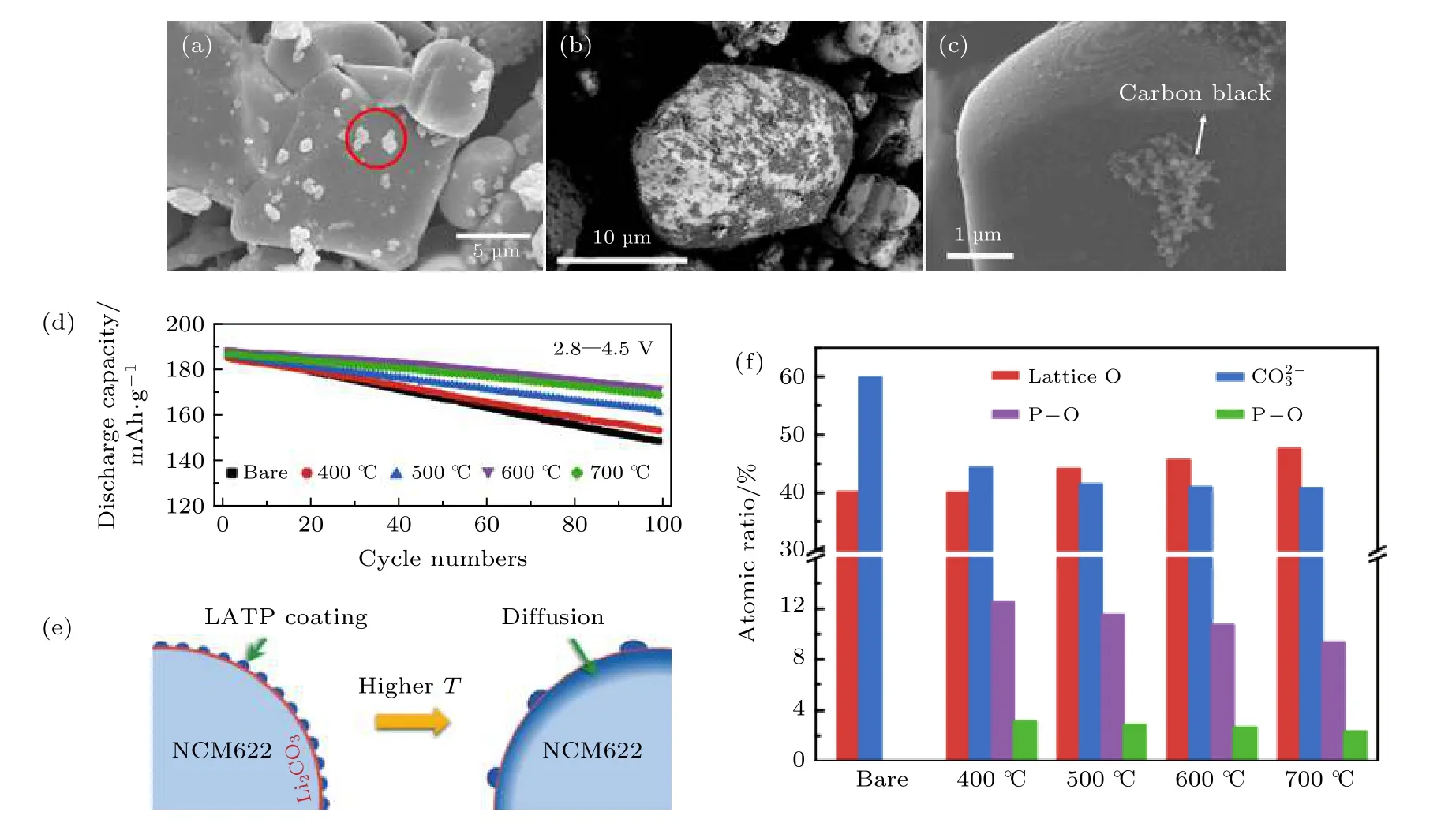
圖6 正極表面改性 (a) 固相法制備的5 wt.% c-LATP 包覆的LiCoO2 的SEM 圖片[76]; (b) 前驅體包覆方法獲得的Li1.3Al0.3Ti1.7(PO4)3 改性LiCoO2 的SEM 圖片[77]; (c) 溶液方法制備的0.5 wt% LATP 均勻包覆的LiCoO2 的SEM 圖片[75]; (d)在2.8-4.5 V 截止電壓下, LATP 包覆及未包覆改性的NCM622 在1 C 倍率下的循環曲線 (1 C = 190 mA/g)[79]; (e) 高溫煅燒過程中LATP 包覆改性及未包覆NCM622 的表面演化示意圖[79]; (f) 定量分析LATP 包覆改性及未包覆改性NCM622 的XPS 的O1s 和P2p[79]Fig. 6. Cathode interface engineering: (a) SEM image of 5 wt.% c-LATP coated LiCoO2[76]; (b) SEM image of LATP precursor coated LiCoO2[77]; (c) SEM image of 0.5 wt.% LATP coated LiCoO2 by solution method[75]; (d) charge discharge curve of NMC622 at 1 C rate between 2.8-4.5 V (1 C = 190 mA/g)[79]; (e) schematic diagram of LATP coated and un-coated NMC during high temperature sintering[79]; (f) XPS O1s and P2p of LATP coated and un-coated NMC[79].
上述研究表明包覆過程的熱處理溫度對正極材料的電化學性能的影響是極其重要的. 然而, 元素在無機包覆層與正極界面的擴散通常是相互的.過渡金屬離子如Co3+也會不可避免地游離到包覆層表面, 從而影響層狀材料在高度脫鋰態下的結構穩定性. 近年來, 原子層(ALD)和分子層沉積(MLD)技術作為先進的氣相薄膜沉積技術被認為是解決固態電池界面問題最為理想的涂層技術[80](圖7(a)).與其他包覆技術相比, ALD/MLD 具有獨特的優勢, 包括較低的沉積溫度, 原子和分子尺度的沉積及優異的均勻性和一致性. Sun 等[81]采用ALD 技術將鈮酸鋰(LiNbO3, LNO)沉積到LiNi0.8Co0.1Mn0.1O2(NCM811)表面用于改善NCM811 與PEO基聚合物電解質的界面性能. 第一性原理計算結果預測LNO 在高電壓下具有良好的化學、電化學穩定性, 高導鋰性能和低電子導電性, 因此是包覆材料較為理想的選擇[82,83]. 通過調控ALD 沉積圈數可以精準地控制涂層厚度至納米級, 而涂層厚度是獲得優異電化學性能的關鍵. 結果表明, 10 nm ALD-LNO 涂層能夠阻礙長循環后層狀結構降解并且抑制晶格氧的損失, 從而穩定了NMC811 活性材料(圖7(b)和圖7(c)). 另外, LNO 的涂層其較低的電子電導率能夠在一定程度緩解高電壓下PEO 基聚合物的化學氧化和電化學分解. 最終, 組裝的ALD-LNO 包覆的NCM811 |PEO|Li 固態電池在60 ℃, 0.2 C 倍率下循環200 次后平均庫倫效率達99.2%, 明顯優于未進行包覆改性的NCM811正極(92.3%)(圖7(d)). 除了LNO, 其他離子導體材料如Li4Ti5O12[84], LiTaO3[85], LiNbO3[86], Li2SiO3[87]和Li3PO4[88]也可通過ALD/MLD 沉積技術解決電極與電解質的界面問題.
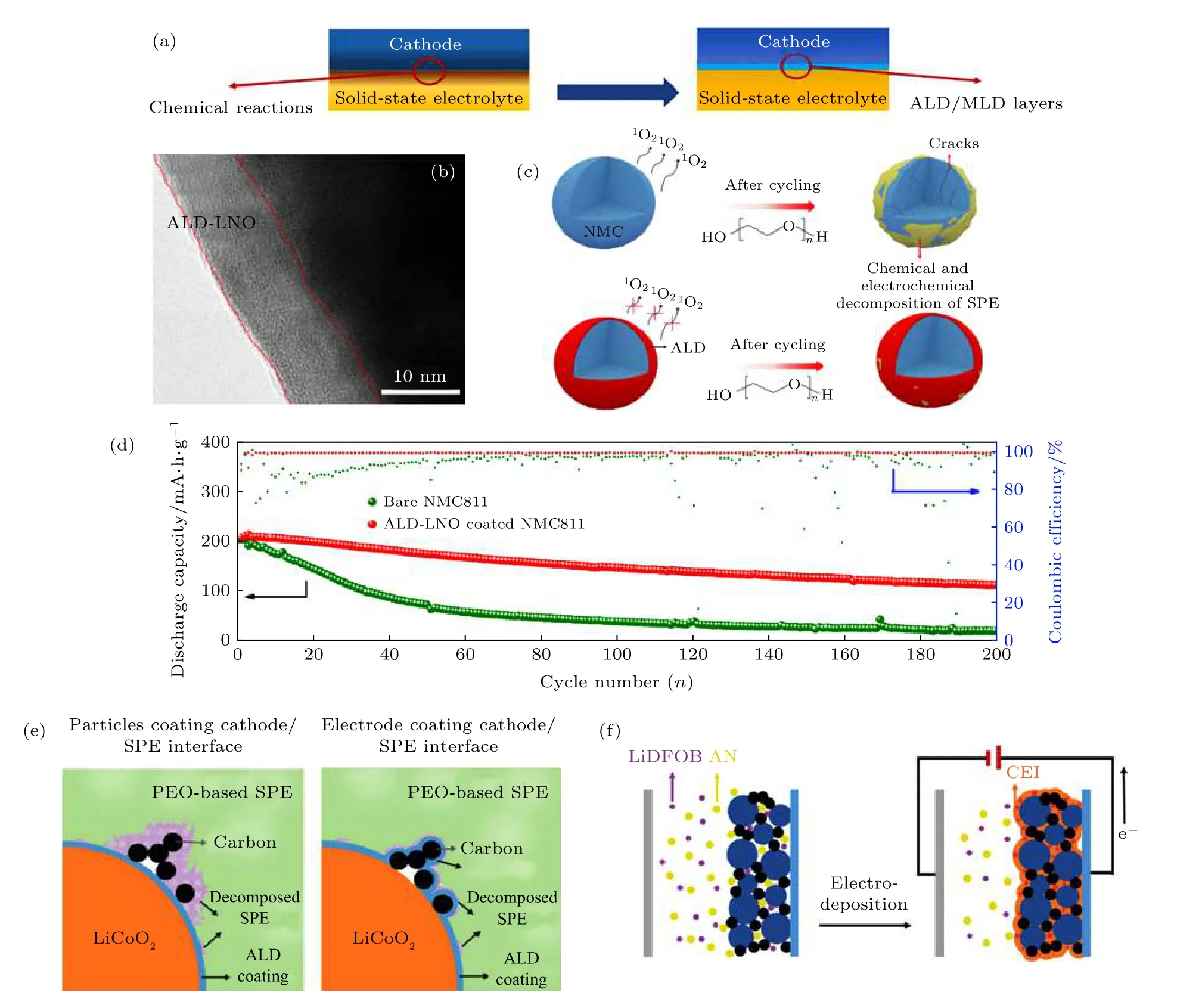
圖7 (a) 示意圖說明ALD/MLD 技術解決固態電池界面問題[80]; (b) ALD 技術制備的LNO 包覆NCM811 的TEM 圖[81]; (c) 示意圖說明包覆改性前后的NCM811 正極在長循環后層狀結構降解及晶格氧的損失情況[81]; (d) 對比改性前后NCM811 在60 ℃,0.2 C 倍率下循環性能曲線[81]; (e) LTO 包覆LiCoO2 顆粒和LTO 包覆LiCoO2 正極(極片包括活性材料, 導電碳和粘結劑)的示意圖[71]; (f) 示意圖說明電沉積方法制備PAN 包覆NCM523[91]Fig. 7. (a) Schematic diagram of ALD/MLD in stabilizing cathode interface[80]; (b) TEM image of ALD LNO coated NCM811[81]; (c)illustration of structure degradation and oxygen release of coated and uncoated NCM811[81]; (d) cycling performance of coated and uncoated NCM811 NCM811 at 60 ℃, 0.2 C rate[81]; (e) illustration of ALD LTO coated LiCoO2 particle and LTO coated LiCoO2 electrode[71]; (f) illustration of PAN coated NCM 523 by electrodeposition[91].
目前, 由于其高昂的成本, ALD/MLD 技術不具備廣泛適用性. 另外, 高比容量正極在循環過程中產生的體積變化會使無機包覆層開裂或剝離, 從而使包覆層的保護作用失效. Ma 等[72]和Liu 等[89]曾提出采用聚(乙烷基-α-氰基丙烯酸酯)PECA)聚合物作為包覆層改性正極LiCoO2和5 V 高電壓正極LiNi0.5Mn1.5O4. ECA 單體能夠在室溫條件下原位聚合成PECA, 該過程無需高溫處理, 并且步驟簡單高效. PECA 由于其強吸電子基團-C≡N使其擁有較高的耐氧化能力和快速離子遷移能力.此外, PECA 聚合物包覆層能夠阻礙過渡金屬離子溶解, 隔絕電解質與電極的直接接觸及緩解顆粒微裂現象. 與未改性的固態電池相比, PECA包覆LiCoO2|PEO-LiDFOB|Li 呈現更小的界面阻抗和更優異的高電壓循環穩定性[72].
忽然,一只漂亮的鳥兒在殿外跳躍,然后展翅飛遠。御座上的孩童對暗潮洶涌的洪流毫無所覺,而是向著飛走的鳥兒,露出了天真的笑容。
先前的大部分研究主要集中在包覆改性正極材料, 往往忽略了導電碳添加劑與PEO 固態電解質的界面穩定性問題. 事實上, Xia 等[90]最早通過循環伏安(C-V)測試結果驗證了PEO 與碳材料接觸時, 在3.8 V 即開始分解. 因此, 系統地探究包覆改性整個正極極片對界面穩定性的影響, 對揭示界面構建機理是至關重要的. Liang 等[71]對比了鉭酸鋰(LTO)包覆LiCoO2顆粒和LTO 包覆LiCoO2正極(極片包括活性材料, 導電碳和粘結劑)的電化學性能. 實驗結果表明LTO 包覆LiCoO2整個正極在高電壓下的循環穩定性更佳. 優異的電化學性能主要受益于LTO 對導電碳/PEO 界面的良好保護, 該研究結果進一步揭示了包覆整個電極對提升正極/電解質界面熱力學和動力學穩定性的重要意義. 對于整個電極表面包覆處理實際上是在電極與電解質界面增加一道屏障, 阻礙界Qiu 等[91]提出將前驅體溶液1 M 二氟草酸硼酸鋰(LiDFOB)10% 丙烯腈(AN)+EC/DMC 注入到LiNi0.5Co0.3Mn0.2O2(NCM532)極片中, 通過電化學沉積方法原位引發AN 聚合形成PAN 包覆NCM532 電極.這種前驅體溶液電沉積的方式可以確保電極與聚合物包覆層有更強的附著力, 更有利于粒子與粒子之間充分的接觸, 在電極內部形成連續快速的離子傳導路徑. 理論計算結果證實PAN 比PEO 呈現更高的電離電勢, 因此具有更高的耐氧化電位. 最終Li|PEO—LiTFSI|NCM523 固態電池在0.5 C 倍率下循環200 次的容量保持率依然可以達到72.3%.Lu 等[92]采用類似的方法, 通過LiDFOB 引發VC原位聚合的方法在LiCoO2表面構筑正極界面層(CEI), 最終該電池可在4.2 V 截止電壓下循環500 圈, 容量保持率為71.5%. 并且ARC 測試表明, 固態電池在350 ℃以下不會發生明顯的熱失控, 證明CEI 膜可同時提升電池的正極界面電化學穩定性和熱穩定性.
綜合分析, 表面包覆高電壓正極能夠有效地避免電極與PEO 聚合物的副反應, 降低界面阻抗.然而, 優化包覆層組分仍然是未來應用在固態電池中的一個極大的挑戰. 未來重點關注的包覆層材料將以含鋰的化合物為主, 篩選的主要依據有: 包覆層材料自身相穩定性、電化學和化學穩定性及離子電導率高低. 除了含鋰氧化物, 聚陰離子型氧化物及含硼鋰鹽作為包覆材料也極具潛力, 未來可應用到高電壓固態電池中解決正極/電解質界面問題.
3.2.2 界面層構建
向界面添加緩沖層是解決高電壓正極/PEO聚合物電解質界面問題的另一個有效方法. 截止目前, 仍缺乏具有合適的氧化還原電化學窗口的單個聚合物電解質. 通常, PEO 電解質與金屬鋰相容較好, 但在高壓正極側表現出高的反應性. 而對于一些正極穩定的高氧化電位電解質在負極一側則表現出高的負極反應性. 為了能夠同時滿足鋰負極無枝晶沉積和高壓正極穩定運行的全固態電池[93], Li 和Lucht[94]以及Smart 等[95]設計了一種雙層聚合物電解質PEO-LiTFSI/聚N-甲基丙酰胺(PMA)-LiTFSI. PMA 分子含有重復的二甲基乙酰胺(DMAc)單元. DMAc 介電常數高, 能更好地促進鹽解離、Li+溶劑化和傳輸, 另外, DMAc 常用作耐氧化的電解液添加劑. 該PEO—LiTFSI/PMA—LiTFSI 雙層電解質能夠使Li/LiCoO2全固態電池在4 V 電壓下穩定運行, 且經過長期循環后, 也能保持較高的離子電導率. 向正極與PEO基電解質界面添加耐高壓界面層的確能夠改善過渡金屬離子催化PEO 分解反應, 但若想將雙層電解質策略廣泛應用到未來高電壓固態電池基礎和產業研究中, 仍需要解決以下問題: 1) 高氧化電位聚合物層的篩選. 高氧化電位聚合物層需要兼具與高電壓正極和PEO 良好的兼容性、快速導鋰特性和優異的機械韌性; 2) 雙層電解質膜的厚度. 未來若要提高能量密度到350 W·h·kg—1高電壓固態鋰電池, 就要求聚合物電解質膜的厚度低于30 μm.這是目前雙層電解質較難突破的技術; 3) 離子在雙層聚合物界面傳導能力. 雙層電解質的應用無疑是在固態電池體系中增加了新的界面, 界面物理接觸是否良好, 離子傳導是否連續, 是雙層電解質能否應用于固態電池中的關鍵.
除了直接引入界面層, 另一種較為常見的界面構建方式是通過化學和電化學過程在電極表面原位生成界面層. 與直接引入界面層的方式相比, 原位構建的穩定界面層不僅與正極和電解質均能呈現良好的接觸性, 而且形成的界面膜的厚度可精確調控.
Qiu 等[96]對PEO 聚合物電解質與LiCoO2正極材料在高電壓電化學循環下的失效機理進行了研究. 他們發現在進行4.2 V 恒電位阻抗測試時,其阻抗值隨時間增加緩慢, 這表明原位生成的CEI 組分具備導Li+特性且PEO 氧化分解反應在動力學上速率較慢. 然而當匹配LiCoO2正極在4.2 V 進行循環時, 全電池的界面阻抗迅速增大,容量快速衰減. 通過共振非彈性X 射線光譜(RIXS)分析發現, LiCoO2在4.2 V 充電狀態時材料中的晶格氧具有強氧化能力, 加速PEO 的氧化分解,而LiCoO2表面失去晶格氧形成尖晶石Co3O4或鹽巖相CoO, 均為Li+不良導體, 導致材料的界面阻抗顯著增大. 該研究提出如果能抑制正極材料的表面氧化性或者采用表面不具有強氧化性的正極材料, PEO 聚合物電解質有可能在更高的電壓下穩定循環. 在實驗上也證實了在使用固態電解質LATP 包覆LiCoO2和LiMn0.7Fe0.3PO4正極材料的PEO 全固態電池, 均實現了4.2 V 充電截止電壓下的穩定循環. 該研究結果表明在電池體系中電解質的穩定性不僅與材料本身的性質有關, 更與電解質和電極之間的界面特性密切相關. 電極和固態電解質之間的界面設計對最終能否實現可實用化的全固態電池是至關重要的.
此外, 鋰鹽陰離子能夠遷移到電極表面, 并且促進其形成穩定的CEI 或負極界面層(SEI)[97-103].因此, 合理設計鋰鹽并深入地理解鋰鹽陰離子分解機制是解決PEO 基聚合物電解質與高電壓正極界面問題的有效途徑. Zhao 等[104]通過調控聚合物體系的鋰鹽比例來調節界面性能. 將三鋰鹽(LiTFSI+5%LiBOB+5%LiNO3)PEO 聚合物電解質組裝在Li/LiNi1/3Co1/3Mn1/3O2(NCM111)固態電池中, 在65 ℃和截止電壓為4.25 V 條件下,100 次循環后的容量保持率為91.2%, 平均庫倫效率達到99%以上. 其中, LiBOB 分解產物主要有BOx, 是CEI 的主要組分, 能夠有地效減少正極與電解質的接觸面積. Wang 等[105]報道了一種新型的鋰硼鹽Li[(CF3)3COBF3](LiTFPFB), 并 將 其與PEO 結合構建多層聚合物固態電解質(DSMSPE)(圖8(a)). 紅外測試結果證實在PEO-LiTFPFB 聚合物電解質中Li+與EO 的絡合作用要強于PEO-LiTFSI, 這種分子間的相互作用有利于降低PEO 電解質的HOMO 值. XPS 測試顯示循環后的LiCoO2表面界面膜組分為鋰硼鹽的分解產物,如BOx, LiBxOyFz及LiF 等, 均有利于固態電池獲得穩定的界面(圖8(b)). 組裝的LiCoO2/Li(2.8—4.3 V)電池在60 ℃, 0.1 C 倍率下循環100 次后容量保持率為83.3%(圖8(c)).
Li 等[70]認為LAGP 納米包覆層存在明顯的晶粒邊界和孔隙, 會導致PEO 的氧化分解, 進而對LiCoO2結構造成損害, 使其近表面晶格結構無序, 從而減緩離子在LiCoO2體相內部的擴散. 因此, 他們提出將LiBOB 調控界面CEI 膜的化學組分策略與LAGP 包覆改性策略相結合, 并應用于改善正極與聚合物的界面穩定性. LiBOB 作為添加劑鹽在電極周圍的原位分解產物恰好可以填充LAGP 包覆層的間隙, 進一步降低了PEO 氧化分解的可能性. 另外, Fu 等[78]直接將PEO-LiBOB聚合物引入到正極中構建復合正極. PEO-LiBOB既可以作為理想的粘結劑, 又可以作為離子導體相, 不僅能夠形成穩定的CEI 膜來抑制聚合物的氧化分解, 同時還能夠避免TFSI—陰離子對鋁箔集流體的腐蝕. 與直接加入聚合物相比, 直接加入可原位聚合的前驅體溶液更能降低正極/電解質界面阻抗. Lu 等[92]將LiDFOB 溶解于碳酸亞乙烯酯(VC)中構成聚合前驅體溶液. VC 在熱引發劑偶氮二異丁氰(AIBN)的作用下原位聚合形成具有耐高壓特性的PVC. PVC 與LiDFOB 的協同作用使LiCoO2正極表面形成一層超薄且均勻、低阻抗的CEI 層(圖8(d)和圖8(e)). CEI 膜改性的LiCoO2|PEO-SPE|Li 固態電池在3.0—4.2 V 電壓范圍下, 0.5 C 倍率進行500 次循環后容量保持率為71.5%, 而未進行改性的固態電池在200 次循環后容量僅保留至34.1 mA·h·g—1(圖8(f)).
綜合以上分析, 原位引發聚合構建CEI 膜是改善高電壓正極/PEO 電解質界面最有效的解決辦法之一. 然而, 目前該類研究工作報道較少, 仍有諸多問題亟待解決, 如原位制備方法的優化, 聚合前驅液的篩選原則, CEI 膜自身柔韌性及導鋰性能和CEI 膜先進表征技術等.
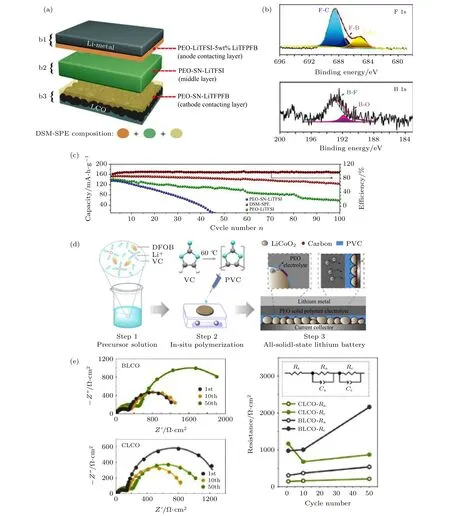

圖8 (a) DSM-SPE 電解質膜的結構示意圖[105]; (b) DSM-SPE 電解質膜循環10 次后, XPS 測試LiCoO2 正極表面F1s 和B1s 譜圖[105]; (c) SPE, DSM-SPE, 和PEO-LiTFSI 電解質組裝的LiCoO2/Li 固態電池在2.8-4.3 V 電壓范圍, 60 ℃, 0.1 C 倍率下循環性能曲線[105]; (d) 原位聚合形成CEI 膜及組裝固態電池的示意圖[92]; (e) LiCoO2|PEO-SPE|Li 和CEI 膜改性的LiCoO2|PEOSPE|Li 在不同循環圈數放電態的EIS 曲線, 及等效電路圖和相應的擬合結果對比圖[92]; (f) LiCoO2|PEO-SPE|Li 和CEI 膜改性的LiCoO2|PEO-SPE|Li 在3.0-4.2 V 電壓范圍, 0.5 C 倍率下的循環性能曲線[92]Fig. 8. (a) Demonstration of DSM-SPE solid electrolyte based solid battery[105];(b) F1s and B1s XPS spectra of LiCoO2 electrode after 10 cycles[105]; (c) cycling performance of LiCoO2/Li cell with SPE, DSM-SPE, and PEO-LiTFSI electrolyte at 60 ℃, 0.1 C rate between 2.8-4.3 V[105]; (d) illustration of in- situ CEI film formation and solid state battery assembly[92]; (e) EIS spectra of LiCoO2|PEO-SPE|Li and CEI modified LiCoO2|PEO-SPE|Li at different cycles[92]; (f) cycling performance of LiCoO2|PEO-SPE|Li and CEI modified LiCoO2|PEO-SPE|Li at 0.5 C rate between 3.0-4.2 V[92].
3.3 PEO 基固態電解質/正極界面反應的先進表征手段
高電壓正極/PEO 的界面行為, 包括如界面的動力學、熱力學穩定性, 是決定高電壓正極固態電池長循環穩定的關鍵. 然而, 目前對高電壓正極固態電池界面的副反應機制和離子傳導機理了解尚淺, 仍需先進的原位/非原位光譜和電鏡技術協助我們更深入地理解高電壓固態鋰電池正極界面行為. 迄今為止, 不同的先進表征技術已被報道應用于研究固態電池體系. 這些研究成果對界面行為從不同角度進行剖析, 對未來穩定界面的設計具有重要的指導意義.
3.3.1 微分電化學質譜法
微分電化學質譜法(DEMS)已被廣泛用來探究電池體系產氣行為, 如鋰氧氣電池中電化學反應, 鋰離子電池中電解液分解反應. 定量分析電化學過程中氣體的生成與消耗對于解釋電池反應機理、界面反應機理和界面膜形成機理等具有指導意義. Nie 等[69]采用in-situDEMS 技術監測PEO基固態電池在循環過程中氣體產生行為. 實驗結果表明PEO 聚合物電解質在電壓達到4.5 V 時才會明顯產生H2. 當PEO 與LiCoO2組裝成固態電池,其在4.2 V 就會探測到H2, 這表明LiCoO2與PEO的接觸反應會促進固態電池在較低電壓下產生H2.他們還通過in-situDEMS 進一步證實Li1.4Al0.4Ti1.6(PO4)3(LATP)包覆改性后能夠有效隔絕LiCo O2與PEO 的直接接觸, 使產氣電位提升到4.5 V.此外, Fu 等[78]通過in-situDEMS 表征手段在循環的PEO-LiTFSI+Super P|PEO-LiTFSI-(Li1.5Al0.5Ge1.5(PO4)3)LAGP |Li 固態電池中探測到CO2(m/z= 44)和O2(m/z= 32)信號, 他們推測, 這些氣體也是PEO 在大于4.2 V 電壓下氧化分解產生的.
3.3.2 原位/非原位顯微鏡技術
顯微鏡技術是一類非常強大的用于研究電極結構和微觀界面形貌的技術手段. 在固態電池中用于監測循環過程中正極結構及界面在原子級和納米級尺度下的演化過程. 例如, Shim 等[77]通過不同的電鏡技術分析LATP 包覆層形貌及其對正極LiCoO2微觀結構的影響. 由透射電鏡(transmission electron spectroscope, TEM)可看出LATP 包覆層呈連續且厚度在0.2 μm(圖9(a)). 與之對應的選區電子衍射(selected area electron diffraction, SAED)確定包覆層為NASICON 型的LATP. 不同元素的能量色散譜(energy dispersive spectroscopy, EDS)圖顯示Co 元素主要存在于正極區, 而Al 元素主要存在于包覆層區域(圖9(b)). 另外, Mg 和Ti 元素在兩個區域均有分布, 該結果表明LiCoO2結構中有Mg 摻雜, 并且包覆層LATP 中的Ti 元素在高溫煅燒條件下會擴散到正極結構中. 為了明確Ti 和Mg 元素在LiCoO2晶格結構中的占位, 研究者采用掃描透射電子顯微鏡-電子能量損失譜(scanning transmission electron microscope-electron energy loss spectroscopy, STEM-EELS)進行分析, 結果證實少量的Co 位被Ti 元素所取代(圖9(c)). 此外, 他們還通過導電原子力顯微鏡(conducting atomic force microscope, C-AFM)證實Mg 擴散到LATP 層提高了包覆層的電子電導率, 使界面阻抗降低(圖9(d)).

圖9 (a) LATP 包覆層 的TEM 和SAED 圖[77]; (b) LATP 包 覆 層的STEM 和EDS 圖[77]; (c) Mg 摻雜的LiCoO2 的 放 大STEM 和EELS 圖[77]; (d) Mg 摻雜的LATP- LiCoO2 和LATP- LiCoO2 的C-AFM 圖[77]; (e) 完全充電態的NCA 顆粒在21 周循環后的2DFF-TXM[106]; (f) 完全電態的NCA 顆粒在21 周循環后的3D-FF-TXM[106]; (g) 未進行循環及循環后的NCA 電極在高分辨率下的BIB-SEM 圖[106]Fig. 9. (a) TEM and SAED of LATP coating layer[77]; (b) STEM and EDS of LATP coating layer[77]; (c) STEM and EELS of Mg doped LiCoO2[77]; (d) C-AFM of LATP coated Mg-LiCoO2 and LATP- LiCoO2[77]; (e) 2D-FF-TXM of NCA particle after 21 cycle[106]; (f) 3D-FF-TXM of NCA particle after 21 cycle[106]; (g) BIB-SEM of NCA electrode before and after cycling[106].
Doeff 和Liu 等[106]采用先進的同步輻射X 射線全場二維/三維成像技術(2D/3D synchrotron full field X-ray microtomography, 2D/3D-FFXTM)和聚離子束/寬離子束掃描電鏡(focused ion beam/broad ion beam-scanning electron microscopy, FIB/BIB-SEM)表征手段觀察在PEO基固態電池中循環后的LiNi0.8Co0.15Al0.05O2(NCA)正極材料形貌和荷電狀態(SOC)的變化情況. 從圖9(e) 2D-FF-TXM 可知NCA 二次顆粒會因循環導致顆粒碎裂和荷電狀態(SOC)不均勻. 但考慮到2D-FF-TXM 無法進行離子束方向上的解析,他們又采用3D-FF-TXM 研究了裂紋的3D 進化及其對顆粒內SOC 非均勻分布的影響. 圖9(f)的結果直觀地呈現了裂紋由顆粒核心向表面傳播. 裂紋的增加會引起Li+傳輸路徑彎曲, 最終導致不可逆容量損失和電池阻抗顯著增加. BIB-SEM 和FIB-SEM 比2D-FF-TXM 和3D-FF-TXM 擁有更高的空間分辨率, 其得到的結論與前兩者結論一致(圖9(g)). 由于沒有電解液的充分浸潤作用,NCA 顆粒的晶間裂痕對固態電池電化學容量和倍率性能的不良影響更為明顯.
3.3.3 同步輻射光源光譜技術
同步輻射X-射線吸收光譜(X-ray absorption spectroscopy, XAS)采集時間短, 光源強度可調,對元素價態、未占據電子狀態和電荷轉移等化學信息非常敏感, 可用于精準判斷循環過程中正極界面結構中過渡金屬的元素價態和周圍電子結構的變化情況. Liang 等[71]對比了未進行包覆改性的LiCoO2在循環前后的XAS 光譜. 循環前后的Co-K 邊吸收在全額電子產量(TEY)模式和熒光產量(FLY)模式下基本一致. 這表明LNO 包覆層若只作用在LiCoO2顆粒上, 則對其電化學性能提升的效果并不明顯, LNO 完全包覆LiCoO2電極(活性顆粒+導電碳)才能獲得明顯的性能提升. Li 等[70]將Co K-邊光譜與2D TXM XANE 技術相結合分析了包覆及未包覆LAGP 的LiCoO2在3 V 放電狀態下Co 價態的變化. 引入2D TXM 技術能夠更直觀地提供Co 價態變化圖像, 方便研究人員清晰地理解材料結構內部價態衍化過程.
同步輻射技術若能廣泛應用于研究聚合物固態鋰電池體系中原位生成的界面膜組分及其對正極表面晶體結構的影響, 不僅對固態鋰電池界面熱力學和動力學研究的意義重大, 而且對固態電解質的結構設計及與高電壓正極材料的匹配具有指導性作用. 但截至目前, 基于同步輻射技術研究高電壓正極與PEO 聚合物固態電解質界面問題的研究結果鮮有報道.
3.3.4 其他重要表征手段
在聚合物固態電池中, XPS 技術常用于分析正極/電解質界面CEI 膜組分[72,78,91,105]. 例如, Ma 等[72]通過XPS 技術分析了LiCoO2|PEO-LiDFOB|Li固態電池正極界面CEI 膜組分. 結果表明CEI 膜主要的組分如LixBOyFz和LiF 是LiDFOB 分解產生的. 除了XPS, 紅外光譜技術(FTIR)也常用于確定CEI 組分, 如Qiu 等[91]在循環后的正極表面探測到新的紅外峰1397 cm—1, 對應的是LixBOyFz中的B-O 伸縮振動峰, 主要是由LiDFOB 分解形成的. 除了用于表征界面組分, XPS 技術也可用于判斷正極中過渡金屬元素是否存在溶解和擴散問題.Yang 等[75]通過XPS 的Co2p 譜分析不同LATP 包覆量對Co3+溶解和擴散的影響. 結果顯示當LATP包覆量大于0.5 wt%時, 能夠完全避免LiCoO2正極在高截止電壓和長循環下的Co3+的溶解和擴散.
安全性是聚合物固態電池能否實際應用的一個重要指標. Lu 等[92]采用加速量熱法(ARC)測試了LiCoO2|PEO-LTFSI|Li 固態電池的安全性.ARC 測試是在絕熱環境中加熱電池, 同時監測加熱后的熱傳遞反應, 通過跟蹤電池熱失控期鏈式反應的動力學可以測量出相關的關鍵溫度參數.
4 結論與展望
本文主要綜述了近期固態電池內PEO 基固態電解質與負極、正極界面問題的研究進展. 對于PEO 基固態電解質而言, 與其匹配的正、負極的選擇是多樣的, 研究的體系也更為復雜. 因此, 分別總結了PEO 基固態電解質與不同的負極和正極的界面問題, 如界面反應機理、界面結構/組分、界面機械穩定性、界面動力學和熱力學穩定性問題等.進而, 綜述了改進各界面問題的方法與策略, 最后還對相應的表征手段和測試方法進行了詳細的介紹. 為了獲得高比能、高安全的聚合物固態電池,未來對PEO 基聚合物電解質的研究不再只是集中于離子電導率的提升, 提高其界面兼容性是未來本領域研究的重中之重. 盡管多種改性策略均能在一定程度上穩定PEO 基聚合物電解質/電極的界面,但復雜的界面膜組分、影響界面穩定性的因素和詳細的界面動力學過程, 仍缺乏系統的理論認識.
在眾多的負極材料中, 金屬鋰負極以其超高的能量密度、超低的電壓平臺及與PEO 良好的化學穩定性, 使得其極具潛力應用在高比能PEO 基聚合物固態電池中. 然而PEO 體系固有低的鋰離子遷移數和較差的機械強度的缺點同樣會導致不均勻沉積, 甚至是鋰枝晶的形成. 未來對于負極一側的界面改性應該更傾向于提升PEO 基聚合物固態電解質的鋰離子遷移數, 增加膜的機械模量. 此外,設計具有低的鋰偏摩爾體積的“軟”快離子導體可以促進鋰的均勻沉積, 減少鋰枝晶的產生.
在正極一側, 抑制PEO 電解質與高電壓正極的界面反應是實現長循環穩定性的關鍵. 雖然眾多的改性方式已應用于改善正極界面問題, 但仍有諸多不足之處. 例如, 現有包覆改性材料很難同時滿足相穩定性、電化學和化學穩定性、高離子電導率及良好機械適應性; 原位引入界面保護膜實際是在復雜的電池體系中增加新的界面, 目前對于該界面是否存在空間電荷層效應, 膜厚度及組分是否可調等問題尚不明確. 未來應該積極開發新的界面改性材料, 通過先進的技術表征手段更深入地理解固態電池的界面化學.
除了以上對于已有改性策略的提升, 未來關于PEO 基固態電解質的研究還應關注以下幾方面:
1)拓寬PEO 基聚合物固態電解質的電化學穩定窗口. 利用分子軌道理論, 通過分子結構設計或引入特性官能團調控PEO 基聚合物電解質自身的HOMO 和LUMO 能級. 升高LUMO 能級同時降低HOMO 能級能夠拓寬PEO 體系的電化學穩定窗口, 使其同時匹配高電壓正極和金屬鋰負極;
2)構建新型固液混合固態電解質, 改善電極界面穩定性及電極內部離子/電子輸運. 添加液體助劑優先在正極和負極界面電化學原位形成穩定的SEI 和CEI 膜, 對正、負極界面起到雙層保護,協同提升固態電池的長循環穩定性; 但對于液體助劑的篩選及與電極和固態電解質的兼容性問題尚未有研究工作深入探討;
3)新型鋰鹽的開發與匹配應用. 從已報道的原位構建穩定界面的文獻可知, 鋰鹽陰離子若能優先于PEO 聚合物進行氧化/還原分解, 可能促進正、負界面形成穩定界面相層. 因此, 未來合理地設計鋰鹽陰離子結構或是采用多鋰鹽的方式有望應用于調控固態電池界面性質;
4)原位實時在線表征手段的運用. 盡管目前材料領域表征手段眾多, 但能夠用來表征界面組分的技術寥寥無幾. 這是由于界面膜組分大多表現出對空氣及電子束高度的不穩定性; 通常固態電池界面膜的空間尺寸在納米級別以下, 而且PEO 基聚合物電解質經過循環后很難從電極上拆解; 高溫或是電子束輻射會導致離子、原子分布改變進而導致界面組分改變. 因此, 未來需要更多的原位、無損且清晰的技術進行表征和分析, 如冷凍電鏡技術(cryo-EM)和同步輻射技術. 此外, 設計可用于原位表征的電化學電池對同步輻射技術的表征也是至關重要的, 良好的裝置能夠獲得足夠強的信號,從而原位實時在線表征界面結構和電荷輸運;
5)由于界面現象涉及多尺度和多維度的性質變化, 因此需要不同表征手段相結合來進行更深入的探究. 例如, 2D XANES 與TXM 聯用可以同時直觀的獲得電子結構信息和價態變化情況. 此外,理論計算協助實驗技術表征能夠給出合理的實驗現象的分析和機理解釋. 例如, 計算聚合物分子的HOMO 和LUMO 能級判斷優先分解的能力; 通過DFT 方法按照不同材料電子隧穿厚度預測CEI/SEI 厚度; 計算聚合物分子與Li+絡合數及解絡合能力, 并分析Li+在聚合物體系中的動力學行為;計算PEO 在不同活性電極上電化學氧化反應的反應能, 可以判斷界面副反應發生的可能性;
6)對于未來PEO 基聚合物固態電池的產業化應用, 首要解決的是高內阻問題. PEO 基固態電池的內阻是等容量液態鋰離子電池內阻的100 倍以上, 高的內阻會影響循環性能和電池容量的發揮. 高內阻除了源于電解質自身相對低的離子電導率之外, 界面離子傳導也是產生高內阻的主要因素. 因此, 未來界面離子傳導動力學的研究有望加速實現PEO 基聚合物固態電池大規模產業化應用.

