明膠海綿聯合Embosphere 微球栓塞治療肝癌破裂出血的效果觀察
方中平,楊功強,許坤,劉鈺
信陽市中心醫院急診內科,河南 信陽 464031
原發性肝癌的發病率呈逐年上升趨勢,但由于早期發病隱匿,多數患者確診時已錯過最佳手術時機[1-2]。原發性肝癌最為嚴重的并發癥是肝癌破裂出血,多起病急驟,伴有劇烈腹痛,極易導致失血性休克,大多預后不佳[3]。近年來,隨著介入外科的飛速發展,經導管動脈栓塞術(transcatheter arterial embolization,TAE)憑借其定位準確、微創性、可重復性強等臨床優勢已逐漸成為肝癌破裂出血的有效治療手段。臨床研究表明,TAE可防止肝癌破裂出血患者側支循環的建立,能夠降低再出血發生率,對于延長患者生存時間、改善其生存質量具有積極的作用[4]。目前,介入栓塞材料的種類多樣,明膠海綿顆粒和Embosphere微球應用較多。既往研究指出,不同的栓塞材料將直接影響TAE的治療效果[5],但目前對于如何選擇栓塞材料和栓塞方式的臨床爭議較大。基于此,本研究旨在探討明膠海綿聯合Embosphere微球栓塞治療肝癌破裂出血的效果,旨在為提高TAE的臨床治療效果提供科學依據,現報道如下。
1 資料與方法
1.1 一般資料
選取2016年2月至2018年5月于信陽市中心醫院行TAE的肝癌破裂出血患者。納入標準:①經病理學檢查或臨床診斷確診為原發性肝癌,伴有急性腹痛,腹部移動性濁音(+),腹腔穿刺抽出不凝固血液,經影像學B超、計算機斷層掃描(CT)等檢查確診為肝癌破裂出血;②符合TAE治療指征;③臨床資料完整。排除標準:①繼發性肝癌;②精神異常或伴有感知覺障礙;③伴有心、腦、肺、腎等其他重要臟器嚴重病變或其他系統良惡性腫瘤;④合并嚴重代謝性疾病;⑤有近期大型手術史;⑥過敏體質或合并嚴重免疫系統疾病;⑦門靜脈主干被癌栓完全阻塞;⑧伴有嚴重全身感染或凝血機制異常;⑨妊娠或哺乳期婦女。根據納入和排除標準,本研究共納入85例肝癌破裂出血患者,其中,男53例,女32例;年齡49~68歲,平均(58.95±8.13)歲。根據術中栓塞方法的不同將85例肝癌破裂出血患者分為明膠海綿組(n=39)和明膠海綿聯合Embosphere微球組(n=46)。兩組患者的性別、年齡、肝功能Child分級、瘤體直徑比較,差異均無統計學意義(P>0.05)(表1),具有可比性。
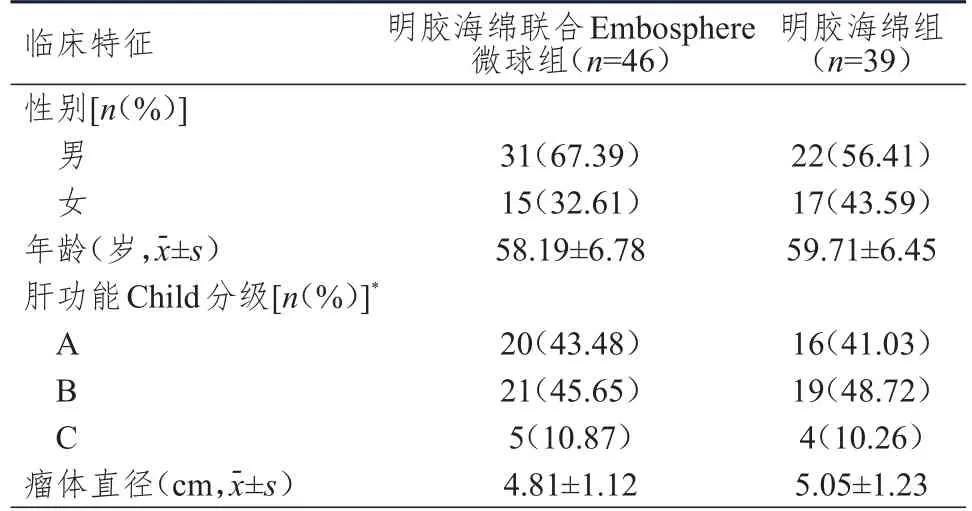
表1 兩組患者的臨床特征
1.2 治療方法
兩組患者均接受抗休克治療,并根據具體情況接受輸血治療及TAE治療。TAE操作步驟具體如下:2%利多卡因局部逐層麻醉成功后,采用Seldinger法穿刺股動脈,在X線電視透視下置入短導絲及導管鞘,封管后使用5 F血管造影導管插管行肝動脈造影,充分了解血管征象,確定出血靶血管,同時采用Philips Allura Xper FD10大型數字減影血管造影儀(digital subtraction angiography,DSA)工作站測量出血靶血管直徑,選擇稍大于出血血管直徑的栓塞材料,將栓塞材料與顯影劑碘普羅胺注射液按照1∶1的比例混合后用超選擇微導管插入靶血管,在X線電視透視下緩慢推注至見顯影劑反流。栓塞后再次進行DSA造影,未見造影劑外溢則證明無出血征象。術中,明膠海綿組注入適量350μm或560μm明膠海綿顆粒栓塞出血血管;明膠海綿聯合Embosphere微球組先注入 100~300 μm 或300~500 μm的 Embosphere微球后,再注入350μm或560μm的明膠海綿顆粒栓塞出血血管。囑患者術后絕對臥床休息,密切觀察其生命體征,警惕再次出血。
1.3 觀察指標
記錄兩組患者手術前后的生命體征(心率、收縮壓、舒張壓)、術中輸血量。抽取患者手術前后空腹靜脈血5 ml,以3000 r/min的速度離心10 min,置于-20℃低溫中保存待檢,采用干化學法檢測血紅蛋白(hemoglobin,Hb)、谷丙轉氨酶(glutamicpyruvic transaminase,GPT,又稱ALT)、谷草轉氨酶(glutamic-oxalacetictransaminase,GOT,又 稱AST)、總膽紅素(total bilirubin,TBil)水平,儀器選用邁瑞公司的BS-2000M型全自動生化分析儀,試劑盒由上海酶聯生物科技有限公司提供。采用溴甲酚綠法測定清蛋白(albumin,Alb)水平,儀器選用美國貝克曼庫爾特有限公司CytoFLEX S系列流式細胞儀,試劑盒由上海恒斐生物科技有限公司提供,操作均嚴格按照說明書步驟進行。評價止血效果:即時止血指栓塞后再次進行DSA造影,未見造影劑外溢;再次出血指TAE術后7 d內肝癌再次破裂出血。
1.4 統計學方法
采用SPSS 20.0軟件對數據進行統計分析。計量資料以均數±標準差(±s)表示,組間比較采用t檢驗或非參數Mann-WhitneyU檢驗;計數資料以例數或率(%)表示,組間比較采用χ2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者手術前后生命體征及Hb水平的比較
術前,兩組患者的心率、收縮壓、舒張壓、Hb水平比較,差異均無統計學意義(P>0.05);術后,兩組患者的心率均低于本組術前,收縮壓、舒張壓、Hb水平均高于本組術前,差異均有統計學意義(P<0.05)。術后,兩組患者的心率、收縮壓、舒張壓比較,差異均無統計學意義(P>0.05);明膠海綿聯合Embosphere微球組患者的Hb水平高于明膠海綿組,差異均有統計學意義(t=2.046,P<0.05)。(表2)
2.2 兩組患者輸血量以及止血情況的比較
兩組患者的即時止血率均為100%,兩組比較,差異無統計學意義(P>0.05)。明膠海綿聯合Embosphere微球組患者的輸血量為(501.22±108.78)ml,明顯少于明膠海綿組患者的(634.17±86.35)ml,差異有統計學意義(t=6.161,P<0.01);明膠海綿聯合Embosphere微球組患者的7 d內再出血率為2.17%(1/46),低于明膠海綿組的15.38%(6/39),差異有統計學意義(χ2=4.874,P<0.05)。
表2 兩組患者生命體征及Hb水平的比較(±s)
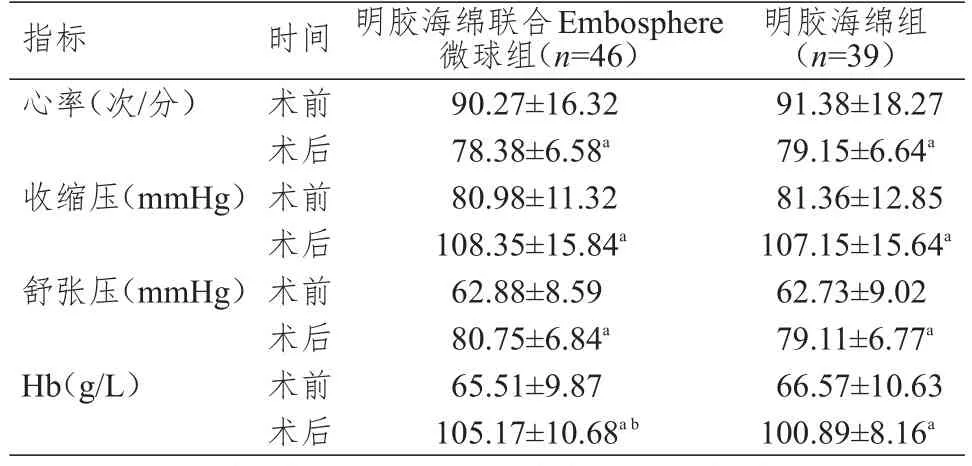
表2 兩組患者生命體征及Hb水平的比較(±s)
注:a與本組術前比較,P<0.05;b與明膠海綿組術后比較,P<0.05
指標心率(次/分)收縮壓(mmHg)舒張壓(mmHg)Hb(g/L)時間術前術后術前術后術前術后術前術后明膠海綿聯合Embosphere微球組(n=46)90.27±16.32 78.38±6.58a 80.98±11.32 108.35±15.84a 62.88±8.59 80.75±6.84a 65.51±9.87 105.17±10.68a b明膠海綿組(n=39)91.38±18.27 79.15±6.64a 81.36±12.85 107.15±15.64a 62.73±9.02 79.11±6.77a 66.57±10.63 100.89±8.16a
2.3 兩組患者肝功能指標的比較
術前,兩組患者的ALT、AST、TBil、Alb水平比較,差異均無統計學意義(P>0.05)。術后,兩組患者的ALT、AST、TBil水平均高于本組術前,Alb水平均低于本組術前,差異均有統計學意義(P<0.05)。術后,明膠海綿聯合Embosphere微球組患者的ALT、AST、TBil水平均明顯低于明膠海綿組,Alb水平明顯高于明膠海綿組,差異均有統計學意義(t=75.201、74.994、21.221、2.875,P<0.01)。(表3)
表3 兩組患者肝功能指標的比較(±s)
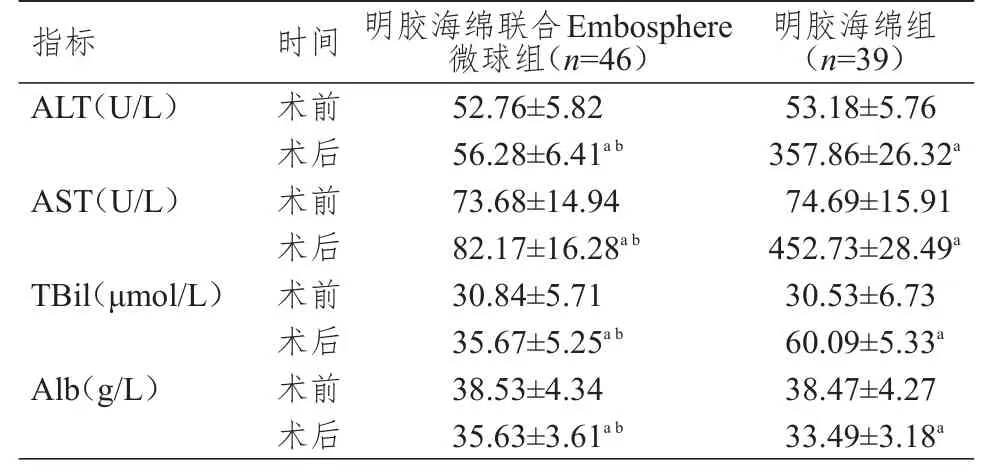
表3 兩組患者肝功能指標的比較(±s)
注:a與本組術前比較,P<0.05;b與明膠海綿組術后比較,P<0.01
A L T(U/L)A S T(U/L)T B i l(μ m o l/L)A l b(g/L)術前術后術前術后術前術后術前術后5 2.7 6±5.8 2 5 6.2 8±6.4 1 a b 7 3.6 8±1 4.9 4 8 2.1 7±1 6.2 8 a b 3 0.8 4±5.7 1 3 5.6 7±5.2 5 a b 3 8.5 3±4.3 4 3 5.6 3±3.6 1 a b 5 3.1 8±5.7 6 3 5 7.8 6±2 6.3 2 a 7 4.6 9±1 5.9 1 4 5 2.7 3±2 8.4 9 a 3 0.5 3±6.7 3 6 0.0 9±5.3 3 a 3 8.4 7±4.2 7 3 3.4 9±3.1 8 a
3 討論
原發性肝癌確診時多已發展至中晚期,較難治愈[6]。流行學調查研究表明,肝癌破裂出血的發生率為2.5%~20%,患者病死率高,約占肝癌死因的10%[7]。肝癌破裂出血的病理機制至今尚未明確,可能與肝癌惡性程度高或腫塊體積增大過快有關。既往研究表明,結節型肝癌更易發生破裂,腫塊直徑越大或突出肝邊緣,破裂出血的風險越大[8-9]。針對肝癌破裂出血,臨床主要采取外科手術、內科止血及介入栓塞治療。外科手術可有效止血,但對于瘤體較大、多發肝癌或身體情況較差的患者并不適用,且多數患者術后可出現嚴重的肝功能損害,甚者出現肝功能衰竭,預后較差[10];內科止血治療適用于出血量較小者,對于出血量多者具有一定局限性,且臨床治療效果不理想,病死率較高。臨床研究表明,TAE可在X線電視透視下將栓塞劑通過導管注入出血靶血管,完全阻塞血管,在有效止血的基礎上可通過阻斷腫瘤供血從而發揮抑制腫瘤生長的作用[11-12]。另有研究表明,TAE在全程影像的引導下通過DSA血管造影技術能夠明確腫瘤的位置、大小以及出血部位,選擇性靶血管插管技術可有效減少對正常肝組織的損傷,對于改善患者預后具有積極作用[13]。
研究表明,TAE的治療效果與栓塞材料的選擇密切相關,有效止血及保護肝功能的關鍵很大程度上取決于合適的、穩定的栓塞劑的選擇[14]。目前,臨床上栓塞材料眾多,其中,固體栓塞劑明膠海綿顆粒、Embosphere微球應用相對較為廣泛。明膠海綿顆粒的栓塞效果良好,能有效止血,但臨床長期追蹤調查顯示明膠海綿顆粒可在血液中自行溶解,同時其因黏附性較高而易導致微導管堵塞,且栓塞過程中不易到達血管末梢,遠期治療效果不理想,血管再通出血率較高[15]。同時,TAE治療中明膠海綿顆粒的用量不易控制,過度栓塞時有發生,極易損傷正常肝組織,進而導致肝功能不全甚至衰竭,導致患者預后不良。
Embosphere微球是一種由丙烯酸聚合物構成的新型栓塞材料[16],由Biosphere Medical公司研發生產并投入使用后引起了介入科專家和學者的廣泛關注,現已逐漸應用于肝癌以及肝癌破裂出血的栓塞治療。相較于其他栓塞材料,Embosphere微球臨床優勢:①由惰性材料構成,安全性較高,是一種穩定的、有效的永久性栓塞劑[17];②球形顆粒,顆粒規則均勻,不易聚集,表面光滑,彈性好;③黏合性低,組織相容性和懸浮性良好,可順利通過微導管,到達出血靶血管后可順血流到達并栓塞比微球直徑小的末梢動脈;④對栓塞控制得更精確,出血控制良好,且再出血發生率低[18]。
本研究結果表明,在TAE治療中單獨使用明膠海綿或聯合Embosphere微球栓塞,患者的心率均明顯降低,舒張壓、收縮壓、Hb水平均較本組術前明顯升高,且兩組患者的栓塞成功率均為100%,表明兩種栓塞方式均可有效治療肝癌破裂出血。本研究亦發現,單獨使用明膠海綿栓塞后的再出血發生率較高,原因可能是明膠海綿屬于短效栓塞劑,穩定性較差,可在血液中自行溶解,導致靶血管再通,引起再出血;而Embosphere微球屬于永久栓塞劑,同時能夠減慢明膠海綿的溶解速度,因此,明膠海綿與Embosphere微球聯合使用后能大大降低栓塞靶血管的再出血發生率。余強等[19]發現,將Embosphere微球應用于TAE治療中,可有效防止因栓塞劑流失導致的血管再通,與本研究結果大體一致。
本研究發現,明膠海綿聯合Embosphere微球栓塞術后患者肝功能損傷較輕,原因可能是聯合Embosphere微球栓塞后患者的再出血發生率較低,因此,減少了TAE治療的次數,最大程度地保護了患者的肝功能;也可能是由于栓塞過程中明膠海綿用量過多,導致一次性過度栓塞,引起肝臟不可逆損傷。楊均等[20]在明膠海綿顆粒與Embosphere生物微球栓塞治療原發性肝癌破裂出血的對比觀察中發現,Embosphere微球栓塞能夠最大程度地保護正常肝組織,減少肝功能損傷的發生率,進而改善患者預后,與本研究結果大體一致。
綜上所述,明膠海綿聯合Embosphere微球栓塞治療肝癌破裂出血的臨床效果良好,能大大降低再出血的風險,對于肝功能的損害較輕。本研究的不足之處在于納入的樣本數量較少,可能會對結果造成一定的統計學誤差,但本研究為優化肝癌破裂出血的臨床治療方案和提高TAE的療效提供了一定的理論支持。

