達氏鱘Elovl4、ELovl5和Elovl7克隆、組織分布及饑餓對其表達的影響
吳曉雲 陳葉雨 劉 亞 賴見生 宋明江 龔 全
(四川省農業科學院水產研究所, 成都 611731)
長鏈脂肪酸延長酶(Elongases of very long chain fatty acids, Elovls)位于細胞內質網上, 是長鏈多不飽和脂肪酸(Long chain polyunsaturated fatty, LCPUFA)合成的關鍵限速酶, 在維持細胞膜結構與功能、能量代謝和信號轉導等生命活動中起重要作用[1,2]。目前在哺乳動物中已發現7種Elovls(Elovl1-Elovl7), 其中Elovl1、Elovl3、Elovl6和Elovl7主要參與長鏈飽和脂肪酸及單不飽和脂肪酸的合成, 而Elovl2、Elovl4和Elovl5主要參與合成多不飽和脂肪酸[3]。水生動物長鏈脂肪酸延長酶的研究相對較晚, 主要集中在Elovl2、Elovl4和Elovl5[2,4],Elovl7僅在欖綠青蟹中被克隆[5]。其中, Elovl4能將C20和C22的多不飽和脂肪酸最高延長到C36[4], 主要參與超長鏈脂肪酸的合成, 因而它主要在哺乳動物視網膜、腦和精巢等脂質含量較多的組織中表達[6]; 在哺乳動物中, Elovl5能夠優先延伸C18和C20多不飽和脂肪酸, 而對C22多不飽和脂肪酸的活性較弱, 很難延長到C22以上[6,7], 魚類的研究也保持一致[8,9];然而, 目前在魚類中對Elovl7的研究較少, Elovl7可對C18和C16表現出較強的活性, 能將C18延長到C20再轉移給Elovl1進一步延長到C24[10]。
達氏鱘(Acipenser dabryanus), 又稱長江鱘, 沙臘子或小臘子。隸屬于鱘形目(Acipenseriformes)、鱘科(Acipenseridae)、鱘屬(Acipenser), 曾是長江上游重要的經濟捕撈對象[11]。但由于水體污染、過度捕撈和棲息地的破壞, 達氏鱘微生境發生改變,極易因時間、空間、季節更替以及環境變化導致的食物短缺而造成饑餓脅迫。本研究通過克隆Elovl4、Elovl5和Elovl7得到了其cDNA開放閱讀框序列, 并研究其在不同組織及饑餓脅迫作用下的表達模式, 以期為進一步了解饑餓脅迫條件下達氏鱘Elovl4、Elovl5和Elovl7表達變化情況, 為進一步探索達氏鱘生理生化變化機制及Elovl4、Elovl5和Elovl7功能奠定基礎, 也為其資源的管理和人工養殖提供理論依據。
1 材料與方法
1.1 實驗材料
實驗用魚為四川省農業科學院水產研究所人工繁殖的F2代達氏鱘(Acipenser dabryanus)幼魚。實驗前將魚在循環水養殖系統暫養2周。每天早晚各投喂1次飼料, 飼料含量為粗蛋白48.62%、粗脂肪8.61%、粗纖維4.68%、粗灰分14.66%和水分12.21%。暫養2周后, 選取75尾體重為(30±2) g, 健康、活力好的達氏鱘隨機分為5個處理, 每個處理3個平行, 每個平行5尾魚, 分別為對照組(饑餓0)、實驗1組(饑餓1d)、實驗2組(饑餓3d)、實驗3組(饑餓7d)和實驗4組(饑餓14d)進行為期14d饑餓脅迫試驗, 期間DO≥5.0 mg/L, 水溫25—27℃。達氏鱘通過MS-222(Tricaine methanesulfonate)進行麻醉后,將不同組織(心、肝、脾、腎、卵巢、精巢、肌肉、腸、鰓、皮膚、腦和胃)取出后放入液氮中速凍, 然后置于–80℃冰箱保存備用。
1.2 RNA提取及cDNA合成
總RNA提取采用RNAisoPlus(寶生物工程大連有限公司, D9108B)按試劑盒說明書的方法操作。將–80℃凍結的組織樣品在液氮中研磨至粉末狀,加入1 mL RNAiso Plus, 在試劑的作用下從組織中抽提出總RNA, 溶解于50 μL DEPC水中。所得RNA溶液用1.0%瓊脂糖凝膠電泳(120 V, 10min)檢查其相對分子質量和完整性。RNA樣品采用Nano Drop 1000分光光度計(Hach, America)檢測其純度和濃度。第一鏈cRNA合成參照ReverTra Ace反轉錄試劑盒(TOYOBO, Japan)進行操作。
1.3 達氏鱘Elovl4、Elovl5和Elovl7基因克隆
根據本實驗室前期達氏鱘轉錄組測序獲得的unigene序列為基礎(Accession numbers: SRR616 7299、SRR6172670、SRR6173479、SRR617 5505、SRR6179331和SRR6179394), 通過NCBI數據庫進行比對分析, 獲得了達氏鱘Elovl4、Elovl5和Elovl7的cDNA全序列。為驗證序列的正確性, 分別在ORF上下游設計驗證引物(表 1), 以反轉錄cDNA為模板進行PCR擴增, 擴增產物連接載體后, 送生工生物工程(上海)股份有限公司進行測序。
1.4 序列分析
運用Vecter NTI軟件分別預測達氏鱘Elovl4、Elovl5和Elovl7 ORF, 并推測其編碼氨基酸序列, 計算編碼產物分子量和等電點; 信號肽序列使用在線工具SignalP 4.0 (http://www.cbs.dtu.dk/services/SignalP/)進行預測; 跨膜結構分析用SMART(http://smart.embl-heidelberg.de/)。利用Cluxtal X將達氏鱘Elovl4、Elovl5和Elovl7氨基酸序列分別與其他物種的相應氨基酸序列進行多重比對。利用Mega 6.0軟件的Neighbor-joining法構建系統進化樹。

表 1 Elovl基因克隆和熒光定量PCR檢測所用引物Tab. 1 Primers for cDNA cloning and real-time PCR of Elovls
1.5 組織表達分析
選取5尾健康達氏鱘, 采用熒光定量PCR法檢測Elovl4、Elovl5和Elovl7在心、肝、脾、腎、卵巢、精巢、肌肉、腸、鰓、皮膚和腦中的相對表達量。熒光定量PCR擴增采用SYBR@PrimeSriptTMRT-PCR Kit Ⅱ(perfect Real Time, 寶生物工程大連有限公司, DRR083A)。10倍連續稀釋的陽性模板作為PCR模板做標準曲線, 擴增效率在95%—105%,r2>0.9, 溶解曲線單一峰。結合瓊脂糖電泳檢測產物長度和特異性, 從而確定引物最優退火溫度。12.5 μL 2×SYBR Green Real-time PCR Master Mix,上下游引物各1 μL(10 μmol/L), 滅菌雙蒸水5.5 μL。PCR擴增程序為: 94℃預變性5min; 94℃變性30s,55℃退火30s, 72℃延伸30s, 42個循環; 最后70—95℃獲取熔解曲線并確保擴增產物的特異性。反應完成后檢測產物的特異性。每個樣品設3個復孔。采用2–ΔΔCt法分別計算樣品中Elovl4、Elovl5和Elovl7 mRNA的相對表達量。
1.6 饑餓脅迫下達氏鱘Elovl4、Elovl5和Elovl7表達量的檢測
實驗魚分別在饑餓實驗的0、1d、3d、7d和14d采集肌肉、腦、胃、腸道及肝臟組織, 每個平行采集3尾。熒光定量方式參考1.5。
1.7 數據分析
采用平均值±標準誤(Mean±SE)表示實驗數據,采用SPSS22.0軟件處理結果。對試驗數據進行方差分析并結合Duncan法進行多重比較檢測顯著性。
2 結果
2.1 達氏鱘Elovl4、Elovl5和Elovl7克隆及序列分析
達氏鱘Elovl4編碼區為753 bp, 編碼250個氨基酸, 相對分子質量為29793.13 Da, 等電點為9.47, 包含7個預測的跨膜區;Elovl5編碼區為885 bp, 編碼294個氨基酸序列, 相對分子質量為34794.38 Da, 等電點為9.42, 5個預測的跨膜區;Elovl7編碼區為846 bp, 編碼281個氨基酸序列, 相對分子質量為33227.82 Da, 等電點為9.19, 7個預測的跨膜區。Elovl4,Elovl5和Elovl7均含還有高度保守的HXXHH組氨酸盒。
2.2 進化樹分析
將達氏鱘Elovl4、Elovl5和Elovl7氨基酸序列分別與其他魚類相應序列進行比對后發現, 三個基因均與斑點雀鱔聚為一支, 表明在進化上與雀鱔親緣較近(圖 1)。
2.3 達氏鱘不同組織Elovl4、Elovl5和Elovl7的表達
達氏鱘Elovl4、Elovl5和Elovl7在各個組織中均有表達, 同時存在著差異性表達(圖 2),Elovl4在卵巢和眼中表達最高, 其次是腦(P<0.05), 其他組間沒有顯著差異(P>0.05);Elovl5在肌肉中表達最多,其次是眼(P<0.05), 其他組間沒有顯著性差異(P>0.05);Elovl7在卵巢中表達最高(P<0.05), 鰓、精巢和肌肉中表達較多(P<0.05), 其他組間沒有顯著差異(P>0.05)。
2.4 饑餓脅迫下達氏鱘Elovl4、Elovl5和Elovl7表達量的變化
在饑餓脅迫下, 達氏鱘Elovls在不同組織中的表達各有不同。饑餓7d時(圖 3A),Elovl4在腦、腸道和肌肉中的表達量顯著提高(P<0.05), 之后顯著下降(P<0.05); 饑餓0和1dElovl4在胃中的表達沒有顯著差異(P>0.05), 之后顯著下降, 14d時顯著上調(P<0.05); 肝臟中Elovl4在0時表達量最高, 隨后顯著下降(P<0.05), 其他組間沒有顯著性差異(P>0.05)。

圖 1 達氏鱘Elovl4、Elovl5和Elovl7與其他脊椎動物的系統發生樹Fig. 1 Phylogenetic tree of the Elovl4, Elovl5 and Elovl7 from other vertebrates based on neighbor-joining method
饑餓7d時(圖 3B),Elovl5在腦和肌肉中的表達量顯著提高(P<0.05), 之后顯著下降(P<0.05); 饑餓3d時Elovl5在胃中的表達量最低, 且顯著低于1d、7d和14d組; 肝臟中Elovl5表達量隨時間推移逐漸下降, 0時表達量顯著高于其他各組(P<0.05), 1d、3d和7d組間沒有顯著性差異(P>0.05), 14d表達量最低; 腸道中Elovl5表達量逐漸升高, 14d時顯著高于其他各組(P<0.05)。
Elovl7在腦和肌肉中的表達量先下降后在7d時顯著提高(圖 3C), 隨后顯著下調(P<0.05); 3d組Elovl7在胃中的表達量最低, 顯著低于0和14d組, 與1d和7d組間沒有顯著性差異(P>0.05),Elovl7在胃中的表達量在0時最高, 之后顯著下降(P<0.05), 其余各組間沒有顯著性差異(P>0.05); 肝臟中Elovl7表達量隨時間推移逐漸下降, 0時表達量顯著高于其他各組(P<0.05); 腸道中Elovl7表達量在0和14d時顯著高于其他各組(P<0.05), 其他組間沒有顯著性差異(P>0.05)。
3 討論
脂肪酸是魚類生長所必須的營養物質, 同時還具有重要的生理學功能。長鏈多不飽和脂肪酸(LC-PUFA), 主要包括二十碳五烯酸(EPA, 20:5n-3)、二十二碳六烯酸(DHA, 22:6n-3)和花生四烯酸(ARA, 20:4n-6)等, 對細胞膜的完整性和流動性、轉錄調控以及細胞信號轉導有重要作用[12]。Elovls作為合成長鏈脂肪酸的關鍵限速酶, 其重要性顯而易見。
3.1 達氏鱘Elovl4、Elovl5和Elovl7的組織表達差異
Elovl4在斑馬魚(Brachydanio rerio)[13]、軍曹魚(Rachycentron canadum)[14]、大西洋鮭(Salmo salar)[4]、河豚(Tetraodontidae)[15]和大黃魚(Larimichthys crocea)[16]等中都得到克隆, 斑馬魚中存在2個亞型,Elovl4a和Elovl4b, 分別編碼309和303個氨基酸[13], 西洋鮭[4]Elovl4編碼306個氨基酸, 而本研究結果顯示, 達氏鱘Elovl4僅編碼250個氨基酸, 說明在進化過程中鱘Elovl4 CDS區能編碼氨基酸數與其他魚類有較大的差異。Elovl4主要在哺乳動物視網膜、腦和精巢等脂質含量較多的組織中表達[6]。魚類與哺乳動物類似, 在大西洋鮭[4]的研究中發現,Elovl4主要在眼中表達; 軍曹魚[14]Elovl4主要在腦、眼和垂體中表達;Elovl4在斑馬魚上的2個亞型,Elovl4b主要在眼、卵巢和精巢中表達, 而Elovl4a除了在肌肉和脂肪組織中沒有檢測到表達信號以外,在其他組織中均有表達; 河豚[15]眼和腦中均能檢測到信號。結合本實驗結果發現, 達氏鱘Elovl4除了在眼中表達較多以外還在腦和卵巢中有較多的表達, 與前人的研究基本保持一致, 推測Elovl4與達氏鱘視覺發育和繁殖功能密切相關。
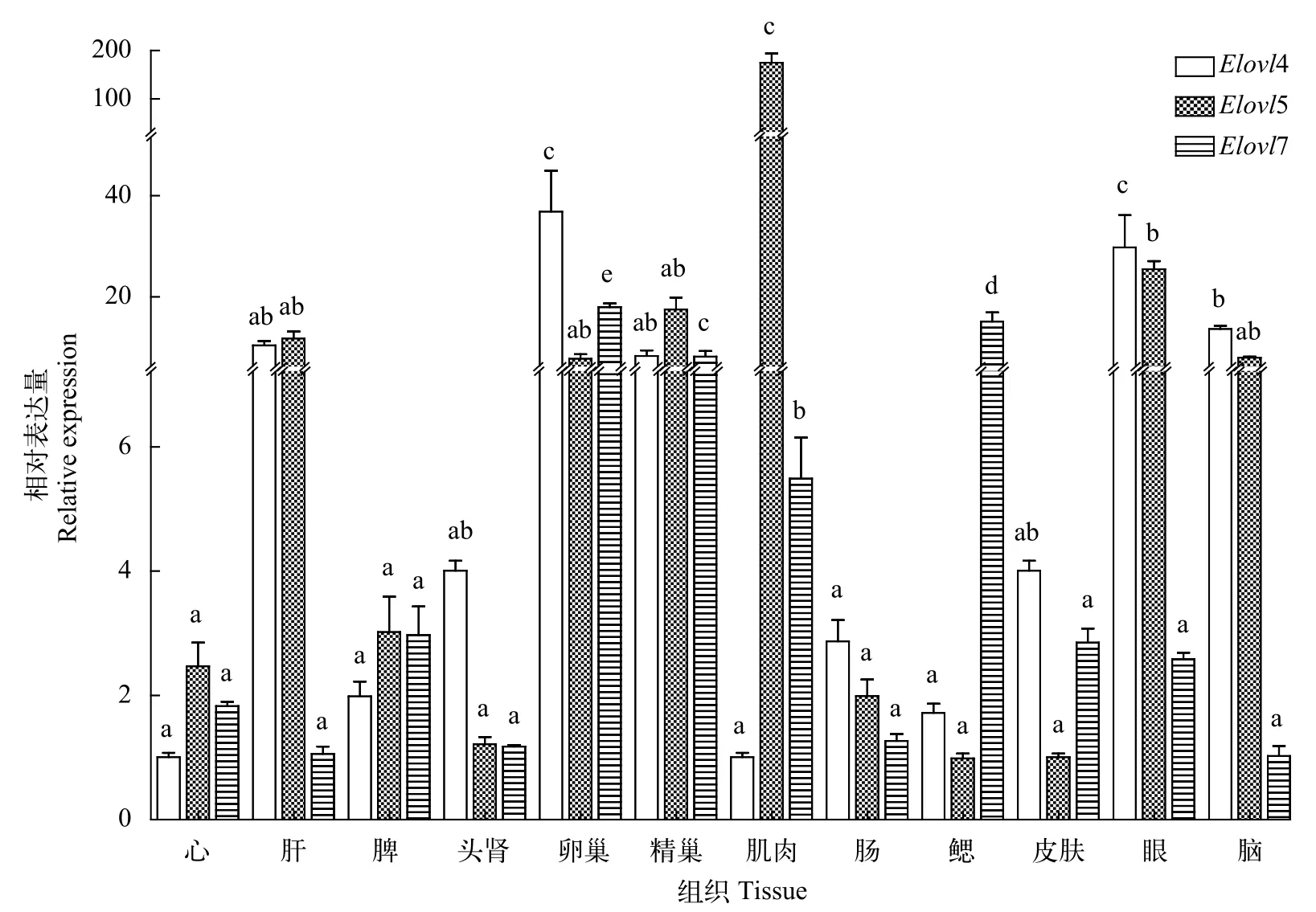
圖 2 不同組織中Elovl4、Elovl5和Elovl7 mRNA的相對表達量Fig. 2 The relative expression of Elovl4, Elovl5 and Elovl7 mRNA in different tissues
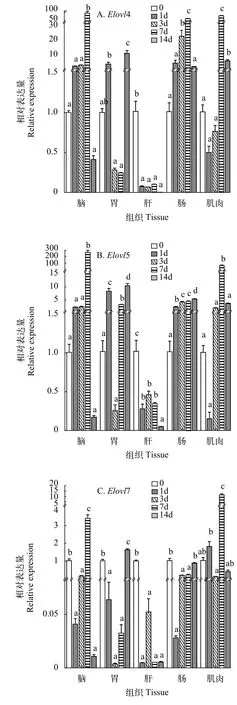
圖 3 饑餓脅迫下不同組織中Elovl4、Elovl5和Elovl7 mRNA的相對表達量Fig. 3 Effect of starvation on the relative expression of Elovl4,Elovl5 and Elovl7 mRNA in different tissues (n=9)
魚類Elovl5最先是在斑馬魚[17]上克隆得到, 可編碼氨基酸291個, 研究相繼發現河豚[15]、鏡鯉(Cyprinus carpio)[18]和銀無須魮(Puntius gonionotus)[19]Elovl5編碼291個, 雙棘黃姑魚(Nibea diacanthus)[20]、南方黑鮪(Thunnus maccoyii)[21]、日本鰻鱺(Anguilla japonica)[8]和軍曹魚[22]Elovl5編碼294個, 大西洋鮭[23]Elovl5有兩個亞型,Elovl5a編碼295個,Elovl5b編碼294個。本實驗達氏鱘Elovl5序列預測跨膜區為5個, 與軍曹魚[22]、河豚[15]和大西洋鮭[23]Elovl5b結果類似。不同種類的魚類Elovl5在組織中的表達存在差異, 但主要還是在腸道、肝臟和腦中表達。塞內加爾鰨(Solea senegalensis)[24]Elovl5在肝臟和腸道中表達較多, 而腦次之, 鰓、心臟、中腎和肌肉中未檢測出信號; 河豚[15]Elovl5主要在肝臟、腦、腸道和眼中表達; 軍曹魚[22]Elovl5在腦、肝臟和心臟中表達較多, 皮膚和鰓中沒有檢測到信號; 銀無須魮[19]Elovl5主要在肝臟和腸道中表達, 其次為腦和肌肉; 日本鰻鱺[8]Elovl5主要在腦、肝臟和腸道中表達較多; 雙棘黃姑魚[20]和大西洋鮭[23]主要在腸道和肝臟中表達。達氏鱘Elovl5在肌肉和眼中表達較多, 腦和肝臟次之, 與其他魚類上的研究基本類似, 可能是由于實驗所用達氏鱘正處于生長發育重要時期, 其肌肉中脂肪代謝活動旺盛,這與本實驗室之前對脂肪酸結合蛋白的研究結果相一致(數據未發表)。另外, 這也暗示Elovl5對達氏鱘視覺的發育有密切聯系。
目前對Elovl7的研究較少, 研究發現橙泥蟹(Scylla olivacea)[25]Elovl7編碼350個氨基酸, 蘇太豬(Sus)[26]Elovl7編碼281個氨基酸, 雞(Gallus gallus)[27]Elovl7編碼279個氨基酸。牛(Bovine)Elovl7在腎臟中表達較多, 在肌肉、胃和肝臟中較少[28],Elovl7在30周齡雞十二指腸、腺胃、腎臟和肺中表達較多[27]; 橙泥蟹Elovl7, 在胃中表達最高, 其次是腸道和鰓[25]。本實驗結果顯示, 達氏鱘Elovl7主要在卵巢、鰓、精巢和肌肉中表達, 這與哺乳動物還是存在差異的, 但與橙泥蟹類似的是在鰓中的表達相對較高, 說明Elovl7在水生動物的鰓中發揮了一定作用, 但具體原因還有待研究。水生動物中對Elovl7的報道較少, 在哺乳動物上已有證明Elovl7與前列腺腫瘤細胞的生長有關[27], 在僅有的研究中發現它可能在脂肪細胞分化的過程中出發脂質積累[30], 而Elovl7在達氏鱘脂肪代謝中的作用和功能還有待進一步研究。
3.2 饑餓對達氏鱘Elovl4、Elovl5和Elovl7表達差異的影響
一般來說, 魚類自身不能或僅少量合成n-3和n-6系列不飽和脂肪酸, 主要通過外界攝取獲得, 淡水魚類的必需脂肪酸主要包括亞油酸(18﹕2n-6)、α-亞麻酸(18﹕3n-3)、γ-亞麻酸(18﹕3n-6)[31]。禁食可以提高肝臟的分解代謝率, 反映了生存所需儲備的調動[32]。肝臟是脂肪酸合成的重要部位[33], 在禁食的條件下, 不飽和脂肪酸攝入減少, Elovls底物減少,導致Elovls合成下降, 這或許可以解釋肝臟中的Elovl4、Elovl5和Elovl7轉錄水平隨時間的增加直線下降的現象。
腦是調節動物生長和發育的重要中樞系統, 肌肉反映生長狀況的重要組織, 而魚類的腦和肌肉中含有豐富的不飽和脂肪酸[34]。禁食過程中的魚類對脂肪酸的代謝, 一般先從飽和脂肪酸開始, 其次是低不飽和脂肪酸, 最后才動用高不飽和脂肪酸[35,36]。這或許是達氏鱘饑餓第7天時腦和肌肉組織中Elovl4、Elovl5和Elovl7的轉錄水平顯著提高的原因之一, 由于饑餓后期高不飽和脂肪酸水平下降,Elovl4、Elovl5和Elovl7轉錄水平上調, 之后可能由于底物減少使其轉錄水平下降; 這也暗示腦與肌肉中的脂質代謝不同于肝臟。另外, 黃紅麗等[37]對大黃魚的研究發現, 饑餓使大黃魚肌肉組織中I-FABPb表達量先上調后下降, 這與本實驗中的結果相一致。
長期的饑餓能顯著影響魚類消化器官的組織結構[36], 其結構的改變必然引起功能的障礙。胃腸道是食物消化和吸收的重要場所, 尤其是腸道, 承載著消化和吸收雙重功能, 并通過腸道絨毛結構增大吸收面積, 其上皮細胞的形成及其流動性都與不飽和脂肪酸密切相關。本實驗的結果顯示, 達氏鱘胃Elovl4、Elovl5和Elovl7三個基因在饑餓3d時均有顯著的下調, 表明饑餓對達氏鱘胃組織LC-PUFA合成可能存在抑制作用。另外, 我們還發現, 在饑餓條件下Elovl4、Elovl5和Elovl7在達氏鱘腸道中的表達趨勢完全不同, 在饑餓1d、3d和7d時Elovl4和Elovl5 mRNA水平于對照組相比呈現增加的趨勢, 而Elovl7 mRNA水平卻顯著下降, 在一定程度上也表明了脂質代謝平衡調節過程復雜[38], 3個基因在腸道中有不同的功能, 具體原因有待進一步研究。
綜上所述, 本研究首次克隆了達氏鱘Elovl4、Elovl5和Elovl7 CDS序列, 并分析了其組織分布和在饑餓脅迫下的表達模式, 發現Elovl4、Elovl5和Elovl7在達氏鱘視覺、腦、性腺以及肌肉的發育與生長過程中可能發揮著重要的作用。研究還發現饑餓脅迫對不同組織中的Elovls作用不同, 能顯著影響達氏鱘Elovl4、Elovl5和Elovl7 mRNA的轉錄水平, 產生差異的原因可能與其主要分布部位以及所參與合成的LC-PUFA功能有關, 具體原因還有待研究, 但能肯定的是饑餓應激能顯著影響肝臟的脂質代謝, 并且可能通過降低Elovl4、Elovl5和Elovl7轉錄來抑制LC-PUFA合成。

