新型冠狀病毒肺炎治療過程中糖皮質激素的應用(附2例報告)
廖付軍,鮑海龍,李潔琪,吳葉婷,楊京,李偉
1 貴州醫科大學附屬醫院,貴州貴陽550004;2 貴黔國際總醫院
2019年12月以來,湖北省武漢市部分醫院陸續發現了多例有華南海鮮市場暴露史的不明原因肺炎病例,現已證實為2019新型冠狀病毒(2019-nCoV)感染引起的急性呼吸道傳染病,即新型冠狀病毒性肺炎(COVID-19)。COVID-19疫情在我國范圍內迅速蔓延,并引發嚴重的公共衛生事件。截至2020年2月29日,我國已確診的COVID-19患者累計達79 251例,其中重癥患者達7 664例,死亡患者達2 835例[1]。新英格蘭醫學雜志納入中國1 099例COVID-19患者對人口統計學特點及臨床特征進行分析,結果表明COVID-19癥狀、影像學特點以及疾病的嚴重程度呈現多樣性,入院時發熱占比僅為43.8%,20.8%的患者入院時未見影像學改變,這給診療過程帶來很高的難度;另外發現其中204例(18.6%)患者接受了糖皮質激素治療,在重癥患者中的比例(44.5%)高于非重癥患者(13.7%),在這204例患者中,有33例(16.2%)進入ICU,17例(8.3%)接受有創通氣治療,5例死亡(2.5%)[2]。而目前國內對于糖皮質激素在COVID-19治療過程中的應用存在爭議,部分專家考慮糖皮質激素的不良反應及治療COVID-19療效的不確定性,對其持保守態度;相反,部分專家認為糖皮質激素已廣泛應用于嚴重感染治療,早期應用可影響重癥肺炎的發生發展,提高治愈率、降低死亡率,對其持開放態度。本研究在觀察糖皮質激素治療效果的同時,結合2例患者的用藥情況探討新型冠狀病毒肺炎治療過程中糖皮質激素的用藥時機、療程、劑量及不良反應等,現報告如下。
1 臨床資料
2020年1月30日,貴州醫科大學附屬醫院感染科隔離病房收治的COVID-19患者2例,為兩姊妹,分別編號為患者A(妹妹)、患者B(姐姐)。
患者A,女,53歲,因“咳嗽、咳黃綠色膿痰2 d”入院。自述長期居住武漢,1月21日返回貴陽探親,1月28日無明顯誘因出現咳嗽、咳痰,無發熱及呼吸困難,未自行服藥。1月30日首次在貴州醫科大學附屬醫院發熱門診就診,考慮其流行病學史,為進一步診治,于同日入院接受治療。患者有高血壓病史3年、糖尿病病史1年,否認食用野味,未去過華南海鮮市場。入院體格檢查結果顯示:體溫37.1 ℃,心率108次/分,心律齊無雜音,血壓160/86 mmHg,咽不紅,扁桃體無腫大,雙下肺可聞及少量濕啰音。血常規檢查顯示:白細胞(WBC)5.59×109/L,中性粒細胞(N)絕對值4.08×109/L,淋巴細胞(L)絕對值0.97×109/L。首次肺部CT檢查提示患者右下肺感染。
患者B,女,61歲,因“發熱、咳嗽1 d”入院。自述長期居住武漢,1月21日返回貴陽探親,1月29日無明顯誘因出現咳嗽,呈干咳無痰,發熱,最高體溫37.8 ℃,伴腹瀉,無呼吸困難,未自行服藥。1月30日在貴州醫科大學附屬醫院發熱門診就診,考慮其流行病學史,為進一步診治,于同日入院接受治療。患者無其他疾病史,否認食用野味,未去過華南海鮮市場。入院體格檢查結果顯示:體溫38 ℃,心率91次/分,心律齊無雜音,血壓153/74 mm Hg,咽不紅,扁桃體無腫大,右下肺可聞及少量濕啰音。血常規檢查顯示:WBC 11.2×109/L,N絕對值8.94×109/L,L絕對值2.07×109/L。首次肺部CT檢查結果顯示:右下肺見多發片狀磨玻璃高密度影,邊界不清,考慮感染病變;右肺上葉、左肺下葉結節,右肺中葉、左肺上葉纖維化灶。
2 治療方法及結果
患者A入院第1天檢查結果顯示:降鈣素原0.02 ng/mL、血沉27 mm/h、血糖7.3 mmol/L、CRP 1.65 mg/L,余血常規、大小便常規、肝腎功、凝血、心肌酶學及心肌標志物檢查未見明顯異常,甲流、乙流病毒核酸檢測陰性,胸部CT平掃見右下肺感染(圖1a)。給予吸氧、頭孢孟多酯抗感染、重組人干擾素α1b霧化吸入、利巴韋林靜滴抗病毒等治療方案,采集咽拭子予2019-nCoV核酸檢查。入院第3天,患者出現呼吸困難,咳嗽咳痰癥狀較前加重,并出現體溫升高至38.0 ℃,復查胸部CT見雙肺斑片滲出影較前明顯增加(圖1b),兩次2019-nCoV核酸檢查結果均呈陽性,血氣分析提示氧分壓69.7 mm Hg、二氧化碳分壓47.2 mm Hg。加用洛匹那韋/利托那韋、鹽酸阿比多爾片及胸腺法新抗病毒,血必凈清熱解毒及抗全身炎癥反應,甲強龍40 mg靜脈滴注抗炎,免疫球蛋白沖擊治療,頭孢孟多酯升級為莫西沙星抗感染,并予以無創呼吸機輔助呼吸。入院第6、7天,患者無明顯呼吸困難,氧分壓108 mm Hg,二氧化碳分壓42.9 mm Hg。復查胸部CT,結果顯示雙肺滲出影較前增高、密度較前增高、部分病灶較前減少(圖1c)。入院第8~10天,患者呼吸困難癥狀逐漸緩解,體溫降至37.3 ℃以下,復查胸部CT,結果顯示雙肺滲出影較前略有吸收(圖1d)。入院第11~14天,患者呼吸困難、咳嗽癥狀較前明顯緩解,2019-nCoV核酸檢測第1次轉陰,停用甲強龍,復查肺部CT,結果顯示雙肺滲出影較前減少(圖1e)。入院第16天,復查胸部CT見病灶明顯吸收(圖1f),兩次2019-nCoV核酸檢測轉陰,無發熱,達到第六版新冠肺炎診治指南出院標準,予以出院。

圖1 患者A不同時間點胸部CT影像
患者B入院第1天檢查結果顯示:降鈣素原<0.02 ng/mL、血沉22 mm/h、血糖6.52 mmol/L,CRP 17.38 mg/L,余血常規、大小便常規、肝腎功、凝血、心肌酶學及心肌標志物檢查未見明顯異常,甲流、乙流病毒核酸檢測陰性,胸部CT平掃見右下肺見多發片狀磨玻璃高密度影,邊界不清,右肺上葉、左肺下葉結節,右肺中葉、左肺上葉纖維化灶(圖2a)。給予吸氧、頭孢孟多酯抗感染、重組人干擾素α1b霧化吸入抗病毒、利巴韋林靜滴等治療,采集咽拭子予2019-nCoV核酸檢查。入院第3天,患者出現呼吸困難、咳嗽咳痰癥狀較前加重,并出現體溫升高至38.5 ℃,復查胸部CT見雙肺滲出影較前明顯增加(圖2b),兩次2019-nCoV核酸檢查結果均呈陽性,血氣分析提示氧分壓53.4 mm Hg、二氧化碳分壓43.6 mm Hg,加用洛匹那韋/利托那韋、鹽酸阿比多爾片及胸腺法新抗病毒,血必凈清熱解毒及抗全身炎癥反應,甲強龍40 mg靜脈滴注抗炎,免疫球蛋白沖擊治療,頭孢孟多酯升級為莫西沙星抗感染,沙丁胺醇、乙酰半胱氨酸霧化吸入,并予以無創呼吸機輔助呼吸。入院第6、7天,患者無創呼吸機輔助下氧分壓72.3 mm Hg、二氧化碳分壓40 mm Hg,復查胸部CT,結果顯示雙肺滲出較前進展、部分病灶較前減少(圖2c)。在治療2 d后,因患者本人考慮激素的不良反應,拒絕使用甲強龍抗炎,遂停止使用。入院第8~15天,患者在無創呼吸機輔助呼吸下仍感呼吸困難,血氣分析提示氧分壓59.2 mm Hg、二氧化碳分壓46.7 mm Hg,經ICU醫生會診后轉入ICU隔離治療,并進行氣管插管,予以有創呼吸機輔助呼吸,并在之前治療基礎上繼續使用甲強龍40 mg靜脈滴注進行抗炎治療。入院16~20天,患者血氣分析提示氧分壓94.8 mm Hg、二氧化碳分壓44.6 mm Hg,復查胸部CT,結果顯示雙肺滲出較前略有吸收(圖2d),予以脫機并轉出ICU。入院第21~24天,患者呼吸困難癥狀明顯緩解,體溫恢復正常,2019-nCoV核酸檢測第1次轉陰,減量并逐漸停用甲強龍,復查肺部CT,結果顯示雙肺滲出較前減少(圖2e),并予以加用磷酸氯喹片口服。入院第25天復查胸部CT,結果顯示病灶明顯吸收(圖2f),兩次2019-nCoV核酸檢測轉陰,無發熱,達到第六版新冠肺炎診治指南出院標準,予以出院。
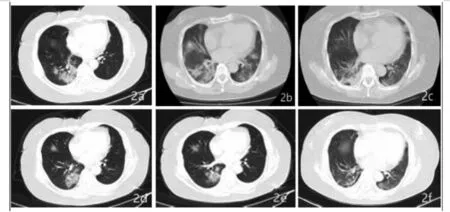
圖2 患者B不同時間點胸部CT影像
3 討論
本研究中兩例患者同時發病,具有典型聚集發病特點,同時具備COVID-19典型影像學特點,參照第六版新冠肺炎診療指南,入院時均考慮為普通型患者[3],同時使用指南推薦的抗病毒藥物治療,包括α-干擾素霧化吸入、洛匹那韋/利托那韋口服、利巴韋林靜脈滴注等,并同時使用了糖皮質激素甲強龍40 mg靜脈滴注抗炎。整個診治過程中,患者A(妹妹)使用甲強龍后未再繼續出現進展惡化情況,而患者B(姐姐)在使用2 d后因考慮激素的不良反應停止使用,隨后出現病情迅速進展惡化,轉入ICU行呼吸機輔助呼吸等生命支持,直至繼續使用糖皮質激素后病情逐漸趨向穩定,撤除呼吸機后轉出ICU至康復出院。A和B患者均是在呼吸頻率增快、有呼吸困難癥狀、血氣分析提示氧分壓明顯下降情況下使用激素治療,且使用的是40 mg小劑量甲強龍治療。當然,出現兩種結局,也可能與患者B(姐姐)開始肺部感染較患者A(妹妹)嚴重有一定的關系,這一點可從初始入院時肺部CT檢查結果得到證實。最新國內指南指出,目前對抗病毒藥物多種聯合使用無確切有效的證據,反而因多種病毒藥物的不良反應而對患者產生不利影響,因此不做常規推薦。對于激素的使用,指南指出,當出現肺內滲出增加、低氧血癥進一步加重、各類細胞因子明顯上升、患者向危重型轉變跡象的時候,可酌情小劑量使用激素1~2 mg/kg,使用時間3~5 d[4]。
新冠肺炎病毒顆粒可吸附在呼吸道黏膜,并在擴散后感染其他細胞,在體內誘發一系列細胞免疫反應,引起外周血白細胞、淋巴細胞、巨噬細胞等免疫細胞變化,產生各種細胞因子,包括白細胞介素(IL)、干擾素、腫瘤壞死因子(TNF)超家族、集落刺激因子、趨化因子、生長因子等,其中一部分細胞因子促進炎癥激活,導致炎癥反應,這一炎癥反應綜合征被稱為細胞因子風暴[5]。新冠肺炎病毒感染后,一般可通過機體免疫反應清除病毒,但失控的、過度的免疫級聯反應反而對人體組織和器官造成傷害,部分患者出現急性呼吸窘迫綜合征和感染性休克,最終導致多器官功能衰竭,出現死亡。因此,因糖皮質激素具有很強的抗炎癥反應和免疫抑制作用,而被廣泛應用于新冠肺炎患者的臨床治療。但Lancet近期發表的一篇文章質疑使用糖皮質激素治療新冠肺炎的效果,因為目前沒有確切的證據表明患者獲益[6],該文章的發表為激素的使用蒙上一層陰影,因此我們國家專門為糖皮質激素的使用發布了專家共識[7],認為糖皮質激素的適應癥應為:年齡≥18歲;新型冠狀病毒感染核酸檢測陽性;癥狀(包括發熱、咳嗽或其他相關感染癥狀)發生10 d以內,影像學證實為肺炎且快速進展;靜息未吸氧狀態下,患者血氧飽和度(SpO2)≤93%或呼吸急促(呼吸頻率≥30次/分鐘)或氧合指數≤300 mm Hg。
目前對病毒性肺炎的病理生理改變過程,一般認為分為三個時相:第一時相,即病毒侵入及復制階段,冠狀病毒在感染者體內迅速復制,引起高熱和流感癥狀,也可以稱作為病毒血癥時期;第二時相,機體過度免疫反應階段,此階段會釋放大量細胞因子,形成細胞因子風暴;第三時相,炎癥反應或者炎癥風暴導致機體組織損傷階段,因失控的免疫反應導致炎癥介質大量釋放,損害機體及器官組織[5]。因此,從病理生理角度的發展規律來理解激素的治療時機,我們認為應該在第二時相和第三時相比較合適。在病毒復制的第一時相內使用激素可能對患者并沒有獲益,反而因激素的不良反應而帶來危害。從藥理機制看,糖皮質激素是抑制第二時相及第三時相的藥物,可用于病毒性肺炎的治療。糖皮質激素抗炎作用強,但不良反應也很明顯,它雖然可抑制炎癥,但也抑制了免疫反應和人體免疫系統對于病毒的清除作用,同時長期使用糖皮質激素導致股骨頭壞死、糖尿病、消化道出血、二重感染、結核播散、電解質紊亂等,并留下后遺癥,既往SARS期間多有報道,近期也有病例報道糖皮質激素在新型冠狀病毒肺炎使用后出現糖尿病[8]。因此,糖皮質激素是一把“雙刃劍”,我們該慎重對待使用激素,參照指南結合患者實際情況正確合理使用這把“雙刃劍”。
綜上所述,在COVID-19治療過程當中,當肺部炎癥、低氧血癥進一步加重,有向危重型轉變的時候,可考慮使用小劑量糖皮質激素。

