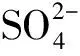用雙功能性離子液體[A336][P204]從硫酸體系中萃取鉬
劉 泉,陸明杰,汪慧剛,于立策,徐紅娟,彭逸超,錢鋮镕,楊華玲
(南通大學 化學化工學院,江蘇 南通 226019)
從酸性溶液中提取鉬有萃取法、沉淀法、離子交換法、活性炭吸附法、液膜分離法等[1-8]。其中,溶劑萃取法因處理量大、反應速度快、分離效果好等優點而廣受關注。萃取劑是影響萃取效果的關鍵因素之一。傳統的有機胺類萃取劑、酸性磷萃取劑和中性磷萃取劑都可以選擇性地從酸性溶液中萃取鉬,但存在萃取劑易流失、選擇性低等問題。近年來,室溫離子液體在金屬萃取領域中的應用得到廣泛研究[9-13]。含有官能團的功能性離子液體中,官能團的可設計性使得制備對某種金屬有較好選擇性的萃取劑成為可能,也為解決傳統萃取工藝中存在的問題帶來了契機。試驗研究了用雙功能性離子液體[A336][P204]作萃取劑,從硫酸體系中萃取鉬;并通過與傳統的有機酸萃取劑磷酸二異辛酯(P204)及中性磷萃取劑磷酸三丁酯(TBP)的萃取能力對比,考察其對鉬的萃取性能,以期為鉬的萃取分離提供一種新方法。
1 試驗部分
1.1 主要試劑及儀器
TBP、P204,純度均大于95%,洛陽市奧達化工有限公司產品;硫酸、正庚烷、硫氰酸鉀、硫脲、異丙醇,分析純,國藥集團化學試劑有限公司產品。
[A336][P204]:根據文獻[11]提供的酸堿中和法制備,工藝路線如圖1所示。
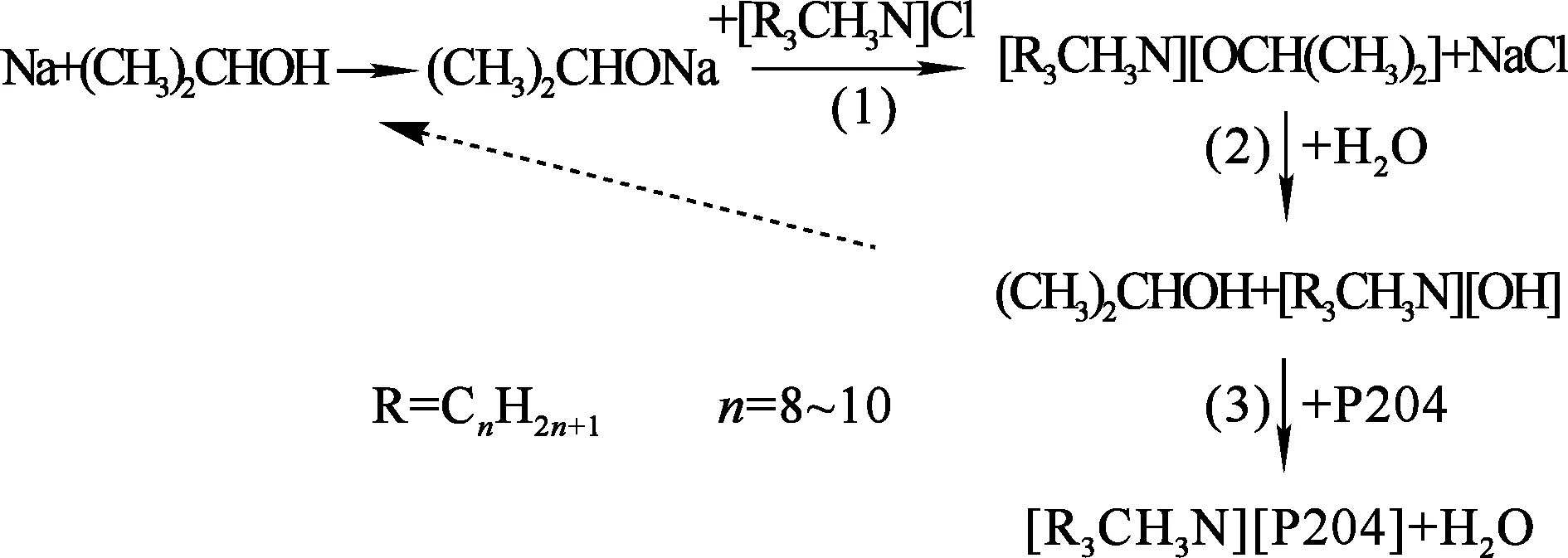
圖1 酸堿中和法制備功能性離子液體[A336][P204]的工藝路線
可見分光光度計(V-1200型),上海美普達儀器有限公司;雷磁pH酸度計(pHS-3C型),上海榮宣儀器有限公司。
1.2 試驗原理及方法
有機相:[A336][P204]、P204和P204+TBP(1/1)為萃取劑,正庚烷為稀釋劑。
水相:一定濃度的鉬酸鈉溶液。
采取控制變量法,通過改變水相酸度、水相鹽濃度、萃取時間、萃取劑濃度考察鉬的萃取效果。有機相與水相按等體積充分混合,振蕩一定時間后離心,兩相分離完全后,采用銅離子催化還原硫氰酸鹽分光光度法測定萃余水相中鉬質量濃度[14],采用質量平衡法計算有機相中鉬濃度,并計算鉬萃取率(E)。
2 試驗結果與討論
2.1 溶劑萃取
2.1.1 萃取時間對Mo(Ⅵ)萃取率的影響
萃取劑濃度0.1 mol/L,水相中鉬濃度0.4 mmol/L,水相pH=2.12,鹽析劑Na2SO4濃度0.07 mol/L,萃取時間對鉬萃取率的影響試驗結果如圖2所示。
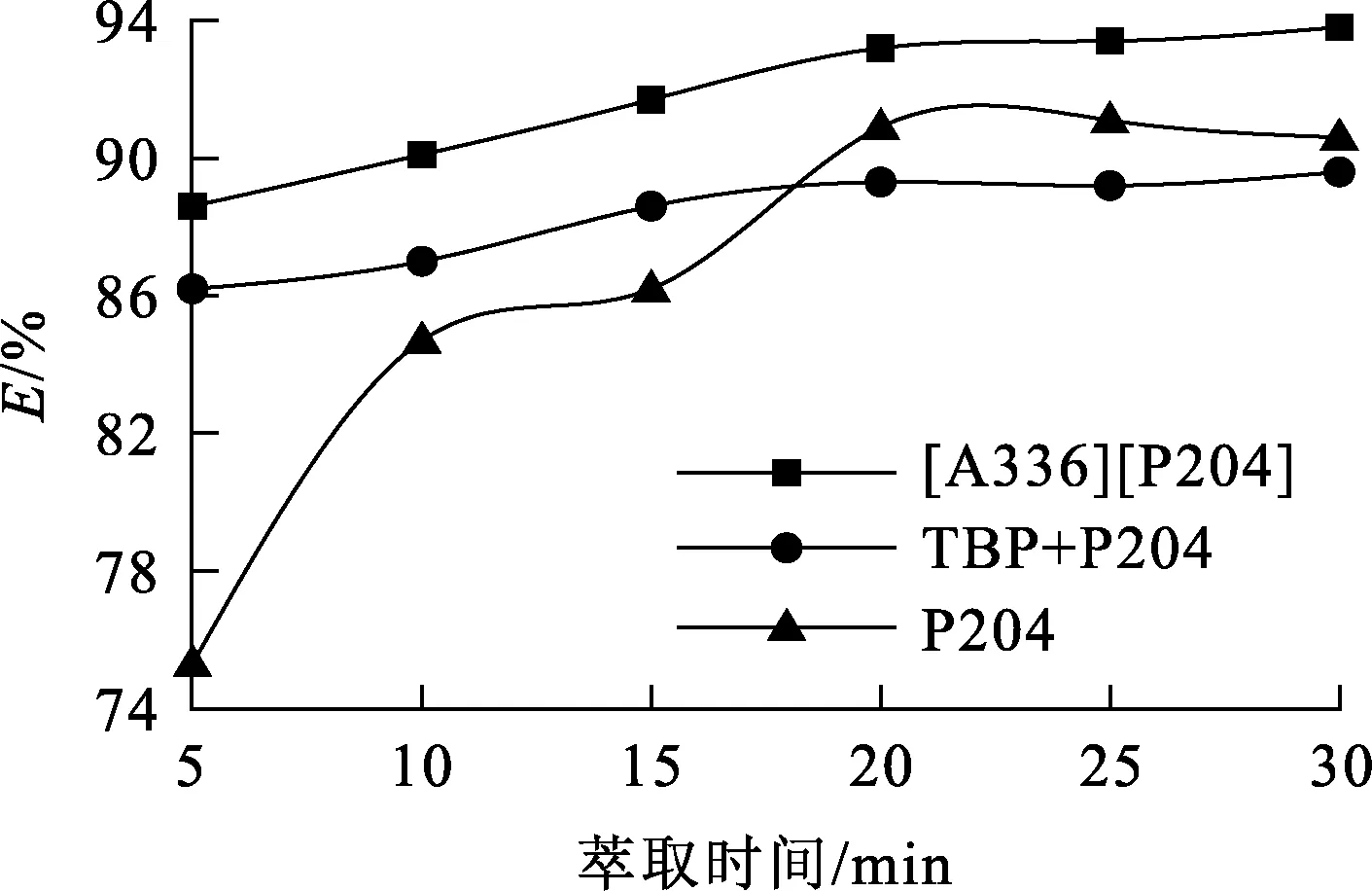
圖2 萃取時間對Mo(Ⅵ)萃取率的影響
由圖2看出:3種萃取劑均隨萃取時間延長,對鉬萃取率升高;[A336][P204]對鉬的萃取能力高于P204和TBP+P204的萃取能力;萃取15 min后,[A336][P204]對鉬萃取率基本不再變化。綜合考慮,確定萃取時間以15 min為宜。
2.1.2 水相酸度對鉬萃取率的影響
萃取劑濃度0.1 mol/L,水相中鉬濃度0.4 mmol/L,鹽析劑Na2SO4濃度0.07 mol/L,萃取時間15 min,水相酸度對鉬萃取率的影響試驗結果如圖3所示。
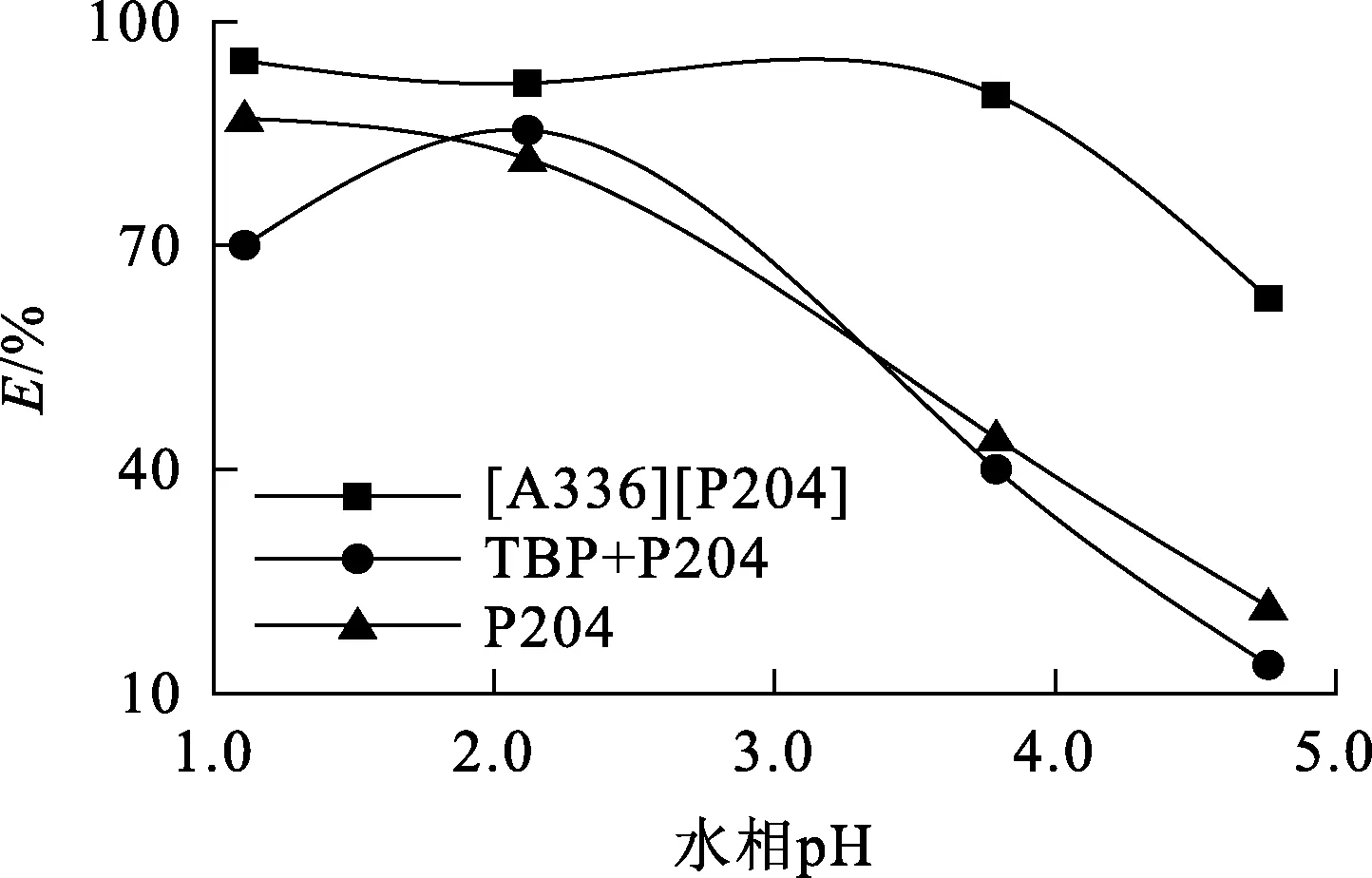
圖3 水相pH對Mo(Ⅵ)萃取率的影響
由圖3看出:水相pH較低條件下,離子液體[A336][P204]體系對Mo(Ⅵ)的萃取率變化不大;pH大于4時,鉬萃取率下降明顯。
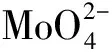
P204體系、P204+TBP協萃體系萃取Mo(Ⅵ)過程中會釋放一定量H+,使體系pH總是低于萃取前的水相pH;而離子液體[A336][P204]體系中,水相pH在萃取前后變化不大。由圖3看出:隨溶液pH升高,P204體系和P204+TBP協萃體系對Mo(Ⅵ)萃取率都明顯下降;而離子液體[A336][P204]體系中,水相pH在較低范圍內變化時,對Mo(Ⅵ)萃取率影響不大,水相pH升至4.0之后,Mo(Ⅵ)萃取率才呈下降趨勢。
2.1.3 鹽析劑濃度對Mo(Ⅵ)萃取率的影響
雙功能性離子液體[A336][P204]萃取鉬時會產生乳化現象,造成分相困難,影響萃取過程進行。以Na2SO4為鹽析劑,加入到水相中可有效緩解乳化現象發生。
萃取劑濃度0.1 mol/L,萃取時間15 min,水相鉬濃度0.4 mmol/L,水相pH=2.12,鹽析劑Na2SO4濃度對鉬萃取率的影響試驗結果如圖4所示。
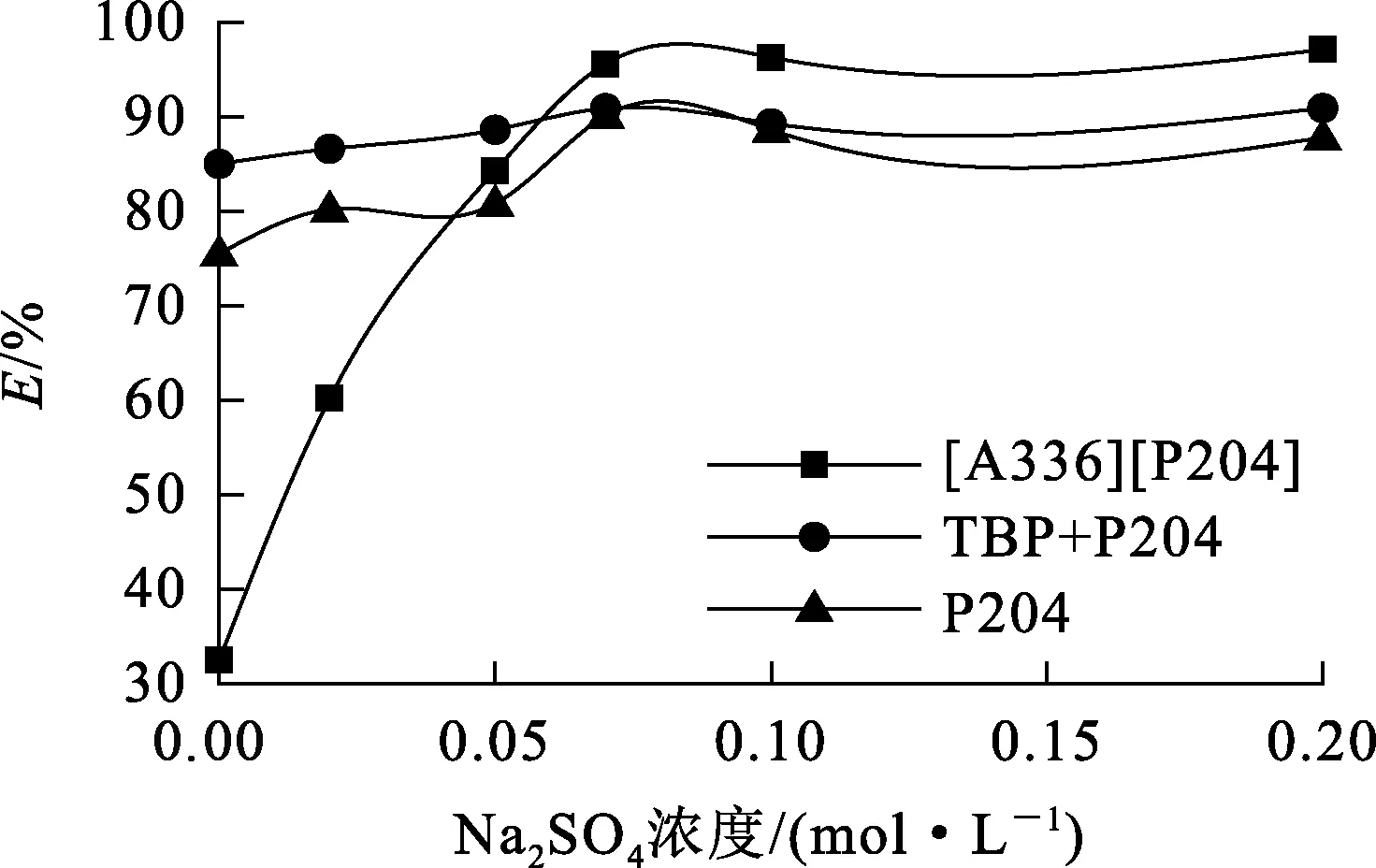
圖4 Na2SO4濃度對Mo(Ⅵ)萃取率的影響
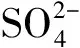
2.1.4 萃取劑濃度對Mo(Ⅵ)萃取率的影響
水相鉬濃度0.4 mmol/L,萃取時間15 mim,水相pH=2.12,鹽析劑Na2SO4濃度0.07 mol/L,有機相中萃取劑濃度對鉬萃取率影響試驗結果如圖5所示。
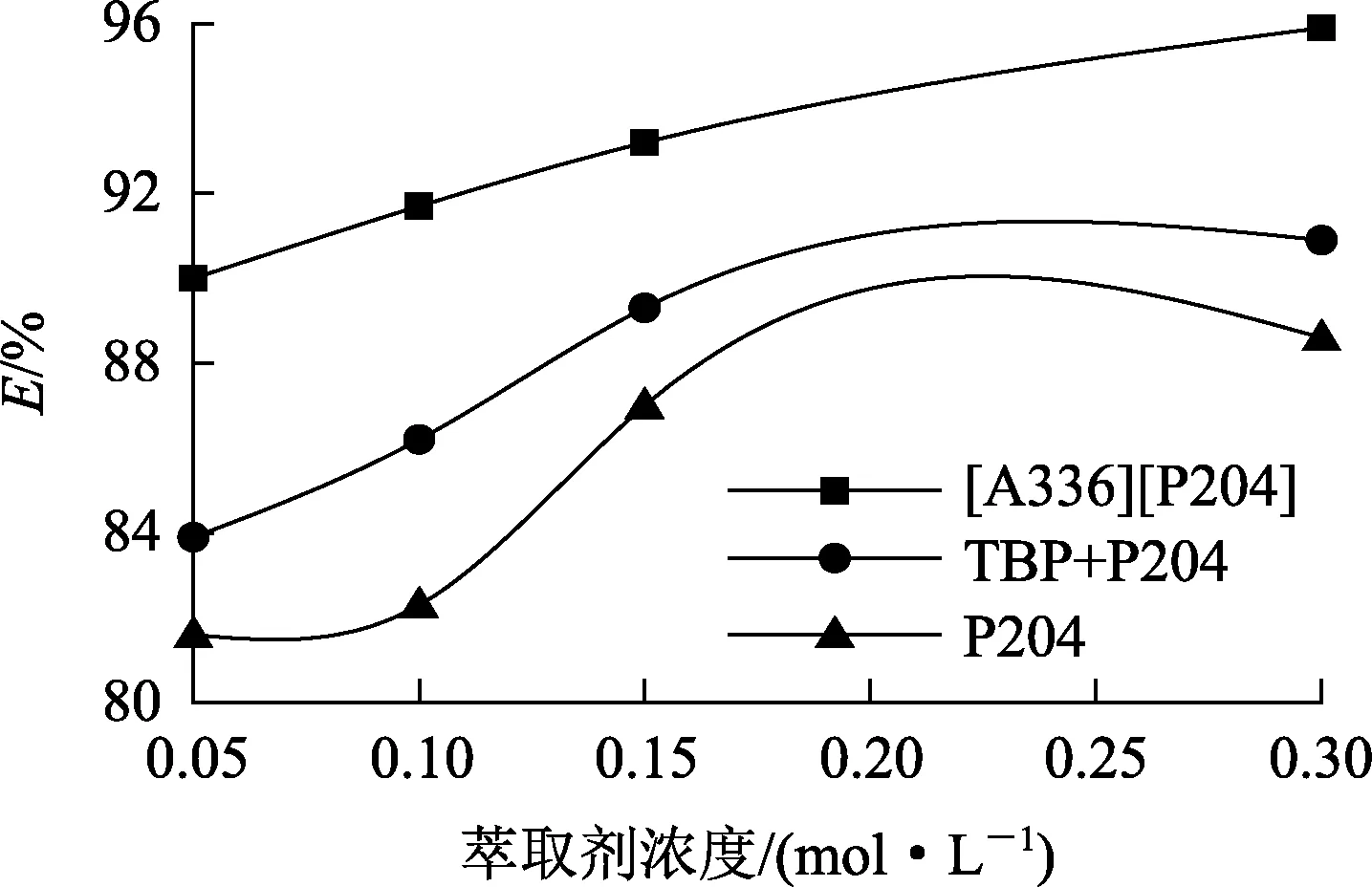
圖5 萃取劑濃度對Mo(Ⅵ)萃取率的影響
由圖5看出:3個萃取體系中,隨萃取劑濃度增大,Mo(Ⅵ)萃取率都提高;而離子液體[A336][P204]對Mo(Ⅵ)的萃取能力明顯強于其他2個萃取體系。
Mo(Ⅵ)濃度對[A336][P204]萃取鉬的影響試驗結果見表1。
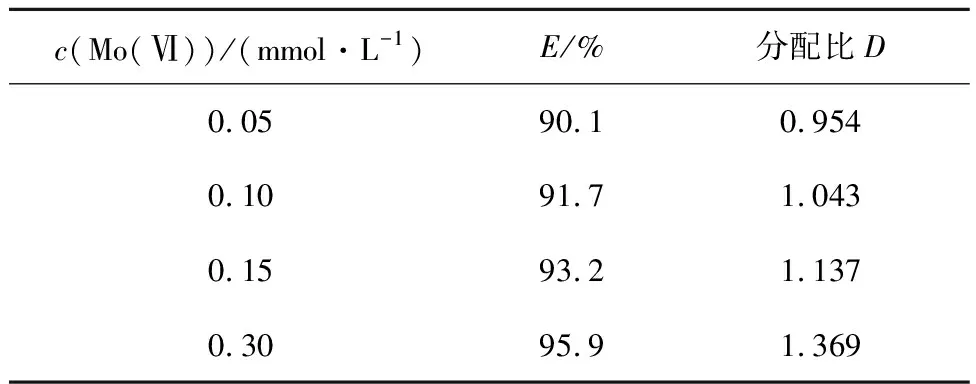
表1 Mo(Ⅵ)濃度對[A336][P204]萃取鉬的影響
根據斜率法,以lg[Mo(Ⅵ)]對lgD繪制關系曲線,結果如圖6所示。可以看出,曲線斜率為0.52,可以推測1個[A336][P204]分子可與2個鉬離子結合。離子液體[A336][P204]對鉬的萃取機制尚未見文獻報道,根據試驗數據,不能給出具體的萃取方程式,詳細的萃取機制還需進一步研究。
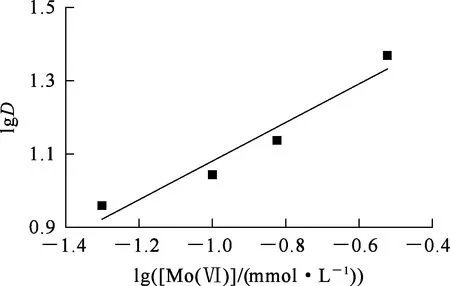
圖6 lg[Mo(Ⅵ)]與lgD之間的關系
2.2 反萃取
直接利用碳酸銨溶液從負載有機相中反萃取鉬,3個萃取體系雖都有很好的反萃取效果,但有機相再生循環使用的后續處理較復雜。因此,試驗采用不同濃度硫酸溶液反萃取,再生有機相可循環使用。不同酸度硫酸溶液對鉬反萃取的影響試驗結果如圖7所示。
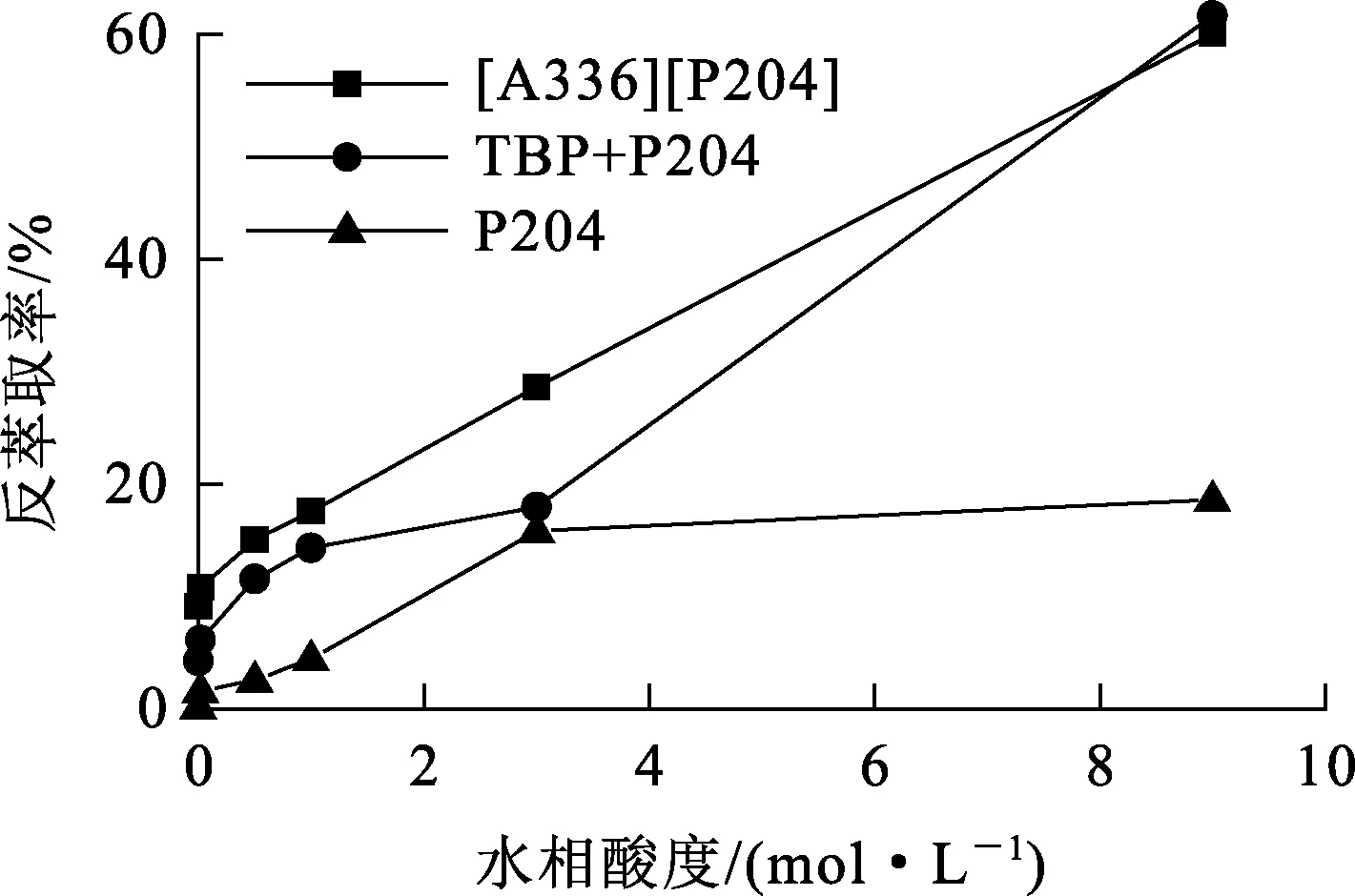
圖7 水相酸度對Mo(Ⅵ)反萃取的影響
由圖7看出:相同條件下,隨硫酸濃度增大,3個萃取體系的鉬反萃取率都逐漸提高,而TBP+P204協萃體系和[A336][P204]體系的反萃取率提高幅度更大;相較于TBP+P204和P204萃取體系,[A336][P204]體系對鉬的反萃取效果更好。
3 結論