單胎妊娠中新鮮胚胎移植妊娠與自然妊娠的圍產期并發癥及新生兒出生結局比較
黃麗棉,李柳銘,張昭
(1.廣西百色市人民醫院,百色 533000;2.廣西醫科大學第一附屬醫院,南寧 530000;3.廣西醫科大學,南寧 530000)
體外受精-胚胎移植(IVF-ET)技術已逐漸成為治療不孕不育患者的重要手段[1],但是該技術給不孕不育家庭解決生育難題的同時,也會帶來一定的隱患。Cavoretto等[2]認為體外受精/卵胞漿內單精子注射-胚胎移植(IVF/ICSI-ET)后單胎妊娠的早產、圍產期死亡率、妊娠期高血壓疾病等風險高于自然妊娠;但Vasario等[3]卻提出不同觀點,指出IVF/ICSI-ET組與自然妊娠組之間母親的圍產期并發癥發病率相似,且新生兒出生體重及畸形率未觀察到顯著差異。IVF/ICSI-ET術后的母兒結局及安全性尚存在爭議[4-5]。IVF/ICSI-ET技術對母體及子代安全性的影響也逐漸成為了當今生殖醫學領域所關注的焦點之一。圍產期主要并發癥及新生兒不良出生結局的發生,給社會帶來嚴重的經濟負擔,以及給患者的家庭帶來不良影響,因此,生殖領域的學者在關注如何提高妊娠率的同時,也不能忽略IVF/ICSI-ET技術對母體及子代安全性的影響[6]。我們采取回顧性分析的方式,比較單胎妊娠中新鮮胚胎移植妊娠與自然妊娠孕產婦圍產期主要并發癥及新生兒出生結局的差異,旨在為預防和減少IVF-ET術后母兒不良結局提供理論依據和數據支持。
一、資料與方法
1.研究對象:2011年1月至2019年11月在百色市人民醫院產科分娩的單胎妊娠孕產婦。排除有不良孕產史及多囊卵巢綜合征或子宮異常(如苗勒氏管異常、子宮腺肌病、粘膜下肌瘤、宮腔粘連、疤痕子宮)的婦女、有與不良妊娠結局相關的慢性疾病(如高血壓、心功能異常的心臟病、糖尿病、肝功能障礙、腎病或腎功能異常、嚴重貧血,有深靜脈血栓形成、肺栓塞或腦血管意外史)的婦女。
共納入符合標準的單胎妊娠孕產婦588例。其中,新鮮胚胎移植妊娠(含IVF-ET及ICSI-ET助孕)的孕產婦106例(鮮胚移植組);并按年齡相近、受孕時間相近、地區相似的原則選取同期在同科室分娩的自然妊娠婦女482例(自然妊娠組)。
2.研究方法及觀察指標:收集入選孕產婦及其子代的出生信息,包括個人基本情況、圍產期主要并發癥及新生兒出生結局的情況,并比較組間的差異。
圍產期(妊娠第28周到出生后1周以內)主要并發癥包括早產、妊娠期高血壓疾病、妊娠期糖尿病、前置胎盤、胎膜早破、產后出血、妊娠期膽汁淤積綜合征;新生兒出生結局包括新生兒窒息、新生兒畸形、新生兒肺炎、小于胎齡兒、低出生體重兒、死胎。觀察指標及診斷依據均參照第八版《婦產科學》[7]。
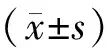
二、結果
1.一般臨床資料:鮮胚移植組與自然妊娠組比較,母親年齡、體質量指數(BMI)差異均無統計學意義(P>0.05)(表1)。
2.圍產期并發癥:鮮胚移植組妊娠期高血壓疾病發病率顯著高于自然妊娠組(7.5% vs. 1.9%,P<0.05),其中囊胚移植亞組顯著高于自然妊娠組(14.8% vs. 1.9%,P<0.05),而卵裂胚移植亞組與自然妊娠組無統計學差異(P>0.05)。組間其他并發癥如妊娠期糖尿病、妊娠期肝內膽汁淤積癥、前置胎盤、胎膜早破、產后出血的發生率均無統計學差異(P>0.05)。鮮胚移植組中卵裂胚與囊胚移植亞組比較,圍產期并發癥均無統計學差異(P>0.05)(表1)。
3.新生兒出生結局:鮮胚移植組(及其亞組)與自然妊娠組比較,各種新生兒出生結局均無統計學差異(P>0.05)(表2)。
表1 鮮胚移植組與自然妊娠組圍產期并發癥比較[(-±s),n(%)]
表2 鮮胚移植組與自然妊娠組新生兒出生結局比較[(-±s),n(%)]
三、討論
目前隨著輔助生殖技術的發展,IVF-ET成功率已突破50%。但IVF-ET與其他醫療干預措施一樣,存在一定的潛在醫療風險。行IVF-ET時,須考慮促排卵、取卵等卵巢刺激可能會引起孕產婦妊娠相關并發癥,以及受精卵體外培養可能導致胎兒畸形的風險[8]。
本研究中,鮮胚移植組妊娠期高血壓疾病的發生率顯著高于自然妊娠組(7.5% vs. 1.9%,P<0.05),與Cavoretto等[2]研究結論一致。進一步按移植胚胎類型分析發現,囊胚移植亞組妊娠期高血壓疾病發病率顯著高于自然妊娠組(14.8% vs. 1.9%,P<0.05),但在卵裂胚移植亞組并沒有觀察到此差異(5.1% vs. 1.9%,P>0.05)。可見,本研究中新鮮胚胎移植妊娠期高血壓疾病發病率顯著高于自然妊娠的結果主要歸功于囊胚移植亞組發病率的升高。Fernando等[9]對囊胚移植妊娠與卵裂期胚胎移植妊娠中的單胎妊娠進行研究,比較兩者的圍產期及新生兒結局并做多因素回歸分析,結果提示囊胚移植妊娠組的先兆子癇和早產的比值比略有增加。
妊娠期高血壓疾病,尤其是重度子癇前期,嚴重威脅孕婦及胎兒的生命健康,目前病因和機制尚未明確。在本研究中,新鮮胚胎移植妊娠期高血壓疾病高于自然妊娠,分析其原因可能是:
首先,IVF過程應用促排卵藥物,如在誘發排卵時一般使用大量的HCG,HCG可激活體內腎素-血管緊張素-醛固酮系統,而該系統與妊娠期高血壓疾病的發生密切相關[10],且Ando等[11]研究認為控制性促排卵(COH)過程中應用血管緊張素轉換酶抑制劑及血管緊張素Ⅱ受體阻斷劑可在一定程度上控制COH引起的RAAS系統紊亂。
其次,IVF孕婦須承受更多的社會和家庭壓力,精神緊張亦誘發妊娠期高血壓疾病的風險[12]。Sazonova等[13]納入了2002~2006年在瑞典接受IVF-ET治療出生的新生兒(共13 544例),并與同期自然受孕出生的新生兒(共587 009例)進行了對比,研究表明IVF-ET組產科并發癥如妊娠期高血壓疾病、前置胎盤、胎盤早剝較自然受孕組高,并指出這些產科并發癥發生率增加的原因可能與促排卵過程中卵巢刺激引起機體內分泌高雌激素,進而影響子宮內膜功能欠佳,導致影響胎盤的生成有關。由此可見,IVF-ET妊娠的婦女應較自然妊娠者受到更規范的人文關懷及精神心理疏導。
再次,IVF的過程(特別是卵巢刺激方案)可能會在妊娠初期誘發激素環境的改變(例如雌激素、孕酮、腎素、胰島素生長因子升高),這些異常的改變均可能會影響血管生成。近些年來內皮細胞損傷、血管生成抑制和血管間炎癥在子癇前期發病機制中的作用越來越被重視。胎盤生長因子(PLGF) 、可溶性血管內皮生長因子受體(sFlt-1)的異常表達是近些年來研究較多的發病機制。PLGF可導致母體對胎兒免疫耐受紊亂,造成滋養細胞浸潤能力受到抑制、胎盤血管網絡重鑄受阻。胎盤滋養細胞分泌的基質金屬蛋白酶可能影響滋養細胞侵襲能力致胎盤淺著床,從而引起妊娠期高血壓的發生[14]。sFlt-1損傷血管內皮細胞,導致子宮內膜細胞及其它血管的收縮,胎盤組織缺血缺氧,進而引起人體內各種細胞因子失調,釋放大量的活性細胞因子,從而加重妊娠期高血壓病情[15]。美國的一項回顧性隊列研究中通過對2 392例單胎妊娠在妊娠過程中的四個時間點監測PLGF和sFlt-1發現,與自然懷孕相比,IVF助孕組在整個妊娠過程的多個時間點均顯示出較高的抗血管生成的證據(即sFlt-1升高和PLGF降低),從而導致妊娠期高血壓疾病的發生[16]。子癇前期迄今仍缺乏有效的治療手段,只能適時終止妊娠,鑒于sFlt-1、PLGF以及兩者的比值在妊娠期高血壓疾病中體現的鑒別診斷意義及其對子癇前期有一定的預測價值,建議高危孕婦在妊娠期嚴密監測血壓,結合血清學標志物水平,尤其是以sFlt-1和PLGF等為代表的血管生成因子類標志物,積極進行產科干預,能最大限度的減少母胎并發癥的發生,改善母嬰結局,進一步保障孕(產)婦的健康。
綜上所述,單胎妊娠中,IVF/ICSI-ET妊娠容易導致妊娠期高血壓疾病發生率升高,但本研究中鮮胚移植組及自然受孕組例數存在一定差距,并不能排除樣本量對結果造成的影響;同時,本研究數據也僅截止至新生兒出生時。尚需納入更多的新鮮胚胎組數據進行比較,并且進行更長時期的觀察。本研究僅是對我院產科長達8年的數據觀察所得,如果未來可以在多家醫院做多中心、大樣本分析,可進一步增強該結果的可信度。同時助孕患者本身患有不孕疾病及接受不孕治療可能是導致不良結局發生的始動因素,本研究沒有評估入選病患的一般情況對圍產結局的影響,比如孕前是否飲酒、吸煙、孕產次等。因此在今后的研究中,我們將擴大樣本量,擴展中心數,進行多中心、大樣本的分析,進一步研究IVF/ICSI-ET助孕技術對母兒結局的不良影響,為預防其不良結局的發生提供理論依據。

