紅光碳點:發光機理、調控及應用探究
王 歡, 徐 晶, 黃昱清, 周鴻磊, 方學林, 李慧珺*, 王現英, 楊俊和
(1. 上海理工大學 材料科學與工程學院, 上海 200082;2. 國家知識產權局專利局專利審查協作江蘇中心化學發明審查部 高分子化學室, 江蘇 蘇州 215000)
1 引 言
碳點(Carbon dots,CDs)具有優異的抗光漂白性、良好的生物相容性、低毒性及合成方法簡單等特點,近年來在光電、生物醫藥及傳感等領域備受關注[1-2]。CDs一般指尺寸小于10 nm且具有熒光發射性質的碳粒子,通常包括石墨烯量子點(Graphene quantum dots,GQDs)和碳量子點(Carbon quantum dots,CQDs)[3]。GQDs內部結晶度更高,層數更少(少于4層,一般為1~2層);而CQDs內部含有大量無定形碳,形態上也更接近球形。GQDs和CQDs均由含有sp2碳的納米晶核和表面官能團組成,而碳核表面環氧基、氨基和羧基等官能團的存在可相應調節CDs在不同溶劑中的溶解性并對其光學性質產生較大影響。CDs結構組成與反應前驅體、分散溶劑等制備條件密切相關,通過控制不同的反應條件能有效調控CDs的形狀、尺寸、表面官能團、雜原子摻雜情況等,進而獲得具有從深紫外到近紅外區域熒光發射甚至雙光子上轉換熒光性質的CDs[4]。
圖1為2004年首次發現CDs以來的研究成果數量年度柱狀圖(于2020年7月11日在ISI Web of Science上獲得)。從圖中可以看出,CDs相關研究成果逐年遞增(灰色柱狀圖)。盡管研究者對CDs的合成、發光機理及性能調控都進行了較多深入探討,但已報道CDs的最優熒光發射峰大多集中在藍綠發光區域。自2014年至今,紅光碳點的研究成果一直呈大幅增長(紅色柱狀圖),這說明紅光碳點的研究價值獲得了越來越多的認可,主要與紅光碳點應用的重要性有極大關系。例如,基于CDs的白色發光二極管(White light emitting diode,WLEDs)如果缺乏高熒光量子產率(Photoluminescence quantum yield, PL QY)窄帶紅光碳點,將很難實現色溫和亮度的精準調控[5];另外,在生物成像時若使用藍綠色熒光CDs,一方面無法避免生物組織自熒光的干擾,另一方面由于光子散射和光吸收水平高也無法獲取大的組織穿透深度。綜合來看,目前紅光碳點的制備體系未見成熟,且該波段發光機理缺乏系統全面的分析,這就使得CDs在相關領域的應用極大受限。為實現紅光發射,研究者在制備條件的調控方面做了諸多嘗試,比如控制前驅體類型、分散溶劑及合成參數等。值得注意的是,報道中一部分紅光碳點是由自身熒光激發依賴性產生的,PL QY普遍較低。因此,進一步明確紅光碳點發光機制,對實現高PL QY激發非依賴紅光具有十分重要的意義。

圖1 2004年至今CDs相關研究結果的年度數量柱狀圖(于2020年7月11日在ISI Web of Science獲得)Fig.1 Histogram of research results numbers of CDs from 2004 to 2020 obtained from ISI Web of Science on July 11, 2020.
基于以上分析,本文首先闡述了量子限域效應、表面狀態、聚集效應等因素對碳點紅光發射性質的作用機制,其次分析了紅光碳點制備過程中前驅體、溶劑類型等的調控機制,最后簡要介紹了紅光碳點在WLEDs和生物成像中的應用現狀。通過綜述已報道紅光碳點的理論和實驗結果,本文針對紅光碳點基礎研究中的薄弱環節提出相應的完善策略,希望有助于推動其在生物學、光學等領域的應用研究。
2 紅光發射機理
CDs紅光發射可通過兩種方式實現:一種是基于激發依賴特性(發射波長隨激發波長改變而改變)的紅光,目前已報道的部分藍/綠光CDs可在較長波長激發下發射紅光,這種激發依賴特性是實現CDs紅光發射的一種重要途徑,但其熒光強度會隨波長增加而急劇降低,紅光PL QY普遍較低;另一種是激發非依賴性紅光發射,其峰值集中在600 nm以上,有的甚至接近近紅外區(700~900 nm)。這種發光由CDs自身結構或聚集態決定,一般可通過改變幾何尺寸大小及表面化學態或引入缺陷能級、生色團等來調控其能帶結構,進而實現較高PL QY且穩定的紅光發射。接下來本文將從CDs紅光發射機理出發,分別討論量子限域效應、表面狀態、聚集效應等因素在紅光發射中的影響機制。
2.1 量子限域效應
CDs內核是由sp2共軛結構組成的無定形納米晶。對于共軛內核結構完整且表面缺陷較少的CDs來說,量子限域效應促使其發射波長連續可調。量子限域效應認為,當納米材料幾何尺寸逐漸減小到小于或等于其激子波爾半徑時,材料的電子能級會由準連續態變為離散分布形式。這表明當CDs尺寸越小,其光生電子和空穴受量子限域效應影響越大,最低未占據分子軌道(Lowest unoccupied molecular orbital,LUMO)與最高占據分子軌道(Highest occupied molecular orbital,HOMO)間帶隙越寬,這將導致熒光發射光譜峰位逐漸藍移。相反地,CDs內核尺寸越大,帶隙寬度越窄,熒光發射峰位置將越紅移。圖2中,Eda等[6]曾用密度泛函理論對CDs共軛尺寸和帶隙關系進行了計算。結果表明,由1個苯環組成的CDs帶隙為7 eV,當苯環數量增加至20個(尺寸增加),CDs帶隙降低至2 eV。Peng等[7]通過理論計算,推斷CDs熒光來源于sp2結構共軛π電子的量子限域效應,且容易受sp2納米簇的尺寸、邊緣結構及形狀影響。
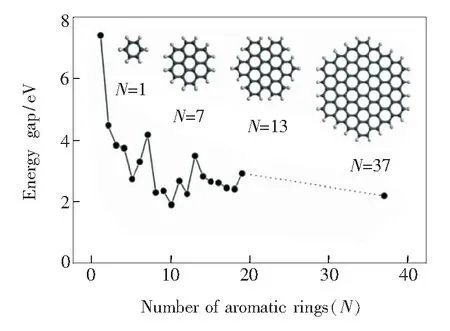
圖2 通過密度泛函理論計算得到的π-π*躍遷能帶與芳香環數目(N)的變化關系圖[6]Fig.2 Energy gap of π-π* transitions calculated based on DFT as a function of the number of fused aromatic rings[6]
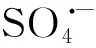

圖3 (a)紅光碳點的sp2結構HRTEM圖;(b)在360 nm激光激發下,不同氧化時間CDs的歸一化光致發光光譜;(c)窄帶寬熒光發射T-CDs的合成圖[9-10]。Fig.3 (a)sp2 domains of R-CDs. (b)Normalized photoluminescence spectra of oxidized CDs treated by different hours under 360 nm laser excitation. (c)Synthesis of narrow bandwidth emission T-CDs[9-10].
為更好地拓展sp2共軛結構、獲得高效紅光發射,研究者還利用一些帶有苯環的芳香族前驅體進行脫水碳化以延伸共軛結構。2018年,Yuan等[10]通過在乙醇或硫酸中回流熱處理間苯三酚合成了三角形CDs(T-CDs),如圖3(c)。表征顯示,T-CDs呈現幾乎沒有缺陷的石墨烯晶體結構,尺寸分布均勻,顏色純度高,且具有非常窄的FWHM(僅為29~30 nm),PL QY高達54%~72%。從圖3(c)中可觀察到,隨著尺寸從1.9 nm增加到2.4,3.0,3.9 nm,T-CDs發射峰也從藍光區域逐漸紅移至綠光、黃光和紅光區域,這直接表明了量子限域效應與熒光發射波長的關系。由于所合成的T-CDs發射峰帶寬窄,其還被用作LED的有源發射層。制備的LED器件色純度高、穩定性好,性能可與傳統量子點基LED相媲美。在眾多芳香族前驅體中,不可忽視的一類還有萘及其衍生物。萘及其衍生物是一類可用于構建較大共軛sp2結構的理想有機小分子前驅體。Yuan等[11]用二氨基萘和檸檬酸(Citric acid,CA)在濃硫酸中水熱制備出了全色發光CDs,其熒光發射波長最高達到604 nm。作者認為,二氨基萘可被視為帶有氨基的剛性共軛碳骨架,在濃硫酸作用下能直接碳化成尺寸合適、缺陷較少的sp2碳內核,這是CDs出現紅光發射的主要原因。基于此,Wang等[12]設計采用了可控順序的脫水縮合和平面脫氫法,使用1,3-二羥基萘和KIO4在乙醇中水熱并通過硅膠柱層析對產物進行純化,制備了628 nm發射的高PL QY紅光碳點,其PL QY可達53%。這一結果證明結構完整的sp2結構對于提高PL QY具有重要作用。隨后,他們制作了紫外泵浦CDs基WLEDs,其顯色指數(Color rendering index,CRI)為97,高于傳統量子點基WLEDs。
由此可見,在紅光調控過程中,量子限域效應是最常見的熒光發射機制。當然,在CDs制備過程,特別是自上而下剝離過程中,強氧化劑的使用往往會增加表面缺陷的產生幾率。因此,我們也發現相關文獻中CDs紅光PL QY較低,且不同批次制備的CDs其紅光PL QY會出現明顯差異。
2.2 表面態
在共軛π結構尺寸合適且比較完整的情況下,紅光碳點熒光發射主要受量子限域效應影響。但實際情況中,大部分紅光碳點表面均存在如環氧基、羥基和羧基等含氧官能團,這些官能團會在CDs共軛結構邊緣引入缺陷,進而誘發另一種熒光發射機理——表面態發射機理[13]。表面態熒光發射的作用機制是:表面氧化引入表面缺陷,并在帶隙中引入新能級;缺陷位點能級捕獲光生電子或空穴,接著激子在缺陷位點發生復合產生熒光。因此,通過調控CDs表面態也是實現有效紅光發射的重要路徑之一[14-15]。
Xiong課題組[16]報道了以對苯二胺和尿素為前驅體(圖4(a)),通過水熱法制備、硅膠柱層析分離獲得的CDs。其熒光發射峰范圍從440 nm到625 nm,表現出激發非依賴特性,PL QY約為24%。由于制備的多色CDs尺寸相似,作者認為CDs熒光發射并不受量子限域效應影響。他們發現,隨著CDs表面羧基含量和氧化程度增加,熒光發射峰值逐漸紅移。因此,作者提出表面氧化程度可影響CDs光致發光性能,誘導紅光發射。Sun等[17]通過微波輔助法使用CA和甲酰胺制備了發射峰為640 nm的紅光碳點,其光學特性具有很高的pH敏感性,熒光激發和發射峰峰位隨pH增加(2~12)逐漸藍移且峰強顯著增加。他們認為,位于CDs表面的羧基和氨基會引入新的能級,并最終導致與表面態有關的發射。Hu等[18]也報道了類似紅光機理,他們通過控制反應前驅體和脫水反應,合成了系列具有可調熒光的全色CDs。各種表征結果顯示,CDs熒光從藍色右移至紅色主要歸因于C—OH和C—O—C基團的增加。如圖4(b),隨著CDs中含氧基團數目的增加,n-π*之間形成了大量與環氧基/羥基相關的局域電子態,這些新缺陷能級的出現是長波發射的主要原因。
此后,研究人員對CDs表面態誘導其熒光紅移機制進行了深入研究,比如通過修飾電子受體基團提高表面氧化程度。Li等[19]利用富含亞砜/羰基的聚合物修飾CDs表面,成功制備了具有近紅外吸收和發射的CDs,這些CDs在二甲基亞砜溶液中混合攪拌一定時間后,可發射715 nm熒光。其他非質子極性分子如N,N-二甲基甲酰胺(DMF)、2-甲基-2吡咯烷酮和聚乙烯吡咯烷酮(PVP)也可提供與CDs邊緣結合的電子受體基團,以提高CDs表面氧化程度、降低石墨片層共面性及層間作用。這些途徑主要通過降低碳點LUMO位置(如圖4(c)所示)來減小帶隙,進而產生熒光紅移。
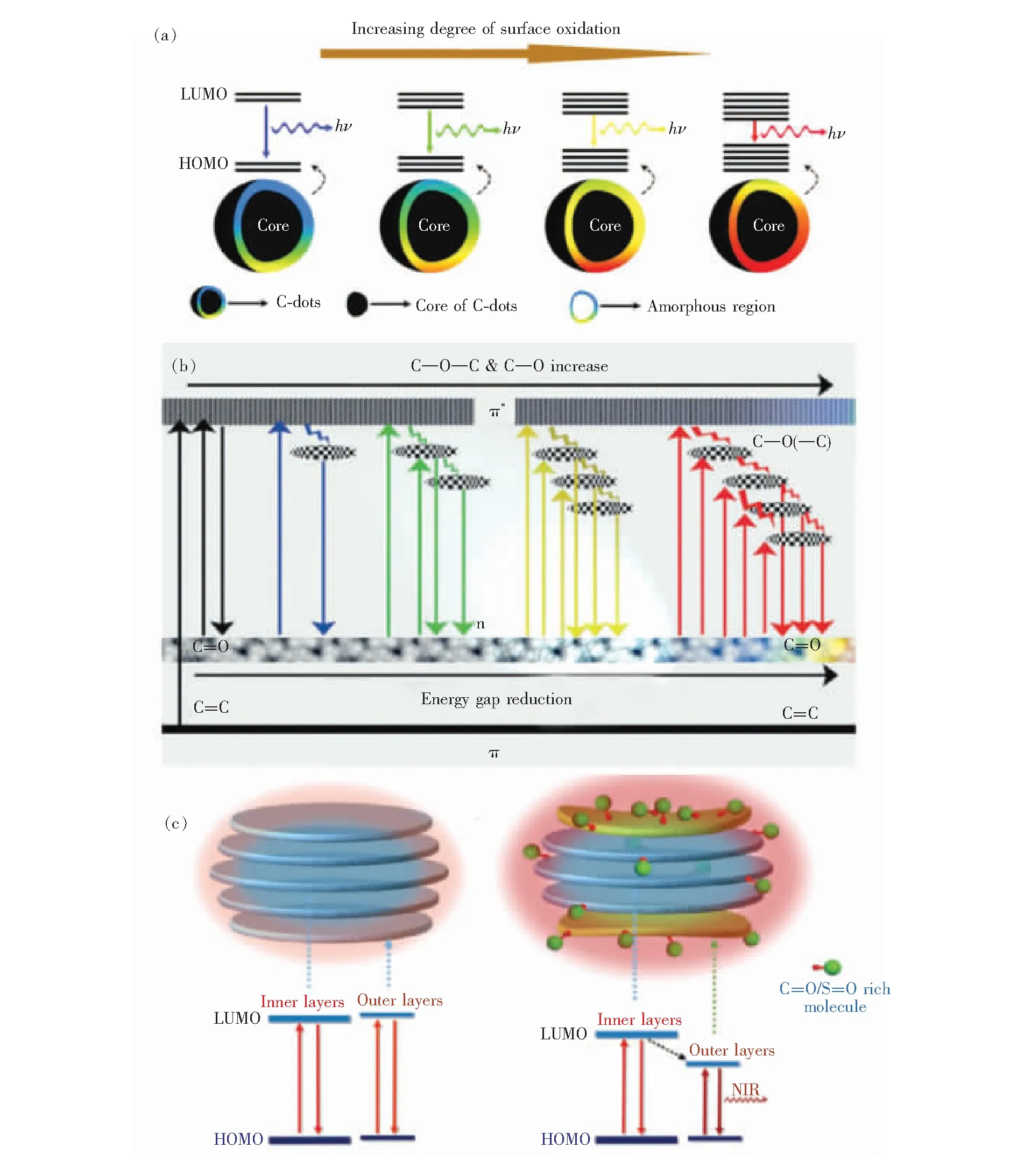
圖4 (a)不同氧化程度CDs可調熒光示意圖;(b)不同表面含氧基團CDs的可調熒光發射圖;(c)未經處理CDs(左)和富含分子修飾CDs(右)的結構和能級對比示意圖[16,18-19]。Fig.4 (a)Model for the tunable PL of CDs with different degree of oxidation. (b)Illustration of the tunable PL emission from CDs containing different O-related surface groups. (c)Schematic of structure and energy level alignments of nontreated CDs(left) and CDs modified with SO/CO-rich molecules(right) affects the carbon dot edge and band gap[16,18-19].
一些聚合物的表面鈍化作用也可以有效促進熒光紅移。朱金陽等[20]首先將尿素和CA在DMF溶劑中熱處理制備了藍光CDs,接著利用十六烷基三甲基溴化銨(CTAB)修飾藍光CDs,促使CDs熒光發生紅移,變成綠光和紅光。Zeta電位顯示,CDs表面連接了雙層CTAB分子,這種雙層結構中一頭是CTAB的季胺基團與CDs表面相連,另一頭是CTAB的親水基團與水分子作用。這種修飾方法不僅可以減少原始藍光CDs表面發生的非輻射躍遷,還可使得CDs具有良好水分散性,有效防止自猝滅或自吸收的發生。表征結果顯示,長波熒光機制是通過本征態受激發電子的能量轉移來實現的,因為CTAB與原始CDs表面連接后會在一定程度上抑制表面基團的非輻射振動和旋轉,本征態與表面態之間的能量傳遞被激活,從而實現長波長發射。
由此可見,CDs熒光發射波長確實與表面態密切相關。但在某些報道中,部分含氧官能團也會充當非輻射陷阱去猝滅熒光,而這些官能團又很難被修飾或鈍化。這意味著表面態的引入實則在CDs表面嫁接了大量激子非輻射復合中心,也就解釋了為什么部分CDs在長波長區域PL QY較低的現象。基于此,在合成長波長發射CDs時,我們應綜合考慮不同因素間的協同效應。
2.3 熒光生色團
除了改性或鈍化CDs的表面結構外,在碳核結構上連接特殊有機熒光生色團也是實現紅光發射的重要方式,這種影響機制常見于自下而上法制備紅光碳點。如前所述,表面態是通過化學基團和碳核的協同雜交作用形成的熒光發射中心,而熒光生色團通過連接在碳核結構上直接形成熒光發射中心。在較高反應溫度下,前驅體分子首先脫水形成具有共軛結構的碳核,然后在較低反應溫度下可在碳核上連接特定有機熒光團。與表面態相比,熒光生色團誘導紅光表現出較強熒光發射和較高PL QY。
Yan等[21]提出了兩種策略來系統性調控CDs帶隙,一種利用量子限域效應,通過將CDs與共軛聚芳環分子縮合來擴大sp2共軛結構以實現長波長發射;另一種則是利用表面修飾作用,在溶劑熱條件下利用羧基和氨基間的縮合反應,在前體CDs共軛結構邊緣連接了P-茴香胺、4-(三氟甲氧基)苯胺和4-(三氯甲氧基)苯胺分子(如圖5(a))。結果表明,引入化學基團的供電子能力越強,越易實現長波長發射。Kwon等[22]也有相似發現,見圖5(b),他們使用了6-氨基喹啉、4-甲氧基苯胺和4-(甲硫基)苯胺三種苯胺衍生物來修飾CDs。這些苯胺衍生物結構中均包含胺基,修飾后CDs氮含量增加了5%~10%,且FWHM急劇縮小。這可歸因于CDs和苯胺衍生物能級之間相互作用形成的非固有能級的影響。
2.4 聚集效應
上述CDs在溶液中顯示紅色熒光,但在聚集態下極易發生聚集誘導猝滅(Aggregation-induced quenching,ACQ)[23],這是由于碳核容易發生π-π堆疊[24]。相比之下,有一類特殊CDs在聚集狀態下也會顯示熒光發射,該現象由唐本忠院士課題組命名為聚集誘導發光(Aggregation-induced emission,AIE)[25]。AIE分子上存在一些轉子基團,使得分子在分散態時會發生轉子轉動,將入射光子能量消耗掉,不顯示熒光;而當其以聚集態存在時,轉子轉動將會受限,使入射光子能量以輻射躍遷方式表現出來[26]。另外,轉子存在還可避免碳核π-π堆疊從而有效防止ACQ的發生。
研究者也探索過AIE在CDs熒光發射增強中的影響[27]。Gao等[28]報導了5′-三磷酸腺苷誘導C60制備CDs時聚集誘導熒光增強的現象。Liu等[29]在由單寧酸水熱制備的CDs中添加四氫呋喃觀察到AIE現象。進一步地,Yang等[30]使用三聚氰胺和二硫代水楊酸作為前驅體,在乙酸溶液中制備出具有藍色液體熒光和紅色固體熒光的疏水H-CDs。如圖5(d)和5(e),當H-CDs分散在四氫呋喃溶液中時,液體呈現藍色熒光,滴加水后,疏水作用導致H-CDs聚集并發出紅色熒光。藍色熒光的猝滅是由于受到碳核π-π堆積的影響,紅色熒光出現則是由于表面分子鍵的分子內旋轉受限所致(如圖5(c))。由于這種可逆的“開-關”熒光,作者設計了發光油墨,用于高級防偽和雙重加密。Lin等[31]也觀察到了摻磷CDs中的聚集紅移現象。通過改變溶液濃度,可以在455~595 nm范圍內調節P-CDs發射波長。結果顯示,摻磷CDs在聚集狀態下粒徑增大,拓展了共軛體系,引起發射峰紅移。CDs的AIE現象為構建新的生物傳感、生物成像和防偽器件提供了更多可能性。
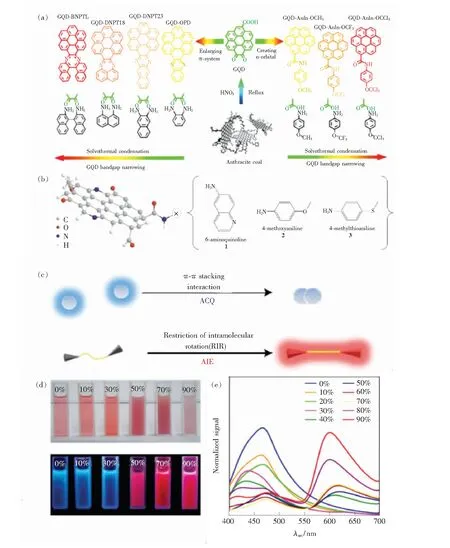
圖5 (a)將CDs與多芳環共軛來擴大π共軛體系或與供電子基團共軛引入中間n軌道使能隙變窄;(b)CDs和苯胺衍生物的化學結構示意圖;(c)H-CDs核心和表面結構及熒光原理示意圖;(d)在日光下(上)和365 nm紫外線下(下),水體積比(0%~90%)變化時H-CDs溶液照片;(e)隨水比例變化的H-CDs溶液的光致發光光譜[20-21]。Fig.5 (a)Illustration of bandgap narrowing by enlarging π-conjugated system via conjugating CDs with poly aromatic rings or by introducing intermediate n-orbital via conjugating with electron-donating groups. (b)Schematic illustration of the chemical structure of GQDs and aniline derivatives. (c)Fluorescence principle and proposed structure of H-CD’s core and surface. (d)Photographs of the as-prepared H-CD solution by varying volume ratios of water(from 0 to 90%) under sunlight(top) and 365 nm ultraviolet radiation(bottom). (e)PL emission spectra of the as-prepared H-CDs solution with different ratios of water[20-21].
3 紅光碳點的制備
目前報道的碳點研究成果涉及了幾百種合成手段和上千種前驅體[32]。然而,只有一小部分CDs可實現紅光發射,這說明紅光碳點制備具有很高難度和壁壘。制備紅光碳點的主要方法為自上而下法(切割或剝離大尺寸的碳材料)和自下而上法(有機小分子脫水、脫氨或直接鍵合碳化)。自上而下法制備CDs的紅光發射通常是量子限域效應導致的,在合成時會采用強酸和強氧化劑等苛刻的反應條件,且獲得的紅光PL QY一般較低。相比之下,在自下而上法中,或者對自上而下合成CDs的進一步修飾過程中,小分子前驅體和分散溶劑對制備的紅光碳點的熒光性能具有十分重要的作用,甚至是決定性作用。本部分著重闡述了自下而上法制備紅光碳點,并總結紅光發射規律。
3.1 前驅體
合成紅光碳點最常用前驅體如CA、氨基酸、糖類等,大多含有羥基和羧基[33],它們易脫水形成缺陷較少的sp2碳核;另一種常用前驅體是帶有苯環的小分子芳香結構,如苯二胺和萘,它們本身具有平面式剛性結構,能夠形成較大尺寸sp2共軛結構,有利于調控碳點的發射波長;另外,使用染料分子(如尼羅藍、中性紅和香豆素等)作為前驅體制備高PL QY紅光CDs也是常用方法之一。部分前驅體中含有的一定數量雜原子如N[34]、S和O等,可在CDs電子結構中引入雜質能級,進而調控帶隙實現紅光發射。
3.1.1 檸檬酸
在眾多前驅體中,CA結構特殊(碳鏈上具有羥基和多個羧基),是自下而上法制備CDs最常用前驅體之一。Qu等[35]首次使用CA作為前驅體合成CDs。在堿性(NaOH)反應條件下,CA分子自組裝成片狀結構,隨后通過分子間脫羥基縮合反應,形成碳核納米晶,其表面具有未反應的羧基和羥基。但這種合成方法獲得的CDs顯示藍色熒光且PL QY較低(約為10%)。為了提升PL QY及研究N摻雜對CDs的影響,他們之后使用了一系列含氮有機物(例如尿素)制備CDs。結構表征證明水熱條件促進了—NH2和—COOH之間酰胺鍵的形成,而酰胺和—COOH基團間會發生分子內水解,最終導致石墨烯骨架中摻入吡咯N。通過優化反應條件,他們使用CA作為碳源、乙二胺(EDA)作為N源,進一步獲得了N摻雜CDs,所獲CDs表現出激發非依賴藍光發射,并具有單指數壽命衰減。在此基礎上,越來越多的研究者嘗試使用含有氨基的前驅體如EDA、甲酰胺、尿素、硫脲和DMF等進行N摻雜,以制備紅光到近紅外發射CDs[36]。
在已報道氮源中,尿素與甲酰胺最常被用于和CA發生溶劑熱反應合成紅光碳點,其中甲酰胺不僅可以作為氮源,還可在溶劑熱過程中作為溶劑。通過使用CA和甲酰胺作為前驅體,Lin的團隊[37]首次提出微波輔助法(160 ℃加熱1 h)制備CDs,這些CDs發射峰在330~600 nm范圍內變化(如圖6(a)、(b)所示)。表征結果證實了所制備CDs中C—N/C—O等化學鍵占比較高是長波長發射的主要原因。2017年,Ding等[38]使用CA在甲酰胺和EDA中通過溶劑熱法合成了PL QY約為53%的紅光碳點,其發射峰集中在627 nm,為激發非依賴性紅光發射。Miao等[39]通過調整CA/尿素比例與反應溫度(140~200 ℃)來控制石墨化和表面功能化,成功制備了一種全色發射CDs。如圖6(c),當CA/尿素的量比超過0.7時(200 ℃時),發射峰紅移至630 nm。紅光碳點的石墨化程度和羧基含量均高于藍光和綠光CDs,后兩者反應時前驅體CA/尿素比例較低。Hola等[40]利用尿素和CA在甲酰胺溶液中制備了全色CDs,并使用柱層析法將混合CDs分離成藍光、綠光、黃光和紅光組分。表征顯示石墨氮會在未摻雜系統的HOMO-LUMO間隙內產生中間能隙狀態,從而導致光吸收發生明顯的紅移,進而產生紅色熒光。
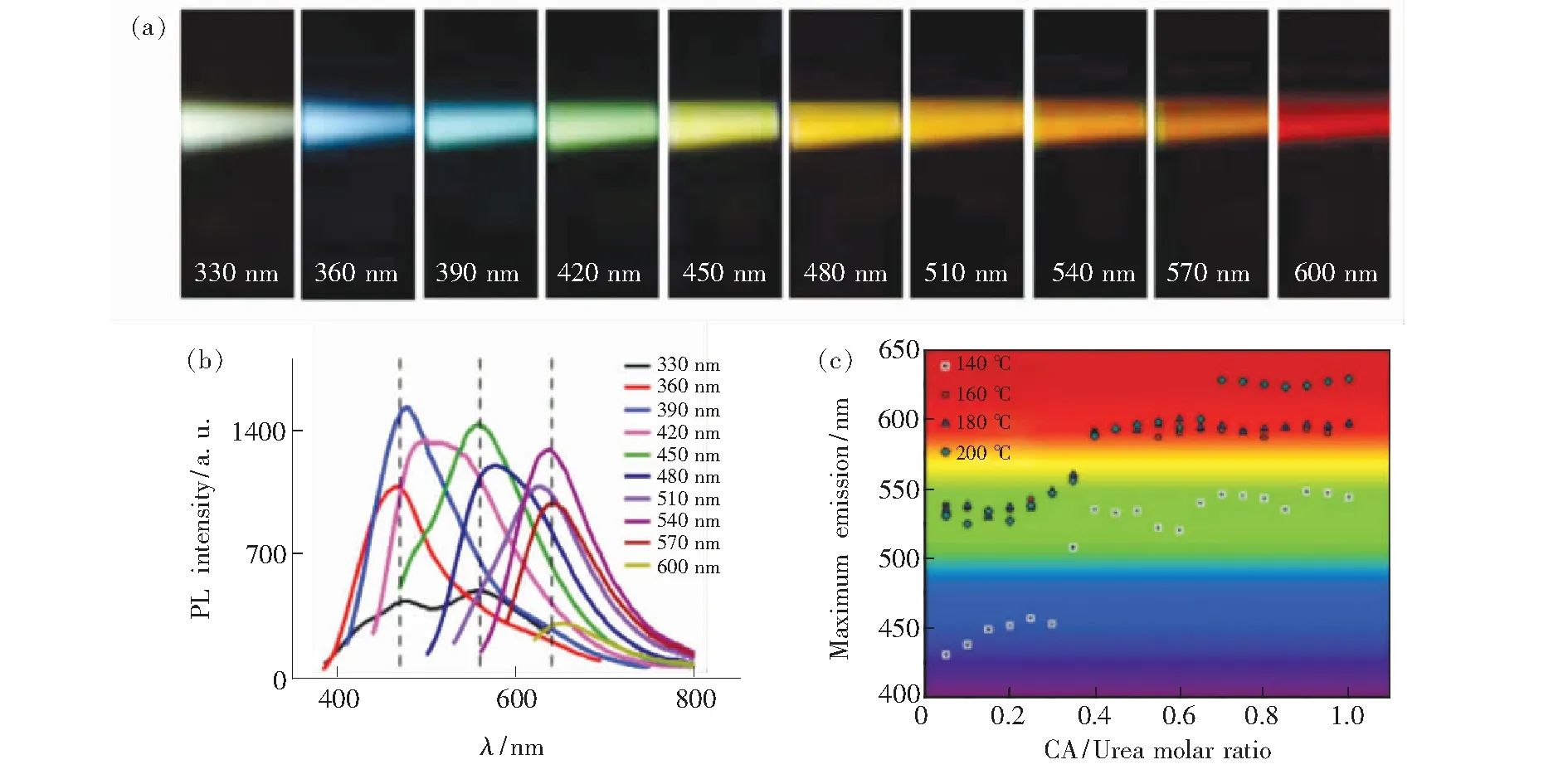
圖6 (a)CDs熒光發射照片;(b)不同激發波長下CDs的熒光光譜;(c)不同反應溫度和CA/尿素量比合成CDs的最大發射峰[37,39]。Fig.6 (a)FL emission photographs of the CDs. (b)FL spectra of the CDs under different excitation wavelengths. (c)Maximum emission peaks of CDs at different molar ratios of CA to urea and different reaction temperatures[37,39].
3.1.2 芳香族小分子
芳香族小分子化合物作為碳源,已多次被報道用于制備長波長熒光碳點。最常見的比如苯二胺的三種異構體:鄰苯二胺(o-phenylenediamine,o-PDA)[41]、間苯二胺(m-phenylenediamine,m-PDA)[42]和對苯二胺(p-phenylenediamine,p-PDA)[16],其中o-PDA和m-PDA較易形成CDs,而p-PDA合成高熒光量子產率紅光碳點仍存在挑戰。
Lin的課題組[43]使用o-PDA、m-PDA和p-PDA這3種同分異構體合成了三色CDs,分別命名為o-CDs,m-CDs和p-CDs(如圖7(a)所示),它們在紫外光下分別顯示出綠、藍、紅光發射。這3種碳點組成元素完全一致,但p-CDs相比其他兩種表現出吸收紅移。與大多數報道不同的是,這些CDs熒光量子產率隨發射峰紅移而增加,文中歸因于粒徑和含氮量不同。隨后,大量研究開始利用苯二胺系列分子作為前驅體制備長波長發射CDs。Yang的課題組[44]選擇使用o-PDA和多巴胺在稀乙醇溶液中水熱合成紅光碳點,其發射波長為710 nm,PL QY約為26.28%。Liu等[45]利用2,5-二氨基甲苯硫酸鹽(DATS)通過溶劑熱法合成了紅光碳點。DATS結構與p-PDA非常相似,只在苯環上多了一個甲基。因此,當激發光波長高于460 nm時,兩種前驅體制備的CDs表現出幾近相同的熒光發射(約603 nm,該發射峰與前面提到的p-PDA相似)。
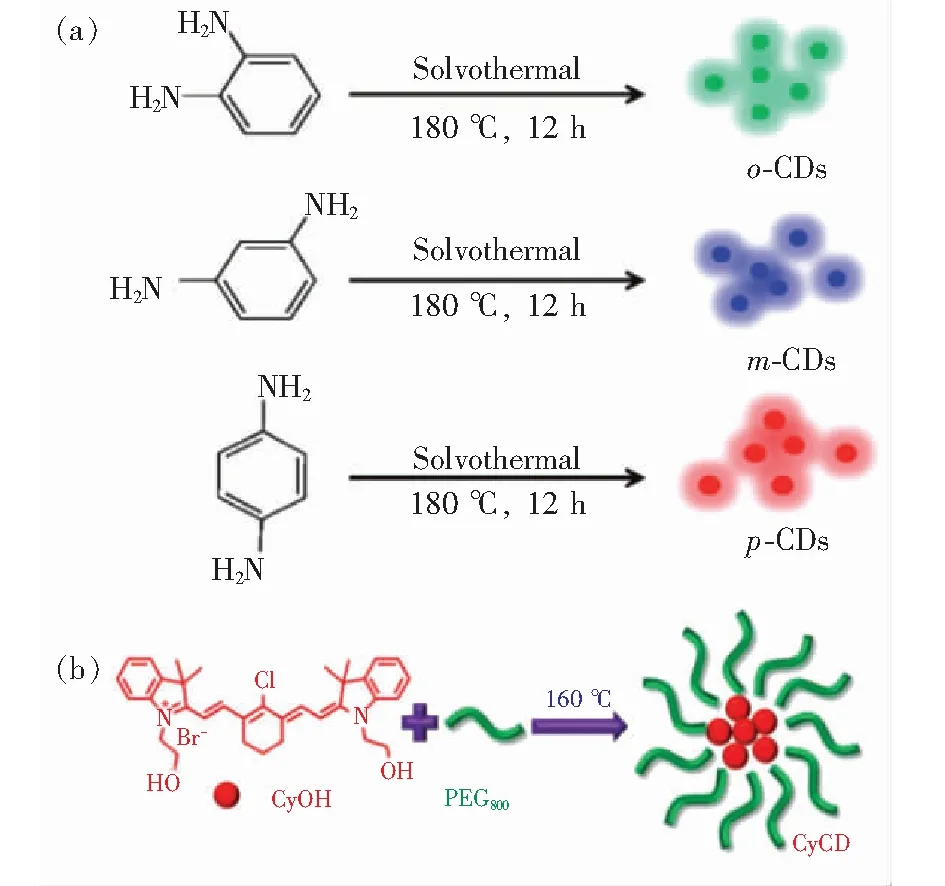
圖7 (a)o-PDA、m-PDA和p-PDA合成多色CDs示意圖;(b)氰基染料制備CDs示意圖[43,47]。Fig.7 (a)Schematic preparation of CDs with different colors from o-PDA, m-PDA and p-PDA. (b)Schematic preparation of CDs with cyanogen dyes[43,47].
萘作為另一種常用的芳香族小分子前驅體,在溶劑熱條件下可形成尺寸較大且缺陷較少的共軛sp2簇。Yu的課題組[46]在室溫條件下使用萘和鈉,在乙腈中獲得了熒光發射在588 nm處且激發非依賴的氮摻雜CDs,作者認為該CDs的熒光特性歸因于熒光官能團的分子狀態,即CDs表面或內部的芳香碳環。由以上例子可知,含苯環的芳香結構對紅光碳點制備來說意義重大。
此外,芳香族小分子中還有一類特殊的常用于制備長波長CDs的前驅體——染料分子。大多數商業染料分子在最佳激發波長處表現出強吸收,但其穩定性較差、容易被氧化漂白、具有一定生物毒性且容易污染環境,因此,研究人員提出使用紅色/近紅外激發染料分子作為前驅體合成紅光碳點,常用的有酞菁鋅、甲酚紫和中性紅。在合成過程中,染料分子固有共軛電子結構可能被部分保留,有利于制備出與染料前驅體分子具有相似激發發射但穩定性大大增強且環境友好的紅光碳點。如圖7(b),Zheng等[47]利用疏水性氰基染料和聚乙二醇分子合成了具有紅色激發(720 nm)和近紅外發射(820 nm)的CDs。與氰基染料相比,紅光碳點不僅保留了近紅外光譜的吸收和發射,還表現出優良的耐光性和親水性,這些特點使其在腫瘤成像等生物應用中扮演著重要角色。中性紅由于其較完整的共軛結構而具有優異光學性能。Gao等[48]利用CA和中性紅(量比為1 000∶1)通過水熱法合成了高穩定性紅光碳點,其在632 nm(激發光波長為530 nm)處表現出最優發射。此外,Jia等[49]使用錳酞菁通過水熱法制備了最高熒光發射峰為745 nm的紅光碳點,作者認為產生長波長發射的原因在于芳族結構的J聚集。這種紅光碳點還可用來驅動細胞產生有毒1O2,以實現光動力療法殺死腫瘤。因此,選擇合適的染料分子作為前驅體是一種有效的紅光碳點制備方法,不僅能夠保證合成長波長激發和發射的CDs,其熒光穩定性也將大大提高。
3.2 溶劑
眾所周知,溶劑熱/水熱法是自下而上制備CDs的常用方法,使用這種方法合成紅光碳點時,不可忽視溶劑性質對前驅體脫水及碳化程度的影響。在CDs研究早期,使用較多的溶劑是水。水溶液中制備的CDs大多發射藍色熒光[50],這是因為水極性高,不利于共軛熒光中心的形成。之后研究者們發現,DMF和甲酰胺等低極性溶劑更易產生具有較大共軛sp2尺寸和較窄能帶的CDs[51],這兩者都有利于產生長波長發射。
3.2.1 有機溶劑
前驅體在非極性溶劑中分散性較好,脫水和碳化程度更高,更易合成長波長發射CDs。如圖8(a),Tian等[52]以CA和尿素為前驅體,分別在水、甘油和DMF(相同反應條件下)中使用溶劑熱法合成了發射峰在448~638 nm的熒光CDs。粒徑最大、脫水碳化程度最高、熒光發射波長最長的CDs在DMF溶劑中合成,其次分別在甘油和水溶劑中合成。與極性溶劑(水)相比,DMF中合成CDs的氧/碳相對原子比較少。Zhu等[53]也得出過相似結論,他們將CA和尿素溶于DMF中制備出紅光碳點,而相同條件下在水和乙醇中只能得到藍光和綠光CDs。這些結果說明DMF在溶劑熱反應中相比水和乙醇更易促進前體脫水和碳化,促使碳點sp2共軛結構更加完整,從而引起光吸收峰和熒光發射峰的紅移。
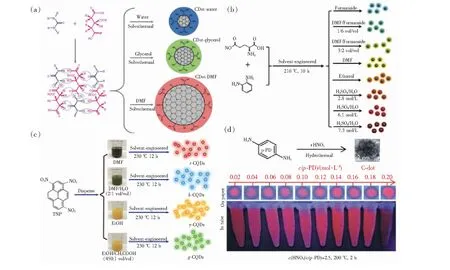
圖8 (a)以水、甘油和DMF為溶劑CDs的生長機理示意圖;(b)o-PDA和l-谷氨酸合成多色CDs示意圖;(c)以TNP為前驅體、DMF或乙醇為主溶劑、H2O或乙酸為輔助溶劑合成CDs示意圖;(d)p-PDA和硝酸合成紅光碳點示意圖及在365 nm紫外光照射下,CDs水溶液在濾紙上(上)和離心管中(下)的光致發光照片[52,54-55,58]。Fig.8 (a)Schematic diagram of the growth mechanism of CDs with water, glycerol and DMF as solvents. (b)Schematic diagram of o-PDA and l-glutamic acid synthesis of multicolor CDs. (c)Schematic diagram of synthesizing CDs with TNP as the precursor, DMF or ethanol as the main solvent, and H2O or acetic acid as the auxiliary solvent. (d)Schematic diagram of the synthesis of red light carbon dots by p-PDA and nitric acid. PL photos of CDs aqueous solution on filter paper(top) and centrifuge tube(bottom) under 365 nm ultraviolet light irradiation[52,54-55,58] .
除了溶劑極性對碳點熒光峰紅移的影響外,溶劑中異質元素比如N、S、O的存在也會影響發射峰紅移。其中,含N溶劑可為CDs提供表面N原子摻雜,進而誘導缺陷發射。甲酰胺、DMF等由于結構式中含N且極性較低,倍受研究者們青睞。Xiong的課題組[54]以o-PDA和l-谷氨酸為前驅體,通過改變溶劑(甲酰胺、甲酰胺與DMF混合液、DMF、乙醇、硫酸)得到系列熒光可調的CDs,熒光發射峰在443~745 nm(如圖8(b))。從表征可知,隨著CDs熒光紅移,其結構中N含量增多、O含量減少。如圖8(c),Zhan等[55]提出了一種分子融合策略,通過改變反應溶劑(DMF、乙醇、乙酸或其混合物)來合成熒光發射可調的CDs。當前驅體分子為1,3,6-三硝基芘時,DMF(或乙醇)溶劑可促使前驅體融合形成窄帶隙CDs,誘導紅光發射;而乙酸作為溶劑時則產生了FWHM相對較寬的藍光和綠光CDs。
除了在合成過程中使用溶劑調控發射波長外,將CDs直接溶于不同溶劑也可觀察到熒光變化。Chao等[56]用o-PDA制備出CDs后,將其分別溶于四氫呋喃、丙酮、DMF、甲醇和乙二醇中,溶液顯示出不同熒光。隨著溶劑極性增加,在單一激發波長下,最大發射峰從512 nm逐漸紅移到565 nm,導致熒光顏色由青變為橙色。作者認為溶劑極性能夠影響CDs的表面態進而影響其熒光發射。
3.2.2 酸類
除了有機溶劑外,酸也是溶劑熱法中的常用溶劑,它們在實現CDs長波長發射方面具有極其重要的作用。為了研究酒石酸對熒光發射的影響,Jiang等[57]在不添加任何酸情況下,先對m-PDA和o-PDA進行溶劑熱處理,制備出具有綠色或黃色發光的CDs,然后在反應介質中加入酒石酸得到了紅光碳點;在他的另一項研究中[43],也發現了不添加任何酸對p-PDA進行溶劑熱處理,只能制備得到綠色或黃色發光CDs,如果在反應介質中加入硝酸則可得到紅光碳點。Tan等[58]以p-PDA水溶液為原料,在硝酸輔助下合成了具有較寬可見激發帶且PL QY為15.8%的紅光碳點(如圖8(d))。熒光發射光譜顯示其在紅色區域(600 nm和680 nm)表現出激發波長非依賴熒光發射,分析結果表明CDs表面羧基、酯基和羥基導致了紅光發射,且適當增加酸用量可以增強其熒光。即在水熱過程中,酸性環境能夠提高前驅體碳化程度并增大其共軛sp2結構尺寸,促使熒光發射峰紅移。


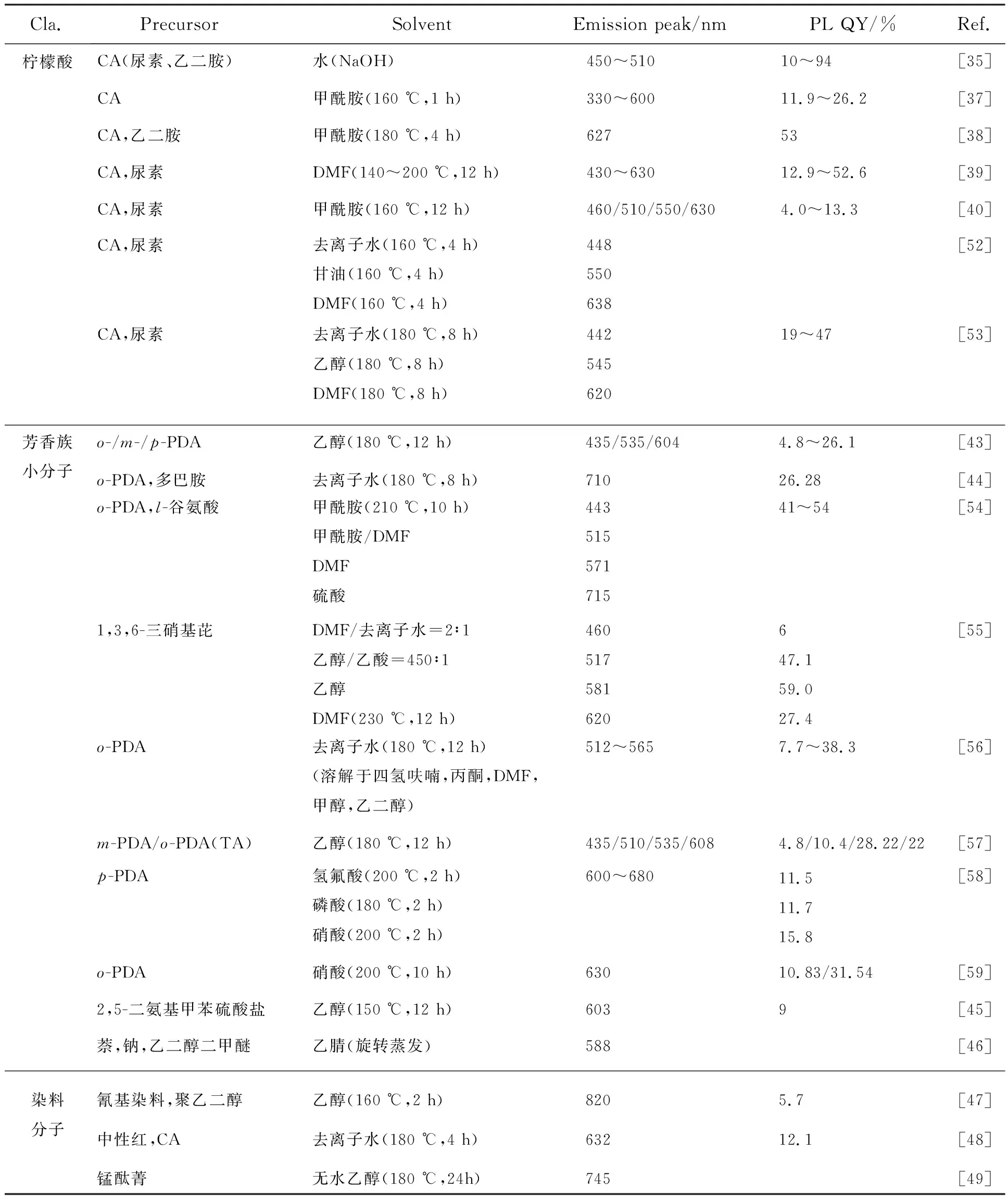
表1 各種前驅體和溶劑制備CDs的光學參數概述
4 紅光碳點的應用
紅光碳點在光電器件[62-65]、生物成像[8]、生物傳感[66]、載藥[67]、加密防偽[30,68-69]和光催化[4,18,70-71]等領域應用非常廣泛,本節將簡要介紹CDs在發光二極管及生物領域的應用現狀。
4.1 紅光碳點用于白光二極管
在發光二極管中,WLED由于高發光效率、高亮度和節能等優點,已成為未來固態光源的有力競爭者[72-75]。當前商用WLED一般是將黃光稀土磷光體涂敷在藍光InGaN芯片上制作而成。磷光體為顏色轉換層,將InGaN芯片藍色發射轉換為其他發射顏色,然后將殘留未被吸收的藍光和磷光體發射混合成白光[74]。盡管這種磷光體是高效的光轉換材料,但它們在生產過程中不可避免地存在原料價格昂貴和高能耗等缺點。于是研究者將目光投向原材料來源廣泛、價格便宜且穩定性良好的CDs。CDs可用于電致發光熒光粉、有機發光體摻雜劑、帶隙調諧器或彩色轉換器等。但是,要達到與目前傳統稀土或無機量子點基WLED相近的性能,還需要解決兩大難題——色純度和發光效率。
色純度需要制備出窄帶發射(一般用發射光譜的FWHM衡量)CDs。發射峰窄的CDs不僅可以為顯示器或照明器件提供鮮艷色彩,還可以提供更好的信噪比,并最大程度減少成像應用中的串擾。前文提到的紅光T-CDs就具有很窄的FWHM,作者通過第一性原理計算發現,剛性三角形結構、完美碳核結晶和較少羧基含量是CDs窄帶發射的主要原因[10]。如圖9(a)、(b)所示,T-CDs被用作發光二極管的有源層,進而制備出最大亮度為4 762 cd·m-2、電流效率為5.11 cd·A-1的LED。關于窄帶CDs的制備方法,多數報道都證明其最重要的實現途徑是使用高度共軛前體來制備[22]或后處理修飾CDs[76];合成或后處理時也要盡量減少表面羧基數量[77]。前者有利于增加結晶度和實現剛性結構,后者可減少吸電子羧基引起的局部畸變和表面缺陷。
發光效率也是非常重要的影響因素。在CDs基WLED中添加高PL QY的紅光成分可獲得暖調WLED(CRI為2 000~3 500 K),其顯示出較高CRI和色溫,且色純度不會隨著工作電流變化而時刻變化,還能夠避免芯片發出過多藍光對人眼視網膜造成傷害[78]。Fan課題組[12]將藍光、綠光及PL QY為53%的紅光CDs,分別分散在PVP和聚甲基丙烯酸甲酯中獲得了三基色熒光粉,通過調整3種熒光粉的配比制備得到了CRI為97、在20 mA驅動電流下發光效率高達31.3 lm·W-1的高性能暖白色LED。其發光效率可與目前稀土及無機半導體量子點基WLED相媲美,且價格存在極大優勢。Yuan等[11]成功制備了藍色、紅色及白色LED,證明了CDs可作為光致LEDs的活性發光層。WLED表現出非常好的穩定性,最大亮度為2 050 cd·m-2,電流效率為1.1 cd·A-1,在色度圖上坐標為(0.30,0.33),其性能幾乎與傳統半導體量子點WLED性能相當。該WLED不含空穴傳輸層結構,作者認為其發光機理是空穴和電子分別通過PEDOT∶PSS的空穴注入層和TPBI的電子傳輸層注入CDs活性發光層,電子和空穴在發光層進行輻射復合實現發光。Zhai等[78]則將綠光碳點嵌入淀粉、紅光碳點嵌入PVP制備熒光粉,并按照熒光峰位從大到小順序依次沉積在InGaN芯片上制備WLED。由于PVP的保護作用,熒光粉可長期維持強發光。如圖9(c)、(g)所示,在WLED中,InGaN芯片的藍光發射(450 nm)首先激發淀粉層發綠光(532 nm),接著綠光激發PVP層發紅光,最終產生寬光譜發射,獲得CIE為(0.33,0.33)、CRI為92的WLED。

圖9 (a)~(b)基于CDs的LED器件及其能級示意圖;(c)基于雙色CDs的WLED制備示意圖;(d)基于雙色CDs的WLED下不同顏色筆帽的圖像;(e)工作中的WLED的CIE色度圖;(f)日光下不同顏色筆帽的圖像;(g)工作中的WLED的發射光譜[10,78]。Fig.9 (a)-(b)LED device based on CDs and its energy level diagram. (c)Schematic diagram of WLED preparation based on two-color CDs. (d)Images of different color caps under WLED based on two-color CDs. (e)CIE chromaticity diagram of WLED at work. (f)Images of pen caps of different colors in daylight. (g)Emission spectrum of WLED at work[10,78].
作者對比了在制備的WLED和日光下不同顏色筆帽圖像,可以發現兩種場景中筆帽顯示出幾乎相同的顏色(如圖9(d)、(f))。
4.2 紅光碳點用于生物應用
紅光碳點一直是生物檢測和治療領域的熱門選擇,可用作熒光探針、光熱治療試劑等。例如,高效紅光發射可有效避免生物組織自吸收、生物分子自熒光、潛在光損傷以及較低組織滲透等缺點,進而實現更佳的成像效果[79-80]。
Liu等[76]在丙酮中利用紅豆杉葉溶劑熱合成FWHM僅為20 nm的近紅外發射CDs,并通過硅膠柱層析法進行純化。在413 nm激發下,深紅色發射CDs的PL QY高達59%,在660 nm激發下PL QY為31%。其在深紅光區具有很強的光吸收和發射能力、毒性低且生物相容性好,作為單光子和雙光子生物成像探針時可通過小鼠腎臟系統和肝膽系統迅速排出。如圖10(a)所示,在640 nm激發下(發射705 nm),作者評估了CDs在裸鼠體內的成像性能。靜脈注射CDs后0.25 h和0.5 h,在小鼠體內可見清晰明亮的熒光,循環24 h后熒光信號變得微弱,表明深紅碳點可以在成像后迅速從小鼠體內排出。另外,他們在注射后不同時間點收集了器官熒光成像,如圖10(b),圖像顯示CDs主要聚集在肝、肺和腎中,而在腦、心臟和睪丸中可忽略不計。
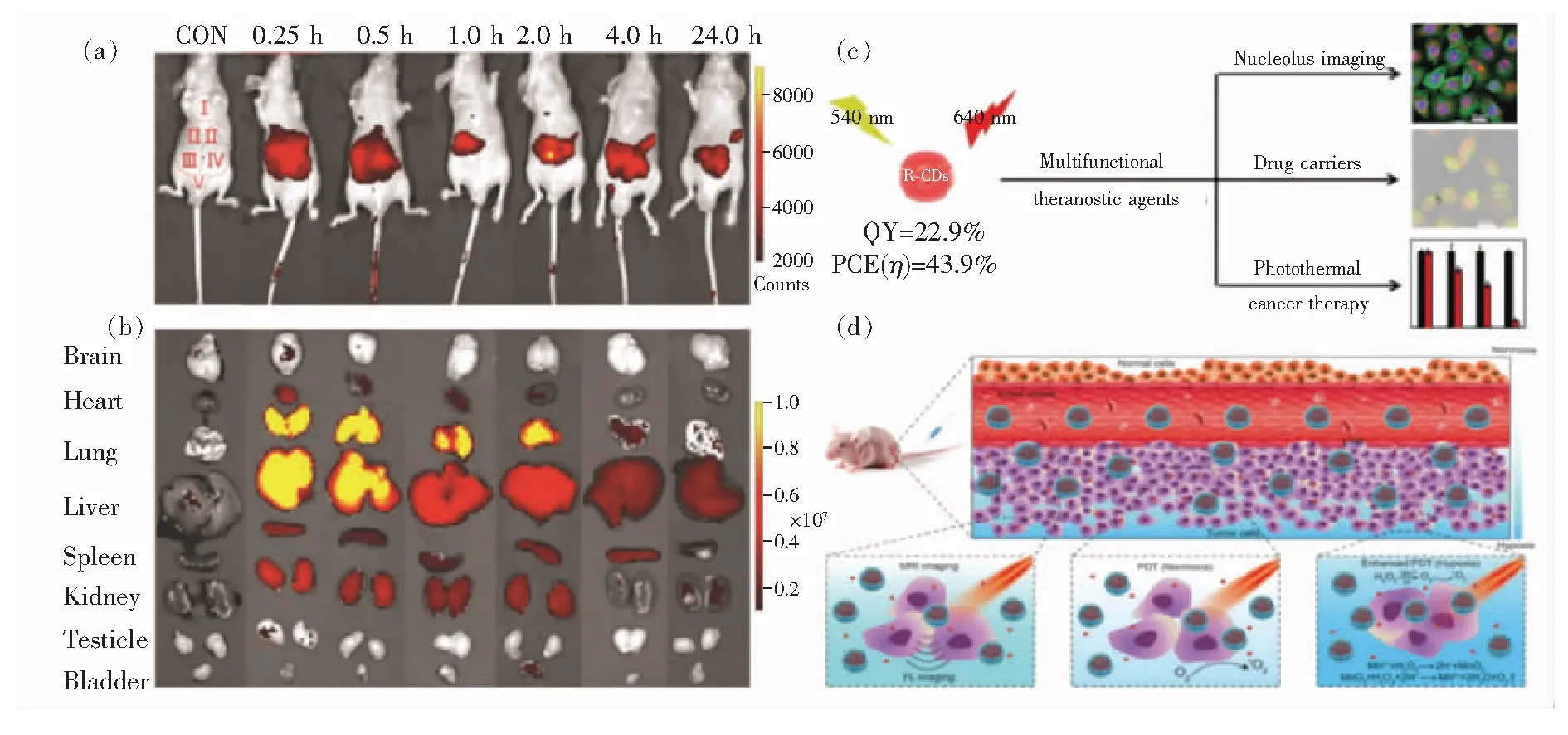
圖10 (a)不同時間靜脈注射CDs仰臥裸鼠體內成像(Ⅰ:胸腔區域,Ⅱ:肝臟區域,Ⅲ:小腸區域,Ⅳ:大腸區域,Ⅴ:膀胱區域);(b)不同時間通過靜脈注射CDs裸鼠器官離體實時成像;(c)近紅外發射CDs用于核仁成像、藥物傳遞和光熱光譜分析癌癥治療示意圖;(d)Mn-CDs組裝體作為酸性H2O2驅動增氧器以增強抗癌效率示意圖[76,17,49]。Fig.10 (a)In vivo imaging of supine nude mice with intravenous injection of CDs at different time points(Ⅰ: thoracic region,Ⅱ: area of liver, Ⅲ: area of small intestine, Ⅳ: area of large intestine, Ⅴ: bladder region). (b)Real-time ex vivo imaging of nude mice with intravenous injection of CDs at different time points. (c)Schematic diagram of prepared near-infrared emission CDs for nucleolus imaging, drug delivery and photothermal spectroscopy for cancer treatment. (d)Schematic illustration of the Mn-CD assembly as an acidic H2O2-driven oxygenerator to enhance the anticancer efficiency of in a solid tumor[76,17,49].
Jia的課題組[81]使用高度共軛芳族胺——三(4-氨基苯基)胺作為前體并引入氧化自由基試劑,合成了超窄FWHM的紅光碳點。其熒光發射為615 nm,PL QY高達84%,而發射光譜FWHM只有27 nm。隨后,他們使用合成的CDs作為上轉換光致發光探針進行近紅外雙光子生物成像實驗。與傳統單光子成像方法相比,利用近紅外光子激發雙光子熒光成像可以滲透到更深生物組織中。在1 100 nm熒光激發下,使用CDs作為探針,對腫瘤球體成像深度可超過200 μm;而在單光子激發下,穿透深度只有100 μm。
除了最傳統的生物成像,紅光碳點在遞送藥物和腫瘤治療[82]方面也大放異彩。Sun等[17]制備的發射峰為640 nm紅光碳點在單光子和雙光子模式下都能使富含RNA的細胞核染色。此外,它還可以與異硫氰酸熒光素配合,并將其帶入活細胞,這意味著紅光碳點可作為載體,將不能或幾乎不能直接進入活細胞的藥物直接輸送至病灶,如圖10(c)所示。由于具有高光熱轉換效率,紅光碳點在體外光熱癌癥治療中同樣表現優異。如圖10(d),Jia等[49]發現制備的磁熒光Mn-CDs可以有效產生單線態氧(1O2),以及高度催化H2O2生成氧氣,用于光動力治療癌癥(富氧條件會抑制腫瘤生長,產氧速率越快治療效果越好)。進一步地,作者采用自組裝法制備出一種用于近紅外熒光(最大峰值在745 nm)成像的智能造影劑。以上特性使Mn-CDs不僅可以作為酸性H2O2驅動產氧器來提高缺氧實體腫瘤中的氧濃度,以增強治療效果,還能同時進行雙峰熒光/加權磁共振成像。
除此之外,紅光碳點可用于制作各種光學探針以檢測活細胞中的金屬離子、陰離子、pH值和生物分子等,某些疏水CDs可到達蛋白質內部以示蹤肽鏈展開軌跡進而揭示肽鏈構象對于蛋白質功能的影響[30]。
5 總結和展望
本文綜述了國內外近年來紅光碳點在制備、發光機理及光電器件、成像等應用方面的研究進展,主要總結了量子限域效應、表面態、聚集效應等在紅光調控方面的作用機制,以及紅光碳點合成過程中前驅體和溶劑的重要性。盡管CDs在長波段發射峰調控方面取得了重要成果,但紅光碳點仍存在熒光量子效率低、FWHM較寬且需要藍綠光激發的缺陷,制備量子效率高、FWHM窄、生物相容性好的深紅光/近紅外光碳點是目前亟需解決的難題。
首先,紅光碳點合成手段在綠色、可重復、規模化、低成本等方面仍存在一定壁壘。迄今為止,多數報道的紅光碳點仍面臨著耗時或者耗能問題,有些試劑不僅昂貴還具有一定毒性,這導致后處理手段繁瑣低效,并進一步限制了紅光碳點的實際發展。因此,使用生物質材料作為前驅體或利用一些可持續方法來綠色批量化制備紅光碳點將是未來重點發展的方向之一。
其次,目前文獻報道的紅光碳點發光機理還不夠系統全面。由于制備方法本身的局限性,大多數機理引入了粒徑、表面態、異質原子摻雜等多重影響因素。在應用層次,紅光碳點相比其他探針而言,由于其表面基團的豐富性,會更易受外界電解質影響,從而降低自身靈敏性和選擇性。因此,探究一種尺寸、結構、成分、表面態等均勻分布紅色碳點的制備方法是解決以上問題的有效途徑。如何通過先進實驗手段來精準調控CDs的結構組成以深入探索其發光機理迫在眉睫。
綜上所述,紅光碳點由于其優異的光電特性,在未來幾年里,會在光電器件、生物成像、生物傳感、載藥、加密防偽和光催化等領域具有重要應用價值。

