血清尿酸預測非瓣膜性心房顫動射頻消融術后復發的相關性研究
雷志博,黃改榮
心房顫動(atrial fibrillation,AF)是臨床上常見的心律失常之一,其發病率隨年齡的增長而逐漸增加,隨著我國進入老齡化社會,心房顫動的高患病率和高致殘率給家庭和社會帶來極大的經濟負擔。近年來,由于導管射頻消融術具有轉復心房顫動和維持竇性心律的作用,已經成為非瓣膜性心房顫動(NVAF)病人的一線治療方法。通過大規模臨床隨訪證實,NVAF病人導管射頻消融術后仍有30%~50%的復發率[1-2],高復發率給病人帶來極大的經濟負擔和心理壓力,所以尋求心房顫動術后復發的預測因素成為新的研究熱點。血清尿酸是人體嘌呤代謝的最終產物,近年來有研究指出,尿酸通過激活促炎因子,促使炎癥反應發生,可影響心房的電重構和結構重構,對心房顫動的發生、發展與復發等方面具有十分重要的作用[3-4]。然而,關于血清尿酸與NVAF射頻消融術后復發的關系研究較少,本研究探討血清尿酸與NVAF病人射頻消融術后復發的關系,明確血清尿酸是否為NVAF術后復發的獨立危險因素,以期指導臨床監測與干預。
1 資料與方法
1.1 臨床資料 收集河南省人民醫院心內科2018年1月—2018年12月因NVAF行射頻消融術治療的86例病人。根據術后心房顫動復發與否分為復發組(27例)與未復發組(59例)。入選標準:入院前根據病史、心電圖或者24 h動態心電圖確診為心房顫動,符合 《2016年ESC心房顫動管理指南》或《2019年AHA/ACC/HRS心房顫動管理指南》中關于心房顫動的消融適應證[5-6]。均為第1次進行環肺靜脈電隔離(CPVI)射頻消融治療的NVAF病人,且臨床資料完整。心臟超聲心動圖檢查:左心房前后徑(LAD)≤50 mm,左心室射血分數(LVEF)≥50%。術前經食道心臟超聲證實無左心房或左心耳血栓形成。排除標準:心臟瓣膜病、心肌病、急慢性心力衰竭、各種急慢性感染、嚴重肝腎功能障礙、甲狀腺功能亢進或減低、惡性腫瘤、血液系統疾病等。
1.2 研究方法 詳細記錄病人臨床資料,包括性別、年齡、心房顫動病程、體質指數(BMI)、既往口服藥物、合并疾病等。入院后完善超聲心動圖檢查,測定LAD、LVEF、左心室舒張末期內徑(LVEDD)等指標。收集術前血常規、肝功能、腎功能、尿酸、超敏C反應蛋白(hs-CRP)等檢驗結果。
1.3 隨訪 術后3個月內發生快速房性心律失常不算復發,計為空白期。隨訪3個月后至研究結束時病人的復發情況,經過電話及門診隨訪,主要隨訪內容包括: ①詢問快速房性心律失常發作的相關癥狀(包括心悸、胸部不適、氣短、乏力等); ②收集病人心律失常發作時的心電圖或24 h動態心電圖。復發標準:復發定義為射頻消融術3個月后,根據體表心電圖或動態心電圖記錄到的持續時間超過30 s的快速房性心律失常(包括房性心動過速、心房撲動、心房顫動)。

2 結 果
2.1 兩組臨床資料比較 86例心房顫動病人均進行射頻消融術,隨訪(4~12)個月,共 27例復發(復發組),復發率31.4%,59例未復發(未復發組)。兩組間基線特征,包括年齡、性別、高血壓病、冠心病、口服藥物、BMI、肌酐、LVEF、LVEDD等比較差異均無統計學意義(P>0.05)。而心房顫動病程、hs-CRP、血清尿酸、LAD比較差異有統計學意義(P<0.05)。詳見表1。

表1 兩組基線資料比較
2.2 多因素Logistic回歸分析 以射頻消融術后是否復發為應變量,以病程、LAD及術前尿酸、hs-CRP、BMI和LVEF水平為自變量行二分類Logistic 回歸分析,結果顯示,LAD及術前尿酸、hs-CRP水平是NVAF射頻消融術后復發的獨立預測因素(P<0.05)。詳見表2。
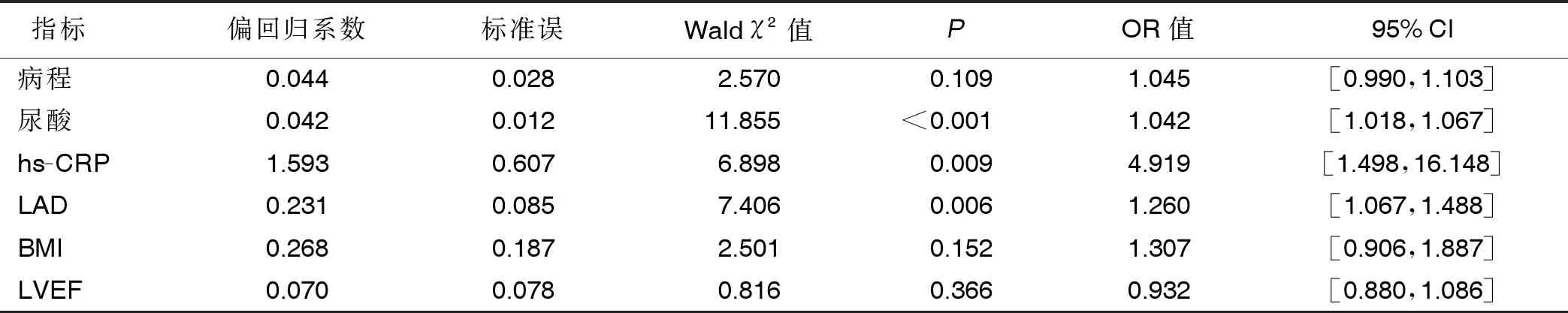
表2 心房顫動病人術后復發預測因子的Logistic回歸分析結果
2.3 尿酸、LAD、hs-CRP在預測NVAF消融術后復發中的ROC曲線分析 尿酸ROC曲線下面積為0.787[95%CI(0.680,0.895),P<0.001],當尿酸取最佳截斷值為0.557時,預測術后復發的敏感度為77.8%,特異度為78%。LAD的ROC曲線下面積為0.717[P=0.001,95%CI (0.600,0.833)],當LAD取最佳截斷值為0.343時,預測術后復發的敏感度為85.2%,特異度為49.2%。hs-CRP的ROC曲線下面積為0.657[P=0.020,95%CI(0.530,0.784)],當hs-CRP取最佳截斷值為0.341時,預測術后復發的敏感度為63%,特異度為71.2%。尿酸在心房顫動射頻消融術后復發中比LAD、hs-CRP更具有預測價值,差異有統計學意義(P<0.05)。詳見圖1。
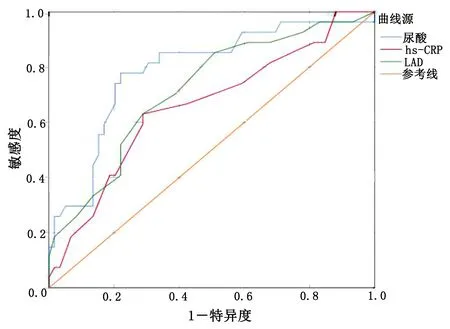
圖1 血清尿酸、LAD、hs-CRP預測NVAF射頻消融術后復發的ROC曲線
3 討 論
心房顫動是臨床常見的心律失常,可引起嚴重并發癥如心力衰竭、缺血性腦卒中、心肌梗死等,嚴重危害人類健康,高患病率和高致殘率對心房顫動的治療提出了巨大的挑戰,藥物通常作為治療心房顫動的首選方案,但在臨床工作中經常出現病人依從性差、抗凝藥物使用不充分、抗心律失常藥物療效欠佳等情況。目前各大指南均給予導管射頻消融術很高的推薦級別,但術后的低有效率和高復發率仍是目前亟待解決的難題。關于心房顫動射頻消融術后復發的機制尚不明確,多認為其與心房電重構、結構重構、炎癥反應、氧化應激水平等相關[7-8]。既往研究表明,心房顫動病程、BMI、C反應蛋白、LAD及心房纖維化等可能是NVAF術后復發的獨立預測因素[9-14]。但是對NVAF導管消融術后復發的預測準確率仍不足,因此,尋找更多的預測因素可以為術后易復發病人的早期識別及干預提供理論依據。
血清尿酸是黃嘌呤氧化酶催化嘌呤代謝產生的最終產物, 血清尿酸水平與多種心腦血管疾病有關,包括高血壓、糖尿病、心房顫動、心力衰竭、冠心病和卒中[15-16]。Tamariz等[17]通過一項前瞻性隊列研究結果表明尿酸是新發心房顫動的獨立危險因素。Nyrnes等[18]對大樣本人群進行Cox回歸分析后發現,尿酸水平增加與心房顫動發生風險呈正相關。Canpola等[19]的前瞻性研究結果表明,術前血尿酸水平與術后心房顫動復發有顯著的相關性,可以作為預測術后復發的獨立預測因素。有研究認為,血清尿酸水平升高可增加氧化應激,并直接損傷內皮功能,同時促進增生和促進炎性反應進一步加重,導致蛋白質變性、細胞壞死、線粒體功能障礙,造成心房的成纖維細胞增殖、遷移、分化,導致心房肌纖維化,引起心房結構重構和電重構[20-23],因此,血清尿酸水平被認為是組織氧化應激和炎癥反應的標志物,與心房顫動的發生、發展和復發具有十分密切的關系。
本研究發現,尿酸、hs-CRP水平和LAD可作為心房顫動病人射頻消融術后復發的獨立預測因素,而心房顫動病程不是術后復發的獨立預測因素,考慮與本研究收集病例時未進行嚴格心房顫動分類有關,陣發性心房顫動病人長期病程可能并不會導致嚴重的結構重構,而BMI與射頻消融術后復發無關,考慮與本研究只進行了術前采集,未進行連續BMI監測以及隨訪時間短有關。血清尿酸作為臨床工作中一種經濟、易檢測的生物標志物,與多種疾病有關,應當受到臨床醫生的重視和關注。本研究提示,血清尿酸可能會對NVAF射頻消融術后復發具有一定的預測價值,但尿酸與射頻消融術后復發的機制和關系仍需今后進行大規模、多中心隨機對照研究來進一步驗證。此外,對術前尿酸進行臨床干預是否可減少術后復發率,仍需進一步的臨床研究證實。
本研究的局限性在于:為小樣本回顧性研究,雖對射頻消融術后的獨立預測因素進行確定,但沒有進行尿酸亞組分析,對臨床工作中將尿酸降低在何種水平缺乏指導。雖然已經進行臨床隨訪,但仍有可能存在部分無癥狀性心房顫動未能被檢出;沒有進行心房顫動分組,不能排除不同心房顫動類型對射頻消融術后復發的影響。

