栓塞微球在原發性肝癌中的研究進展
閆歌 周學素 程玉瑩 秦若夢 田啟威 楊仕平

摘 ?要: 原發性肝癌是目前致死率較高的癌癥,如何在治療過程中減輕癌癥患者的痛苦,且提高治療效果是各國學者研究的熱點.經導管動脈栓塞(TAE)被認為是一種微創的、目的性強的且風險低的治療方法,已成為非手術治療原發性肝癌的首選方法.TAE治療是通過微導管將栓塞材料堵塞實體瘤的肝動脈,從而阻礙了腫瘤的氧氣和營養的供給,達到殺死腫瘤細胞的目的.介入栓塞治療效果的好壞歸因于栓塞材料,即栓塞材料的設計及使用.文章基于不同種類的栓塞材料展開綜述,歸納了栓塞微球在原發性肝癌中的研究進展,并對開發新型的栓塞材料提供了可借鑒的思路.
關鍵詞: 原發性肝癌; 經導管動脈栓塞(TAE); 栓塞微球; 靶向治療
中圖分類號: TQ 460.1 ? ?文獻標志碼: A ? ?文章編號: 1000-5137(2021)06-0714-07
Abstract: Primary liver cancer is currently a cancer with a high fatality rate, which has always been a difficult problem for people to overcome. How to reduce the pain of cancer patients and improve the treatment effect during the treatment process is a hot spot for scholars from all over the world. Transcatheter arterial embolization(TAE) is considered as a minimally invasive, purposeful and low-risk treatment, and has become the first choice for non-surgical treatment of primary liver cancer. TAE kills the tumor cells via blocking the hepatic artery of the solid tumor through microcatheter, which can hinder the supply of oxygen and nutrition to the tumor. The effect of interventional embolization is attributed to the design and use of embolic materials.Therefore, based on embolic materials, this paper reviews different kinds of embolic materials, summarizes the research progress of embolic microspheres in primary liver cancer, and provides ideas for the development of new embolic materials.
Key words: primary liver cancer; transcatheter arterial embolization(TAE); embolic microsphere; targeted therapy
0 ?引 言
癌癥一直是人們努力攻克的難關之一,由于環境污染日益加重、不健康的生活方式、人口老齡化等問題,導致癌癥的發病率大幅度增加,嚴重危害了人們的健康[1-2].肝癌是最常見的腫瘤之一,傳統的治療方法有外科手術切除、化學藥物治療、放射治療和介入治療等[3-5].目前,外科手術切除是治療肝癌的重要手段,但是大多數腫瘤具有侵襲性,難以通過手術完全切除病變區域,所以需要考慮和使用有效的非手術治療手段.
近些年來,栓塞治療在臨床醫學上異軍突起,已成為了熱門話題,且不斷地被人們提及和應用.經導管動脈栓塞(TAE)是一項微創治療手段[6-7],能夠借助導管選擇性地將栓塞材料注入到腫瘤的供血動脈中,將實體瘤的肝動脈堵塞,切斷腫瘤供血,使其無法獲取生存所需的氧氣和營養,從而有效地抑制了腫瘤生長.TAE具有微創、目的性強、風險低等優點,已成為非手術治療肝癌的首選方法.經過人們在臨床中的不斷摸索和實踐,TAE技術已被公認為是可以有效改善癌癥患者病情、能明顯提高癌癥患者生存率的有效介入治療方法,且栓塞材料是TAE治療的關鍵所在[8].本文作者就目前已研發的栓塞材料在肝癌治療中的現狀和進展作一綜述.
1 ?栓塞材料
在TAE技術中,栓塞材料的選擇決定了介入栓塞的治療效果.近年來,微球在生物醫學領域受到了廣泛的關注,理想的栓塞材料應具有以下特征:1) 良好的生物相容性;2) 原料簡單,易于制備;3) 材料粒徑達到栓塞要求,可通過微導管進行遞送;4) 無黏連,能在血管中均勻分散.基于此,以下將主要綜述目前醫學治療中使用的栓塞微球.
1.1 傳統栓塞微球
傳統的栓塞微球與其他不規則栓塞顆粒相比,具有均一且規則的形貌,在微導管中具有良好的流動性,不易在體內與周圍組織發生反應,具有其他不規則形狀材料所沒有的優良性能.
傳統的栓塞微球按照材料性質分為兩種:一種是非生物可降解材料,在體內具有良好的生物相容性,能夠長期栓塞肝動脈,例如聚乙烯醇(PVA)微球、海藻酸鹽(SAL)微球[9-10];一種是生物可降解的高分子材料,天然獲取沒有毒性,可以降低長期栓塞對血管的傷害性,這類微球有聚乳酸(PLA)、聚丙交酯-乙交酯(PLGA)、淀粉微球和明膠微球[11-12].栓塞微球能夠利用微導管準確遞送到肝動脈,使血管栓塞不能給腫瘤細胞提供氧氣和營養,抑制腫瘤細胞的增殖,從而提高了抗腫瘤性能.
1.2 載藥微球
化學藥物治療,即利用化療藥物進行消除腫瘤的治療,能夠快速被細胞攝取,阻礙細胞的復制和增殖,在低濃度和短時間內便可表現出強烈的細胞毒性[13-14].化療藥物在腫瘤部位的停留時間和藥物濃度決定了其治療效果,但是化療藥物在體內對細胞缺乏了選擇性,在殺傷腫瘤細胞的同時,對正常組織細胞和免疫細胞也會一同進行損傷.如何提高化療藥物在腫瘤部位的停留時間和藥物濃度,是目前研究的熱點.由于栓塞微球具有較大比表面積,可以裝載大量的化療藥物,將化療與血管栓塞進行結合,借助微導管準確地將材料靶向遞送到腫瘤部位,實現化療藥物的原位控制釋放,明顯提高了腫瘤部位的藥物濃度,實現化療性栓塞腫瘤,產生協同治療作用,可以極大地提高治療腫瘤的效率.
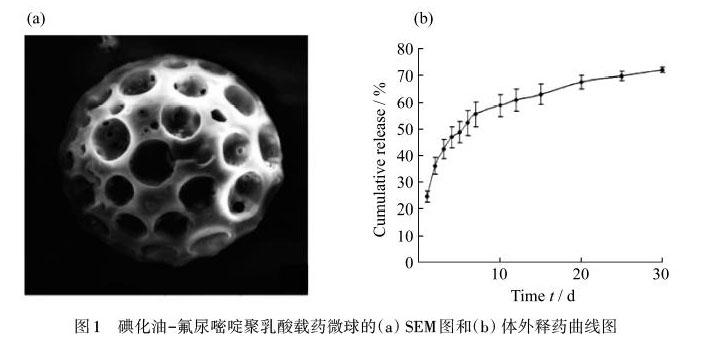
王新霞等[15]采用具有良好生物相容性的聚乳酸(PLA)作為載體,加入了陽性造影劑碘化油,利用復乳法制備了微球,將化學藥物氟尿嘧啶(5-Fu)裝載到可顯影的碘化油-氟尿嘧啶聚乳酸微球中,研制了具有顯影和治療雙重效果的碘化油-氟尿嘧啶聚乳酸載藥微球.所合成的碘化油-氟尿嘧啶聚乳酸載藥微球如圖1所示,表面有孔且球形圓整,平均粒徑約100 μm,通過微導管選擇性地將載藥微球注入腫瘤供血動脈,通過阻斷血管將微球固定在腫瘤部位,使肝動脈血流減少了80%~100%,使病灶組織缺血、缺氧壞死;并且該微球具有一定的藥物緩釋作用,在栓塞的同時能緩慢釋放5-Fu,使化療藥物能夠長期作用于病灶部位,有利于治療效果的提高;通過增強納米載體的滲透性和滯留(EPR)效應,以及納米材料的持續釋放來延長藥物的藥理時間和藥效,達到殺傷腫瘤的目的.說明了碘化油-氟尿嘧啶聚乳酸載藥微球具有誘導栓塞、顯影和緩釋化療等多種功能,在栓塞動脈腫瘤血管的同時釋放并積累藥物,可以達到良好的治療效果.
1.3 智能響應微球
智能響應性材料是指具有根據環境的變化使自身結構或者功能快速發生變化的一類載體[16-17].近年來,智能響應性載體因具有優異的穩定性、對外界刺激快速智能響應且有優異生物治療能力等特點,對其在治療和診斷領域的研究顯得十分活躍.由于栓塞微球為高分子材料,具有優異的可修飾性,可以與不同類型的刺激響應性官能團修飾而進行改性,同時有些智能響應性材料也可以在不同環境進行響應,開發成智能響應性微球[18].智能響應微球載體的構建,提高了載體的安全性和靶向性,能夠在腫瘤部位進行聚集,根據不同的微環境的刺激做出響應,達到增強療效的目的.根據智能響應微球在腫瘤部位對不同刺激的響應,可以將其分為pH響應性微球、溫度響應性微球和多重刺激響應性微球.
1.3.1 pH響應性微球
pH響應性材料含有可電離的基團或者酸致斷裂的化學鍵,可以在低pH環境下發生材料的構象變化,表現出溶脹或者坍塌的現象[19].由于腫瘤細胞繁殖能力強,代謝旺盛,導致大量乳酸的生成,使腫瘤具有微酸環境,所以利用腫瘤組織和正常組織中不同的pH梯度,將pH響應性材料接枝在微球表面,當微球達到低pH環境時,可通過基團結構變化或化學鍵斷裂來響應,以此制備pH響應性微球載體.
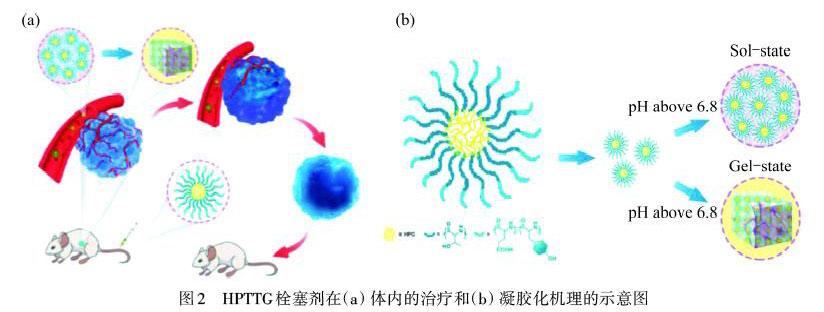
LU等[20]受pH響應性藥物傳遞系統的啟發,開發了一種新的無創、靶向靜脈注射栓塞治療方法.該方法基于一種酸性微環境響應性超支化聚(氨基酸)(HPTTG),通過L-氨基酸N-羧酸酐(NCA)的開環聚合,制備了具有pH響應性的栓塞微球,簡化了栓塞治療程序,提高了栓塞治療的依從性和普適性.通過調節共聚物中酸性氨基酸的比例,控制溶膠-凝膠相變的pH值,降低HPTTG的pH值.如圖2所示,當HPTTG到達腫瘤部位時,由于酸性的微環境,它會轉化為水凝膠,并停留在腫瘤部位.通過荷瘤動物實驗結果表明:HPTTG具有良好的靶向性和栓塞能力,注射后8 h在腫瘤部位蓄積最多,腫瘤血管閉塞;20 d左右腫瘤被抑制壞死.因此,HPTTG不僅可以作為新型栓塞材料用于多種實體腫瘤的有效無創栓塞治療,而且為設計pH響應性微球載體提供了很好的范例.
1.3.2 溫度響應性微球
溫敏性材料具有較低的臨界溶解溫度(LCST)[21-22],在LCST附近溫敏性材料會快速響應溫度的變化而發生結構改變,并進行降解.同時,由于腫瘤組織病變或者外界環境的改變都能引起其溫度局部升高,所以將溫敏性材料修飾在微球表面,使栓塞微球具有溫度敏感性,以此制備溫度響應性微球載體.
JEONG等[23]運用了微流控技術以水包油(W/O/W)雙乳液滴作為模板,制備了具有核殼結構且粒徑均勻的PVA微球.聚N-異丙基丙烯酰胺(PNIPAAm)是溫度敏感性聚合物,含有熱響應性,以PNIPAAm為載體,將金納米棒包裹其中,形成了一種生物相容性良好的乙基纖維素殼層.如圖3所示,金納米棒吸收了近紅外光,提高了水凝膠顆粒的溫度,當高于聚合物的LCST時,水凝膠顆粒收縮,導致了顆粒和殼層基質之間形成宏觀間隙,相對較大的分子可以通過這些間隙,這種結構的結合可以通過近紅外光遠程控制膜的通透性.
由于PNIPAAm的相變行為是高度可逆的,通過去除激光照射足夠的時間讓金納米棒冷卻,這種光觸發的滲透性可以被重復地打開和關閉.因此,將所開發的微球和溫敏性材料進行結合具有巨大的應用潛力,特別是對于基于植入的高分子量藥物的釋放.
1.3.3 多重刺激響應性微球
僅有單一響應性的微球載體已經難以滿足多元化應用的需求,多種響應性微球隨之應運而生,受到了人們越來越多的關注.多重響應性微球通常裝載了2個或者2個以上的單體聚合物,可以針對不同的刺激進行多重響應[24],達到更好的治療效果,成為了多功能、多方式診療癌癥的重要方法.
MU等[25]利用聚苯乙烯磺酸鹽(PSS)、殼聚糖(CS)和SAL層層組裝技術形成PSS@(CS/SAL)4微球,運用硝酸鈰銨作為氧化還原引發劑,與N-異丙基丙烯酰胺(NIPAm)接枝聚合,成功制備了具有pH/離子強度/溫度多響應殼結構的PSS@(CS/SAL)4-g-PNIPAm微球.如圖4所示,當聚N-異丙基丙烯酰胺(PNIPAm)聚合物在LCST約為32 ℃時,稀水溶液中會發生從盤繞到球狀的相變,而且pH值的降低會削弱SAL和CS之間的鹽鍵強度,使微球殼層之間沒有離子交聯.所以在pH/離子強度雙響應型微球殼層中引入PNIPAm刷子,不僅實現了藥物分子在溶液pH和溫度雙重控制下的可控釋放,而且防止了多響應型微球在較高鹽濃度溶液中的絮凝.與采用層層組裝法制備的普通聚電解質微球或微膠囊相比,多響應微球具有結構穩定、獨特的雙重控制(pH和溫度)等特點,可作為優良的智能藥物微球載體應用于臨床.
2 ?總結與展望
近年來,伴隨著人們對肝癌的病理基礎與臨床治療的深入研究,TAE技術慢慢出現在人們的視野中,逐漸突破了肝癌的治療瓶頸,并在臨床上具有廣闊的應用前景.本文作者著重討論了微球介入治療技術的發展進程:1) 栓塞微球能夠通過微導管精準地進行物理靶向,能夠有效地栓塞肝動脈;2) 將藥物與栓塞進行結合,具有物理靶向栓塞和藥物打擊作用的聯合治療效果;3) 將不同的刺激響應性基團與微球載體進行修飾,進一步給予了微球載體不同的響應能力.栓塞微球技術在國內應用比較晚,單一的治療方式往往難以達到預期的效果,亟需開發新型高效、精準靶向且具有良好生物相容性的栓塞微球.應不局限于栓塞與藥療的結合,在后續的研究中將其與綜合療法進行結合,可以落實到多學科交叉治療,合理地構建多功能的栓塞治療平臺,經導管介入的栓塞治療領域必將取得重大突破.
參考文獻:
[1] ARBYN M, WEIDERPASS E, BRUNI L, et al. Estimates of incidence and mortality of cervical cancer in 2018: a worldwide analysis [J]. Lancet Global Health,2020,8(2):E191-E203.
[2] SUNG H, FERLAY J, SIEGEL R L, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries [J]. CA:A Cancer Journal for Clinicians,2021,71(3):209-249.
[3] WANG Z, PENG Y F, HU J W, et al. Associating liver partition and portal vein ligation for staged hepatectomy for unresectable hepatitis B virus-related hepatocellular carcinoma A single center study of 45 patients [J]. Annals of Surgery,2020,271(3):534-541.
[4] SUN J Y, YIN T, ZHANG X Y, et al. Therapeutic advances for patients with intermediate hepatocellular carcinoma [J]. Journal of Cellular Physiology,2019,234(8):12116-12121.
[5] LIU D, LIU F, XIE X Y, et al. Accurate prediction of responses to transarterial chemoembolization for patients with hepatocellular carcinoma by using artificial intelligence in contrast-enhanced ultrasound [J]. European Radiology,2020,30(4):2365-2376.
[6] ZHU Y X, FENG B, MEI L, et al. Clinical efficacy of TACE combined with apatinib in the treatment of advanced hepatocellular carcinoma [J]. Journal of Buon,2019,24(2):608-614.
[7] KIM W, CHO S K, SHIN S W, et al. Combination therapy of transarterial chemoembolization (TACE) and radiofrequency ablation (RFA) for small hepatocellular carcinoma: comparison with TACE or RFA monotherapy [J]. Abdominal Radiology,2019,44 (6):2283-2292.
[8] BAIK S H, PARK H J, KIM J H, et al. Mechanical thrombectomy in subtypes of basilar artery occlusion: relationship to recanalization rate and clinical outcome [J]. Radiology,2019,291(3):730-737.
[9] WANG Q, XIAO A, LIU Y M, et al. One-step preparation of nano-in-micro poly(vinyl alcohol) embolic microspheres and used for dual-modal T-1/T-2-weighted magnetic resonance imaging [J]. Nanomedicine:Nanotechnology Biology and Medicine,2018,14(8):2551-2561.
[10] HOU F L, ZHU Y H, ZOU Q, et al. One-step preparation of multifunctional alginate microspheres loaded with in situ-formed gold nanostars as a photothermal agent [J]. Materials Chemistry Frontiers,2019,3(10):2018-2024.
[11] SOMMER C M, DO T D, SCHLETT C L, et al. In vivo characterization of a new type of biodegradable starch microsphere for transarterial embolization [J]. Journal of Biomaterials Applications,2018,32(7):932-944.
[12] ZHANG L P, LIU M, QI T, et al. Preparations and properties of drug-eluting embolization microspheres based on modified gelatin [J]. Soft Materials,2018,16(2):117-125.
[13] KASHYAP D, TULI H S, YERER M B, et al. Natural product-based nanoformulations for cancer therapy:opportunities and challenges [J]. Seminars in Cancer Biology,2021,69:5-23.
[14] CUI D, HUANG J G, ZHEN X, et al. A semiconducting polymer nano-prodrug for hypoxia-activated photodynamic cancer therapy [J]. Angewandte Chemie International Edition,2019,58(18):5920-5924.
[15] 王新霞, 張麗, 周閨臣, 等. 可顯影碘化油-氟尿嘧啶聚乳酸微球的研制 [J]. 第二軍醫大學學報,2010,31(10):1100-1103.
WANG X X,ZHANG L,ZHOU G C,et al. Preparation of visualized iodized oil-5-fluorouracil loaded polylactic acid microspheres [J]. Academic Journal of Second Military Medical University,2010,31(10):1100-1103.
[16] GAO S T, TANG G S, HUA D W, et al. Stimuli-responsive bio-based polymeric systems and their applications [J]. Journal of Materials Chemistry B,2019,7(5):709-729.
[17] SUN H, KABB C P, SIMS M B, et al. Architecture-transformable polymers: reshaping the future of stimuli-responsive polymers [J]. Progress in Polymer Science,2019,89:61-75.
[18] BI Y G, LIN Z T, DENG S T. Fabrication and characterization of hydroxyapatite/sodium alginate/chitosan composite microspheres for drug delivery and bone tissue engineering [J]. Materials Science and Engineering C,2019,100:576-583.
[19] LIANG Y P, ZHAO X, MA P X, et al. pH-responsive injectable hydrogels with mucosal adhesiveness based on chitosan-grafted-dihydrocaffeic acid and oxidized pullulan for localized drug delivery [J]. Journal of Colloid and Interface Science,2019,536:224-234.
[20] LU D D, WANG J C, LI Y F, et al. Tumor noninvasive and target embolization therapy platform by intravenous injection based on acidic microenvironment-responsive hyperbranched poly(amino acid)s [J]. ACS Central Science,2020,6(11): 1977-1986.
[21] SPONCHIONI M, PALMIERO U C, MOSCATELLI D. Thermo-responsive polymers: applications of smart materials in drug delivery and tissue engineering [J]. Materials Science and Engineering C,2019,102:589-605.
[22] BORDAT A, BOISSENOT T, NICOLAS J, et al. Thermoresponsive polymer nanocarriers for biomedical applications [J]. Advanced Drug Delivery Reviews,2019,138:167-192.
[23] JEONG W C, KIM S H, YANG S M. Photothermal control of membrane permeability of microcapsules for on-demand release [J]. ACS Applied Materials and Interfaces,2014,6(2):826-832.
[24] WANG S M, YANG Y, SHI X Y, et al. Multiple stimuli-responsiveness fluorescent probe derived from cyclopolymers and pyrene-ended ammonium salts [J]. ACS Applied Polymer Materials,2020,2(6):2246-2251.
[25] MU B, LIU P, LI X R, et al. Fabrication of flocculation-resistant pH/ionic strength/temperature multiresponsive hollow microspheres and their controlled release [J]. Molecular Pharmaceutics,2012,9(1):91-101.
(責任編輯:郁慧,馮珍珍)

