重組人促紅細胞生成素治療新生兒缺氧缺血性腦病的效果分析
朱 萍 李德亮 張偉業
南陽市中心醫院,河南 南陽 473000
新生兒缺氧缺血性腦病(hypoxic-ischemic encephalopathy,HIE)是指在孕婦待產及分娩期間胎兒在母體內因臍帶、羊水異常等各種原因造成宮內窘迫,進而導致缺血缺氧引起的腦部病變,也常見于出生后的窒息缺氧引起的腦損傷[1-3]。該病是新生兒科臨床常見病,多見于足月兒,但也可出現于早產兒,是導致新生兒時期死亡的主要殺手和造成嬰幼兒時期生長發育障礙的主要原因,嚴重影響新生兒的遠期預后[4-6]。因此,早診斷、早治療對患兒救治成功率和康復率具有重要意義。目前臨床對新生兒HIE的診斷方法除根據具有明顯的圍生期窒息史且見于生后12 h或24 h內出現異常神經癥狀,如意識障礙、肌張力改變及原始反射異常等臨床表征進行診斷外[7-9],影像學技術已經成為新生兒HIE診斷的常用方法,其更有利于臨床有效揭示病理和及時掌握病程及治療進展,如計算機斷層掃描顯像(computed tomography,CT)、磁共振成像(magnetic resonance imaging,MRI)等影像學技術。CT和MRI在診斷新生兒HIE時各有優缺點和側重點,目前將CT與MRI聯合診斷HIE的應用價值已經被醫學界所重視,并得到多數臨床醫生的肯定,將兩種方法聯合應用可以彌補相互的不足,進一步提高診斷準確率[10-13]。新生兒HIE早期治療方法主要有對癥支持、高壓氧及亞低溫等。對癥支持即“三支持、三對癥”,是綜合措施療法,而高壓氧與亞低溫療法在新生兒HIE治療中有異曲同工之處,目的均在于促進有氧代謝或抑制異常代謝,以減少有害代謝產物,如兒茶酚胺等毒性物質損傷腦組織,通過保護血腦屏障以降低顱內壓和減輕腦水腫,從而促進腦細胞及神經功能修復等[14-17]。
目前新生兒HIE尚缺乏有效對癥治療的藥物,中國倉鼠卵巢細胞(Chinese hamsters ovary,CHO)系表達的重組人促紅細胞生成素(recombinant human erythropoietine,rHu-EPO)被發現在人體或受試動物模型中具有調控造血的功能,即通過促進骨髓紅系細胞的分化和增殖,從而使得造血功能和貧血癥狀得到恢復和改善,其在新生兒臨床常見病治療中早期被用來防治早產兒貧血,后來亦被證實其對HIE患兒神經有保護作用[18-22]。為觀察rHu-EPO對新生兒HIE早期干預的效果和評價其對患兒神經生長發育的影響,南陽市中心醫院結合實際接診的病例情況在遵循一般治療方案前提下采用rHu-EPO治療新生兒HIE。
1 資料與方法
1.1一般資料選擇2016-09—2018-08南陽市中心醫院收治的HIE患兒,入選標準均遵循新生兒HIE的診斷標準[23]。(1)符合中度-重度HIE診斷及分型標準;(2)胎齡≥37周的足月兒;(3)入院時間<72 h;(4)出生時體質量≥2 500 g;(5)無嚴重心腦、氣管及肺等先天性發育畸形;(6)無染色體及先天性代謝性疾病;(7)無大量顱內出血;(8)無嚴重感染及呼吸困難等疾病。選擇符合上述條件的50例患兒隨機分成對照組25例和試驗組25例,2組患兒在性別、胎齡、體質量、HIE分度及分娩方式等方面差異無統計學意義(P>0.05)。
1.2治療方法2組患兒在出生當日的治療開始階段根據新生兒HIE治療指南方案進行對癥支持的常規治療,包括予以營養腦細胞藥物和高壓氧治療等早期干預及康復治療措施。試驗組在上述常規治療基礎上的第3天予以rHu-EPO治療,400 IU/kg,首次為皮下注射,后改為靜脈注射,2天1次,每周3次,連續4周。
1.3療效評價2組在出生后第7天、第14天及第28天分別進行新生兒行為神經測定(neonatal behaviral neurological assessment,NBNA),該評分涵蓋了行為能力、主動肌張力、被動肌張力、原始反射及一般狀況等5大列項20小分項內容,滿分40分,以分值35劃界評定歸屬正常或者異常,即評分≥35分為正常,評分<35分為異常[24]。患兒治療3個月后返院復診,根據中國嬰幼兒智能發育量表(CDCC)對2組復診患兒分別進行智能發育指數(MDI)和運動發育指數(PDI)的測定,即MDI和PDI評分均>90分為正常,70~90分屬于邊緣狀態,<70分視為異常[25]。

2 結果
2.1rHu-EPO對HIE患兒的近期療效分析經rHu-EPO治療后,試驗組3次的NBNA評分均明顯高于對照組,差異有統計學意義(P<0.01)。見表1。
2.2rHu-EPO對HIE患兒生長發育的影響對照組MDI、PDI評分均低于試驗組,差異有統計學意義(Z=17.286,P<0.05),根據復診和隨訪未發現與rHu-EPO相關的不良反應,無短期危害和風險。見表2。
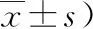
表1 2組療程內3次NBNA評分比較 (分,

表2 2組治療3個月后的智能測試評分比較 [n(%)]
3 討論
新生兒HIE為臨床中高發病癥,其臨床主要癥狀可表現為興奮或遲鈍、昏迷或驚厥、肌張力改變、意識障礙、神經反射異常等,是導致新生兒死亡的主要原因之一,調查顯示約25%的存活患兒存在智力障礙、癲癇、腦癱等神經系統后遺癥[26-28]。新生兒HIE的發生與孕婦自身貧血、妊娠期高血壓、糖尿病、心肺疾病、臨產期羊水中度及重度污染、胎盤前置或早剝、胎兒臍帶繞頸或過度扭轉甚至打結以及產程異常等一系列圍生因素密切相關,具有發病危急且機制復雜的特征,因此有效預防、及時診斷和積極治療是關鍵[29-31]。新生兒HIE治療方案至今仍未完整統一,現行均強調綜合支持療法,臨床對圍生期新生兒HIE亦缺乏特效對癥的藥物,近年來用于臨床研究和早期干預性治療的藥物主要有神經節苷脂、納洛酮、腦苷肌肽、地塞米松、苯巴比妥、神經生長因子、rHu-EPO、丹參及川芎注射液等,其中rHu-EPO應用于HIE治療一直為醫學界所關注[32]。促紅細胞生成素(EPO)是一種具有生物活性的內源性糖蛋白激素,具有刺激和促進紅細胞生成的作用,又稱紅細胞刺激因子、促紅素,早已有外源性rHu-EPO用于臨床中各種原因引起的貧血治療。
隨著近二十年來研究的不斷深入,EPO的這種“非造血”作用已逐漸被闡明,同時基于腦損傷模型的研究表明EPO亦被證實具有神經營養及神經保護作用。研究發現人體神經系統的很多組織和細胞(如脊髓、神經元、神經膠質細胞、血管內皮細胞和海馬細胞等)都存在EPO及EPOR受體的表達,同時這種內源性表達量可受缺氧刺激調控,亦可被低血糖、氧化應激所誘導。研究已證實靜脈或腹腔注射EPO后腦脊液中EPO濃度明顯升高,且與血濃度相關,表明EPO自身能通過血腦屏障,同時由于新生兒血腦屏障發育不完善,再加上血腦屏障受損,也導致其通透性增加,可見外源性rHu-EPO應用于臨床治療HIE具備了有效的通道條件。隨著rHu-EPO逐漸應用于臨床實踐,其應用越來越廣泛,尤其是rHu-EPO聯合其他藥物的療法用于新生兒HIE及早產兒貧血治療獲得更為滿意的療效。EL-LAHONY等[33]采用rHu-EPO聯合鐵、維生素E和葉酸治療早產兒貧血,表明rHu-EPO可促進紅細胞生成,并顯著減少患兒輸血的需要。研究表明rHu-EPO與神經節苷脂聯合用藥可以明顯改善HIE患兒的神經行為和中樞神經系統功能,具有良好的臨床療效,且安全性較高,基于rHu-EPO的神經保護作用采用這種聯合用藥療法具有較高的臨床應用價值。本研究也證實rHu-EPO對新生兒HIE具有顯著療效,經rHu-EPO治療后試驗組NBNA評分均明顯高于對照組(P<0.01)。
EPO對HIE神經保護作用機制十分復雜,基于已有研究主要包括:(1)拮抗谷氨酸興奮毒性作用;(2)通過抑制炎癥相關因子生成而具有抗炎作用;(3)通過調控NO表現出抗氧化作用;(4)通過維持神經細胞生存表現出抗凋亡作用;(5)通過與血管內皮生長因子互作促進腦血管生成作用;(6)通過增加神經營養因子的生成起到神經重構作用;(7)通過促進少突膠質前體細胞的分化和成熟以減少白質損傷;(8)通過影響鈣離子振動頻率進而改變谷氨酸鹽受體的傳導來改善腦水腫。本研究中對照組MDI、PDI評分均低于試驗組(P<0.05),說明rHu-EPO具有神經保護和恢復作用,由此可推測rHu-EPO應用于新生兒HIE的臨床治療將有助于患兒遠期的生長發育,根據復診和隨訪情況,本文所報告病例在治療和觀察期內均未發現與rHu-EPO相關的不良反應,無短期危害和風險。
本研究探討了新生兒HIE應用rHu-EPO治療的短期療效,并預見了遠期預后,表明rHu-EPO可有效減輕HIE患兒神經細胞損害,并促進神經功能恢復,改善認知障礙及行為異常,rHu-EPO對HIE患兒的生長發育有利無害。本次研究不足之處在于受樣本量的限制本治療方案僅進行了單一恒定劑量的短期給藥治療,而聯合用藥、縱向不同劑量給藥、治療周期及遠期影響等方面還需進一步探索。

