萬古霉素/PLGA/TCP多孔復合材料修復羊感染性骨缺損
許剛 何純青 張飛 克里木 尹東峰 吾木爾 劉劍 賈勇
新疆軍區總醫院1全軍骨科中心創傷骨科(關節組),2藥劑科(烏魯木齊830000)
近年來,隨著工業的發展,越來越多的工傷、車禍傷以及術后繼發感染導致的感染性骨缺損愈發常見,尤其以合并慢性骨髓炎的感染性骨缺損的治療一直是骨科領域中的一大難題[1]。針對慢性骨髓炎的治療,目前臨床上在一期清創后會植入混合抗生素的骨水泥(polymethyl methacrylate,PMMA)珠鏈作為間置器,其在填充死腔及骨缺損的同時可通過釋放抗生素來控制感染。但因其無法降解,2~3月后如感染得到完全控制,則需行二期手術取出骨水泥珠鏈,安裝外固定架進行骨搬運治療骨缺損[2]。但該方案將導致患者面臨治療周期長、手術次數多、醫藥花費高等情況,這將對患者造成沉重的負擔。因此,是否能研制出一種既具有抗感染效果,又具有良好生物降解性的骨移植材料,在有效控制感染的同時又可不斷降解,為同時進行的骨修復提供充足的空間,這已成為當前骨科領域的研究熱點之一。研究表明,利用聚乳酸?羥基乙酸[poly(lactic?co?glycolic acid),PLGA]與磷酸三鈣(tricalcium phosphate,TCP)構建的復合多孔支架材料具有良好的生物相容性和降解性,并且還具有一定的生物力學支撐性[3-4]。但因傳統的增材制造打印法工作溫度高,無法將抗生素添加進材料中,導致該類材料不具有抗感染效果,無法應用于感染性骨缺損的治療中[5]。
然而,低溫3D 打印技術的出現,使得抗生素在打印墨水中的添加成為了可能。3D 打印技術是利用計算機輔助設計(computer aided design,CAD)和計算機輔助制造(computer aided manufacturing,CAM)技術,在低溫(零下30 至40 攝氏度)條件下將復合高分子材料層層堆積得到的個性化三維實體。本次研究結合臨床實際,利用低溫3D 打印技術首次將廣泛用于治療甲氧西林耐藥金葡菌引起的慢性骨髓炎的萬古霉素[6-7]復合進PLGA 與TCP的支架材料中,成功打印出復合萬古霉素/PLGA/TCP 的多孔支架,并在前期已通過體外實驗證實其具有良好的生物相容性及萬古霉素緩釋效應。所以,本次研究采用山羊股骨感染性骨缺損為模型,進一步通過動物實驗證實復合萬古霉素/PLGA/TCP 的多孔支架的抗感染效果和生物降解效應,為其后期的臨床運用提供可靠的實驗數據。
1 資料與方法
1.1 主要儀器設備和材料主要儀器設備:(1)低溫沉積生物3D 打印機(型號SUNP BP11 上普博源生物科技有限公司,北京);(2)真空冷凍干燥機(型號LGJ?12 松源華興,北京);(3)X 射線機(Faxitron X?ray 公司,美國);(4)HP1100 高效液相色譜儀(惠普,美國)。主要試劑:(1)聚乳酸?羥基乙酸,PLGA75/25(山東省藥學科學院中試廠,特性粘度:1.0 ± 0.1 dL/g);(2)β?磷酸三鈣TCP(Sigma公司,美國);(3)1,4?二氧六環(Sigma 公司,美國);(4)蘇木素伊紅(HE)染色試劑盒(碧云天,中國上海)。
1.2 新型復合萬古霉素/PLGA/TCP支架的制備低溫快速成型3D 打印PLGA/TCP 基本支架可參考既往文獻[9-11]。本次實驗用支架打印具體步驟及參數如下:(l)用Mimics 軟件MEDCAD 模塊創建CAD 模型,支架規格:長×寬×高為20 mm × 20 mm× 15 mm;(2)材料配制比例:15%PLGA+1.5%TCP+1.5% 萬古霉素;有機溶劑(1,4?二氧六環)占比80%;(3)打印機參數:噴頭溫度35 ℃,口部直徑0.6 mm,打印速度9 mm/s,平臺溫度-25 ℃,填充圖案為鋸齒狀,走線距離1.8 mm,孔隙率設置為80%;(4)固化方式:將低溫3D 打印材料于-40 ℃靜置24 min,轉移至冷凍干燥機,設置真空度10 Pa 冷凍干燥48 h,以1 ℃/h 速度升溫至20 ℃,此過程有機溶劑(1,4?二氧六環)可被完全移除。
1.3 萬古霉素骨水泥珠鏈制備將聚甲基丙烯酸甲酯粉體與萬古霉素粉(重量比10∶1)混合后,加入聚甲基丙烯酸甲酯單體,混合后注入模具,用手術縫線串起,制備成萬古霉素骨水泥珠鏈,骨水泥珠直徑5 mm,備用。
1.4 山羊股骨感染性骨缺損建模新疆軍區總醫院動物實驗倫理委員會批準了此項研究計劃。蘇博美利奴羊12只,不分雌雄,體質量(51.2±3.5)kg,建立股骨感染性骨缺損模型。具體方法如下:采用氯胺酮(2 mg/kg 體質量)和鹽酸賽拉嗪(50 mg/kg 體質量)(體積比為1∶1)進行全身麻醉,以維持動物在整個手術過程中的麻醉狀態;剔除右側髖部及右下肢羊毛,肥皂水和清水依次沖洗后將羊固定在手術臺,常規聚維酮碘溶液消毒右下肢,鋪無菌單,貼隔離膜。大腿表面縱向切開并剝離皮下軟組織,暴露股骨,使用擺鋸(Synthes 公司,瑞士)截除股骨中段皮質骨,長15 mm,用生理鹽水充分沖洗切口。在骨缺損位置滴入1 mL 金黃色葡萄球菌液(1.0 ~1.25)×109CFU/mL,繼續圈養4周,觀察到手術傷口有膿性分泌物,確立以骨髓組織的細菌培養陽性及有死骨、或竇道形成的臨床表現為標準,則為建模成功,可進行材料移植實驗。
1.5 復合萬古霉素/PLGA/TCP 的多孔支架材料的植入手術麻醉及切開同上一步驟。對感染股骨進行截骨清創,擺鋸股骨截除殘端,去除炎性肉芽直至正常組織顯露,碘伏消毒創面后,用生理鹽水充分沖洗切口。選取合適長度的支架,末端接觸殘留的骨斷端以壓配的方式放入缺損區,股骨骨缺損處植入修復材料,實驗組1(3D 多孔支架組)植入復合萬古霉素/PLGA/TCP 的多孔支架材料,實驗組2(骨水泥珠鏈組)植入萬古霉素骨水泥珠鏈,空白對照組不植入任何材料,每組設立4 只實驗動物,術后放置引流管,逐層縫合傷口。
1.6 術區萬古霉素濃度測定及殺菌活性分析術后1、4、6 周在利多卡因局部麻醉下,采用骨活檢針鉆取植入區組織或組織液,組織粉碎后采用生理鹽水500 μL 洗提,采用高效液相色譜儀測量洗提液中萬古霉素含量。將8 μL 組織洗提液滴加至直徑7 mm 的圓紙片上,風干后在長滿金黃色葡萄球菌標準株(ATCC25923)的血瓊脂平板上進行抑菌環實驗,35 ℃后培養18 h 后測量殺菌圈直徑。
1.7 不同時間點的血液分析術后1、4、8、12 周分別抽取血液行血常規、血沉、C?反應蛋白的檢測。
1.8 術區X?Ray 及組織學檢測術后12 周行X?Ray 檢測,觀察骨缺損愈合及支架吸收情況。同時術后12 周過量麻醉處死實驗動物術區行手術取材,移植區樣品在4%多聚甲醛(pH 7.2)固定24 h,取出并用磷酸鹽緩沖液(PBS)清洗后,在37 ℃恒溫搖床里放入脫鈣液乙二胺四乙酸(EDTA)2月,大約每7 d 更換脫鈣液,脫鈣完全后,沿股骨冠狀平面方向切開缺損部位,觀察面朝向底面放入一次性包埋盒,進入制作組織切片程序。自動組織脫水機(Leica?ASP200S,德國)按骨組織標準程序進行脫水,然后將脫水處理后的組織用石蠟包埋機(BMJ?1,天津天力航空機電,中國)進行包埋。下一步,用切片機(Leitz?1516,德國),制備了5 mm厚的組織切片,HE 染色。
1.9 統計學方法數據統計分析以及制圖運用GraphPad Prism version 5(GraphPad software,San Diego,CA)軟件,計量資料以均數±標準差表示,不同組間比較采用方差分析(ANOVA),P< 0.05為差異有統計學意義。
2 結果
2.1 總體情況所有實驗動物均存活。對照組2只動物跛行,創面破潰,表面肉芽組織形成。3D 多孔支架組和骨水泥珠鏈組傷口愈合良好,無跛行。
2.2 不同時間點各組血液中白細胞、血沉、C?反應蛋白的變化術后1、4、8、12 周各組血液檢測結果提示空白對照組各時間段的白細胞、血沉及C?反應蛋白均維持在較高水平,而3D 多孔支架組和骨水泥珠鏈組在第一周時三種指標均顯著低于對照組,第4、8、12 周時數值均逐漸下降,相比空白對照組具有統計學意義(P<0.05,表1 ~3)。該結果證實骨水泥珠鏈組和3D 多孔支架組均有著良好的抗感染效果。
2.3 不同時間點術區萬古霉素濃度測定術后第1 周骨水泥珠鏈組和3D 多孔支架組感染性骨缺損區的組織液中均能檢測到萬古霉素,其濃度都在20 mg/L 之上,但骨水泥珠鏈組顯著高于3D 多孔支架組(P<0.05),而術后4、6 周時3D 多孔支架組的萬古霉素濃度顯著高于骨水泥珠鏈組(P< 0.05),證明骨水泥珠鏈組和3D 多孔支架組均能有效釋放萬古霉素,3D 多孔支架組的長期釋放效果更好(圖1)。
表1 各組實驗羊血液中白細胞的動態變化Tab.1 The dynamic changes of white blood cells counts in the three groups ±s,×109/L

表1 各組實驗羊血液中白細胞的動態變化Tab.1 The dynamic changes of white blood cells counts in the three groups ±s,×109/L
注:3D 多孔支架組與對照組相比,*P<0.05
指標對照組骨水泥珠鏈組3D 多孔支架組1 周24.04±3.6 14.45±2.3*13.58±3.1*4 周20.24±1.6 9.04±2.8*8.71±3.2*8 周16.34±1.7 8.04±2.3*8.53±1.3*12 周15.32±4.7 7.64±1.3*7.13±1.1*
表2 各組實驗羊血液中CRP 的動態變化Tab.2 The dynamic changes of C?reactive protein in the three groups ±s,mg/L

表2 各組實驗羊血液中CRP 的動態變化Tab.2 The dynamic changes of C?reactive protein in the three groups ±s,mg/L
注:3D 多孔支架組與對照組相比,*P<0.05
指標對照組骨水泥珠鏈組3D多孔支架組1周286.40±23.1 167.50±25.3*147.580±21.1*4周207.40±17.6 46.40±12.8*43.10±14.2*8周180.30±16.7 18.40±3.3*15.53±3.9*12周150.30±14.7 8.64±3.3*7.13±2.1*
表3 各組實驗羊血液中血沉的動態變化Tab.3 The dynamic changes of erythrocyte sedimentation rate in the three groups ±s,mm/h

表3 各組實驗羊血液中血沉的動態變化Tab.3 The dynamic changes of erythrocyte sedimentation rate in the three groups ±s,mm/h
注:3D 多孔支架組與對照組相比,*P<0.05
指標對照組骨水泥珠鏈組3D 多孔支架組1 周68±7 54±6*56±4*4 周57±6 33±5*36±7*8 周47±6 18±4*16±7*12 周38±5 10±2*9±3*
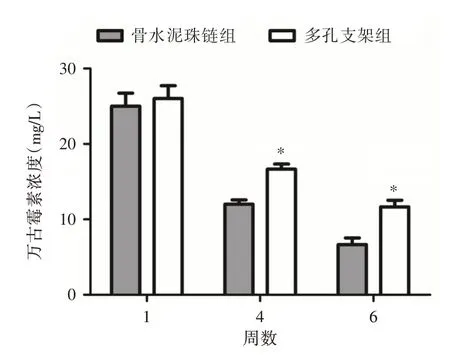
圖1 不同時間段萬古霉素濃度測定Fig.1 The concentration of Vancomycin in different time periods
2.4 不同時間點術區萬古霉素活性測定術后第1 周骨水泥珠鏈組和3D 多孔支架組感染性骨缺損區的組織液均有抗菌活性,兩者抗菌效果相當,但術后4、6 周時3D 多孔支架組的抗菌效果顯著優于骨水泥珠鏈組(P< 0.05),證明3D 多孔支架組的長期抗菌效果更優(圖2)。
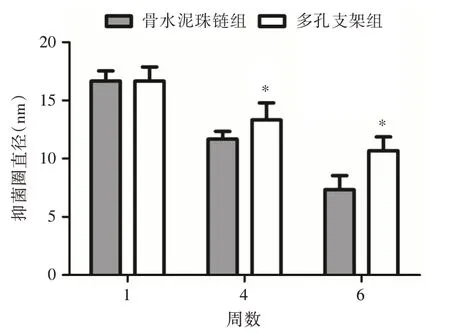
圖2 不同時間段萬古霉素活性測定Fig.2 The determination of Vancomycin activity in different time periods
2.5 術后12 周時X?Ray 評估對照組無支架植入的缺損區,新生骨組織結構分散,大約在4 周截骨末端逐漸閉合。3D 多孔支架組植入缺損部位之后,觀察到新生骨沿股骨長軸生長,并在缺損區內向中間部分延伸,最后與缺損遠端骨組織橋接(圖2 ~5)。術后12 周時3D 多孔支架組X?Ray 影像顯示骨缺損處支架信號模糊,可見明顯吸收跡象。骨水泥珠鏈組也可以見到不同程度的骨生長,受珠鏈占位影響,其新生骨的面積顯著低于3D 多孔支架組和對照組。缺損區骨量分析結果顯示,3D 多孔支架組的缺損區骨量明顯高于骨水泥珠鏈組和對照組,新生骨占缺損區面積的93%、42%和64%(P<0.05)。
2.6 組織學結果分析HE 染色結果發現:沒有植入支架的空白組的缺損區見大量結締組織填充,骨缺損近端和遠端可見新生骨質向缺損中心延伸,但沒有形成骨橋連接。3D 多孔支架組可見板層骨位于兩端,中間是骨髓組織,斷端與正常板層骨連接在一起。3D 打印支架表面可見新生骨組織直接沉積在支架小梁表面。成骨細胞樣細胞排列在新形成的骨組織表面,在支架小梁表面類骨質覆蓋,可見新生骨橋連接骨缺損的兩個斷端。骨水泥珠鏈組亦可見到新生骨組織,但受到骨水泥珠影響,缺損區新生骨面積小于3D 多孔組和空白對照組。
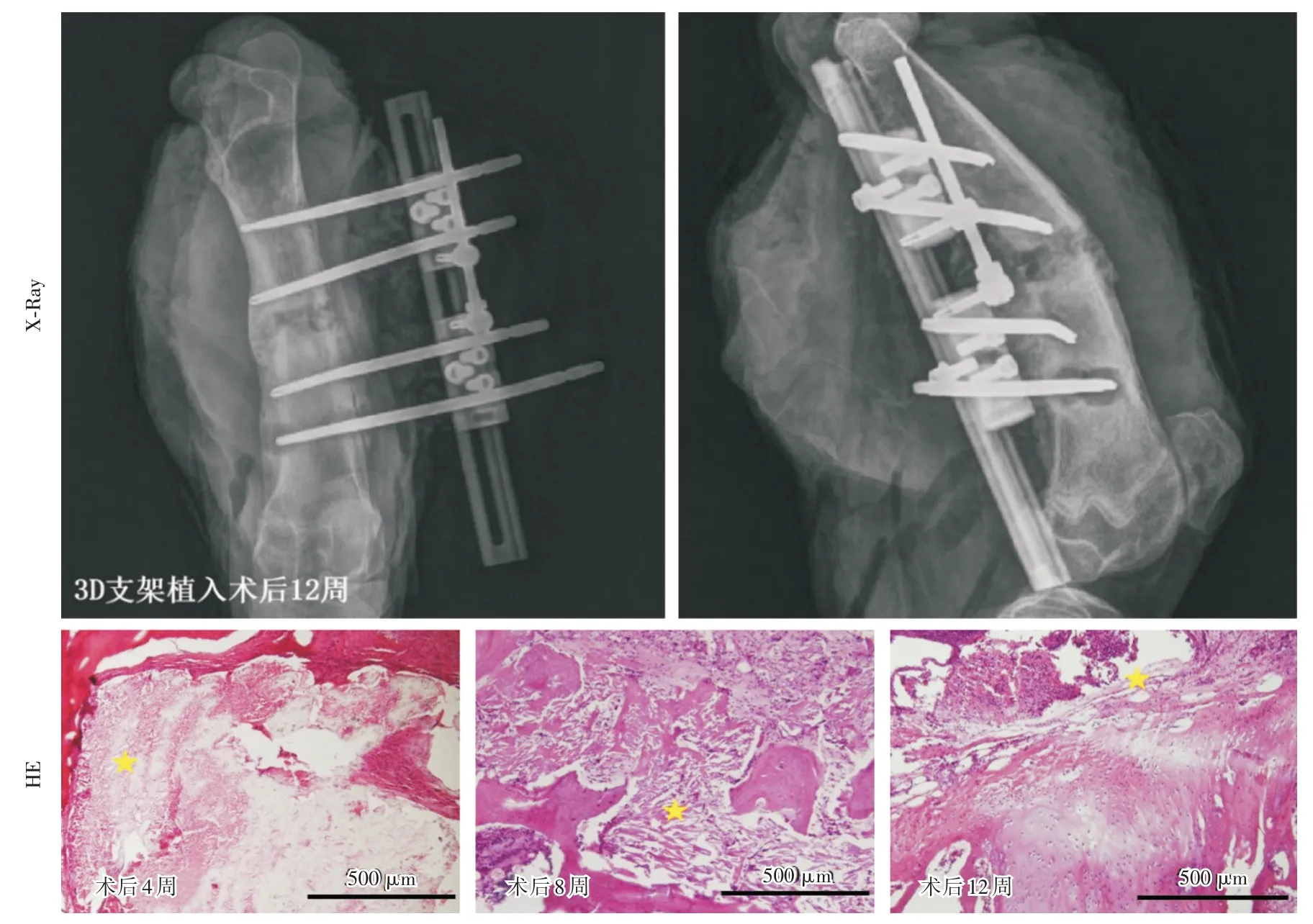
圖3 術后12 周3D 多孔支架組X?Ray 及術后4、8、12 周HE 染色評估支架降解情況Fig.3 The X?Ray and HE stain of 3D scaffold group at the different time points after the operation
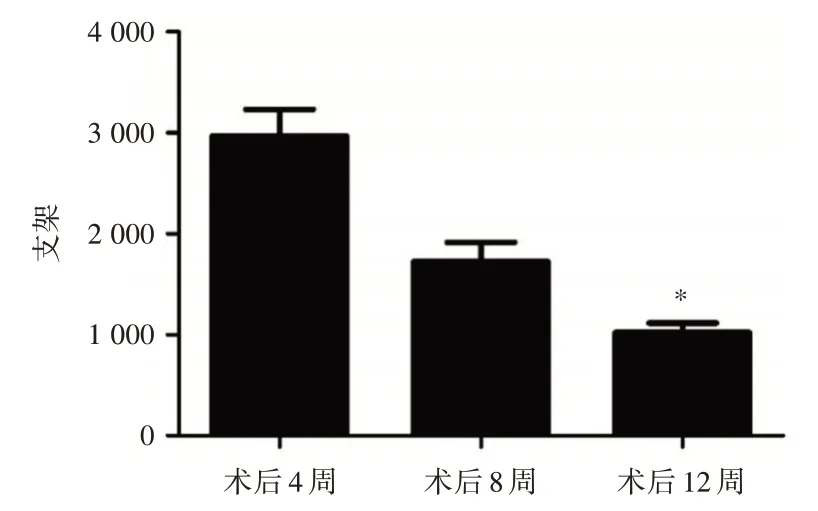
圖4 術后4、8、12 周3D 多孔支架降解情況Fig.4 The degradation of 3D scaffold at the different time points after the operation
3 討論
慢性骨髓炎伴骨缺損的治療一直是骨科臨床工作中面臨的一大難題,其具有骨質破壞、死骨形成、竇道反復流膿的病理特點,而一期病灶清除配合骨水泥珠鏈植入控制感染,二期外固定支架行骨搬運術已成為治療該類疾病的常規手段[8-9]。對于治療慢性骨髓炎而言,徹底的清創和抗生素的有效運用是治愈的關鍵[10-11]。作為局部抗生素代入的介質,骨水泥珠鏈的使用已有30年歷史,其治療效果在臨床中也已得到驗證[12]。混合抗生素的骨水泥珠鏈不僅可以填補局部死腔和骨缺損,提供一定的力學支撐,還可以在局部逐漸釋放高濃度抗生素,避免全身用藥時血液中的抗生素濃度過高而產生毒副作用[13-15]。
但是,骨水泥珠鏈的缺點是不能進行有效的生物降解,植入后存在占位效應,無法在初期為骨缺損的愈合提供有效的空間,這勢必將使患者面臨多次手術帶來的創傷及經濟壓力,而同時具備抗感染效果和生物降解性的骨移植材料的成功研發將有可能解決這一難題。如何在抗感染治療的同時,實現骨的長入成為骨科醫生的夢想。所以,要想制備的植入物具備多種特性,靠單一的材料構成無法滿足,而復合材料的出現和進一步應用為上述研究目標的達成提供了一條捷徑[16]。
因此,本次研究利用3D 低溫打印技術,創新性的將PLGA、TCP 及萬古霉素融合在一起,打印出復合萬古霉素/PLGA/TCP 的多孔支架材料,具備多種優點。首先,3D 打印技術具有優異的個體化制定特點,可以利用CT/MRI 等影像學數據,根據患者自身特征性的骨缺損來打印與之匹配的植入材料,保證了尺寸及空間的完美匹配,為支架提供更好的力學支撐提供了保障[17-18]。其次,3D 打印技術可以參考前期的體外實驗數據,個性化的定制材料的孔隙率和結構,使材料的生物力學及緩釋效應達到最優化[19-20]。
筆者前期的實驗結果證實3D 打印的復合萬古霉素/PLGA/TCP 的多孔支架在孔隙率為80%時,其具有最優的抗生素緩釋效應。不僅如此,在本次動物實驗中,3D 多孔支架組的抗感染效果與骨水泥珠鏈組相當,充分證實了該種材料的抗感染效果已達到臨床應用標準,能夠有效控制慢性骨髓炎的局部感染病灶。最后,該材料的生物降解效應是本研究關注的重點。在山羊股骨感染性骨缺損模型中,通過植入3D 多孔支架材料,在術后12 周時發現其本身相對于4 周時發生了顯著的降解,這證明復合萬古霉素/PLGA/TCP 的多孔支架在具備抗感染效應的同時,還具有良好的生物降解性。
由此可見,將復合萬古霉素/PLGA/TCP 的多孔支架運用于臨床治療慢性骨髓炎伴骨缺損患者時,可在一期清創植入該種材料后即刻安裝骨搬運支架,隨著感染的完全控制和材料的逐漸吸收,骨搬運的治療可以同步進行,免除了二次手術取出植入物才可進行骨搬運這一步驟,避免多次手術所造成的創傷,同時將顯著縮短患者的治療周期和費用,這無疑將產生良好的社會效應。
應用低溫3D 打印技術設計研發的新型復合萬古霉素/PLGA/TCP 多孔支架材料不僅具有良好的抗感染效應,而且還具有穩定的生物降解性,其應用于臨床后將極大的縮短慢性骨髓炎伴骨缺損患者的治療周期及費用。同時該材料構成合理、價格低廉、較易獲得,具有極大的臨床應用潛力,將有望成為一種治療慢性骨髓炎伴骨缺損的理想骨移植材料。

