miR?17?5p通過下調肌球蛋白調節輕鏈相互作用蛋白促進結直腸癌細胞增殖和轉移的機制研究
凌旭坤 謝文鴻 張喆 胡琛
惠州市中心人民醫院胃腸外科(廣東惠州516200)
結直腸癌(colorectal cancer,CRC)是嚴重威脅全球人群健康的主要公共衛生問題之一,在男女性高發腫瘤中常年位居前3 位,且男性的發病率明顯高于女性[1]。許多研究表明[2-3],CRC 的發展與腫瘤細胞的惡性增殖和轉移有關。因此,探討CRC增殖和轉移的分子機制對其臨床治療十分關鍵。
miRNA 的異常表達被證明與腫瘤細胞的增殖和轉移密切相關,其可靶向下游mRNA,調控腫瘤的發展進程[4-6]。研究表明,miR?17?5p 與腫瘤的發生發展相關[7-9]。但miR?17?5p 在CRC 中的作用機制仍有待探討。肌球蛋白調節輕鏈相互作用蛋白(myosin regulatory light chain interacting protein,MYLIP)參與細胞運動和遷移的調節[10-11]。通過生物信息學網站預測得知MYLIP 是miR?17?5p 的潛在靶基因,然而,目前還沒有關于MYLIP 在CRC 發展過程中的重要作用的研究,因此,本文將探討miR?17?5p 調控MYLIP 表達的潛在機制及其在CRC 增殖及轉移中的作用,為尋找CRC 的有效治療靶點探索新的道路。
1 材料與方法
1.1 組織標本、細胞系及主要試劑收集2017年12月至2018年1月在惠州市中心人民醫院切除的60 例CRC 患者的癌及癌旁組織標本。研究方案征得醫院倫理委員會批準。CRC 細胞系SW620(貨號:ATCC CCL?227),Caco?2(貨號:ATCC HTB?37),HT29(貨號:ATCC HTB?38),Lovo細胞(貨號:ATCC CCL?229)及結腸上皮細胞FHC(貨號:ATCC CRL?1831)均購買自美國ATCC 公司。胎牛血清、RPMI?1640培養基購自美國Gibco公司,miR?17?5p抑制劑(miR?17?5p inhibitor)及其陰性對照(NC)和siRNAs購自上海吉瑪制藥技術公司,TRIzol RNA 提取試劑盒及SYBR PCR Master Mix 購自Thermo Fisher Scientific 公 司,LipofectamineTM2000轉染質粒和siRNA 購自日本TaKaRa 公司,Transwell 小室購自Corning 公司,ECL 化學發光液購于美國BioRad 公司,逆轉錄試劑盒和雙熒光素酶報告基因購自Pro?mega 公司,RIPA 細胞裂解液及BCA 試劑盒購于北京碧云天公司,一抗購于美國Abcam公司。
1.2 細胞培養與轉染CRC細胞系SW620、Caco?2、HT29、Lovo 細胞和FHC 細胞分別培養在含10%胎牛血清和雙抗的RPMI?1640 培養基中。培養條件5%CO2、37 ℃恒溫箱。參照LipofectamineTM2000 轉染試劑盒的說明書將培養好的miR?17?5p inhibitor及陰性對照進行瞬時轉染,培養48 h 后檢測其轉染效率。混合轉染HEK?293 和Lovo 細胞48 h 后進行試驗。實驗前期分為2 組:對照組(NC)和轉染miR?17?5p 的敲降組(miR?17?5p inhibitor),實驗后期分為3 組:對照組(NC),敲降MYLIP 組(si?MYLIP)和回復組(si?MYILP+miR?17?5p inhibitor)。
1.3 RT?qPCR檢測miR?17?5p的表達TRIzol提取CRC組織和各組細胞中總RNA,測定其濃度和純度,逆轉錄試劑盒合成cDNA。根據SYBR PCR Master Mix 的說明進行PCR 反應,條件為:95 ℃10 min、95 ℃15 s、58 ℃30 s,72 ℃30 s,進行30 個循環,72 ℃延伸7 min。U6為內參,2?ΔΔCt法計算miR?17?5p的表達(表1)。
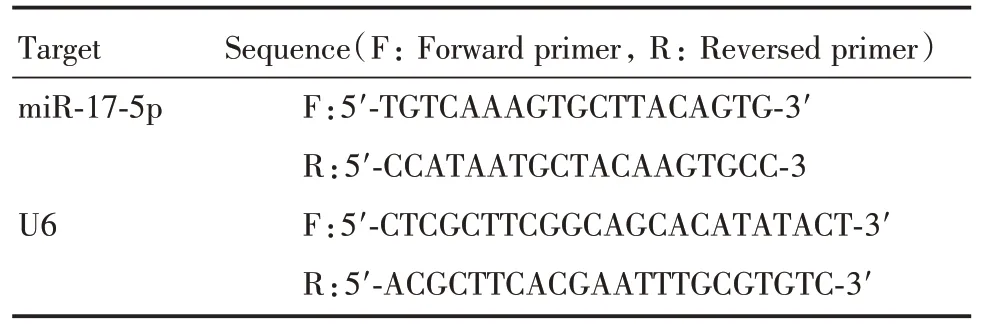
表1 引物序列Tab.1 Primer sequence
1.4 生物信息學預測、雙熒光素酶報告基因實驗檢測MYLIP 與miR?17?5p 的靶向關系使用生物信息學網站starBase 預測miR?17?5p 的靶基因,將miR?17?5p 的種子序列與所預測的靶基因3′?UTR區域進行堿基互補比對。將與miR?17?5p 具有靶向結合位點的MYLIP 片段進行PCR 擴增,構建野生型MYLIP 載體,對MYLIP 與miR?17?5p 的結合位點進行突變構建MYLIP 突變型載體。將miR?17?5p mimics 和野生或突變型MYLIP 載體轉染至293T 細胞中,48 h 后,以海腎熒光素酶活性為內參,檢測螢火蟲熒光素酶活性。
1.5 MTT 法檢測Lovo 細胞增殖活力將對數生長期CRCLovo 細胞用胰蛋白酶消化后,加入MTT液混合均勻,在37 ℃下孵育4 ~6 h 后吸出上清液,每孔加入150 μL 二甲基亞砜(DMSO)形成單細胞懸浮液并以1 × 103細胞/孔的密度接種到24 孔板中。培養7 d 后,加入20 μL DMSO,在室溫下攪拌10 min 使晶體充分溶解。分別在0、24、48、72 和96 h 測定490 nm 處的OD值。
1.6 Transwell小室法檢測Lovo細胞侵襲和遷移將50 mg/L 的基質膠按1∶8 的比例稀釋,平鋪于Transwell 小室上室,靜置30 min。遷移實驗不需要基質膠。收集培養的Lovo 細胞饑餓培養1 d,消化后離心,PBS 洗滌,重懸細胞并計數,按每室2 ×104個細胞的密度接種到Transwell 小室上室,將含20%胎牛血清的RPMI 1640 培養基加入下室,在37 ℃的恒溫培養箱中培養24 h 后,取出小室,用棉簽輕輕擦去上室表面未穿過膜的細胞,并用95%乙醇固定滲透膜,結晶紫染色,在光學顯微鏡下觀察并計數。
1.7 Western blot檢測蛋白的表達水平用PBS清洗樣本組織和細胞,RIPA 裂解組織和細胞提取總蛋白,BCA 試劑盒檢測蛋白純度和濃度,用SDS?PAGE凝膠電泳分離蛋白,PVDF進行轉膜,含5%脫脂奶粉的TBST室溫封閉2 h,在4 ℃條件下加入一抗(MYLIP,1∶1 000;E?cadherin,1∶2 000;N?cadherin,1∶1 000;vimentin,1∶1 000;GAPDH,1∶1 000)孵育。次日,TBST 洗滌。加入二抗(1∶1 000),在室溫環境中孵育1 h,洗膜,ECL 發光,凝膠成像系統,采集圖像并對蛋白條帶進行定量分析,GAPDH 作為內參,Image J 分析蛋白相對表達量。
1.8 統計學方法SPSS 16.0 和GraphPad Prism 7軟件分析數據并作圖,多組間比較采用單因素方差分析(ANOVA),兩組間比較采用t檢驗,數據以表示。P<0.05或P<0.01表示差異有統計學意義。所有實驗均設置3 個實驗組。
2 結果
2.1 CRC組織和細胞中miR?17?5p表達上調RT?qPCR 結果表明,miR?17?5p 在CRC 組織中的表達水平明顯高于與其相鄰的癌旁組織(P< 0.05,圖1A);miR?17?5p 在CRCSW620,Lovo,Caco?2 和HT29 細胞中的表達水平明顯高于結腸上皮細胞FHC(P< 0.05,圖1B),其中,miR?17?5p 在CRC Lovo 細胞中的表達水平最高,后續選取Lovo 細胞進行實驗。
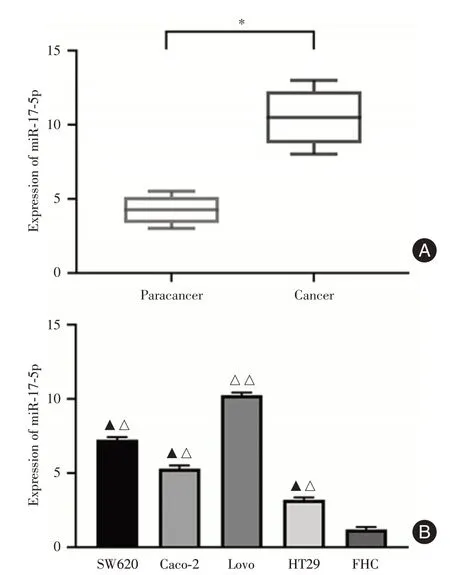
圖1 CRC 組織及其細胞中miR?17?5p 的表達水平Fig.1 The expression of miR?17?5p in CRC tissues and cells
2.2 敲降miR?17?5p 抑制Lovo 細胞的增殖和轉移RT?qPCR 檢測表明,轉染miR?17?5p inhibitor組中miR?17?5p的表達低于NC組(P<0.05,圖2A),表明miR?17?5p inhibitor 成功轉染。MTT 法檢測結果顯示,與NC相比,敲降miR?17?5p對Lovo細胞的增殖能力有明顯的抑制(P< 0.05,圖2B)。Transwell小室法檢測結果顯示,與NC 相比,敲降miR?17?5p明顯抑制Lovo 細胞的侵襲和遷移能力(P< 0.05,圖2C,D)。此外,Western blotting 檢測結果表明,E?cadherin 表達顯著高于NC 組(P< 0.05),Vimentin和N?cadherin 蛋白的表達則低于NC 組(P< 0.05,圖2E)。由此可知,敲降miR?17?5p 抑制Lovo 細胞的增殖和轉移。
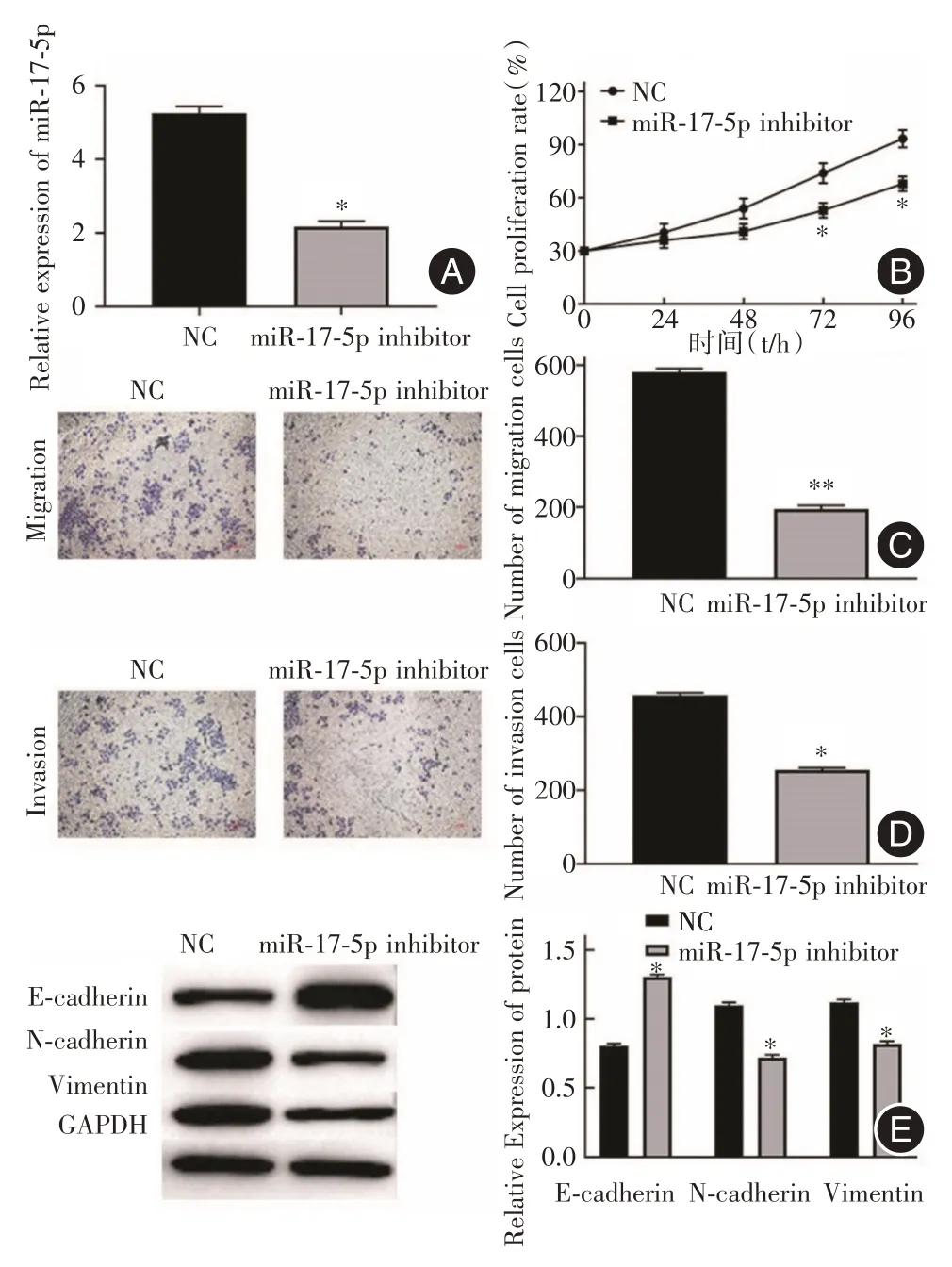
圖2 敲降miR?17?5p 對Lovo 細胞增殖和轉移能力的影響Fig.2 The effect of knockdown of miR?17?5p on proliferation and metastasis of Lovo cells
2.3 MYLIP與miR?17?5p的靶向關系及其在CRC組織中的表達水平通過生物信息學網站starBase的預測顯示(圖3A),MYLIP 與miR?17?5p 存在靶向結合位點。雙熒光素酶報告基因檢測表明,與NC 組相比,轉染miR?17?5p mimics 進入HEK293 細胞后,MYLIP 3′?UTR?WT 報告基因的相對熒光素酶活性顯著下調(P<0.05),而MYLIP 3′?UTR?MUT報告基因的熒光素酶活性與NC 組相比無明顯變化(P>0.05)(圖3B)。Western blot 檢測結果顯示,與NC組相比,過表達miR?17?5p顯著下調MYLIP 的表達水平(P<0.05,圖3C),由此可知miR?17?5p 可以靶向調控MYLIP 的表達水平。
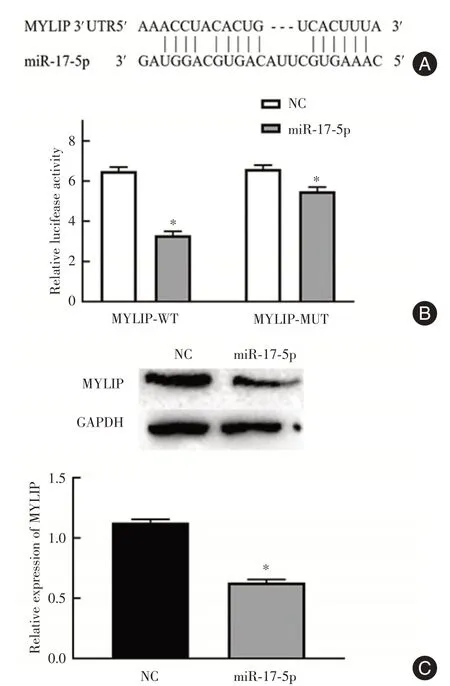
圖3 miR?17?5p 靶向調控MYLIP 的蛋白表達水平Fig.3 miR?17?5p targeted regulation of MYLIP protein expression level
2.4 miR?17?5p下調MYLIP的表達促進Lovo細胞的增殖和轉移Western blot結果顯示,相比較于NC組,敲降MYLIP后Lovo細胞中MYLIP、N?cadherin 及Vimentin 蛋白水平顯著下調(P< 0.05),E?cadherin表達顯著上調(P<0.05),同時轉染si?MYLIP+miR?17?5p inhibitor 組中MYLIP、N?cadherin、Vimentin 和E?cadherin 蛋白的表達水平與NC 組無顯著差異(圖4A)。MTT 法檢測結果顯示,與NC 相比,敲降MYLIP 對Lovo 細胞的增殖能力有明顯的促進作用(P< 0.05),而同時在Lovo 細胞中轉染si?MYLIP+miR?17?5p inhibitor 后Lovo 細胞的增殖能力與NC差異無統計學意義(圖4B)。Transwell 小室法檢測結果顯示,與NC 相比,敲降MYLIP 顯著促進Lovo細胞的侵襲和遷移能力(P< 0.01),而同時敲降MYLIP+ miR?17?5p 后Lovo 細胞侵襲和遷移能力與NC 差異無統計學意義(圖4C,D)。由此可知,miR?17?5p 通過靶向下調MYLIP 來促進CRC 細胞增殖和轉移。
3 討論
CRC 是預后極差的惡性腫瘤,在世界范圍內死亡率較高,每年有數百萬人罹患CRC[12]。CRC主要影響直腸、乙狀結腸和降結腸遠端[13]。結直腸腫瘤的發生始于上皮細胞的進行性轉變[14]。CRC的危險因素包括老齡化、不健康的飲食習慣、吸煙、肥胖、體育鍛煉不足、膽囊溶解鏈球菌血癥、炎癥性腸病和遺傳因素等。目前,CRC 的臨床治療包括手術、放療、化療和消融[15]。然而,由于對CRC 發展的詳細機制尚不完全了解,CRC 的5年生存率較低,特別是晚期[16]。因此,更好的了解CRC發病機制對于為CRC 患者提供有效的診斷和預后策略具有重要意義。
研究[17-20]表明,異常表達miRNA 的可能是腫瘤發生和進展的重要調節因子,參與調控腫瘤的發展進程。因此,研究miRNA 在CRC 腫瘤發生中的細胞和分子機制,有助于開發新的診斷和預后生物標志物。本研究發現,miR?17?5p 在CRC 中表達升高,敲降miR?17?5p可顯著抑制Lovo細胞增殖、侵襲、遷移和EMT。近來,SONG 等[21]研究發現,miR?17?5p 在胃癌患者的血漿組織中表達上調,過表達miR?17?5p可抑制細胞凋亡促進細胞增殖和侵襲,miR?17?5p可通過靶向負調控RUNX3,促進胃癌腫瘤生長;WANG 等[22]報道,miR?17?5p 在喉鱗狀細胞癌組織和細胞系中異常高表達,敲降miR?17?5p 可抑制喉鱗狀細胞癌細胞增殖和Bcl?2 表達,促進Bax 和Caspase 蛋白表達,誘導細胞凋亡。此外,miR?17?5p 也被報道作為抑癌基因調控腫瘤的發展進程,如:LIU 等[9]發現,miR?17?5p 在甲狀腺癌組織和細胞中下調,可逆轉Lnc HOTAIR 的敲低對甲狀腺癌細胞活力、侵襲和遷移的抑制作用。
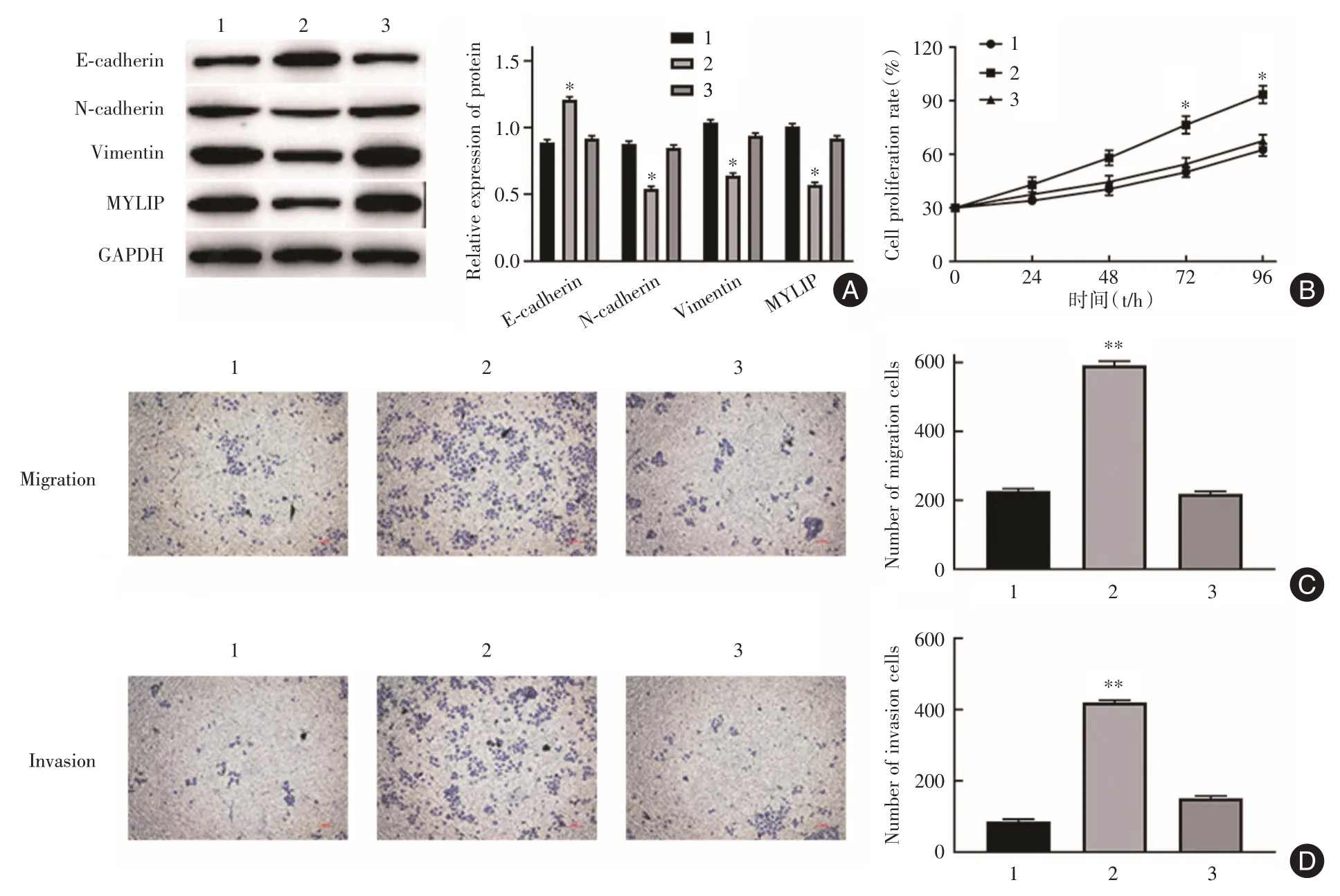
圖4 miR?17?5p 靶向下調MYLIP 對Lovo 細胞增殖和轉移的影響Fig.4 The effect of miR?17?5p on proliferation and metastasis of Lovo cells by targeting down?regulation of MYLIP
MYLIP 通過細胞膜蛋白與肌球蛋白細胞骨架的相互作用,在維持細胞形態、調節細胞運動、重塑細胞骨架蛋白以及細胞與細胞外基質的粘附中起著關鍵作用[11]。此外,MYLIP可以通過與細胞粘附分子的密切相互作用,對細胞的擴展、生長、分化和遷移具有重要影響[23]。一旦這些細胞粘附分子中出現蛋白表達水平或基因突變,細胞間的接觸和連接就會發生改變,細胞會變得更松散而分散,從而促進腫瘤細胞的遷移、侵襲和轉移[24]。筆者通過生物信息學網站預測發現,MYLIP 是miR?17?5p 的潛在靶基因,敲降miR?17?5p 靶向上調MYLIP,抑制CRC細胞的增殖和轉移。此外,ZHAO等[25]發現,MYLIP 在乳腺癌患者中表達降低,過表達miR?19b 靶向下調MYLIP 的表達,促進乳腺癌生長和轉移;在前列腺癌中,CNPY2 通過抑制通過MYLIP 介導的AR 泛素化作用的雄激素受體(AR)蛋白降解,促進前列腺癌的細胞生長[10]。然而,本研究結果并不能排除其他下游目標也可能受到miR?17?5p 影響的可能性。此外,MYLIP 在抑制增殖機制中的作用還有待進一步探索。
綜上可知,miR?17?5p 在CRC 中表達升高,敲降miR?17?5p 可靶向上調MYLIP 的表達,抑制Lovo細胞增殖和轉移。

