經支氣管動脈和非支氣管性體動脈栓塞治療原發性肺癌咯血臨床效果
李奮強,蘇東君,李更相,彭玉星,黨 磊,王文輝
咯血是多種疾病的臨床癥狀,大咯血危及生命,保守治療預后差,死亡率超過 50%[1]。Remy 等[2]1974年首次報道支氣管動脈栓塞術(bronchial arterial embolization,BAE)控制危及生命的咯血,臨床報道顯示其治療不同嚴重程度咯血安全有效[3-6]。BAE 治療結核所致咯血效果最好,其次是支氣管擴張、支氣管炎和肺炎所致咯血,且應用越來越廣泛[7-8]。原發性肺癌患者疾病過程中10%~30%會出現咯血,其中10%~20%表現為大咯血[9-10]。BAE+非支氣管性體動脈栓塞(non-bronchial systemic artery embolization,NBSAE) 治療肺癌所致咯血的臨床效果較滿意,但絕大多數研究中僅作為亞組分析且樣本量小,臨床應用價值未得到很好證實。本研究旨在探討本中心11 年施行BAE+NBSAE 治療肺癌所致咯血的經驗,同時對無咯血時間相關影響因素進行分析。
1 材料與方法
1.1 臨床資料
回顧性分析蘭州大學第一醫院2007 年7 月至2018 年12 月收治并經病理證實后成功實施BAE+NBSAE 術治療的原發性肺癌伴咯血患者。研究對象納入標準: ①影像學資料證實有可見的肺部腫瘤,有明確的病理結果;②成功實施BAE+NBSAE。排除標準:①病理結果不支持原發性肺癌診斷;②胸部增強CT 資料缺失;③支氣管動脈(BA)栓塞影像缺失;④未接受BAE 治療;⑤失隨訪;⑥未到隨訪期限(BAE+NBSAE 術后至死亡)。最終納入 38 例患者,其中男 30 例,女 8 例,平均年齡(65.08±5.91)歲。所有患者本人或直系親屬均簽署知情同意書。
1.2 治療方法
為明確全部責任血管、避免遺漏并明確出血潛在原因,術前患者均接受胸部增強CT 檢查,糾正缺氧、穩定血壓和輸血等支持治療,重癥患者持續心電監護。根據胸部增強CT 薄層掃描檢查結果,選擇適宜的 5 F Cobra/Yashiro/Vertebral(日本 Terumo 公司)/Mik(美國Cook 公司)造影導管。經股動脈途徑,先行選擇性責任BA 或非支氣管性體動脈(NBSA)造影,明確目標血管(腫瘤染色明確,BA 迂曲擴張,對 比 劑 外 滲,假性動脈瘤[2-3,8,11]);同軸 引 入 Stride(日本 Asahi 公司)/Progreat(日本 Terumo 公司)微導管,盡可能遠地送至腫瘤供血血管并避開非責任動脈,進一步造影明確診斷;根據造影表現選擇栓塞劑[直徑 350~710 μm 聚乙烯醇(PVA)顆粒(杭州艾力康醫藥科技公司)、 直徑300~500 μm 三丙烯明膠微球(Embosphere)(美國 Merit Medical Systems公司)、可吸收明膠海綿顆粒(金陵藥業公司)],緩慢注射栓塞劑,責任血管內對比劑減緩后暫停注射,3~5 min 后再次緩慢注射,直至對比劑在責任動脈內停滯[7-10]。
1.3 觀察指標
技術成功: 超選擇進入異常BA 或NBSA 并進行完整栓塞。臨床成功:BAE+NBSAE 術后咯血完全停止或部分停止(咯血明顯減少);臨床失敗:BAE+NBSAE 術后咯血仍持續存在且咯血量未減少,或短期內咯血停止、減少但在住院期間再次咯血。無咯血時間:BAE+NBSAE 術至再次咯血發作或死亡時間[3,8,10]。
1.4 統計學分析
采用SPSS 25.0 軟件對數據進行統計學分析。定量數據以均數±標準差(±s)表示,分類數據以例數和構成比表示,無咯血時間以中位數描述。無咯血時間影響因素分析分別用單因素Kaplan-Meier法和多因素Cox 回歸法分析,Cox 回歸變量篩選用Backward-Wald 法,變量剔除水準為0.10。
2 結果
入組患者基線特征見表1。原發性肺癌組織類型和腫瘤分期通過組織活檢、胸部增強CT、全身骨掃描或 PET-CT 證實。患者中 19 例(50%)為鱗癌,11 例(28.9%)為腺癌,8 例(21.1%)為小細胞肺癌。BAE+NBSAE 術開始前咳血量 21 例(55.3%)>300 mL/24 h,10 例(26.3%)<300 mL/24 h,7 例(8.4%)血痰。28例(73.7%)為肝癌終末期(Ⅳ期)。

表1 38 例肺癌伴咯血患者基線特征
38 例 BAE+NBSAE 術均獲成功。行單純 BAE 術33 例(86.8%),BAE+NBSAE 術 5 例;應用 PVA 顆粒栓塞 31 例(81.6%),PVA+明膠海綿顆粒 2 例(均發現胸廓內動脈參與供血,先用自制較大明膠海綿予保護性栓塞,再用PVA 顆粒栓塞責任動脈),Embosphere 微球 4 例,明膠海綿顆粒 1 例(單純BAE)。超選擇責任動脈造影可見所有患者腫瘤染色明顯,幾乎所有患者增粗、迂曲的BA 和/或NBSA,部分患者假性動脈瘤形成;僅3 例(7.9%)可觀察到BA-肺動脈瘺(圖1)。
31 例(81.6%)患者取得臨床成功,7 例(18.4%)失敗(2 例術后咯血量未明顯減少,5 例住院期間再發咯血),其中2 例經內科保守治療咯血停止后出院,1 例住院期腫瘤持續進展導致死亡,1 例自動放棄治療后1 周內因咯血死亡,3 例保守治療后無明顯好轉,遂復查造影發現1 例BA 再次開放,再行栓塞術后咯血停止,2 例未發現異常血管。臨床成功患者中有5 例隨訪中發生再次咯血,再行栓塞術后咯血停止。
所有患者隨訪期限6~466 d,死于咯血6 例(15.8%)、腫瘤進展 19 例(50.0%)、感染 11 例(28.9%)、并發癥 2 例(5.3%)。患者術后總平均生存時間為141(103.7~178.3) d,總中位生存期為 92(86.0~98.0)d;臨床成功、失敗患者 6 個月、1 年累計生存率分別為 29.0%、9.7%,28.6%、14.3%,中位生存期分別為 92(52.7~131.3) d、21(13.3~28.7) d。臨床成功、失敗患者中位無咯血時間分別為87(76.4~97.6) d、10(7.4~12.6) d(P=0.001)(圖2)。
采用Cox 回歸法分析影響無咯血時間的因素。單因素分析顯示大咯血(中位無咯血時間54 d,95%CI=18.45~89.55,P=0.019)、癌性空洞(中位無咯血時間 10 d,95%CI=1.41~18.59,P=0.001)與無咯血時間顯著相關(表2);多因素分析顯示大咯血(OR=0.504,95%CI=0.318~0.800,P=0.004)、 癌性空洞(OR=7.818,95%CI=2.206~27.722,P=0.001)、 腫瘤直徑大(OR= 1.517,95%CI=1.144~2.012,P=0.004)(表3)為BAE+NBSAE 術后縮短無咯血時間的獨立影響因素。
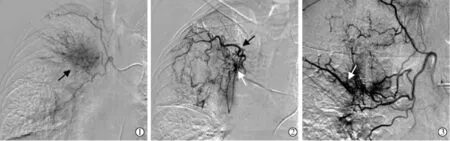
圖1 肺癌伴咯血患者BA 造影特征
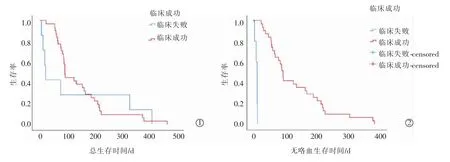
圖2 臨床成功、失敗患者中位生存期和無咯血時間曲線
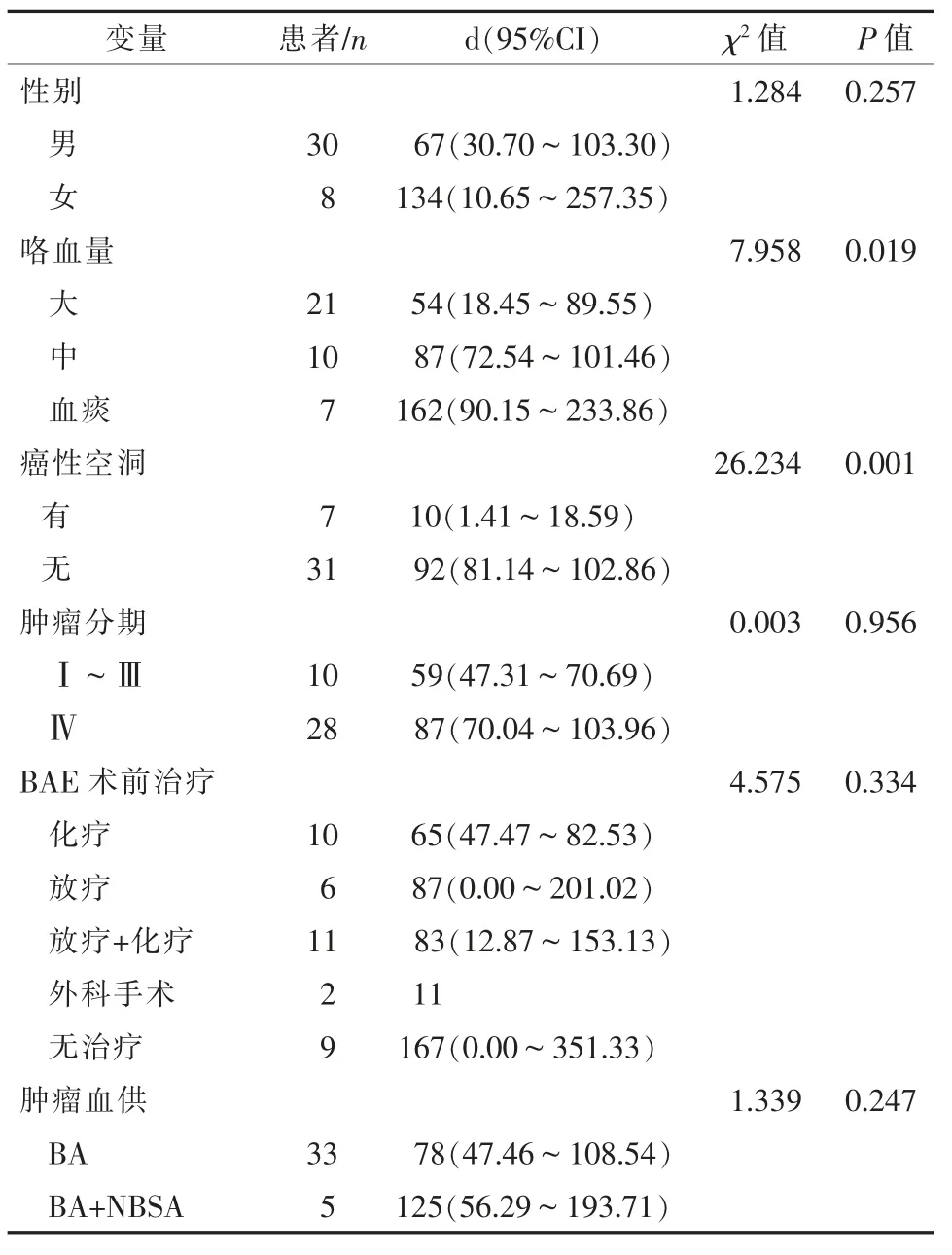
表2 BAE+NBSAE 術后影響中位無咯血時間的單因素分析
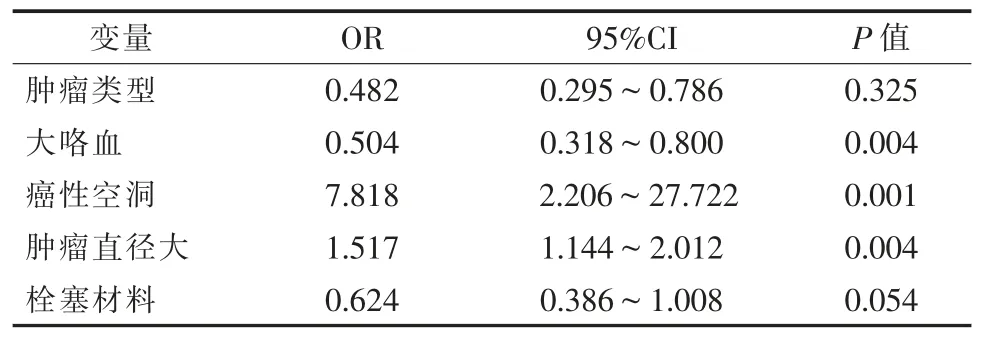
表3 影響無咯血時間的Cox 回歸分析
3 討論
目前文獻報道顯示BAE 是治療原發性肺癌所致咯血的安全、有效方法,其技術成功率為77%~100%,臨床成功率為58.3%~89%,咯血復發率為14.3%~50%[12-15]。本研究中技術成功率為 100%,臨床成功率為83.7%,咯血復發率為23.8%,與既往文獻報道相似。
本研究中BAE+NBSAE 術后總平均生存時間為141 d,總中位生存期僅92 d,主要因為患者中73.4%為腫瘤Ⅳ期; 術后死亡原因主要為腫瘤進展或伴發其他疾病,由咯血直接導致死亡僅6 例(15.8%);術后臨床成功患者中位生存期高于臨床失敗患者(92 d 對 21 d),但差異無統計學意義(P=0.052),與文獻報道不符[10,12-15],可能與樣本量少有關。Witt等[15]前瞻性研究接受彈簧圈BAE 治療的30 例支氣管肺癌所致咯血患者,并回顧性對照分析15 例接受保守治療患者,發現BAE 組患者平均生存時間明顯長于對照組(162 d 對 62 d,P< 0.05),盡管總預后還是很差,但BAE 控制咯血復發持久有效,并在一定程度上可延長此類患者總生存時間。
咯血復發原因包括潛在的疾病進展、血管再通或血運重建、不完全栓塞、出現新的如體循環血管參與腫瘤供血以及惡性腫瘤所致血管壁彈力纖維破壞,血管破裂后最終形成肺動脈假性動脈瘤(pulmonary artery pseudoaneurysm,PAPA)[3,11,13]。本研究中未發現PAPA 形成所致咯血,可能與病例數少有關。早期咯血復發與不完全栓塞有明確關系,而晚期復發是疾病進展的典型表現[11,13,16]。本研究中7 例臨床失敗,4 例經內科保守治療后咯血減少或停止后出院,僅3 例接受復查造影,發現1 例BA再次開放,再行栓塞術后咯血停止,2 例未發現異常血管。因此,由于現今臨床上影像設備先進,遺漏責任血管的可能性很小,加之惡性腫瘤栓塞治療所用主要材料為永久性栓塞劑,并予末梢完全栓塞,發生責任血管再通的可能性很低,患者接受再次BAE術的必要性有限。
既往文獻報道中患者樣本量較小或研究重點為非原發性肺癌,原發性肺癌所致咯血患者BAE+NBSAE 術后無咯血時間相關因素尚未全面評估[11-15]。本研究中患者術后總平均生存時間為141 d,總中位生存期為92 d;臨床成功、失敗患者中位無咯血時間分別為 87 d、10 d(P=0.001);多因素分析顯示大咯血(OR=0.504,95%CI=0.318~0.800,P=0.004)、癌性空洞(OR=7.818,95%CI=2.206~27.722,P=0.001)、腫瘤直徑大(OR=1.517,95%CI=1.144~2.012,P=0.004)為BAE+NBSAE 術后縮短無咯血時間的獨立影響因素。江森等[11]報道提示肺部腫瘤患者可形成PAPA。但本研究中未發現腫瘤所致PAPA 病例。
肺內惡性腫瘤局部組織缺氧和腫瘤細胞分泌血管生長因子刺激BA 新生血管形成,因此腫瘤組織內血管明顯增多。但是這些新生血管往往因發育不完善導致血管壁很薄,容易破裂和形成假性動脈瘤[11-12]。因此,有研究推測肺癌患者局部腫瘤組織周圍廣泛的新生血管形成和假性動脈瘤形成是導致大咯血的主要原因,并可能與BAE+NBSAE 術后復發和死亡率高相關。既往文獻報道癌性空洞與大咯血有明確相關性[10-11]。本研究結果表明癌性空洞患者大多伴有大咯血,且接受BAE+NBSAE 術后無咯血時間明顯較短。
本研究還顯示腫瘤直徑也是導致肺癌患者咯血的危險因素,且直徑較大腫瘤患者BAE+NBSAE術后無咯血時間較短,與現有文獻報道不同。可能腫瘤直徑大小本身即為縮短BAE+NBSAE 術后無咯血時間的危險因素。
總之,BAE+NBSAE 術控制原發性肺癌所致咯血安全有效,但患者死亡率仍很高。大咯血、癌性空洞、腫瘤直徑大是BAE+NBSAE 術后縮短無咯血時間的重要預測因素。

