LC-MS/MS 法測定大活絡丸中血竭素的含量
易徐航,張鈺祺,楊恢檢
萍鄉市食品藥品檢驗所,萍鄉 江西 337000
大活絡丸是由血竭、麝香、牛黃、烏梢蛇、蘄蛇、兩頭尖、防風、羌活、全蝎等48 味藥材研成細粉,混合均勻加煉蜜制成的丸劑。具有祛風止痛、舒筋活絡等功效,臨床上常用于中風痰厥引起的癱瘓,足痿痹痛,腰腿疼痛,跌打損傷,胸痹等癥狀[1]。大活絡丸中含有多味傳統的名貴中藥材,其中,血竭更是被譽為“活血療傷之良藥”。血竭作為處方中的臣藥,具有生肌斂瘡,活血定痛,化瘀止血之功效[2],其主要活性成分為血竭素[3]。現代研究表明,血竭素具有活血與止血的雙向調節作用[4-7]。目前大活絡丸的執行標準多為衛生部藥品標準中藥成方制劑第六冊WS3-B-1082-92[8],該標準已經執行多年,僅有簡單的丸劑通則檢查,并不能對其質量進行有效地控制。近年來,高效液相色譜-串聯質譜(LC-MS/MS)在中成藥中有效成分的含量測定中應用日益廣泛[9-10]。本試驗采用LC-MS/MS 法測定大活絡丸中血竭素的含量,以期為控制和提高大活絡丸的質量提供科學依據。
1 材料
1.1 試藥
血竭素高氯酸鹽對照品(批號:110811-201707,含量:96.3%),購自中國食品藥品檢定研究院;甲醇(HPLC 級,購于ThermoFisher 公司);甲酸(HPLC 級,天津市科密歐化學試劑有限公司);水為屈臣氏蒸餾水。樣品信息見表1。
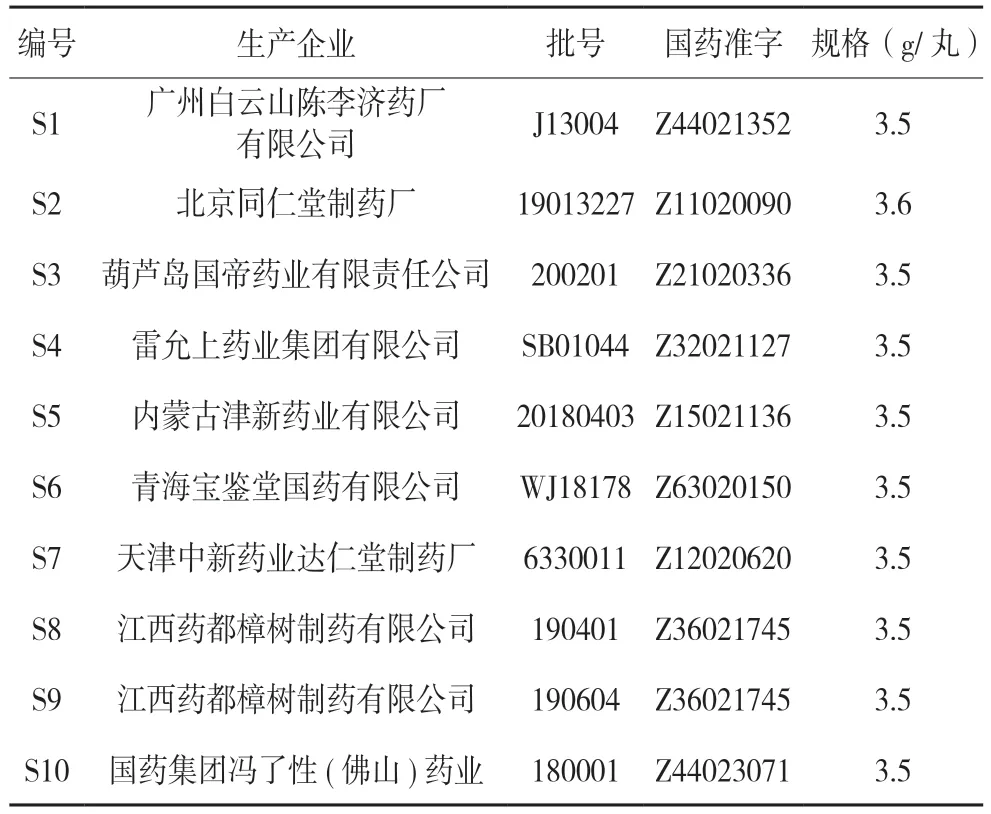
表1 樣品信息
1.2 儀器
安捷倫6460 型高效液相色譜-三重四級桿質譜聯用儀;CP-225D 型電子天平(十萬分之一,SARTORIUS 公司);ME-204 型電子天平(萬分之一,METTLER TOLEDO 公司);KQ-500DB 型超聲儀(江蘇昆山市超聲儀器有限公司)。
2 方法與結果
2.1 色譜條件
選擇Agilent Poroshell 120 EC-C18色譜柱(2.1 mm×100 mm,2.7 μm);流動相為甲醇(A)-0.1% 甲酸(B),梯度洗脫(0~3 min,40% A;3~8 min,40% A →100% A;8~10 min,100% A;10~10.5 min,100% A →40% A;10.5~15 min,40% A);流速0.2 mL/min;柱溫為35 ℃;進樣量10 μL。血竭素對照品和大活絡丸供試品的總離子流色譜圖見圖1。
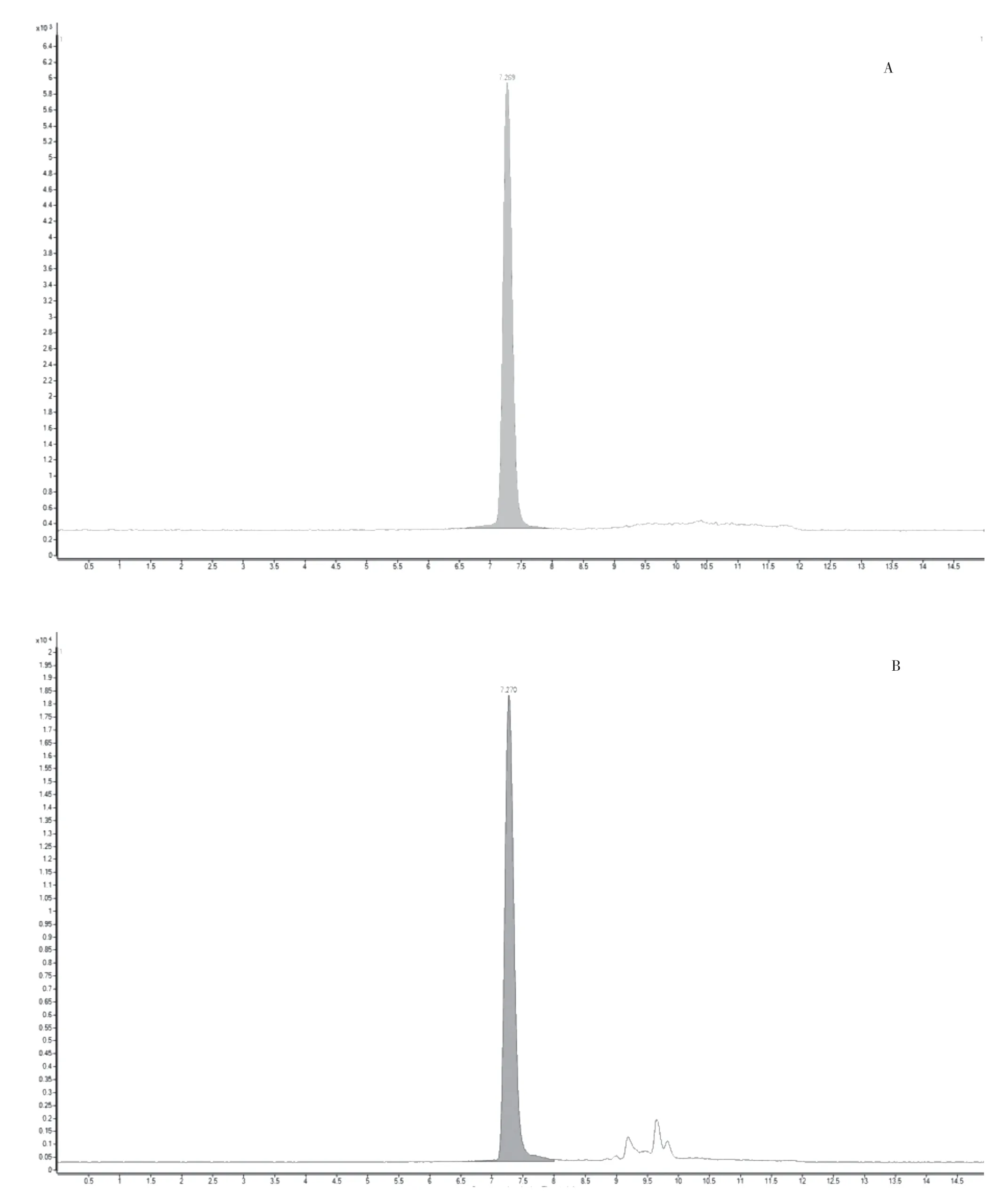
圖1 總離子流色譜圖:A.血竭素對照品;B.供試品
2.2 質譜條件
采用電噴霧離子源(ESI)正離子檢測,多反應監測(MRM)方式進行掃描。干燥氣和霧化器均為高純氮氣,毛細管電壓4 000 V;干燥氣溫度300 ℃;干燥氣流量8 L/min;霧化氣壓力30 psi。選擇質荷比(m/z)267.0 →222.9 作為定量離子對,m/z 267.0 →251.0、m/z 267.0 →196.9 作為定性離子對。傳輸電壓(Fragmentor)為135 V,碰撞能量(Collision Energy)為34 V。血竭素對照品和大活絡丸供試品的二級質譜見圖2。

圖2 二級質譜圖:C.血竭素對照品;D.供試品
2.3 溶液的配制
2.3.1 對照品儲備液的制備 精密稱取血竭素高氯酸鹽對照品10.66 mg,置100 mL 量瓶中,加甲醇溶解并定容至刻度,搖勻,即得含血竭素74.6 μg/mL的儲備溶液(血竭素重量=血竭素高氯酸鹽重量/1.377)[2]。
2.3.2 供試品溶液的制備 取樣品大蜜丸2 丸,剪碎,加入等量硅藻土,研勻,取約7 g(相當于1 丸量)置具塞錐形瓶中,加入甲醇25 mL,稱定重量,超聲處理(功率:500 W,頻率:40 kHz)30 min,放冷至室溫,再稱定重量,用甲醇補足減失的重量,搖勻,4 000 r/min 離心10 min,取上清液用0.22 μm微孔濾膜濾過,取續濾液,即得供試品溶液。
2.3.3 陰性樣品溶液的制備 按工藝方法制備缺少血竭藥材的陰性樣品,按“2.3.2”項下方法操作,制成陰性樣品溶液,依法測定,結果顯示陰性樣品的總離子流色譜圖中,無呈現與血竭素對照品保留時間相同的色譜峰,見圖3。
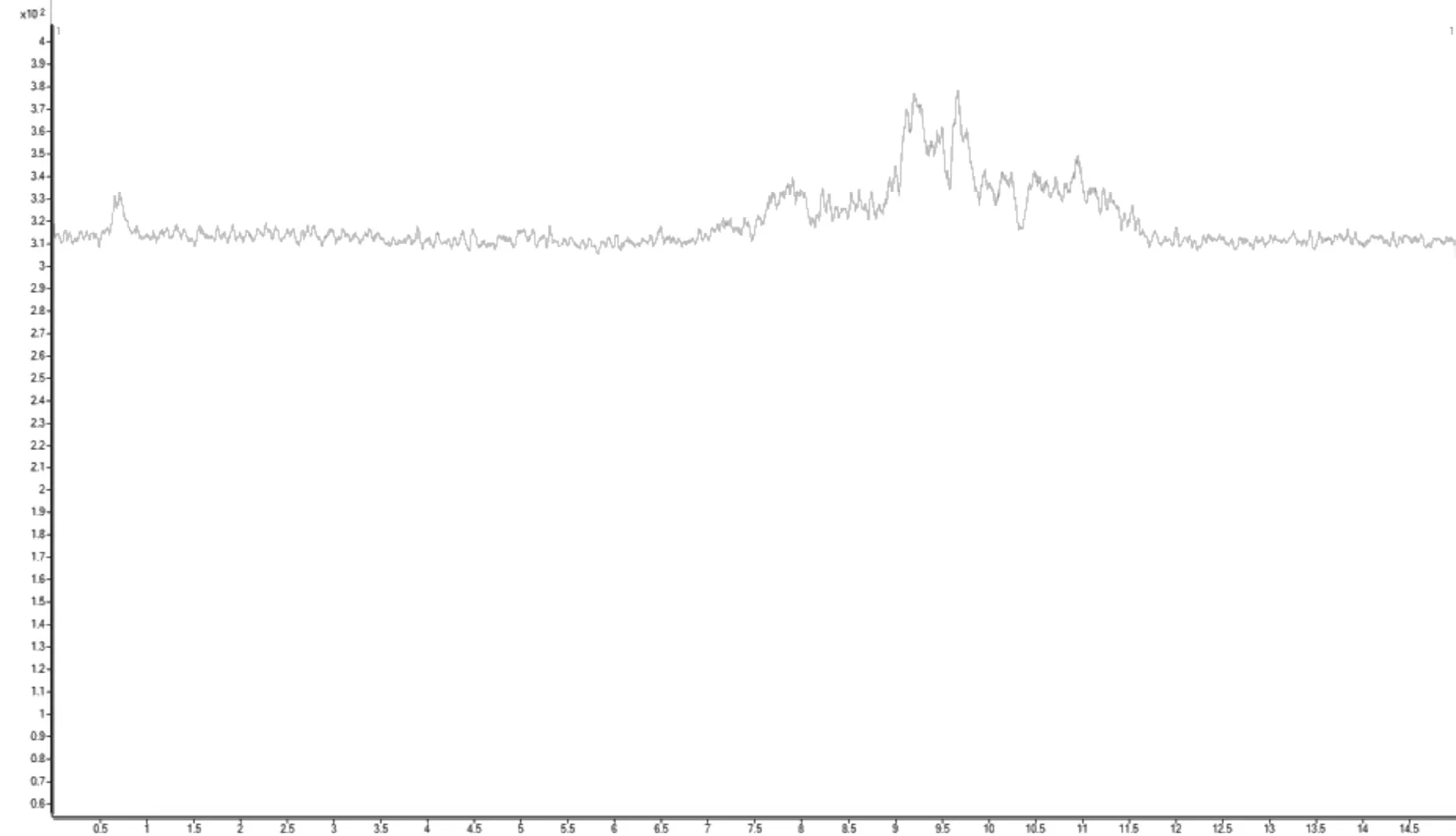
圖3 陰性樣品總離子流圖
2.4 方法學考察
2.4.1 線性關系考察 精密吸取上述血竭素對照品儲備液,加甲醇逐級稀釋得系列標準溶液,濃度分別為37.3、74.6、373.0、746.0、1 492.0、3 730.0 ng/mL。按“2.1”“2.2”項下的色譜和質譜條件進行測定,以血竭素對照品的進樣濃度(ng/mL)為橫坐標(X),相應的峰面積值為縱坐標(Y),繪制標準曲線,得線性回歸方程:Y=328.53X+57 753,r=0.999 8。結果表明,血竭素的進樣濃度在37.3~3 730.0 ng/mL 呈良好線性關系。
2.4.2 精密度試驗 精密吸取血竭素對照品溶液(373.0 ng/mL)10 μL,按“2.1”“2.2”項下的色譜和質譜條件連續進樣6 針,測定峰面積。血竭素峰面積的RSD 為0.40%,表明儀器的精密度良好。
2.4.3 穩定性實驗 取同一份大活絡丸供試品溶液(編號S1),分別于制備后0、2、4、6、8、10、12、24 h 精密吸取10 μL 進樣,按“2.1”“2.2”項下的色譜和質譜條件,測定血竭素的峰面積,其RSD 為1.28%,結果表明大活絡丸供試品溶液在室溫下24 h 內穩定。
2.4.4 重復性試驗 取同一批號(編號S1)樣品六份,按“2.3.2”項下方法制備大活絡丸供試品溶液,按“2.1”“2.2”項下的色譜和質譜條件進樣測定,計算血竭素的含量(μg/g)。結果計算得血竭素含量的RSD 為1.02%,表明該方法重復性良好。
2.4.5 加樣回收率試驗 取已知含量(編號S1:3.97 μg/g)的大活絡丸樣品2 丸,剪碎,加入等量硅藻土,研勻,取約3.5 g,精密稱定,置具塞錐形瓶中,精密加入血竭素對照品溶液(3.73 μg/mL)適量,按“2.3.2”項下方法制備大活絡丸加樣回收溶液,按“2.1”“2.2”項下的色譜和質譜條件進樣測定含量,計算加樣回收率。結果表明血竭素的平均回收率為100.09%,RSD 為1.42%,結果見表2。

表2 加樣回收率試驗結果(n=6)
2.4.6 檢測限與定量限 取血竭素對照品溶液加甲醇逐級稀釋后進樣測定,以信噪比3∶1的對照品溶液濃度為檢測限(LOD),以信噪比10∶1的對照品溶液濃度為定量限(LOQ)。結果血竭素檢測限為1.33 ng/g;定量限為4.00 ng/g。
2.4.7 耐用性試驗 取同一批號(編號S1)樣品,按“2.3.2”項下方法制備大活絡丸供試品溶液,分別選擇Agilent Poroshell 120 EC-C18(2.1 mm×100 mm,2.7 μm);Waters XBridge BEH C18(2.1 mm×100 mm,2.5 μm);Welch Ultimate XB-C18(2.1 mm×100 mm,3 μm)3 種品牌的色譜柱,按“2.1”“2.2”項下的色譜和質譜條件測定,結果無明顯差別。
2.5 樣品測定
取不同廠家的10 批大活絡丸(編號S1-10),按“2.3.2”項下方法制備大活絡丸供試品溶液。分別精密吸取血竭素對照品溶液與大活絡丸供試品溶液各10 μL 注入液相色譜儀,測定,即得。結果見表3。

表3 大活絡丸樣品中血竭素含量測定結果(n=3)
3 討論
3.1 紫外與質譜檢測器的比較
本文曾采用高效液相紫外檢測器對大活絡丸中血竭素進行含量測定,由于大活絡丸處方龐大,成分復雜,通過優化流動相以及改進提取方式等方法,其樣品中的主峰分離效果均不理想,且血竭素在處方中的含量較低,紫外檢測器難以滿足分析要求。質譜檢測器具有專屬性強、靈敏度高等[11-12]優勢,故本試驗建立了LC-MS/MS 法測定大活絡丸中血竭素含量的方法。
3.2 流動相的選擇
在試驗中還考察了甲醇-水、乙腈-水、甲醇-0.1%甲酸水溶液、甲醇-0.01 mol/L 醋酸銨溶液、乙腈-0.1%甲酸水溶液、乙腈-0.01 mol/L 醋酸銨溶液等多組流動相體系,結果表明,流動相為甲醇-0.1%甲酸時梯度洗脫能得到較好的峰型和分離度。
3.3 提取方法及時間的考察
本次收集的大活絡丸樣品均為大蜜丸,采用加入等量的硅藻土研勻的方式,以便于目標成分的溶出。提取條件采用超聲提取法分別考察了甲醇、50%甲醇、乙醇、50%乙醇四種提取溶劑,結果表明甲醇提取效率最高。在此基礎上,分別考察了超聲和回流2 種提取方式,結果顯示超聲與回流提取效率相當,故選用提取簡便的超聲提取方式。同時對甲醇溶液用量10、25、50 mL,以及超聲時間10 min、30 min、1 h 進行考察,最后確定采用甲醇超聲(500 W,40 kHz)處理30 min 為宜。
3.4 質譜條件的優化
在對質譜條件進行優化時,分別考察了毛細管電壓、干燥氣溫度、干燥氣流量和霧化氣壓力對含量測定的影響,最終確定毛細管電壓4 000 V,干燥氣溫度300 ℃,干燥氣流量8 L/min,霧化氣壓力30 psi 為最優狀態。采用ESI 電離模式,分別比較了血竭素在正離子掃描和負離子掃描模式下的響應信號,發現血竭素在正離子化模式下響應值較高。通過全掃模式(Full Scan),確定血竭素的母離子。通過選擇單離子檢測模式(SIM)和子離子檢測模式(Product Ion Scan)對傳輸電壓和碰撞能量等關鍵參數的優化,以確保定量檢測的準確性。
3.5 小結
從對10 批大活絡丸中血竭素的含量測定結果來看,血竭素的含量為0.29~7.15 μg/g。不同廠家生產的大活絡丸血竭素含量相差較大,提示血竭原藥材的質量或廠家的生產工藝存在差異。為避免由原藥材或生產工藝引起中成藥的療效差異,建議廠家進一步完善質控標準和生產工藝,確保產品質量的均一性和有效性。本文建立了LC-MS/MS 法測定大活絡丸中血竭素含量的方法,經方法學驗證,該方法結果準確、快速,重復性好,操作簡便,可用于大活絡丸中血竭素的含量測定。

