不同途徑獲取的蒼術飲片質量情況分析
胡生亮 鄭金芳 肖京力 劉小寶
(江西省新余市綜合檢驗檢測中心 新余 338000)
根據《中華人民共和國藥典》的規定,蒼術的正品來源為菊科植物茅蒼術Atractylodes lancea(Thunb.)DC.或北蒼術Atractylodes chinensis(DC.)Koidz.[1]。市場上根據蒼術基原不同,分為茅蒼術和北蒼術2 個規格,經過凈制、切制或麩炒后,以蒼術片、麩炒蒼術2 種主要形式入藥。蒼術主要來源于野生資源[2],由于野生資源逐步萎縮[3],而家種還不能完全取代野生貨源,特別是2020 年由于新冠疫情時期,療效確切的中醫藥方中有蒼術這味藥材,使蒼術價格一直居高不下。為全面了解市售蒼術質量狀況,課題組從網絡平臺、藥材市場、藥店和醫院等不同銷售渠道收集到39 批次蒼術飲片,依據《中華人民共和國藥典》2020 年版一部蒼術項下規定開展檢驗工作,對不合格品進行偽品甄別和分析,對市售蒼術質量進行評價,以期為加強不同渠道蒼術飲片的監管提供建議。現報道如下:
1 儀器與試劑
1.1 儀器 Agilent 1200 型高效液相色譜儀;CP225D 電子天平;SZ61 體式顯微鏡;SX2-5-12 箱式電阻爐;DVS612C 恒溫干燥箱;雙槽展開缸;硅膠G 薄層板。
1.2 試劑 蒼術素(批號:111924-201806,來源:中國食品藥品檢定研究院);甲醇:色譜純、分析純;石油醚(60~90℃)和丙酮均為分析純。
2 樣品信息
針對市售蒼術飲片進行質量評價,課題組分別從淘寶網購樣10 批、各藥材市場購樣19 批、藥店購樣5 批、醫院購樣5 批。淘寶平臺供應商以安徽亳州、河北安國為主;市場購樣主要涉及安徽亳州、河北安國、廣西玉林、湖南廉橋、江西樟樹等藥材市場;藥店和醫院為江西新余轄區內。蒼術飲片產地來源以內蒙古、安徽、東北、河北為主。從不同途徑獲取的39 批蒼術飲片覆蓋9 個產地,大部分來自內蒙古、安徽、東北、河北,市場供應以北蒼術為主,這與目前全國蒼術產銷狀況基本相一致[4]。見表1。
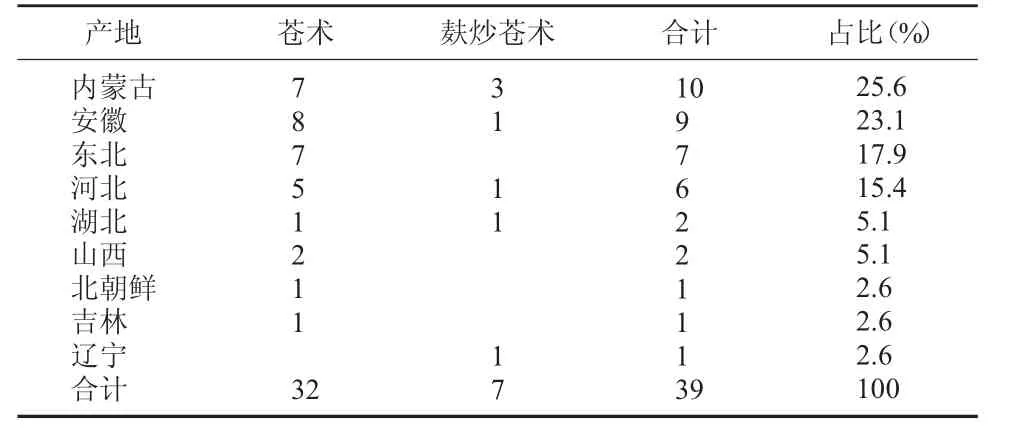
表1 39 批蒼術飲片和麩炒蒼術飲片的產地
3 方法與結果
3.1 性狀 對39 批次蒼術(含麩炒蒼術)飲片的性狀進行檢驗,15 批次符合規定,合格率為38.5%。主要偽品有關蒼術、皖南白術;正品蒼術飲片與偽品的主要區別是:北蒼術或茅蒼術的切面黃白色或灰白色,散在有多數橙黃色或棕紅色油室,部分可析出白色細針狀結晶,氣香特異,味微甘、辛、苦;麩炒蒼術形似蒼術片,表面深黃色,散有多數棕褐色油室,有焦香氣[1]。關蒼術:質地疏松,斷面不平坦,纖維性強,淺黃白色或灰白色,有少數黃棕色油室散在,氣特異,久聞有不適感,味辛、微苦[5]。皖南白術:斷面淺褐色,有較多的棕褐色點狀油室散在,放射狀紋理明顯。氣香,味辛、苦[6]。
3.2 鑒別
3.2.1 顯微鑒別 正品粉末呈棕色,草酸鈣針晶細小;纖維大多成束,長梭形;石細胞類圓形、多角形或類長方形,壁極厚;菊糖多,其表面有放射狀紋理;油滴淡黃色[7]。關蒼術、皖南白術與正品蒼術相比,其顯微特征基本與正品蒼術一致,但關蒼術石細胞、針晶相對較少,油滴少且近無色,導管更多。見圖1~圖5。
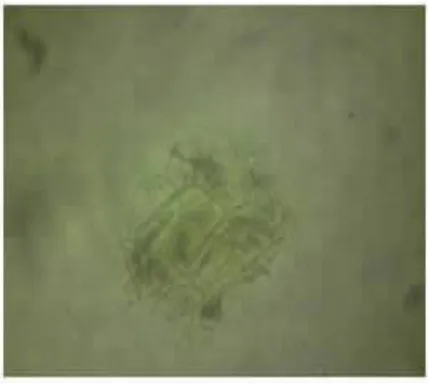
圖1 正品蒼術針晶10×20 倍顯微鑒別圖
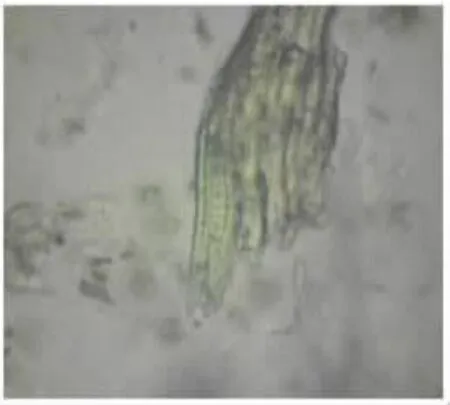
圖2 正品蒼術纖維束10×20 倍顯微鑒別圖
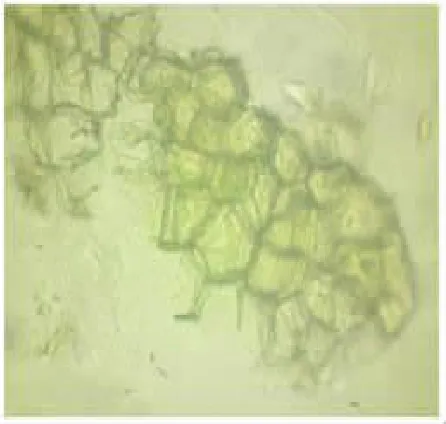
圖3 正品蒼術石細胞10×20 倍顯微鑒別圖

圖4 正品蒼術菊糖10×40 倍顯微鑒別圖
圖5 正品蒼術油滴10×40 倍顯微鑒別圖
3.2.2 薄層鑒別 從薄層色譜來看,正品蒼術所顯斑點的位置和顏色與對照藥材一致,在與蒼術素對照品色譜相應位置上顯相同污綠色斑點;皖南白術在與對照品蒼術素的位置上顯相同污綠色斑點,但其他斑點位置和顏色與對照藥材不同;關蒼術的薄層色譜中,在與蒼術素對照品色譜相應位置上無相同污綠色斑點,與文獻記載關蒼術不含蒼術素(未檢出污綠色斑點)一致[8],其他斑點位置和顏色與對照藥材也不相同。見圖6。
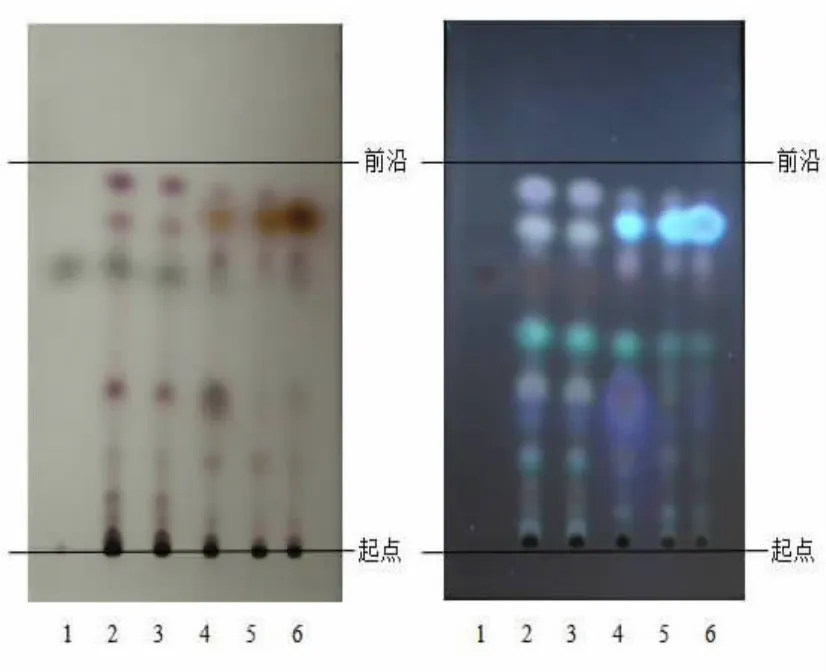
圖6 正品蒼術、皖南白術、關蒼術在日光與紫外光(365 nm)下薄層色譜圖
3.3 檢查
3.3.1 水分 按照《中華人民共和國藥典》2020 年版四部(通則0832)第四法甲苯法對本次收集的39批次蒼術(含麩炒蒼術)飲片檢查項下水分(標準規定:蒼術≤11.0%,麩炒蒼術≤10.0%)進行測定,結果26 批不符合規定,不合格率為66.7%。見表2。
3.3.2 總灰分 按照《中華人民共和國藥典》2020年版四部(通則2302)第一法總灰分測定法對本次收集到的蒼術(含麩炒蒼術)飲片檢查項下總灰分(標準規定:≤5.0%)進行測定,結果11 批飲片不符合規定,不合格率為28.2%。見表2。
3.3.3 酸不溶性灰分 按照《中華人民共和國藥典》2020 年版四部(通則2302)第二法酸不溶性灰分測定法對本次收集到的蒼術(含麩炒蒼術)飲片檢查項下酸不溶性灰分(建議標準:≤1.0%)進行測定。見表2。
3.3.4 二氧化硫殘留量 按照《中華人民共和國藥典》2020 年版四部(通則2331)二氧化硫殘留量測定法第一法(酸堿滴定法),對本次收集到的39 批蒼術(含麩炒蒼術)飲片中二氧化硫殘留量(標準規定:150 mg/kg)進行測定,結果檢出7 批樣品中二氧化硫殘留量不符合規定,不合格率為17.9%。見表2。
3.4 含量測定 按照《中華人民共和國藥典》2020年版一部蒼術藥材含量測定項下蒼術素含量(標準規定:蒼術≥0.30%;麩炒蒼術≥0.20%)要求測定結果,檢出24 批樣品蒼術素含量不符合規定,不合格率為61.5%。見表2。
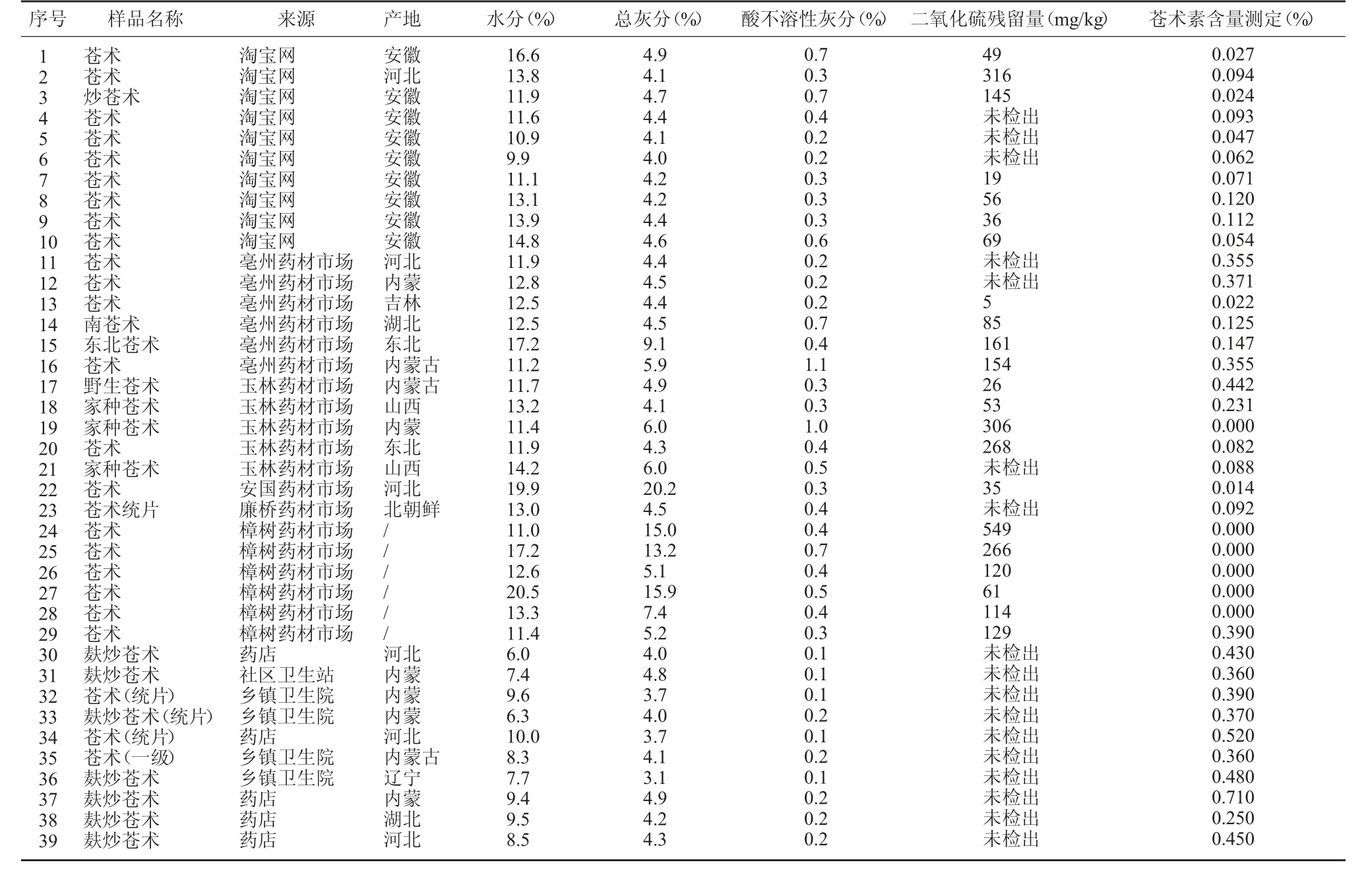
表2 不同途徑獲取的蒼術(含麩炒蒼術)飲片檢驗情況
4 異常情況檢驗
檢驗過程中發現8 批樣品斷面有發亮的結晶,課題組懷疑存在樣品人為添加無機鹽增重的跡象,對這8 批樣品進行鋁鹽、鎂鹽檢查。取蒼術飲片粗粉6 g 放置具塞三角瓶中,加水60 ml 攪拌3 min 后濾過,取濾液2 ml 置試管中,加濃氨溶液2 滴。要求溶液不得出現明顯渾濁,結果8 批樣品均出現明顯渾濁。按照《中華人民共和國藥典》2020 年版四部(通則0412)電感耦合等離子體質譜法進行測定,結果證實測定的數值與鋁鹽、鎂鹽的鑒別反應一致。8 批樣品均存在鋁鹽、鎂鹽反應呈現陽性現象,且大都灰分存在超標現象,可能存在人為添加無機鹽增重的現象。見表3。
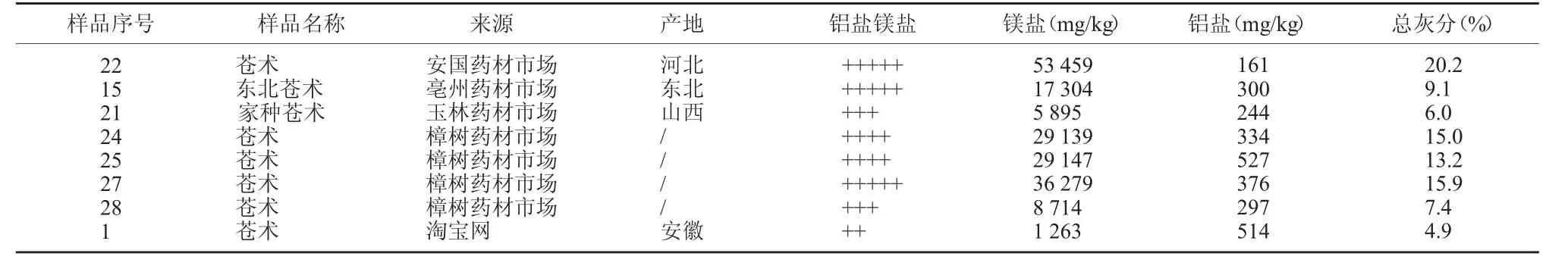
表3 鋁鹽、鎂鹽理化鑒別與質譜測定結果對比
5 討論
分析不合格率產生的主要原因是用偽品替代或摻偽、人為增重、硫磺過度熏蒸等,導致飲片性狀、鑒別、檢查、含量測定等項目不符合規定。經檢驗,39批被檢樣品中有24 批為不合格品,包括2 批摻偽品、22 批偽品,不合格率高達61.5%。從檢驗數據和樣品性狀來看,《中華人民共和國藥典》2020 年版一部蒼術項下各項檢驗項目能較好地對蒼術飲片進行真偽鑒別和質量評價。另外發現有部分樣品鋁鹽、鎂鹽反應呈陽性,可能存在人為添加增重現象。
根據市場調研了解到蒼術飲片存在偽品或摻偽現象,從樣品性狀鑒定,此次39 批樣品中涉及的偽品可能涉及關蒼術、皖南白術等,可通過《中華人民共和國藥典》一部蒼術項下性狀特征、薄層特征和含量測定等項目對其進行有效地區別,其中朱砂點亦是判斷蒼術真偽的重要依據[9]。
對監管工作的建議:(1)加強中藥飲片產地加工的監管。從網絡平臺上購樣、藥材市場銷售的蒼術飲片不合格情況來說,部分個體戶在蒼術藥材產地加工后,直接包裝成飲片,在網絡平臺上以個體店注冊通過網絡進行銷售,所切制的飲片厚薄不一、水分未控制,而且摻雜使假,以次充好現象嚴重。中藥材產地加工作為體現中藥材安全性、有效性、穩定性的關鍵環節,但其前端卻被定位為農副產品,產地加工市場準入門檻低,經營者多以個體戶為主,人員素質參差不齊,也是中藥材產業鏈條監管中最薄弱的環節,監管主體不明確。目前對該環節的管理只能依靠中藥飲片生產企業將質量管理體系延伸到藥材的種植、采收、加工環節。因此要進一步明確中藥材產地加工監管的主體責任,加強監管力度。(2)加強對中藥材和中藥飲片多渠道的監管[10]。在藥品監管越來越嚴厲的趨勢下,藥店、醫院銷售的中藥飲片質量逐漸得到提升,一些藥材偽品開始從電商渠道流入市場,而且有愈演愈烈的趨勢,導致消費者網上購買藥品的風險遠高于實體店。因此中藥材、飲片多渠道質量整治任重道遠。

