左室壓力-應變環評價乳腺癌患者化療后心肌損害的應用研究
崔瑞雪, 陳 勇, 楊 菲, 馬 勇, 曹司琪
(1. 大連醫科大學 研究生院, 遼寧 大連, 116044;2. 江蘇省蘇北人民醫院 超聲心動圖室, 江蘇 揚州, 225001)
目前,蒽環類藥物是治療乳腺癌、淋巴瘤等疾病最常用的一類化療藥物,但治療過程中會引發心功能下降和心力衰竭等心臟不良事件[1]。臨床醫生一般根據左心室收縮功能指標的變化推測蒽環類藥物引起的早期心肌毒性情況,最常使用的指標為左心室射血分數(LVEF), 但其負荷依賴性導致早期診斷不敏感。一般情況下,應用蒽環類藥物化療的乳腺癌患者在較長化療周期后才會發生LVEF降低情況,此時往往提示心肌病變難以逆轉。左心室整體縱向應變(GLS)是一種較常見的與負荷相關的左心室功能評估方法,在某些血流動力學條件下和隨訪評估時對左心室功能進行評估可能會受限。二維斑點追蹤技術(2D-STI)得出的左室壓力-應變環(PSL)為較新的左心室心肌評估方法,創新之處為加入了后負荷,考慮了心肌變形情況,克服了LVEF和左心室心肌應變的前、后負荷依賴性問題[2]。PSL由動脈血壓估測的左心室壓力與GLS結合得出[3], 本研究應用PSL對乳腺癌患者化療前后的左心室心肌做功進行評價,旨在為監測乳腺癌患者化療后的早期心臟毒性提供新方法。
1 資料與方法
1.1 一般資料
選取2018年12月—2019年8月在江蘇省蘇北人民醫院甲乳外科治療的40例乳腺癌患者納入研究組,患者均為女性,平均年齡(43.5±10.4)歲,平均收縮壓(112.3±10.4) mmHg, 平均舒張壓(82.7±4.6) mmHg。納入標準: 經病理檢查確診乳腺癌者; 已行手術治療者; LVEF>60%者; 采用蒽環類藥物化療(共4個化療周期,每個周期21 d, 每次用藥劑量為90~120 mg/m2)。排除標準: 擬行輔助化療的患者; 超聲心動圖圖像質量較差(>3個節段的圖像無法分析)者; 持續性心房顫動、嚴重心律失常影響超聲資料采集和分析者; 配合度較差、失訪者。另選取同期體檢的40名健康人員納入對照組,均為女性,平均年齡(45.3±5.5)歲,平均收縮壓(114.2±6.3) mmHg, 平均舒張壓(82.6±7.5) mmHg。2組性別、年齡、血壓情況比較,差異無統計學意義(P>0.05)。
1.2 儀器與方法
應用GE Vivid E95彩色多普勒超聲診斷儀及M5s探頭進行檢查,囑受檢者取左側臥位,同步連接心電圖,調整采集深度及幀頻,圖像幀頻為50~60 MHz,進行常規二維超聲檢查,用辛普森雙平面法測量,記錄LVEF、左心室縮短分數(FS)、左心室舒張末期容積(EDV)、左心室收縮末期容積(ESV)、左心室每搏量(SV)參數。連續采集5個心動周期心尖四腔切面、心尖長軸切面和心尖兩腔切面的圖像,采用 ECHOPAC工作站通過2D-STI分別手工描記心尖四腔切面、心尖長軸切面和心尖兩腔切面中左心室的心內膜邊界,獲得2D-STI參數GLS。獲得2D-STI參數后在ECHOPAC工作站上標記安靜狀態下所有受檢者的收縮壓與舒張壓,然后采用GE特定的軟件構建1個無創PSL,得出左室整體做功指數(GWI)、左心室整體有效功(GCW)、左心室整體無效功(GWW)、左心室整體做功效率(GWE)。
1.3 統計學分析
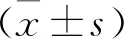
2 結 果
2.1 二維超聲心動圖參數比較
研究組化療2、4個周期后的LVEF、FS、EDV、ESV、SV水平與化療前比較,差異無統計學意義(P>0.05); 研究組不同時點的LVEF、FS、EDV、ESV、SV水平與對照組比較,差異均無統計學意義(P>0.05)。見表1。
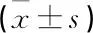
表1 2組二維超聲心動圖常規參數比較
2.2 2D-STI參數比較
研究組化療前的GLS、GWI、GCW、GWW、GWE與對照組比較,差異無統計學意義(P>0.05)。研究組化療2、4個周期后的GLS、GWI、GCW均低于化療前及對照組,差異有統計學意義(P<0.05), 其中GLS是以絕對值進行比較。研究組化療2、4個周期后的GWW、GWE與化療前及對照組比較,差異無統計學意義(P>0.05)。見表2。
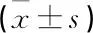
表2 2組2D-STI常規參數比較
2.3 相關性分析
乳腺癌患者化療后的GLS與左心室做功參數GWI、GCW均呈正相關(r=0.582、0.433,P<0.05); 乳腺癌患者化療后的GLS與左心室做功參數GWW、GWE均無顯著相關性(r=0.168、0.299,P>0.05)。
2.4 重復性試驗
Bland-Altman分析顯示,觀察者內及觀察者間的分析結果均具有良好的一致性,提示PSL測得的GWI、GCW重復性良好,測量結果的差異可被接受,見圖1。




A: 觀察者內左室整體做功指數分析圖; B: 觀察者間左室整體做功指數分析圖;C: 觀察者內左心室整體有效功分析圖; D: 觀察者間左心室整體有效功分析圖。
3 討 論
Ⅰ型化療藥物如蒽環類藥物可引起永久性心臟毒性,加速氧化應激和細胞凋亡,改變DNA修復心臟和線粒體功能所必需的心肌基因表達,如細胞合成、拓撲異構酶受到抑制及線粒體障礙、鈣超載、蛋白降解等,導致左心室心肌細胞超微結構改變引起細胞損傷[4]。化療藥物心臟毒性可以立即發生,也可能在治療數月或數年后才會發生。
本研究中,研究組化療前后的二維超聲心動圖常規參數LVEF比較,差異無統計學意義(P>0.05), 提示化療早期可能會低估左心室收縮功能受損程度,不能及時發現心臟毒性并采取心臟保護措施。本研究還顯示,研究組化療2、4個周期后的2D-STI參數GLS低于化療前,差異有統計學意義(P<0.05), 表明GLS可以較早地發現心臟損傷,但GLS僅反映對微血管更加敏感的且由心內膜下心肌纖維控制的左室整體縱向應變[5],不能反映整體徑向及扭轉收縮運動,可能會低估心臟受損程度。當左心室對抗動脈壓力升高時,SV短期內會下降,這是通過增加左心室的做功量來補償泵血功能,GLS無法在這種情況下監測到早期心臟功能變化[6]。研究[7]顯示,心肌做功參數可早期、敏感地反映心臟收縮功能改變,并更好地反映不同負荷條件下的心臟變化情況。
左心室收縮運動主要由3個變化引起,分別為基底至心尖縱向縮短、心外膜向心內膜徑向增厚、周向旋轉和縮短,可以推斷心肌變形中所有變化均有助于左心室做功[8]。臨床通過應變曲線的微分和這個值乘以瞬時左心室壓力計算節段縮短率來量化心肌做功[9]。GCW被定義為心肌收縮時肌細胞縮短,等容舒張時肌細胞延長[10-12]。GWI是指從二尖瓣關閉到二尖瓣開放這段時間內以左室壓力-應變面積表示的總功,反映了左心室總做功量[13-14]。GWE是指所有節段的左室整體有用功除以左室整體有用功及左室整體無用功之和,反映了在心動周期中機械能的消耗效率[10, 15-17]。
研究[8]表明,GWI、GCW為反映心肌受損情況的重要參數。本研究中,研究組化療2、4個周期后的GLS、GWI、GCW低于化療前,差異有統計學意義(P<0.05), 說明乳腺癌患者化療后心肌一定程度受損,可能因為蒽環類藥物產生的氧源性自由基與心肌細胞親和力較強,分解出損傷心肌細胞的物質。與化療2個周期后相比,研究組化療4個周期后的GLS、GWI、GCW降低,差異有統計學意義(P<0.05), 說明隨著蒽環類藥物劑量的增加,乳腺癌化療患者的心肌損害會逐漸加重,提示左心室心肌做功參數可作為判斷早期心肌毒性的有效指標。本研究中,研究組患者化療前、化療2個周期、化療4個周期的GWE平均值分別為93%、92%、90%, 對照組GWE平均值為93%, 相比以往研究[5]中挪威健康人的GWE平均值96%有所下降,這可能與不同地區人群體質、運動耐力不同有關。心力衰竭且射血分數下降的患者GWE明顯下降,可能因為其大量左室非同步化[18], 以及整體或局部左室應變值降低,反映了收縮功能受損[19]。CHAN J等[6]研究顯示,高血壓患者和健康對照組的GWE無顯著差異。在沒有結構或功能改變的情況下,單獨存在心血管危險因素,似乎不會對GWE產生影響[6]。本研究中,研究組化療后GWW、GWE與化療前相比,差異無統計學意義(P>0.05), 說明化療前后無大量左心室非同步運動[20]。此外,乳腺癌患者化療后的GLS與左心室做功參數GWI、GCW呈正相關(r=0.582、0.433,P<0.05), 與GWW、GWE均無顯著相關性(r=0.168、0.299,P>0.05), 說明心肌受損, GLS下降,則GWI、GCW下降。
本研究中應用的GE超聲心動圖超聲設備為目前唯一能提供左心室做功參數計算軟件的儀器,RUSSELL K等[3]采用從2D-STI中獲得的無創性PSL方法計算心肌做功。PSL是在估測的左心室壓力曲線與斑點追蹤技術得出的應變聯合基礎上形成的,無需考慮曲率的半徑和不同纖維的方向[3]。心肌做功以PSL表示,患者化療后PSL面積相比化療前縮小,即左心室心肌做功降低,說明PSL對乳腺癌患者化療早期的左心室收縮功能評價效果較好。PSL可通過有創性方法與無創性方法獲得,有創性方法是使用左心導管插入術測量壓力,無法在臨床廣泛應用。相關研究[10]顯示,無創PSL和有創PSL的測量結果具有極好的相關性。本研究采用無創方法測量的肱動脈壓力值是左心室壓力的估計值,在臨床中較容易獲得,但當肱動脈壓力和左心室壓力不協調時,動脈壓可能偏大或偏小,例如左室流出道梗阻的患者和主動脈重度狹窄的患者,若患者合并有上臂動脈疾病,估測的動脈壓也可能不準確。
綜上所述,PSL可定量評估乳腺癌患者化療后的心肌做功情況,對心肌受損的評價具有一定價值,有利于提高蒽環類藥物引起的相關心血管系統并發癥的早期檢出率,從而盡早調整化療方案,防止嚴重心臟不良事件的發生。

