衣藻二氧化碳濃縮機制及其調控的研究進展
秦燕 范波 苗貴東
摘要 當低濃度CO2限制微藻光合作用時,CO2濃縮機制(CCM)是一種有效的無機碳(Ci)吸收策略,以保證微藻的正常生存和繁殖。CCM主要是通過升高1,5-二磷酸核酮糖羧化酶/加氧酶(Rubisco)附近的CO2濃度增強光合作用的效率,同時抑制光呼吸的進行。CCM的關鍵步驟包括無機碳的聚集吸收、Rubisco對CO2的固定和碳酸酐酶催化的不同Ci的轉換。CCM中分子調控元件的有序協作,不僅可以幫助細胞感知周圍CO2的濃度,誘導調節CCM基因的表達,還可以協調衣藻在低濃度CO2環境下光合作用中碳和其他代謝途徑的相互作用。總結了目前以衣藻作為模式生物對真核藻類CCM的研究概況、調控機理,以及CCM機制在農業方面的應用和展望。
關鍵詞 衣藻;二氧化碳濃縮機制;調控機理;無機碳吸收系統
中圖分類號 Q949.21? 文獻標識碼 A
文章編號 0517-6611(2021)04-0020-06
doi:10.3969/j.issn.0517-6611.2021.04.006
Research Progress on the CO2 Concentrating Mechanism and Its Regulation in Chlamydomonas
QIN Yan,FAN Bo,MIAO Gui-dong (College of Biology and Chemistry,Xingyi Normal University for Nationalities,Xingyi,Guizhou 562400)
Abstract CO2 concentrating mechanism (CCM) is an effective way for carbon assimilation that enables microalgae to survive and proliferate in the limiting CO2 concentration.CCM can improve the CO2 concentration near the Rubisco to enhance the photosynthetic efficiency and suppress the photorespiration.The key components of CCM include inorganic carbon (Ci) uptake,Ci fixation by Rubisco and the interconversion of different Ci catalyzed by CA.An array of the molecular regulatory elements can facilitate cells to sense the CO2 concentration,regulate the expression of the CCM and to coordinate the photosynthetic carbon metabolism and other metabolic processes in response to limiting CO2 conditions.This review summarized the current understanding of the eukaryotic algal CCM,based largely on chlamydomonas as a model organism,to illustrate how chlamydomonas adapts to the limiting CO2 and how its CCM was regulated.
Key words Chlamydomonas;CO2 concentrating mechanism;Regulation mechanism;Ci absorption system
基金項目
貴州省教育廳青年科技人才成長項目(黔教合KY字〔2019〕221號);興義民族師范學院博士科研基金項目(18XYBS02);黔西南州2019年州級科技計劃自籌資金項目(2019-2-50)。
作者簡介 秦燕(1980—),女,山東萊蕪人,副教授,博士,從事細胞與分子生物學研究。
收稿日期 2020-07-11
光合作用中的碳代謝可稱為地球上最重要的化學反應,地球上全部綠色植物的生長都離不開光合作用,是全球碳循環的關鍵環節。光合作用過程中核心的途徑是卡爾文循環(CCB),此循環包含一系列的生化反應,通過這些反應無機碳(Ci)轉化成有機碳,并將太陽能儲存在碳水化合物中。CCB循環最初是在綠藻Chlorella和Scenedesmus中闡明的[1]。綠藻中的萊茵衣藻(Chlamydomonas reinhardtii)以其獨特的優勢,逐漸成為模式生物來研究生物學的熱點問題,如光合作用、光合趨光性、鞭毛/纖毛生物學、藻脂生物學。因為衣藻是一種單倍體生物,生活周期短、遺傳背景清楚,衣藻的光合作用結構、光合作用中的光反應和暗反應中碳的代謝與高等植物非常相似[2-5],因此在衣藻中的很多發現可以直接適用于高等植物。衣藻作為一種生活在特殊環境中的單細胞生物,與其他藻類一樣,有其獨特和靈活的代謝特征和基因表達調控的獨特機制,使其能夠在外界條件波動極大的環境中生存下來[3-4,6-7]。
光合自養的生物已經進化出許多適應策略來應對周圍各種不利的環境條件,其中一個例子就是CO2濃縮機制(CCM),這是藍細菌和真核微藻為適應地球上古老大氣中CO2濃度降低和O2濃度升高進化出來的一種響應機制。 1,5-二磷酸核酮糖羧化酶/加氧酶(Rubisco)是光合作用過程中碳吸收的核心酶,它在CCB循環中催化第一步也是最重要的一步羧化反應,催化CO2與RuBP的結合,實現無機碳向有機碳的轉化。Rubisco是一種古老的酶,進化中存在于高濃度CO2低濃度O2的環境中。目前大氣中的CO2濃度遠遠低于Rubisco羧化酶的活性所需要的飽和濃度,大氣中高比率的O2/CO2提高了Rubisco加氧酶的活性,這使其進入既消耗能量又釋放CO2的光呼吸途徑[8]。CCM機制則通過彌補Rubisco羧化酶效率低的特點,提高CO2濃度,增加光合作用的效率。目前在植物中已經進化出不同的策略提高Rubisco附近CO2濃度,增強Rubisco羧化酶的活性同時降低加氧酶活性,實現高效率的光合作用。這些策略出現在不同類群植物的不同發育階段,包括高等植物中多樣化的C4代謝途徑和微藻、藍細菌中多樣化的CCMs[9-10]。
CCM與藻類植物光合作用、代謝活動、生長發育等方面密切相關,也是提高藻類生物量的關鍵因素。了解CCM可以更好地理解這些微觀的生產者們是如何影響全球環境的,并可指導對藻類進行遺傳和分子手段的操作,以提高其生物產量。對CCM機制的理解,還有助于實現人工設計將藻類特定特征引入到C3植物提高其光合效率[11-12]。藍細菌的CCM已經在幾個模式藍細菌中得到廣泛研究[13]。近幾年,以衣藻作為真核光合模式生物,對CCM分子機制的理解也有了極大的進步。筆者主要是結合目前對衣藻CCM的理解及與無機碳吸收的相互作用,來總結衣藻是如何適應低CO2濃度的環境條件以及它的CCM是如何調節的。
1 CO2濃縮機制的概述
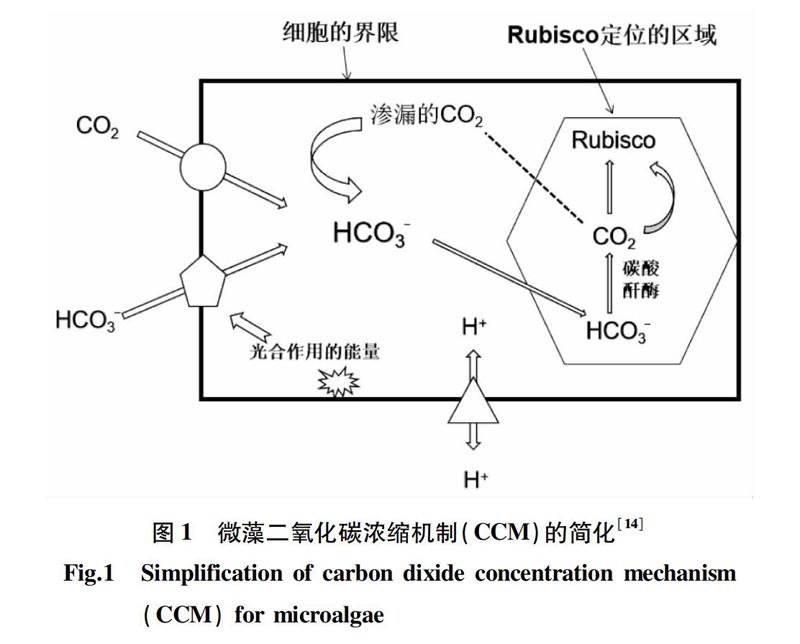
微藻CCM是基于單細胞的CO2濃縮機制,其依賴于多種無機碳吸收系統(圖1)。這些無機碳吸收系統在細胞內形成以HCO3-為主的Ci庫,庫內的CO2濃度比水中的CO2濃度高1 000倍,這可能是目前已知最有效的Ci吸收系統[14]。CCM主要是通過升高Rubisco附近的CO2濃度增強光合作用的效率,同時抑制光呼吸的進行。
CCM是一種非常靈活調控的機制,可適應多種低濃度的CO2條件,通過不同的調控網絡與其他生理過程協調,如光合作用、光呼吸中的碳代謝、細胞周期和晝夜節律等。微藻在多種低CO2濃度條件下發生了一系列的適應性反應,包括CCM基因的誘導表達、代謝活動的變化、生理的變化等。許多CCM研究將自然界的CO2濃度區分為2種生理狀態:高CO2濃度狀態(CO2 濃度1%~5%)和受限制的低CO2濃度狀態(CO2濃度0~0.03%)。事實上,自然界存在多種CO2濃度的環境條件,如有的藻類生活在CO2濃度高的土壤中,有的生活在富含有機質的CO2濃度極低的水生條件。微藻在多種CO2濃度條件下的適應性研究都已被闡明,這反映了微藻可以適應多種自然生境條件。
2 衣藻中的二氧化碳濃縮機制
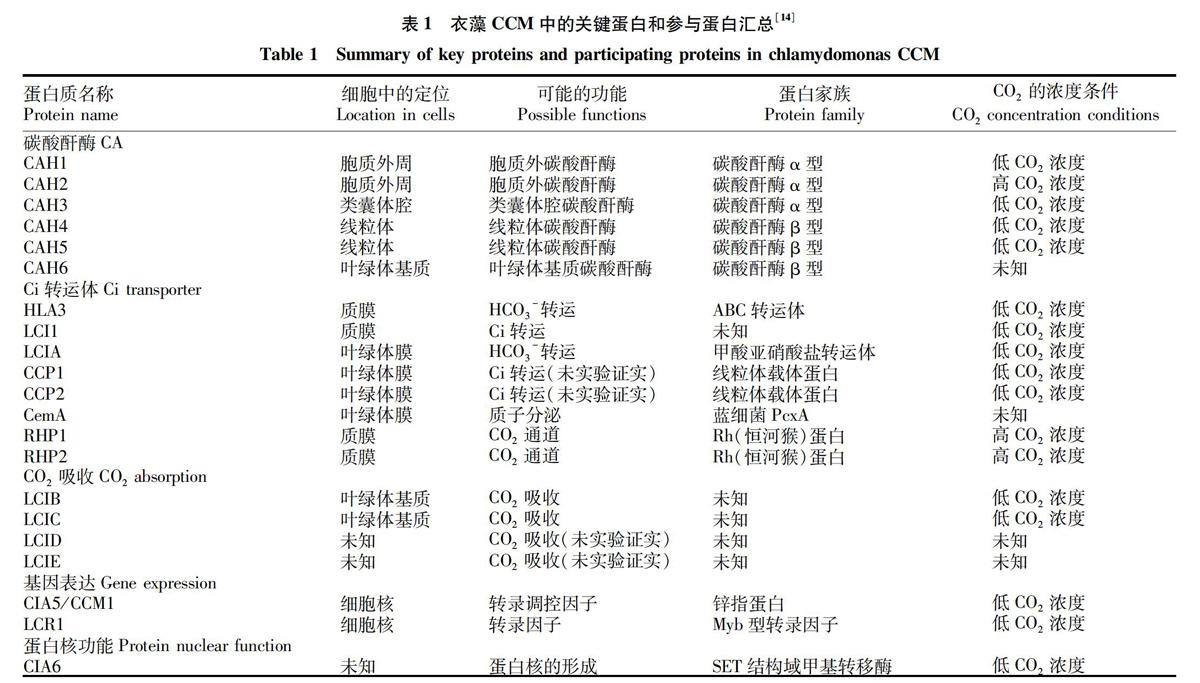
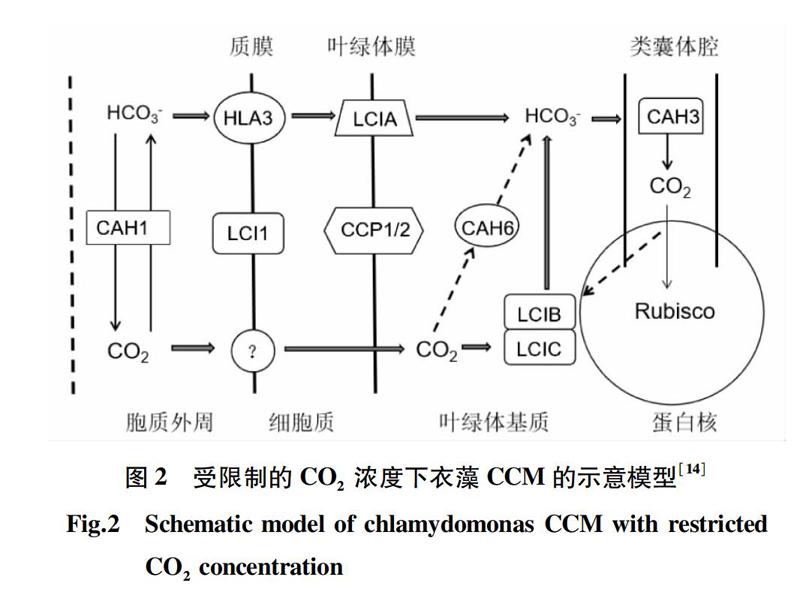
本質上講,CCM的核心是活性Ci的吸收系統,而活性Ci的吸收包括HCO3-的跨膜運輸、CO2的吸收、碳酸酐酶(CA)對不同狀態Ci的轉化和遺漏CO2的重新捕獲。在衣藻中,Ci的吸收主要發生在質膜、葉綠體膜和葉綠體類囊體膜上[15]。通過轉錄組分析,確定了許多低CO2濃度條件下響應的基因如編碼Ci的轉運體、CO2吸收系統和CA(表1)。通過對CCM突變體的分子生物學研究,確定出許多Ci吸收的關鍵成分。在受限制的低CO2濃度條件下,不同的膜Ci轉運體、CO2吸收系統和不同的CA參與了CCM的過程[14](圖2)。這些Ci吸收系統通過一系列調控元件的調控,從轉錄水平和翻譯后水平2個層面調控基因的表達,使衣藻快速地適應不同的環境條件。
以下主要介紹了活性Ci如何從細胞外通過各種膜系統進入到類囊體基質中的過程,以及膜上和膜內有哪些Ci轉運體蛋白參與了此過程。
2.1 細胞表面
在水生環境中,有CO2和HCO3-這2種無機碳形式。當CO2在液相和氣相達到平衡時,溶解CO2的量取決于氣相中CO2的分壓,但是水中的CO2擴散速率比空氣中慢104倍。水中CO2轉化成HCO3-的速率依賴于pH。因為碳酸酐酶的解離常數(pKa值)接近6.4,在中性到堿性pH時,HCO3-占主導地位。為了保持細胞表面有足夠多的HCO3-和CO2,需要大量有活性的HCO3-轉運體或有活性的CO2吸收系統驅動大量的Ci流,這就需要有多個CA維持Ci的供應來保持HCO3-和CO2的平衡。CAH1是質膜外的碳酸酐酶,該蛋白在受限制的低CO2濃度條件下誘導表達,其功能可能是維持質膜HCO3-轉運體運輸的HCO3-的平衡或活性CO2吸收系統中CO2的平衡[16]。
2.2 穿越質膜
Ci進入細胞的第一道屏障是質膜。因為細胞膜對帶電荷的Ci如HCO3-是不能通透的,所以Ci進入細胞需要膜上的Ci轉運體的協助。 目前已經從衣藻中鑒定出2個HCO3-轉運體HLA3和LCI1參與此過程。
HLA3是一種定位于質膜上的ABC轉運體蛋白,含有ABC轉運體特有的結構域,在衣藻和很多綠藻中都發現了HLA3轉運體,該蛋白在CO2濃度低時發揮作用。ABC轉運蛋白介導的HCO3-的吸收在藍細菌中也有報道[13]。
LCI1是質膜上的另一個Ci轉運體[17]。該蛋白有幾個預測的跨膜結構域,但是未鑒定出具有功能的模體。如果在lcr1突變體中過表達LCI1可以在低CO2濃度下提高光合作用對Ci的親和力,并能促進HCO3-的吸收[18]。此蛋白對Ci種類吸收的偏好性仍不清楚。與其他參與Ci吸收的蛋白不同,LCI1蛋白被認為是一種孤兒蛋白,即在與衣藻親緣關系很近的物種(即使在團藻Volvox)中,沒有確定出序列同源物,只在衣藻和其他幾個綠藻基因組中預測出幾個膜蛋白與該蛋白的空間結構相似。
2.3 細胞質內 目前仍不清楚胞質中哪些成分參與活性Ci的吸收以及Ci是否會在胞質中積累。如果胞質中Ci濃度低時,則需要CA的存在捕獲更多的CO2。自然界中,CA一般分為α、β、γ 3類,目前從衣藻中已經鑒定出12個編碼碳酸酐酶蛋白的基因CAs,包括3種α-CAs、6種β-CAs和3種γ-CAs,分別定位于線粒體(5個)、葉綠體基質(1個)、類囊體基質(1個)、胞質(1個)、壁膜間隙(3個),CAH7的定位仍然未知[19]。定位于胞質中的CAH9蛋白,其基因序列獨特,與其他幾種基因的序列差別較大,目前功能未知。定位于線粒體中的CAH4、CAH5,兩者的核酸序列高度相似可達95%,均形成反向重復的結構[19],這2個蛋白在受限制的CO2濃度下可被誘導大量表達,但這2個蛋白的功能未知,有可能不直接在CCM中發揮作用[20]。有研究發現如果將衣藻細胞從CO2濃度高的區域移動到CO2濃度低的區域,線粒體將會從中間位置移動到靠近質膜的位置,這種線粒體位置的移動可能是因為質膜上轉運體的電荷發生變化引起的[21]。
2.4 穿越葉綠體膜
Ci吸收過程中的另一道障礙是葉綠體膜。有人從衣藻中分離出游離葉綠體,在葉綠體中觀察到了活性Ci吸收的整個過程,并鑒定出許多葉綠體膜上的Ci轉運體[17]。
LCIA是唯一確定參與低CO2濃度下跨葉綠體膜轉運HCO3-的蛋白。在衣藻中,LCIA是一個主動運輸的轉運體,LCIA作為一種通道協助Ci進入葉綠體,其發揮功能需要與質膜上其他蛋白如HLA3或LCI1協同作用完成,它們共同將HCO3-逆著葉綠體膜上的電位轉運至葉綠體內[15-22]。
葉綠體膜上還鑒定出CCP1和CCP2這2種Ci轉運體,這2個葉綠體蛋白幾乎完全相同,它們的序列與線粒體運載蛋白超家族高度相似[23]。但是有人推測此蛋白可能不參與Ci吸收[24],認為或許CCP1/2的功能被掩蓋[20]或者它們只是參與了適應低CO2濃度其他代謝物的轉運[24]。有關CCP1/2在CCM中的功能需要更深入的研究。
葉綠體膜上另外一種膜蛋白CemA可能也是一種Ci轉運體,它是質體ycf10基因的表達產物,ycf10基因的破壞會引起葉綠體中Ci吸收的降低[25]。此蛋白在藍細菌中的同源物對于CO2的傳遞是必不可少的[26]。
2.5 葉綠體基質
葉綠體基質中有很多蛋白參與Ci的積累。LCIB是廣泛分布于葉綠體基質中的蛋白質[15],催化基質中CO2轉化為HCO3-而保持基質中Ci的積累,此功能類似藍細菌中ChpX和ChpY蛋白(也稱為CupA和CupB)[27]。一般認為LCIB只在極低CO2濃度下發揮功能。在一些真核藻類和多種藍細菌基因組中只發現一個LCIB的同源物[3,20,28],可能LCIB是以單體的形式發揮功能。在極低CO2濃度下,LCIB與LCIA協同完成HCO3-的吸收[15]。但是LCIB參與的Ci吸收的分子機制沒有太多證據支持。
LCIB還與其同源物LCIC形成異源多聚體LCIB/LCIC復合物[15],但LCIC在Ci吸收中是否起作用仍不清楚。LCIB/LCIC復合物一般定位于2個分開的區域,分散在整個基質中或集中分布在蛋白核周圍。在極低CO2濃度時,復合物會特異地定位于蛋白核周圍,在低CO2濃度或高CO2濃度時,復合物會分布在整個基質中[15]。調控LCIB/LCIC復合物定位的分子機制還不清楚。
在衣藻葉綠體基質中還有一種碳酸酐酶CAH6,其功能是在堿性基質條件下將CO2轉化成HCO3-,以維持基質中高濃度的Ci或者重新捕獲滲漏的CO2[29]。
除了LCIB/LCIC和CAH6以外,還發現了另外2種LCIB同源物——LCID和LCIE,推測它們可能在Ci吸收中起作用[30]。
2.6 類囊體和蛋白核
在大多數藻類中,Rubisco定位于葉綠體內一個稱為蛋白核的結構中(圖3)。在衣藻中,蛋白核是一個液體樣的細胞器,Rubisco的小亞基(SSU)和EPY1蛋白對蛋白核的形成起重要作用,利于其形成液體樣的結構[31]。蛋白核外面被淀粉鞘包圍,淀粉鞘的形態直接影響蛋白核的數量和CCM的功能[32]。蛋白核由Rubisco的大小亞基組成[33],在蛋白核內部,HCO3-被碳酸酐酶CAH3催化脫水生成CO2,被附近的Rubisco羧化進入卡爾文循環。碳酸酐酶CAH3催化HCO3-脫水轉化成CO2的效率很高,會促進細胞內Ci的大量積累,可達到野生型的5倍[34]。Blanco-Rivero 等[35]將衣藻從高CO2濃度轉移到低CO2濃度時,發現CAH3被磷酸化,碳酸酐酶的活性提高,但CAH3蛋白的量并沒有增多,這說明CAH3翻譯后加工也可以調控CCM,使其適應低CO2濃度條件。
利用原位低溫電子斷層掃描術已觀察到衣藻蛋白核的三維結構[36],顯示類囊體的垛疊層和蛋白核通過圓柱形的蛋白核小管連接在一起。在蛋白核小管中有成束的多個平行的小管。蛋白核小管上的CAH3催化平行小管中的HCO3-轉化成CO2,釋放到蛋白核中。
Rubisco主要分布在葉綠體基質和蛋白核中,其動態分布與CO2濃度有關:在受限制的低濃度CO2條件下,幾乎所有的Rubisco都分布在蛋白核中,而在高濃度CO2條件下,只有50%的Rubisco定位在蛋白核[33]。Rubisco的大小亞基對蛋白核的形成起重要作用[33],尤其是小亞基含有重要的結構元件,負責將Rubisco定位于蛋白核中。另外,蛋白CIA6和SAGA1也參與蛋白核的形成[37-38]。SAGA1可調節蛋白核周圍淀粉鞘的形態,但CIA6是否直接參與Rubisco的定位和誘導CCM基因表達仍不確定。
2.7 滲漏CO2的重新捕獲
蛋白核周圍的CO2如果沒有及時被Rubisco羧化,則會擴散滲漏。而CO2屏障和CO2循環機制則可防止多余CO2的滲漏。 有研究表明,低CO2濃度下,蛋白CAH6和LCIB/LCIC復合物參與了滲漏CO2的重新捕獲過程[29,35];在極低CO2濃度下,蛋白CAH6、LCID或LCIE可重新固定滲漏的CO2。
3 衣藻中CCM的調控
3.1 低濃度CO2環境下CCM的調控
3.1.1 CCM相關基因的調控 。
CCM相關基因在低濃度CO2條件下會出現動態的變化趨勢。轉錄水平上分析發現,許多CCM關鍵基因在受限制CO2濃度下表達會上調,如LCI1、LCIA、LCIB、HLA3及參與光呼吸的基因[14,17]。蛋白水平上分析發現,低CO2濃度條件下,許多蛋白如碳酸酐酶CAH1、CAH4和CAH5以及2個Ci轉運體CCP1和CCP2也會誘導表達[14]。
Brueggeman等[39]
對衣藻轉錄組數據進行了分析,并統計了低CO2濃度下基因調控的情況;當把衣藻從高CO2濃度轉移至受限制的CO2濃度時,15 500個衣藻基因中14%~38%(2 200~5 880個)的基因表達發生改變;在低CO2濃度或者極低CO2濃度下,1 000~2 000個基因表達明顯上調,其中許多是CCM相關的基因[39]。另外,一些響應CO2脅迫基因的表達水平發生了劇烈的變化,也包括很多重要的CCM基因,如Ci轉運基因(LCI1、LCIA、HLA3、CCP1/2、LCIB等)和CA基因(CAH1、CAH4/5)[40],其中有些是編碼可溶性蛋白和膜蛋白的功能未知的基因,這些基因可用來作為候選基因研究是否參與Ci轉運、吸收或其他CCM的功能。另外,有些基因在低CO2濃度下高表達、高CO2濃度下不表達,如LCI1、LCIA、LCR1、HLA3、CCP1、CAH4/5等;也有些CCM關鍵基因如LCIB和CAH3在低CO2濃度下則表達水平顯著上調,而在高CO2濃度下表現為低水平的組成型表達,說明這些基因可能參與了低CO2濃度下CCM的過程。
3.1.2 調控CCM基因表達的元件。大量證據證明,在衣藻中存在一個從多層面調控CCM表達的網絡系統,但是對CCM調控的分子機制仍不清楚。目前只有2種調控蛋白CIA5(也稱CCM1)和LCR被確認可能調控衣藻中CCM相關基因的表達。
3.1.3 CCM基因的翻譯后調控。
基因的翻譯后調控在調節細胞功能中廣泛存在,這種機制比轉錄水平的調控更能使細胞快速地應對環境的變化。很早就有研究表明衣藻為了適應受限制CO2濃度會發生蛋白磷酸化,但是CCM相關蛋白的磷酸化是最近才鑒定出來的,如將衣藻從高濃度CO2轉移到受限制CO2濃度時,2個類囊體蛋白LCI5和UEP發生了磷酸化[41], 以及CAH3在受限制CO2濃度時也發生了磷酸化。對衣藻的磷酸化蛋白組進行系統分析也發現了許多CCM相關蛋白的磷酸化,如HLA3、LCIC、LCID、LCI15、CAs以及低CO2濃度下誘導表達的其他蛋白[42]。
除了磷酸化,蛋白質的谷胱甘肽化也是一種翻譯后調控,如在衣藻中的LCIB和許多參與卡爾文循環的蛋白[43]。另外,CIA5中存在的SUMO的修飾位點可能也是一種翻譯后調控機制,盡管功能未知。
在衣藻適應受限制CO2濃度時可能存在多種翻譯后修飾作為信號,但這些修飾的分子機制仍不確定。
3.2 低CO2濃度條件下碳同化的調控
衣藻光合作用的光反應和暗反應過程與高等植物非常相似[20],然而衣藻因為具有其獨特而靈活的碳代謝特征以及細胞內獨特的區室化,使其能夠在不同的環境中生存和繁殖[3]。在衣藻中,前期固定的Ci最終都要進入卡爾文循環:CO2首先與五碳化合物RuBP在Rubisco的催化下生成兩分子的3-磷酸甘油酸(3-PGA),然后通過兩步反應將3-PGA還原成3-磷酸甘油醛,此步反應將會消耗光反應中產生的ATP和NADPH,而后3-磷酸甘油醛經過一系列反應重新生成RuBP,其中產生的許多中間產物可參與細胞內其他代謝途徑。Rubisco除了催化RuBP與CO2的羧化反應,還會催化RuBP與O2的加氧反應,此反應產生一分子的3-PGA和一分子的磷酸乙醇酸,進入光呼吸代謝途徑。當外界環境條件中CO2濃度受限制時,則會有一些代謝的碳從卡爾文循環中流入光呼吸代謝途徑。然而,在低CO2濃度條件下,衣藻的卡爾文循環和光呼吸這2種代謝途徑都會被調控以適應底物濃度受限的條件。
3.2.1 卡爾文循環。
在衣藻中已經鑒定出卡爾文循環的全部基因,這些基因在高CO2濃度和受限制的低CO2濃度的條件下均發揮作用。研究表明,大多數卡爾文循環中的酶受底物濃度限制,有些酶的濃度比其底物還高[44]。在細胞內只有幾種酶的濃度是與底物濃度相似接近飽和的,如Rubisco、FBP(1,6-二磷酸果糖酶)、SBP(1,7-二磷酸景天庚酮糖酶),通過調節這些酶的活性來提高光合效率是一種翻譯后調控過程。
為適應低CO2濃度條件,衣藻卡爾文循環中的基因表達會發生變化,如Rubisco亞基RbcS1、RbcS2和RbcL的轉錄表達會升高;Rubisco小亞基RBCS1、ALD3(醛縮酶)、PGK(磷酸甘油酸激酶)、GAP(3-磷酸甘油醛脫氫酶)和SBP的轉錄水平則會下調。有研究表明,卡爾文循環中酶的蛋白數量的變化并非與轉錄本數量的變化一致[44]。卡爾文循環的調控可能是翻譯后修飾或者底物抑制/激活等方面。許多卡爾文循環酶通過翻譯后修飾如谷胱甘肽化或鐵氧還蛋白二硫鍵的變化進行氧化還原調控[43,45]。氧化還原調控是建立起來的一種很好的系統,可將光合作用中的光反應和暗反應融合在一起,使細胞在適應多變環境時通過不同的細胞過程進行能量的分配。
3.2.2 光呼吸。
當周圍環境中CO2/O2比率降低時,Rubisco加氧酶的活性增強,產生磷酸乙醇酸,進入光呼吸代謝途徑,抑制磷酸丙糖異構酶的活性,從而干擾RuBP的再生。轉錄組水平和代謝水平的研究表明將衣藻從高濃度CO2轉移到低濃度CO2后,衣藻會有一個快速且短暫的光呼吸代謝的升高過程。轉錄組數據顯示,當將衣藻細胞從高濃度CO2轉入低濃度CO2 4 h后,編碼丙氨酸轉氨酶(ALT)的基因、甘油酸激酶(GLYK)的基因、乙醇酸脫氫酶(GYD1)的基因、羥基丙酮酸還原酶1(HPR1)的基因、絲氨酸乙醛酸氨基轉移酶1(SGA1)的基因和所有編碼甘氨酸脫羧酶亞基的基因(二氫硫辛酸脫氫酶1DLDH1除外)均出現基因表達的上調[40],這些基因的表達受CO2濃度和CIA5的調控。代謝組學的研究表明,光呼吸途徑中的中間產物如甘氨酸、甘油酸鹽、乙醛酸絲氨酸和3-磷酸甘油醛的量會明顯升高。代謝物的水平在衣藻轉入低濃度CO2 30 min后升高,但24 h內恢復至初始水平。一般認為衣藻在適應低CO2濃度時,光呼吸途徑中酶基因的表達、酶活性和代謝物水平的升高是暫時的,而后隨著CCM被誘導,均會恢復至初始的水平,CCM提高了Rubisco周圍的CO2濃度從而抑制了Rubisco加氧酶的活性,降低光呼吸。
盡管認為光呼吸是衣藻對外界低CO2濃度時調節碳代謝的重要機制,但許多其他的碳代謝途徑如淀粉代謝、糖酵解或脂代謝、呼吸作用中碳代謝均與光合作用過程中碳代謝密切相連,這些代謝與其他營養成分的代謝如氮、硫、磷和金屬元素的吸收使得藻類能快速適應多變的環境進行生長繁殖,闡明這個復雜的網絡體系將是未來研究的方向。
4 衣藻CCM轉入高等植物的研究
為了滿足不斷增長的全球人口的物質需求,到2050年糧食產量要提高85%以上。僅通過傳統農作物選育的方法或者農田擴展的方法,這個目標產量是不可能實現的。已經證實的一個可行的方法是通過遺傳工程提高作物的光合效率。光合作用中限制CO2固定的重要因素是Rubisco酶的催化效率低。為了減少光呼吸,一些光合產物會通過CCMs提高Rubisco活性位點周圍CO2/O2比率。有模型表明,如果將CCM成功引入主要糧食作物如水稻、小麥和大豆,可以使碳固定提高60%,同時還能提高水和氮的利用率[46]。許多CCM和光合作用工程的策略正在繼續研究,最有前景的是將衣藻的CCM轉入農作物中以提高農作物的光合效率。為了提高Rubisco周圍的CO2濃度,目前正在進行衣藻CCM蛋白核和HCO3-轉運體的改造、藍細菌CCM羧酶體和無機碳轉運體的改造、Rubisco蛋白動力學的改造、光呼吸中基因的改造以及優化卡爾文循環中RuBP的再生等[47]。
為了將衣藻的CCM引入高等植物,需要系統完整的分析方法。前期的工作已經取得了重大的進展,如已將藍細菌的Rubisco轉化入煙草質體中以改造C3植物[48];藍細菌中的HCO3-轉運蛋白BicA也成功地在煙草的質體中表達[49];衣藻CCM蛋白HLA3、LCIA和LCIB成功在高等植物中表達,衣藻的Rubisco成功引入擬南芥中并能在擬南芥中穩定表達[50];在大腸桿菌中功能性組裝完成了卡爾文循環[51]等。如果要鑒定高等植物中CCM的核心成分,可以將CCM引入到一個異源的、生長迅速、無CCM的光合系統中,如苔蘚(小立碗蘚)、地錢、植物細胞培養系統或者不含CCM的綠藻中。人工建造一套有功能的CCM的核心成分對于指導植物基因工程有重要作用。
未來研究CCM功能可以通過雜交系統實現,CCM成分可取自多種來源的物種,如綠藻、藍藻、硅藻、定鞭藻類和角苔。另外,還可通過合成蛋白質執行特定功能,如合成Rubisco連接體用于匹配連接高等植物的Rubisco,合成一種嵌合蛋白用于多種成分的正確組裝[52]。
5 總結與展望
衣藻CCM可以增加Rubisco周圍的CO2濃度,從而增強光合效率。衣藻CCM中除了典型的Ci吸收系統中轉運蛋白HLA3、LCIA和CAs外,衣藻內還發現了許多新的Ci吸收系統,包括LCIB/LCIC、LCI1和未被描述的蛋白,這些蛋白均是受限CO2濃度下誘導表達的。對這些蛋白的分子功能及其他Ci吸收系統進行研究,不僅可以更好地理解CCM,還可以提供一套完整的方案提高藻類和高等植物獲取Ci的效率。目前實驗室正在研究喀斯特水體中綠藻的CCM與非喀斯特水體中綠藻的CCM的不同,以期能為更深入地理解CCM補充數據支持。
因為真核藻類和高等維管植物進化上有比較近的親緣關系、相似的光合作用,所以真核藻類的CCM可能有更大的優勢轉入高等植物。未來迫切需要一個模型用來指導將衣藻的成分轉化到高等植物中。將衣藻CCM或者雜交CCM引入C3植物將是一個巨大的挑戰,但是正確利用資源一定能將其變成現實。
因為水生環境的復雜多變,以衣藻為模式生物對CCM的許多研究還不是很系統。從細胞水平和分子水平上對藍細菌和真核微藻CCM機制更詳盡的研究以及準確將CCM引入高等植物以提高高等植物的光合作用效率將是未來的研究方向。
參考文獻
[1]BENSON A A,CALVIN M.Carbon dioxide fixation by green plants[J].Annu Rev Plant Physiol,1950,1(1):25-42.
[2] HARRIS E H.Chlamydomonas as a model organism[J].Annu Rev Plant Physiol Plant Mol Biol,2001,52:363-406.
[3] GROSSMAN A R,CROFT M,GLADYSHEV V N,et al.Novel metabolism in Chlamydomonas through the lens of genomics[J].Curr Opin Plant Biol,2007,10(2):190-198.
[4] MERCHANT S S,PROCHNIK S E,VALLON O,et al.The Chlamydomonas genome reveals the evolution of key animal and plant functions[J].Science,2007,318(5848):245-250.
[5] SPALDING? M H.Photosynthesis and photorespiration in freshwater green algae[J].Aquat Bot,1989,34(1/2/3):181-209.
[6] GROSSMAN A R,CATALANOTTI C,YANG W,et al.Multiple facets of anoxic metabolism and hydrogen production in the unicellular green alga Chlamydomonas reinhardtii[J].New Phytol,2011,190(2):279-288.
[7] SPALDING M H.Microalgal carbon-dioxide-concentrating mechanisms:Chlamydomonas inorganic carbon transporters[J].J Exp Bot,2008,59(7):1463-1473.
[8] SPREITZER R J,SALVUCCI M E.RUBISCO:Structure,regulatory interactions,and possibilities for a better enzyme[J].Annu Rev Plant Biol,2002,53:449-475.
[9] GIORDANO M,BEARDALL J,RAVEN? J A.CO2 concentrating mechanisms in algae:mechanisms,environmental modulation,and evolution[J].Annu Rev Plant Biol,2005,56:99-131.
[10] SAGE R F,SAGE T L,KOCACINAR F.Photorespiration and the evolution of C4 photosynthesis[J].Annu Rev Plant Biol,2012,63:19-47.
[11] PRICE G D,PENGELLY J J L,FORSTER B,et al.The cyanobacterial CCM as a source of genes for improving photosynthetic CO2 fixation in crop species[J].J Exp Bot,2013,64(3):753-768.
[12] MCGRATH J M,LONG S P.Can the cyanobacterial carbon-concentrating mechanism increase photosynthesis in crop species? A theoretical analysis[J].Plant Physiol,2014,164(4):2247-2261.
[13] PRICE G D,BADGER M R,WOODGER F J,et al.Advances in understanding the cyanobacterial CO2-concentrating-mechanism (CCM):Functional components,Ci transporters,diversity,genetic regulation and prospects for engineering into plants[J].J Exp Bot,2008,59(7):1441-1461.
[14] WANG Y J,STESSMAN D J,SPALDING M H.The CO2 concentrating mechanism and photosynthetic carbon assimilation in limiting CO2:How Chlamydomonas works against the gradient[J].The plant journal,2015,82(3):429-448.
[15] WANG Y J,SPALDING M H.Acclimation to very low CO2:Contribution of limiting CO2 inducible proteins,LCIB and LCIA,to inorganic carbon uptake in Chlamydomonas reinhardtii[J].Plant Physiol,2014,166(4):2040-2050.
[16] COLEMAN J R,LUINENBURG I,MAJEAU N,et al.Sequence analysis and regulation of expression of a gene coding for carbonic anhydrase in Chlamydomonas reinhardtii[J].Can J Bot,1991,69(5):1097-1102.
[17] BUROW? M D,CHEN? Z Y,MOUTON T M,et al.Isolation of cDNA clones of genes induced upon transfer of Chlamydomonas reinhardtii cells to low CO2[J].Plant Mol Biol,1996,31(2):443-448.
[18] OHNISHI N,MUKHERJEE B,TSUJIKAWA T,et al.Expression of a low CO2-inducible protein,LCI1,increases inorganic carbon uptake in the green alga Chlamydomonas reinhardtii[J].Plant Cell,2010,22(9):3105-3117.
[19] MORONEY J V,MA Y B,FREY W D,et al.The carbonic anhydrase isoforms of Chlamydomonas reinhardtii:Intracellular location,expression,and physiological roles[J].Photosynth Res,2011,109(1/2/3):133-149.
[20] SPALDING M H.The CO2-concentrating mechanism and carbon assimilation[M]//HARRIS E H,STERN D B,WITMAN G B.
The chlamydomonas sourcebook:Vol 2.2nd ed.London:Academic Press,2009:257-301.
[21] AMOROSO G,SLTEMEYER D,THYSSEN C,et al.Uptake of HCO3- and CO2 in cells and chloroplasts from the microalgae Chlamydomonas reinhardtii and Dunaliella tertiolecta[J].Plant Physiol,1998,116(1):193-201.
[22] WU W,PETERS J,BERKOWITZ G A.Surface charge-mediated effects of Mg2+ on K+ flux across the chloroplast envelope are associated with regulation of stromal pH and photosynthesis[J].Plant Physiol,1991,97(2):580-587.
[23] CHEN Z Y,LAVIGNE L L,MASON C B,et al.Cloning and overexpression of two cDNAs encoding the low-CO2-inducible chloroplast envelope protein LIP-36 from Chlamydomonas reinhardtii[J].Plant Physiol,1997,114(1):265-273.
[24] POLLOCK S V,COLOMBO S L,PROUT D L,et al.Rubisco activase is required for optimal photosynthesis in the green alga Chlamydomonas reinhardtii in a low-CO2 atmosphere[J].Plant Physiol,2003,133(4):1854-1861.
[25] ROLLAND N,DORNE A J,AMOROSO G,et al.Disruption of the plastid ycf10 open reading frame affects uptake of inorganic carbon in the chloroplast of Chlamydomonas[J].EMBO J,1997,16(22):6713-6726.
[26] KATOH A,LEE K S,FUKUZAWA H,et al.cemA homologue essential to CO2 transport in the cyanobacterium Synechocystis PCC6803[J].Proc Natl Acad Sci USA,1996,93(9):4006-4010.
[27] PRICE G D,MAEDA S I,OMATA T,et al.Modes of active inorganic carbon uptake in the cyanobacterium,Synechococcus sp.PCC7942[J].Funct Plant Biol,2002,29(3):131-149.
[28] YAMANO T,TSUJIKAWA T,HATANO K,et al.Light and low-CO2-dependent LCIB-LCIC complex localization in the chloroplast supports the carbon-concentrating mechanism in Chlamydomonas reinhardtii[J].Plant Cell Physiol,2010,51(9):1453-1468.
[29] MORONEY J V,YNALVEZ R A.Proposed carbon dioxide concentrating mechanism in Chlamydomonas reinhardtii[J].Eukaryot Cell,2007,6(8):1251-1259.
[30] WANG? Y J,SPALDING M H.An inorganic carbon transport system responsible for acclimation specific to air levels of CO2 in Chlamydomonas reinhardtii[J].Proc Natl Acad Sci USA,2006,103(26):10110-10115.
[31] FREEMAN ROSENZWEIG E S,XU B,CUELLAR L K,et al.The eukaryotic CO2-concentrating organelle is liquid-like and exhibits dynamic reorganization[J].Cell,2017,171(1):148-162.
[32] MUKHERJEE A,MORONEY J V.How protein-protein interactions contribute to pyrenoid formation in Chlamydomonas[J].J Exp Bot,2019,70(19):5033-5035.
[33] MEYER M T,GENKOV T,SKEPPER J N,et al.Rubisco small-subunit a-helices control pyrenoid formation in Chlamydomonas[J].Proc Natl Acad Sci USA,2012,109(47):19474-19479.
[34] SHUTOVA T,KENNEWEG H,BUCHTA J,et al.The photosystem II-associated Cah3 in Chlamydomonas enhance the O2 evolution rate by proton removal[J].EMBO J,2008,27(5):782-791.
[35] BLANCO-RIVERO A,SHUTOVA T,ROMN? M J,et al.Phosphorylation controls the localization and activation of the lumenal carbonic anhydrase in Chlamydomonas reinhardtii[J].PLoS One,2012,7(11):1-10.
[36] ENGEL B D,SCHAFFER M,CUELLAR L K,et al.Correction:Native architecture of the Chlamydomonas chloroplast revealed by in situ cryo-electron tomography[J/OL].eLife,2015,4[2020-03-25].https://pubmed.ncbi.nlm.nih.gov/26367339/.doi:10.7554/eLife.11383.
[37] MA Y B,POLLOCK S V,XIAO Y,et al.Identification of a novel gene,CIA6,required for normal pyrenoid formation in Chlamydomonas reinhardtii[J].Plant Physiol,2011,156(2):884-896.
[38] ITAKURA A K,CHAN K X,ATKINSON N,et al.A Rubisco-binding protein is required for normal pyrenoid number and starch sheath morphology in Chlamydomonas reinhardtii[J].Proc Natl Acad Sci USA,2019,116(37):18445-18454.
[39] BRUEGGEMAN A J,GANGADHARAIAH D S,CSERHATI M F,et al.Activation of the carbon concentrating mechanism by CO2 deprivation coincides with massive transcriptional restructuring in Chlamydomonas reinhardtii[J].Plant Cell,2012,24(5):1860-1875.
[40] FANG W,SI Y Q,DOUGLASS S,et al.Transcriptome-wide changes in Chlamydomonas reinhardtii gene expression regulated by carbon dioxide and the CO2-concentrating mechanism regulator CIA5/CCM1[J].Plant Cell,2012,24(5):1876-1893.
[41] TURKINA M V,BLANCO-RIVERO A,VAINONEN J P,et al.CO2 limitation induces specific redox-dependent protein phosphorylation in Chlamydomonas reinhardtii[J].Proteomics,2006,6(9):2693-2704.
[42] WANG H X,GAU B,SLADE W O,et al.The global phosphoproteome of Chlamydomonas reinhardtii reveals complex organellar phosphorylation in the flagella and thylakoid membrane[J].Mol Cell Proteomics,2014,13(9):2337-2353.
[43] ZAFFAGNINI M,BEDHOMME M,GRONI H,et al.Glutathionylation in the photosynthetic model organism Chlamydomonas reinhardtii:A proteomic survey[J].Mol Cell Proteomics,2012,11(2):1-15.
[44] METTLER T,MHLHAUS T,HEMME D,et al.Systems analysis of the response of photosynthesis,metabolism,and growth to an increase in irradiance in the photosynthetic model organism Chlamydomonas reinhardtii[J].Plant Cell,2014,26(6):2310-2350.
[45] MORISSE S,MICHELET L,BEDHOMME M,et al Thioredoxin-dependent redox regulation of chloroplastic phosphoglycerate kinase from Chlamydomonas reinhardtii[J].J Biol Chem,2014,289(43):30012-30024.
[46] LONG S P,MARSHALL-COLON A,ZHU X G.Meeting the global food demand of the future by engineering crop photosynthesis and yield potential[J].Cell,2015,161(1):56-66.
[47] MACKINDER L C M,CHEN C,LEIB R D,et al.A spatial interactome reveals the protein organization of the algal CO2-concentrating mechanism[J].Cell,2017,171(1):133-147.
[48] LIN M T,OCCHIALINI A,ANDRALOJC P J,et al.A faster Rubisco with potential to increase photosynthesis in crops[J].Nature,2014,513(7519):547-550.
[49] PENGELLY J J,FRSTER B,VON CAEMMERER S,et al.Transplastomic integration of a cyanobacterial bicarbonate transporter into tobacco chloroplasts[J].J Exp Bot,2014,65(12):3071-3080.
[50] ATKINSON N,LEITN,ORR D J,et al.Rubisco small subunits from the unicellular green alga Chlamydomonas complement Rubisco-deficient mutants of Arabidopsis[J].New Phytol,2017,214(2):655-667.
[51] ANTONOVSKY N,GLEIZER S,NOOR E,et al.Sugar synthesis from CO2 in Escherichia coli[J].Cell,2016,166(1):115-125.
[52] GONZALEZ-ESQUER C R,SHUBITOWSKI T B,KERFELD C A.Streamlined construction of the cyanobacterial CO2-fixing organelle via protein domain fusions for use in plant synthetic biology[J].Plant Cell,2015,27(9):2637-2644.

