基于尿液代謝組學的冠心病血瘀證模型大鼠生物學基礎研究
李靜 ,鐘森杰,李亮,吳華英,資源,袁志鷹,黃惠勇
1.湖南中醫藥大學,湖南 長沙 410208;2.湖南中醫藥大學中醫診斷研究所,湖南 長沙 410208;3.衡陽市中醫醫院,湖南 衡陽 421001
冠狀動脈粥樣硬化性心臟病(coronary atherosclerotic heart disease,CHD)是指因冠狀動脈發生粥樣硬化或痙攣引起管腔閉塞或狹窄,導致心肌缺血、缺氧或壞死而引發的心臟病變[1]。據統計,在我國CHD 是死亡率最高的疾病[2]。CHD 屬中醫學“胸痹”“心痛”等范疇,屬本虛標實之證,本虛為氣血陰陽虧虛,標實為寒凝、血瘀、痰濁、氣滯等,而血瘀證是CHD 中最常見的證型之一[3-4]。CHD 血瘀證主要表現為胸部刺痛、絞痛,固定不移,痛引肩背或臂內側,胸悶,心悸不寧,唇舌紫黯,或有瘀斑,舌下絡脈青紫,脈沉澀或結代[5]。
代謝組學是系統生物學研究的重要組成部分,分析技術具有高通量、高靈敏度、高精確度的特點,使生物體內源性代謝物質變化規律與疾病生理病理變化相契合[6]。代謝組學研究思路具有整體性、動態性和系統性的特點,與中醫學的哲學思想具有一致性[7]。因此,本研究以CHD 血瘀證模型大鼠為研究對象,運用超高效液相色譜-質譜聯用(UPLC-QE-MS)代謝組學技術進行檢測,分析CHD 血瘀證模型大鼠尿液內源性代謝物及代謝通路的變化,以期從代謝組學角度闡明CHD 血瘀證潛在的生物學基礎,為CHD 有效防治提供新思路。
1 材料和方法
1.1 動物
SPF 級雄性SD 大鼠20 只,體質量(220±20)g,購自湖南斯萊克景達實驗動物有限公司,動物許可證號SCXK(湘)2019-0004。分籠飼養于湖南中醫藥大學實驗動物中心SPF 級動物房,溫度22~26 ℃,相對濕度40%~65%。適應性飼養1 周后開始實驗。
1.2 藥物、試劑與儀器
注射用青霉素鈉(80 U/支,華北制藥股份有限公司,批號20190418),鹽酸利多卡因注射液(5 mL,0.1 g/支,國藥集團容生制藥有限公司,批號20190618)。甲醇(批號67-56-1,CNW Technologies),乙腈(批號75-05-8,CNW Technologies),乙酸銨(批號 631-61-8,CNW Technologies),氨水(批號1336-21-6,CNW Technologies)。小動物呼吸機-220V(深圳市瑞沃德生命科技有限公司),P150 型16 通道多導電生理記錄儀(美國BIOPAC 公司),Vanquish型超高效液相色譜儀(Thermo Fisher Scientific),Q Exactive HFX 型高分辨質譜儀(Thermo Fisher Scientific),BSA124S-CW 天平(Sartorius),Heraeus Fresco17 離心機(Thermo Fisher Scientific),D24UV純水儀(Merck Millipore),PS-60AL 超聲儀(深圳市雷德邦電子有限公司)。
1.3 分組與造模
20 只大鼠按隨機數字表法分為假手術組、CHD血瘀證模型組,每組10 只。CHD 血瘀證模型組大鼠參考文獻[8-9]方法,采用結扎左冠狀動脈前降支方法制備CHD 血瘀證模型。CHD 血瘀證模型組大鼠腹腔注射10%水合氯醛麻醉,背位固定,頸部消毒,暴露氣管,連接小動物呼吸機,行氣管插管,設置呼吸頻率85 次/min,潮氣量8~10 mL/kg,呼吸比為2∶1。大鼠機械通氣正常后,于左側第3、4 肋間切開皮膚,鈍性分離,充分暴露心臟,用6-0 帶線縫合針在左心耳與肺動脈圓錐交界稍下約2~3 mm 處結扎左冠狀動脈前降支,以結扎部位以下心肌變白、搏動減弱且心電圖表現為ST 段弓背抬高或/和T 波高聳或與其形成單向曲線為造模成功。關閉胸腔,縫合傷口。術后連續3 d 肌肉注射青霉素鈉預防感染。假手術組開胸后,只穿線不結扎,其余步驟同CHD 血瘀證模型組。大鼠自由飲水,正常進食。
1.4 觀察指標
1.4.1 HE 染色
造模成功后第3 日處死大鼠,開胸取心肌組織,4%多聚甲醛固定,常規石蠟包埋,連續切片,依次脫水,行HE 染色,光學顯微鏡下觀察心肌形態。
1.4.2 尿液代謝組學檢測
造模成功后第3 日7:00 輕提大鼠尾根部,按摩膀胱,多次采集大鼠晨尿樣本,用尿液存儲器迅速收集尿液,過濾,分裝至1.5 mL EP 管,4 ℃、1000 r/min離心5 min,取上清液,并移至凍存管,液氮速凍30 s后取出,置于-80 ℃冰箱保存。樣本4 ℃融化,進行上機檢測前處理:①根據樣品滲透壓,加入一定體積的水;②加入400 μL 提取液[(甲醇∶乙腈=1∶1(V/V),含同位素標記內標混合物)],渦旋混勻30 s;③超聲10 min(冰水浴);④-40 ℃靜置1 h;⑤將樣品4 ℃、12 000 r/min 離心15 min;⑥取上清液于進樣瓶中上機檢測;⑦所有樣品另取等量上清,混合成質控樣品上機檢測。
UPLC-QE-MS檢測條件:采用Vanquish超高效液相色譜儀,通過WatersACQUITY UPLCBEH Amide 液相色譜柱(2.1 mm×100mm,1.7μm)對目標化合物進行色譜分離。流動相A為水相,含25mmol/L乙酸銨和25mmol/L氨水,B為乙腈。采用梯度洗脫:0~0.5 min,95%B;0.5~7 min,95%~65%B;7~8 min,65%~40%B;8~9 min,40%B;9~9.1min,40%~95%B;9.1~12 min,95%B。流速:0.5mL/min;柱溫:25℃;樣品盤溫度:4℃;進樣體積:3μL。
1.5 數據處理
ThermoQExactive HFX 質譜儀能在控制軟件(Xcalibur,Thermo)控制下進行一級、二級質譜數據采集。經UPLC-QE-MS檢測,得到原始數據,利用ProteoWizard 軟件轉成mzXML格式后,使用自主編寫的R程序包(內核為XCMS)進行峰識別、峰提取、峰對齊和積分等處理,然后與BiotreeDB(V2.1)自建二級質譜數據庫匹配進行物質注釋,算法打分的Cutoff 值設為0.3。
1.6 統計學方法
使用SIMCA 軟件(V15.0.2)對原始數據進行對數轉換加中心化(CTR)格式化處理,然后進行主成分分析(PCA)和正交偏最小二乘法-判別分析(OPLS-DA)。以t檢驗P<0.05和VIP>1.5為條件,篩選潛在內源性差異代謝物。運用Metabo Analyst4.0(https://www.metaboanalyst.ca/)通路軟件,利用鑒定出的差異代謝物KEGG ID進行通路富集分析,以原始P<0.05為條件,篩選出富集顯著的代謝通路。采用SPSS24.0統計軟件進行分析,實驗數據以表示,符合正態分布及方差齊性者采用獨立樣本t檢驗,不符合則采用秩和檢驗。P<0.05表示差異有統計學意義。
2 結果
2.1 HE 染色結果
假手術組大鼠心肌細胞橫紋清晰,排列整齊,細胞核清晰,多呈橢圓形,細胞質染色均勻,未見血管擴張及炎細胞浸潤;CHD血瘀證模型組大鼠心肌細胞排列紊亂,心肌纖維化粗大,細胞核邊緣不清,可見血管擴張,淋巴細胞浸潤。見圖1。
2.2 尿液正負離子基峰譜圖
在正負離子模式下,尿液樣本經UPLC-QE-MS檢測后,繪制代表性尿液正負離子基峰譜圖,見圖2。
2.3 代謝輪廓分析
2組大OPLS-DA 代鼠尿液樣本在謝輪廓分析正負離子模,獲得相應式下,經P得分圖。PC CA 和A 得分圖見圖3,樣本在二維空間上表現出分離狀態,無重疊部分,反映2組大鼠尿液樣本代謝輪廓的改變。OPLS-DA 得分圖見圖4,樣本呈對稱分布,2組間分離明顯,表明2組樣本存在顯著差異,提示建模后大鼠機體正常生理代謝受影響。

圖1 2 組大鼠心肌組織形態(HE染色,×200)

圖2 2 組大鼠尿液樣本正負離子模式基峰譜圖
2.4 差異代謝產物篩選
以VIP>1.5、P<0.05為篩選條件,最終得到36種組間差異代謝物。與假手術組比較,CHD血瘀證模型組甘油、L-硒代蛋氨酸、尿嘧啶含量增加,N-乙酰基-L-天門冬氨酸、丙氨酰亮氨酸、D-丙氨酸、氨基葡萄糖6-磷酸、D-核糖5-磷酸、纈氨酸賴氨酸、丙氨酰谷氨酸、賴氨酰纈氨酸、草酰乙酸、丙酮酸、纈氨酸、D-木酮糖、脯氨酰脯氨酸、5’-磷酸吡哆醛、4-乙酰氨基丁酸、假尿苷、D-核糖、尿酸、海藻糖、1H-吲哚-3-甲醛、5-磷酸-α-D-核糖1-二磷酸、α-D-核糖1,2-環磷酸鹽5-磷酸鹽、脫氧腺苷、泛酸、N-乙酰丙酮酰谷氨酸、D-木糖醇、磷酸烯醇丙酮酸鹽、乳糖、L-硒代半胱氨酸、硒代胱氨酸、5-氨基咪唑-4-羧酰胺、D-葡糖醇-1,5-內酯6-磷酸鹽、磷酸甘油含量減少,代謝產物信息詳見表1。

圖3 2 組大鼠尿液液正負離子模式PCCA 得分圖

圖4 2 組大鼠尿尿液正負離子模式式OPLS-DA 得分圖圖
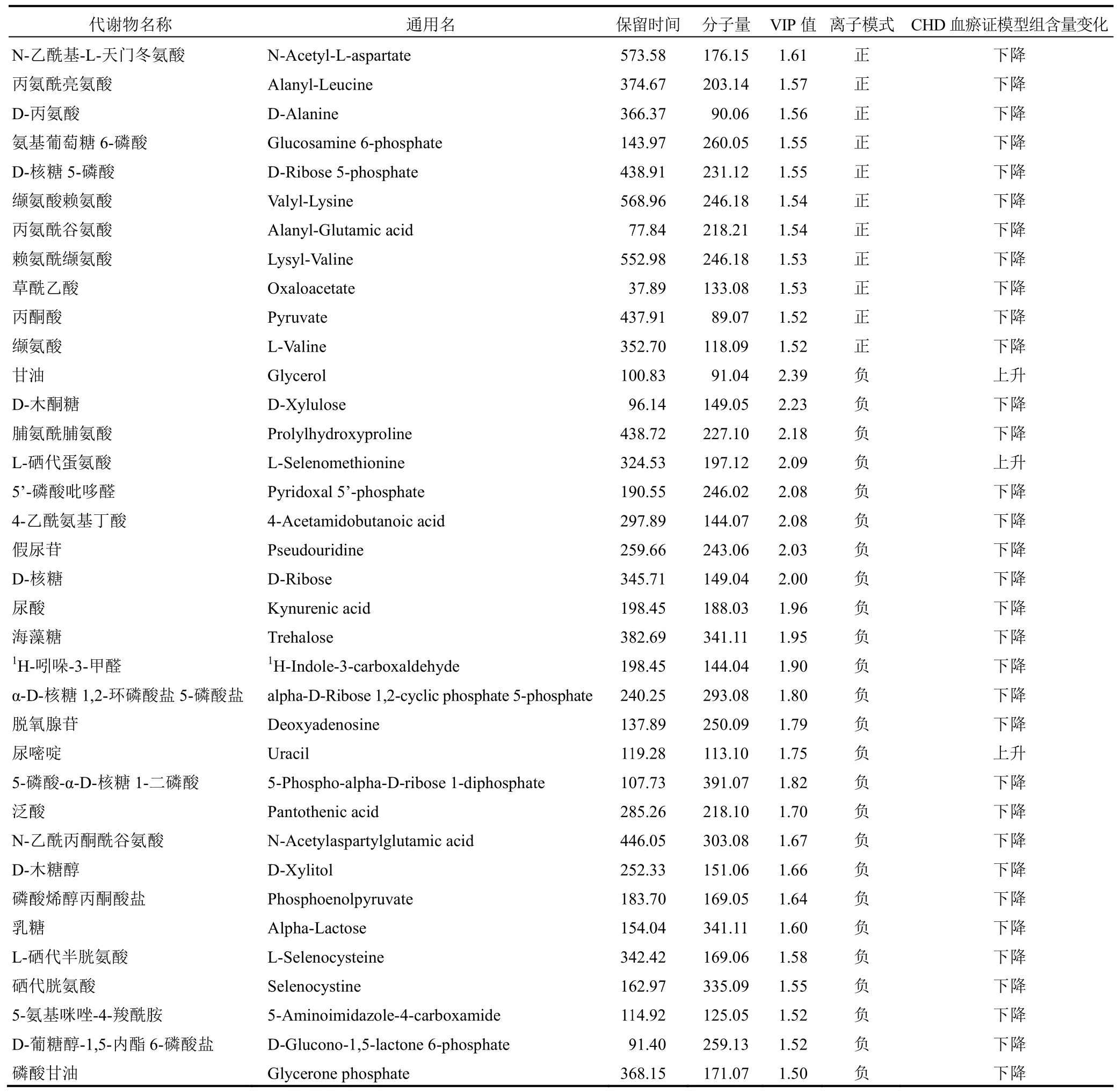
表1 2組組大鼠尿液差異代代謝物
2.5 顯著代謝通路分析
為進一步探討差異代謝物與CHD 血瘀證的關系,運用Metabo Analyst4.0通路軟件進行生物代謝通路富集及拓撲分析,代謝通路分析概要圖見圖5。以原始P<0.05為篩選條件,鑒定涉及9條顯著代謝通路:丙氨酸、天冬氨酸和谷氨酸代謝,磷酸戊糖途徑,糖酵解/糖異生,泛酸和輔酶A(CoA)生物合成,檸檬酸鹽循環(TCA 循環),丙酮酸代謝,嘌呤代謝,甘油脂代謝,戊糖和葡萄糖醛酸酯的相互轉化。差異代謝物代謝通路具體信息見表2。
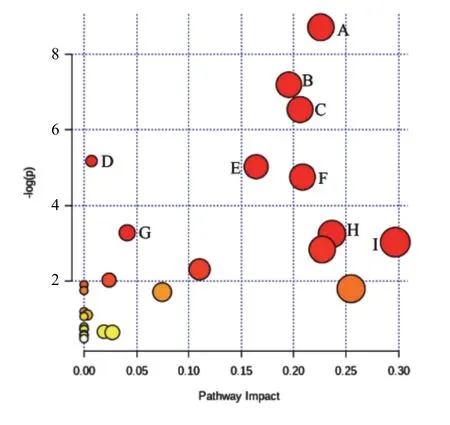
圖5 代謝通路分析概要圖

表2 顯著代謝通路具體信息
3 討論
代謝組學作為系統生物學研究的重要組成部分,直接反映疾病病理過程代謝化合物的共性和特征性指標,能在區分疾病模型上發揮獨特作用[10]。尿液樣本所含的信息豐富,采集樣本具有無創性、可重復性,因此,尿液在代謝組學研究中具優勢[11]。本研究結果顯示,與假手術組比較,CHD血瘀證模型組大鼠尿液中代謝產物含量紊亂,篩選出36個代謝標志物,涉及丙氨酸、天冬氨酸和谷氨酸代謝,磷酸戊糖途徑,糖酵解/糖異生,泛酸和CoA 生物合成,檸檬酸鹽循環(TCA 循環),丙酮酸代謝,嘌呤代謝,甘油脂代謝,戊糖和葡萄糖醛酸酯的相互轉化等顯著代謝通路。
其中3條糖代謝通路分別為磷酸戊糖途徑、戊糖和葡萄糖醛酸酯的相互轉化、糖酵解/糖異生。磷酸戊糖途徑通路包括D-核糖5-磷酸、D-核糖、D-葡糖醇-1,5-內酯6-磷酸鹽、5-磷酸-α-D-核糖1-二磷酸。磷酸戊糖途徑是機體糖代謝的重要途徑之一,是葡萄糖氧化分解的重要方式,以6-磷酸葡萄糖為起點,直接進行脫氫和脫羧反應,生成大量NADPH 和磷酸核糖,為體內多種代謝供氫體和碳源[12]。戊糖和葡萄糖醛酸酯的相互轉化通路包括D-木酮糖、D-木糖醇。葡萄糖醛酸形成木酮糖,可與磷酸戊糖途徑相連,研究表明戊糖和葡萄糖醛酸酯的相互轉化通路與軛合反應有關[13]。糖酵解/糖異生通路有丙酮酸、磷酸烯醇丙酮酸鹽、草酰乙酸、磷酸甘油參與。心臟缺氧時,ATP生成減少,糖酵解途徑通過加強底物磷酸化,糖酵解途徑通過加強底物磷酸化以生成ATP,從而補充心肌能量的不足[14]。糖異生通路是生物合成葡萄糖的重要途徑,以補充糖供應的不足。已有研究表明,心肌缺血狀態下,蛋白質功能產能不足,通過糖代謝分解產生能量以此供應心肌[15]。以上研究表明,CHD血瘀證病理過程中存在多條糖代謝紊亂,提示糖氧化供能障礙,機體處于磷酸戊糖途徑、戊糖和葡萄糖醛酸酯的相互轉化、糖酵解/糖異生等糖代謝途徑過度激活的應急代謝狀態。
丙氨酸、天冬氨酸和谷氨酸通路包括N-乙酰基-L-天門冬氨酸、N-乙酰丙酮酰谷氨酸、草酰乙酸、丙酮酸、氨基葡萄糖6-磷酸參與。丙氨酸、天冬氨酸和谷氨酸途徑經過氨基化的底物為丙酮酸、草酰乙酸、α-酮戊二酸。有研究表明,草酰乙酸是TCA 循環的起點,α-酮戊二酸是TCA 循環的重要中間產物,丙酮酸參與TCA 循環的回補反應,維持TCA 循環的進行[16]。因此,丙氨酸、天冬氨酸和谷氨酸通路異常將影響丙酮酸、草酰乙酸、α-酮戊二酸,最終影響TCA循環。本研究也發現丙酮酸代謝和TCA 循環通路的紊亂。冠狀動脈粥樣硬化引起心肌缺氧,使心肌能量發生代謝障礙,而TCA循環途徑異常則是能量代謝紊亂的標志[17]。心臟能量利用率低下,需氧量增加,因此出現心率加快、呼吸不暢、胸悶胸痛等表現。
泛酸、纈氨酸、尿嘧啶參與泛酸和CoA 生物合成途徑,其中泛酸、纈氨酸含量減少,尿嘧啶含量增加。泛酸是CoA 生物合成的重要前體物質之一,并參與生物體內氨基酸類、糖類、脂類、蛋白質類的能量代謝。研究表明,泛酸對脂質過氧化損傷的細胞和大鼠具有保護作用[18]。本實驗結果顯示,當CHD 血瘀證發生時,由于泛酸和纈氨酸含量降低,導致生物體內CoA 合成減少,引起相關代謝途徑紊亂。甘油、磷酸甘油參與甘油脂代謝,其脂代謝異常視為CHD發病的危險因素之一。脂代謝異常時,動脈內膜細胞功能發生改變、受損,脂質物質在血管內皮下沉積引起動脈粥樣硬化[19-20]。有研究表明,脂代謝異常引起血液黏度增高等血液流變學變化是CHD 血瘀證微觀辨證的重要指標[21],與本研究結果一致。
嘌呤代謝途徑有D-核糖5-磷酸、5-磷酸-α-D-核糖1-二磷酸、脫氧腺苷、5-氨基咪唑-4-羧酰胺參與。嘌呤代謝途徑經嘌呤堿基最終分解生成尿酸,是人體嘌呤代謝的終末產物。生成尿酸部位主要是血管壁,特別是血管內皮細胞,尿酸含量減少,在血管壁上沉積,損傷血管內膜,引起脂質過氧化反應和低密度脂蛋白膽固醇的氧化,導致冠狀動脈粥樣硬化加重[22]。
本研究利用代謝組學技術檢測分析,揭示了CHD血瘀證潛在的生物學基礎,病理機制涉及能量代謝失衡及氨基酸代謝、糖代謝、嘌呤代謝紊亂,脂質堆積等多個層面,提示CHD 血瘀證發病的復雜病理過程,為疾病早期預測和臨床診斷提供了依據。

