淺論β-內(nèi)酰胺類抗生素對肺結(jié)核的治療
桑嘉翌
(西安高新第三中學(xué) 陜西西安 710000)
肺結(jié)核由結(jié)核桿菌引起,通過活性肺結(jié)核患者打噴嚏,咳嗽等方式,散播在空氣中,然后經(jīng)呼吸道進(jìn)入健康人群的肺部[1],接著人體免疫系統(tǒng)的巨噬細(xì)胞很快將其捕獲,被捕獲的大部分結(jié)核桿菌都被巨噬細(xì)胞殺死,但是仍有少量結(jié)核桿菌可以在巨噬細(xì)胞里生存下來,如果人體免疫系統(tǒng)正常,結(jié)核桿菌將被層層免疫細(xì)胞包圍,形成一個(gè)肉芽腫的組織,以保護(hù)人體其他部位不被結(jié)核桿菌感染,此時(shí)患者不會(huì)顯示任何肺結(jié)核癥狀,同時(shí)不具有傳染性,稱為潛伏性肺結(jié)核[2]。據(jù)估計(jì)世界上有三分之一的人口患有潛伏性肺結(jié)核,其中85%到90%的潛伏性肺結(jié)核患者可以終生維持這種狀態(tài),但是當(dāng)其免疫系統(tǒng)不能正常運(yùn)轉(zhuǎn),比如癌癥患者,艾滋病患者及器官移植患者等,他們轉(zhuǎn)化為活性肺結(jié)核的幾率會(huì)大大提高[3]。活性肺結(jié)核就是我們常說的肺結(jié)核,臨床顯示咳嗽,消瘦,盜汗,咳血等癥狀,同時(shí)也具有傳染性。對肺結(jié)核的治療,目前通常使用國際健康組織(WHO)推薦的療法:異煙肼,利福平,吡嗪酰胺和乙胺丁醇一起使用兩個(gè)月,之后再使用異煙肼和利福平四個(gè)月。共計(jì)六個(gè)月時(shí)間[4]。聯(lián)合用藥的主要目的是為了避免耐藥菌的產(chǎn)生,盡管如此,當(dāng)前耐藥性肺結(jié)核的發(fā)展仍然十分迅速,對其的治療只能使用包括喹諾酮和氨基糖苷類在內(nèi)的二三線抗結(jié)核藥物,通常是八到十種不同藥物同時(shí)用藥達(dá)兩年之久。二三線抗結(jié)核藥往往毒性大,治療活性比一線藥物差,因此,耐藥性肺結(jié)核的治愈率低,所以研發(fā)新的抗結(jié)核藥迫在眉睫[5]。
β-內(nèi)酰胺類抗生素是目前使用最廣泛的抗生素[6],最早的β-內(nèi)酰胺類抗生素是青霉素,也是第一個(gè)發(fā)現(xiàn)的抗菌藥。β-內(nèi)酰胺類抗生素的作用機(jī)理為抑制青霉素結(jié)合蛋白(也稱為D,D-轉(zhuǎn)肽酶)的活性,從而抑制細(xì)菌細(xì)胞壁肽聚糖層的合成。其耐藥機(jī)理一般有兩種,第一種,也是最主要的一種,細(xì)菌通過分泌β-內(nèi)酰胺酶,水解青霉素的β-內(nèi)酰胺環(huán)使其失活。第二種,細(xì)菌可以改變青霉素結(jié)合蛋白的結(jié)構(gòu),使得β-內(nèi)酰胺類抗生素?zé)o法與靶標(biāo)結(jié)合,從而失去其抗菌活性[7]。為了解決β-內(nèi)酰胺類抗生素的耐藥性問題,藥物化學(xué)家不斷的對其結(jié)構(gòu)進(jìn)行改造,同時(shí)也改善了其抗菌譜窄,化學(xué)性質(zhì)不穩(wěn)定的特點(diǎn)。目前,根據(jù)結(jié)構(gòu)來分,除了青霉素外,還有頭孢菌素類(也可稱為先鋒霉素)、碳青霉烯類和單環(huán)內(nèi)酰胺類抗生素[8]。現(xiàn)在β-內(nèi)酰胺類抗生素作為廣譜抗菌藥,對革蘭氏陽性菌及革蘭氏陰性菌都有殺傷作用。結(jié)核桿菌屬于特殊的革蘭氏陽性菌,其細(xì)胞壁肽聚糖的合成也需要青霉素結(jié)合蛋白,也就是說正常情況下,青霉素可以抑制結(jié)核桿菌的青霉素結(jié)合蛋白的活性,從而殺死結(jié)核桿菌,但是現(xiàn)實(shí)情況卻是β-內(nèi)酰胺類抗生素很少用于肺結(jié)核的治療,本文在此對該現(xiàn)象進(jìn)行了深入分析。
一、β-內(nèi)酰胺類抗生素對肺結(jié)核無效的原因
(一)結(jié)核桿菌的細(xì)胞壁
跟普通的革蘭氏陽性菌和陰性菌細(xì)胞壁相比,結(jié)核桿菌的細(xì)胞壁干重占其總干重的40%,而大多數(shù)革蘭氏陽性菌和陰性菌的細(xì)胞壁干重占比則分別為5%和10%[9]。結(jié)核桿菌細(xì)胞壁的主要組成部分是稱之為霉菌酸的一類脂肪酸,為分支桿菌屬所特有,是至今發(fā)現(xiàn)碳鏈最長的天然脂肪酸,脂肪酸的親脂性取決于碳鏈的長度,因此可以推定結(jié)核桿菌擁有自然界脂溶性超強(qiáng)的細(xì)胞壁[10]。這樣的蠟狀細(xì)胞壁為結(jié)核桿菌形成了一層天然的保護(hù)屏,阻擋了大多數(shù)抗菌藥的入侵。
(二)結(jié)核桿菌的肉芽腫結(jié)構(gòu)
結(jié)核桿菌可以在肺部形成肉芽腫的結(jié)構(gòu)。肉芽腫結(jié)構(gòu)主要是以感染的免疫細(xì)胞為內(nèi)核,然后更多的免疫細(xì)胞將其包裹起來,從而保護(hù)人體的其他組織不被結(jié)核桿菌感染[11]。表面上看來這個(gè)肉芽腫組織主要是用于限制結(jié)核桿菌的復(fù)制與活動(dòng),從而保護(hù)人體。但是科學(xué)家逐漸發(fā)現(xiàn),這樣的肉芽腫組織同時(shí)也阻擋了抗結(jié)核藥物接觸到其內(nèi)部的結(jié)核桿菌,因此在某種程度上對結(jié)核桿菌也產(chǎn)生了保護(hù)作用[12]。
(三)結(jié)核桿菌的其他保護(hù)機(jī)制
結(jié)核桿菌有高度發(fā)達(dá)的外排泵系統(tǒng),主要功能是將有毒的物質(zhì)或代謝廢物排到細(xì)菌外面。當(dāng)細(xì)菌將抗生素排到細(xì)胞外面時(shí),抗生素就很難在細(xì)菌內(nèi)部積累,達(dá)到殺菌所需要的濃度。這樣一來,細(xì)菌沒有被殺死,反而衍生出耐藥性菌,因此結(jié)核桿菌的耐藥性與這個(gè)外排泵系統(tǒng)有關(guān)[13]。此外結(jié)核桿菌的復(fù)制周期長達(dá)20個(gè)小時(shí)左右,然而大多數(shù)細(xì)菌的復(fù)制周期,如大腸桿菌則在20秒之間。鑒于大多數(shù)抗菌藥的靶標(biāo)都是針對細(xì)菌的復(fù)制周期,因此繁衍慢的細(xì)菌天然就對大多數(shù)抗菌藥有抵抗作用。綜合以上幾點(diǎn)原因,當(dāng)醫(yī)生發(fā)現(xiàn)β-內(nèi)酰胺類抗生素對肺結(jié)核無效的時(shí)候并沒有感到非常意外。
(四)結(jié)核桿菌分泌的β-內(nèi)酰胺酶
科學(xué)家在研究耐藥性肺結(jié)核時(shí),發(fā)現(xiàn)同時(shí)使用β-內(nèi)酰胺類抗生素與克拉維酸對其有效。這樣之前關(guān)于β-內(nèi)酰胺類抗生素對肺結(jié)核無效原因的推論就不能成立[14]。后來通過研究發(fā)現(xiàn),該類抗生素對肺結(jié)核無效的真正原因是結(jié)核桿菌可以表達(dá)大量的β-內(nèi)酰胺酶,該酶可以水解青霉素類抗生素的β-內(nèi)酰胺環(huán)從而使其失活。而當(dāng)β-內(nèi)酰胺類抗生素與克拉維酸同時(shí)使用的時(shí)候,克拉維酸可以結(jié)合β-內(nèi)酰胺酶,與其形成不可逆的復(fù)合物,使β-內(nèi)酰胺酶失活[15]。從而減小該酶對于β-內(nèi)酰胺類抗生素的影響,因此β-內(nèi)酰胺類抗生素與克拉維酸合用時(shí)對肺結(jié)核就產(chǎn)生了治療效果。
二、β-內(nèi)酰胺類抗生素對持留結(jié)核桿菌的影響
(一)持留性結(jié)核桿菌
在治療結(jié)核病的過程中發(fā)現(xiàn),有一些結(jié)核桿菌始終不能被殺死,這類結(jié)核桿菌在人體內(nèi)可以調(diào)整其代謝狀態(tài),轉(zhuǎn)化為休眠或代謝慢的結(jié)核桿菌,我們稱之為持留結(jié)核桿菌[16]。持留結(jié)核桿菌是造成結(jié)核病復(fù)發(fā)率高,治療周期長的主因。而肺結(jié)核的長治療周期不僅給病人造成很大的藥物負(fù)擔(dān),同時(shí)也導(dǎo)致大多數(shù)病人不能完成肺結(jié)核的治療周期。治療周期的縮短為殘存在病人體內(nèi)的結(jié)核桿菌發(fā)生基因突變提供可能,從而進(jìn)一步導(dǎo)致耐藥性肺結(jié)核的產(chǎn)生。因此可以推斷持留性結(jié)核桿菌不僅是導(dǎo)致肺結(jié)核治療長周期的關(guān)鍵,也是造成耐藥性肺結(jié)核加劇的主要因素。當(dāng)前一線抗結(jié)核藥物中異煙肼,乙胺丁醇只對代謝正常的結(jié)核桿菌有效,而對持留菌無效[71],剩下的一線藥物中吡嗪酰胺被證實(shí)有抑制持留性結(jié)核桿菌的療效,利福平對代謝時(shí)快時(shí)慢的結(jié)核桿菌有殺傷作用[17]。事實(shí)上,在最初研究抗結(jié)核的治療方法時(shí),隨著利福平和吡嗪酰胺的加入,肺結(jié)核的治療周期有原先的1到2年縮短到6到8個(gè)月[18]。這就證明了對持留菌有效的藥物可以大幅度的縮小肺結(jié)核的長治療周期。但是隨著異煙肼及利福平耐藥菌的出現(xiàn),我們需要研發(fā)出新的抑制持留菌的藥物[19]。
(二)結(jié)核桿菌的L,D-轉(zhuǎn)肽酶
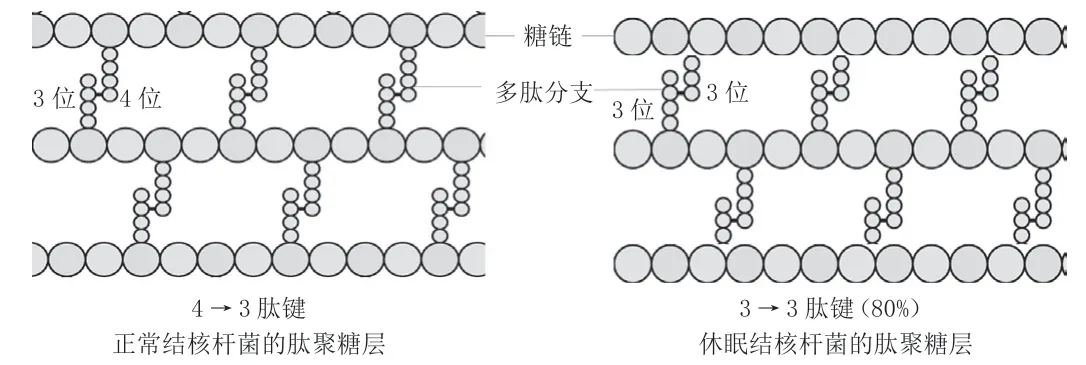
圖1 結(jié)核桿菌肽聚糖層的結(jié)構(gòu)
細(xì)菌細(xì)胞壁的肽聚糖層是由糖鏈和多肽分支組成,多肽鏈之間有肽鍵鏈接(圖1)。對于正常的細(xì)菌來說,該肽鍵為4→3位的氨基酸連接而成,由D,D-轉(zhuǎn)肽酶合成,也就是俗稱的青霉素結(jié)合蛋白,即β-內(nèi)酰胺類抗生素殺菌的作用靶標(biāo)。而持留性結(jié)核桿菌80%的肽鏈分支由3→3位的氨基酸連接,由L,D-轉(zhuǎn)肽酶合成[20]。研究發(fā)現(xiàn),碳青霉烯類的抗生素可與該酶結(jié)合為不可逆的復(fù)合物,從而抑制其活性。因此,該類抗生素可作為抗結(jié)核藥物研發(fā)的先導(dǎo)物,進(jìn)行深入的結(jié)構(gòu)優(yōu)化,也許可以發(fā)現(xiàn)新的對持留性結(jié)核桿菌有活性的藥物。
三、結(jié)束語
綜上所述,β-內(nèi)酰胺類抗生素與克拉維酸合用時(shí)對耐藥性肺結(jié)核有效,另外持留性結(jié)核桿菌是造成肺結(jié)核長治療周期和耐藥性加劇的主要因素,因此找到對持留菌有效的藥物至關(guān)重要。而研究發(fā)現(xiàn)碳青霉烯類抗生素有望成為研發(fā)抗持留結(jié)核菌的先導(dǎo)物。相信在不久的將來,該類抗生素會(huì)對肺結(jié)核的治療做出應(yīng)有的貢獻(xiàn)。

