種植體周角化組織增寬的臨床意義和研究進展
孫堅煒,雷利紅,陳莉麗
種植修復因其穩定和理想的療效已被廣泛應用于牙列缺損或牙列缺失患者中[1]。然而,在種植體修復過程中不僅要有良好的骨整合,還應關注種植體周軟組織的管理,尤其是角化組織。種植體周角化組織是指從游離齦邊緣到膜齦聯合之間的區域。多項研究顯示種植體周角化組織寬度<2 mm時將更容易引起菌斑積聚和種植體周軟組織炎癥。用于角化組織增寬的術式主要包括以下幾類:根向復位瓣術(apically repositioned flap,ARF)、自體組織移植和異體組織移植等。而部分學者持不同觀點,認為種植體周圍疾病的發生與角化組織無關[2-3]。本文就種植體周角化組織寬度的意義及各類角化組織增寬術的研究進展作一綜述,旨在為臨床治療方案選擇提供參考。
1 種植體周軟組織的解剖形態
種植體周黏膜和牙槽骨共同構成了種植體周圍組織。其中面向基臺方的種植體周黏膜包括三個部分:①冠部的種植體溝內上皮;②長約2 mm的結合上皮;③寬為1.5~2.0 mm的結締組織[4]。與天然牙不同,種植體周結締組織中的膠原纖維呈環形包繞種植體,無纖維插入種植體表面,外層較為疏松,僅含少量血管[5]。這種解剖學上的差異,導致它們對細菌感染的反應也不一致[6]。動物實驗發現,通過絲線結扎合并飲食控制誘導菌斑堆積后,種植體周軟組織損傷、牙槽骨吸收量、炎癥細胞浸潤程度均較天然牙更為嚴重[7]。在齦溝的口腔側,從牙齦邊緣到根方,依次為游離齦、附著齦、牙槽黏膜,其中游離齦和附著齦為角化組織,而位于膜齦聯合根方的牙槽黏膜上皮無角化。角化組織表面被一層厚的角化上皮所覆蓋,角化上皮由一層角蛋白和多層角化細胞組成,其下方富含膠原纖維,附著齦通過黏骨膜直接附著在骨面上,活動性小,可有效耐受食物的摩擦,對炎癥反應的抵抗能力更強[8]。種植體周圍擁有足夠寬度的角化組織,可以使種植體的軟硬組織穩定性更好,菌斑積累更少,種植體周圍黏膜炎的發生率更低[9]。
2 種植體周角化組織寬度的臨床意義
2.1 角化組織寬度對口腔衛生的影響
在種植修復后,良好的口腔衛生狀況將有利于種植體的長期穩定[10-11]。然而,種植體頸部的直徑一般比天然牙窄,頸部陡峭的倒凹亦使得植體周圍的衛生不易保持[6]。多項研究顯示,充足的種植體周角化組織寬度,有助于患者提高刷牙舒適度,利于菌斑的清除。Souza等[12]通過視覺模擬量表法發現,在種植體周角化組織寬度<2 mm的人群中,刷牙不適感為中、重度的人占30%,而該數值在角化組織寬度≥2 mm組中僅為2%,且前者的菌斑堆積更為嚴重。一項為期4年的前瞻性研究發現,窄角化組人群中有51.4%的患者反映刷牙時有不同程度的不適感,且改良菌斑指數(modified plaque index,mPI)較寬角化組織者的更高[13]。與該結果類似,Gobbato等[14]的Meta分析顯示較寬的角化組織能夠減少菌斑的積聚。缺乏角化組織的口腔黏膜,表面僅覆蓋一層菲薄的非角化上皮,下方的固有層缺乏膠原纖維而富含彈性纖維,這一解剖學特點可能與刷牙時的疼痛及不適感相關。刷牙不適感可能會降低刷牙效率,進一步影響種植體和天然牙周的衛生狀況。而另一項橫斷面研究的結果卻與此相悖,Ueno等[6]發現種植體周角化組織寬度<2 mm時,菌斑聚集更多,但并不會引起刷牙疼痛或增加刷牙難度。綜上,充足的角化組織可能有助于提高患者的刷牙舒適度,利于種植修復體的清潔,從而限制細菌的定植、聚集。但由于患者自身的疼痛閾值、刷牙力度或黏膜厚度等解剖因素都有可能影響刷牙舒適度,這一結論仍有待進一步探究。
2.2 角化組織寬度對植體周軟組織健康的影響
種植體周角化組織寬度不足可引起種植體周探診出血比例升高[12-13,15-16]、探診深度[17-18]及牙齦指數(gingival index,GI)的顯著增加[16,18]。Ueno等[6]甚至發現,當角化組織寬度<2 mm時,種植體周軟組織發生化膿的概率有所增加。Wennstrom等[19]對19篇種植體周角化組織相關文獻進行系統性綜述,有一半文獻表明角化組織寬度<2 mm的種植體,其探診出血指數顯著增加,而大多數文獻都無法證明角化組織寬度對探診深度有影響。
種植體周圍黏膜炎的定義為:①種植體周軟組織紅腫有探診出血;②沒有持續性的牙槽骨吸收[20]。Grischke等[21]將不定期牙周維護,存在種植體周圍炎和吸煙等引起種植體周圍黏膜炎的危險因素排除在外后,通過廣義估計方程模型分析發現,種植體周角化組織寬度不足與種植體周圍黏膜炎的發生顯著相關,其OR值為3.3,進一步敏感性分析顯示,角化組織的缺失還與疾病嚴重程度有關,OR值為1.7。然而,Lim等[3]通過Spearman相關系數分析發現,種植體周角化組織寬度和種植體周病相關參數之間的Spearman相關系數為-0.2<ρ<0.2,兩者之間沒有相關性。在一項回顧性研究中,Frisch等[2]將種植體周角化組織<1 mm的患者分為兩組,對照組僅進行種植體周支持治療,試驗組在種植體周支持治療的同時進行角化組織增量手術。在軟組織手術平均10.69年后,發現對照組的種植體周圍黏膜炎的發病率為31.91%,手術組為38.98%,無統計學差異。有效的種植體周支持治療似乎更利于種植體周軟組織健康的維持。
部分學者還研究了種植體周角化組織和軟組織退縮的關系。Warrer等[22]將30枚種植體植入到猴子的下頜無牙區中,并通過絲線結扎的方式誘導菌斑堆積,6個月后發現無角化組織的種植體有更多的軟組織退縮。該研究表明角化組織的缺失增加了種植體周圍區域對于菌斑所引起的組織破壞的敏感性。此外,Lin等[18]的Meta分析也發現種植體周角化組織的缺失可能會加速軟組織的退縮。2017年的世界牙周病學研討會已明確指出種植體周缺少角化組織是軟組織退縮的主要原因之一[4]。
目前的研究結果并不能說明種植體周角化組織的缺少與種植體周圍黏膜炎的發生有必然聯系,但角化組織的缺失似乎能增加種植體周軟組織疾病的易感性。系統全面的種植體周支持治療仍是種植修復過程中不可或缺的。
2.3 角化組織寬度對骨組織的影響
部分學者認為種植體周角化組織寬度與牙槽骨的高度密切相關,運用角化組織增寬術,可使種植體周的邊緣骨水平更加穩定。Perussolo等[13]根據種植體周角化組織寬度進行分組,記錄基線和4年后的邊緣骨水平,多層回歸分析顯示角化組織寬度不足可引起植體周邊緣骨水平降低。同樣的,Monje等[17]的橫斷面研究發現在種植體維護治療不當患者中,當角化組織寬度<2 mm時,牙槽骨吸收更多,種植體周圍炎的發生率更高,可達53.8%。Thoma等[23]的研究也支持了這一論證,發現通過軟組織增量術獲得足量的角化組織,可顯著減少牙槽骨的吸收。與此相反,Ladwein等[24]對967枚種植體進行了長達15年的研究,結果顯示種植體周角化組織的存在與否,并不會影響垂直骨向骨水平。綜上,關于種植體周角化組織是否與牙槽骨吸收有關的結論尚未明確,還需設計更加完善的臨床隨機對照實驗進行更深入的研究。
3 種植體周角化組織增寬的適應證和時機
盡管種植體周角化組織的必要性仍存在爭議,多數學者認為2 mm寬的角化組織帶將有利于口腔衛生及種植體周的軟硬組織健康,可為種植體的長期穩定提供保障。已有共識報告指出當種植體周角化組織缺如或角化組織寬度<2 mm時,可以進行角化組織增寬[25]。特別是在種植體周角化組織不足并同時伴有以下情況時:①口腔清潔過程及功能活動時有不適感;②骨再生過程中植體周黏膜不穩定;③持續的軟組織退縮;④菌斑控制效果不理想。需要注意的是,吸煙、糜爛型扁平苔蘚及類天皰瘡等情況可能影響自體結締組織移植物的存活,導致手術失敗[9]。
理論上,在種植修復治療過程的任何階段都可以進行種植體周角化組織增寬,包括:種植體植入前、種植體植入同期、種植體第二階段手術同期或種植體負載后[9, 26]。與種植體負載后相比,前三種方案的結果更具預測性[27]。當需要在負載后進行角化組織增寬時,往往已經出現美學問題、種植體周圍黏膜炎或種植體周圍炎等情況。一般而言,在種植術前進行角化組織增寬將具有更好的預測性,并在一定程度上降低后期種植手術的難度,如在進行大量骨增量前,可以使用軟組織增量手術來降低軟組織開裂的風險;在美學區,軟組織增量術的合適時機為基臺連接前的4~6周[28]。
4 種植體周角化組織增寬的方法
目前的角化組織增寬技術主要包括以下幾類:①根向復位瓣(apically repositioned flap,ARF);②自體組織移植,如游離齦移植術(free gingiva graft,FGG)、結締組織移植術(connective tissue graft,CTG)、自體血小板濃縮物(autologous platelet concentrates, APCs)移植等;③異體組織移植,如脫細胞真皮基質(acellular matrix derivative, ADM)、異種膠原基質(xenogenic collagen matrix,XCM)等;④口腔黏膜組織工程。
4.1 根向復位瓣術
傳統ARF需要將半厚瓣向根方推移,縫合固定于骨膜,使暴露的骨膜面自行愈合形成新的角化組織。1999年,Carnio[29]在原術式的基礎上進行改進,提出了改良根向復位瓣術(modified apically repositioned flap,MARF),與傳統的ARF不同,該術式水平切口冠方的角化組織未與牙齒分離,避免了傳統術式帶來的軟組織退縮問題(圖1)。暴露的骨膜面完全被角化組織所包繞,從而利于上皮細胞從創緣向內爬行,最終形成角化組織[30]。Carnio等[31]分別采用FGG和MARF治療附著齦≤1 mm的位點,術后1年對比發現兩種方法均有效增加了角化組織寬度,而FGG較MARF平均多產生1.52 mm角化組織。MARF不需要開辟第二術區,相較FGG的手術時間短、難度低,術后不適感更輕,且局部組織顏色具有更好的預測性。一項平均隨訪9年的研究顯示MARF能可預期地增加角化組織寬度,且具有長期穩定性[32]。隨后,Carnio等[33]進一步對21個無角化組織的位點進行MARF,作者在距齦緣根方2 mm左右處做一水平內斜切口,在對各個病例追蹤1~11年(平均3.2年)后發現角化組織寬度平均增加(3.6±0.8)mm,因此認為MARF甚至可以在無角化組織區域產生角化組織。由于MARF不影響美學表現,在前牙美學區,或許MARF是一個更好的選擇。但MARF所增加的角化組織量較FGG更少,且無法用于需要根面覆蓋和存在骨開裂的患者,在臨床應用時仍須把控適應證[31]。

圖1 改良根向復位瓣術Fig.1 Modified apically repositioned flap
4.2 自體組織移植
4.2.1 游離齦移植術 游離齦移植術需要根據受植區的形狀和大小在腭部切取厚度適宜覆蓋上皮的結締組織,將其縫合于受植區的骨膜上(圖2)。FGG能增加的角化組織寬度大,術后收縮率小,被視為角化組織增寬的金標準[9]。但FGG需要開辟第二術區,存在手術難度大、手術時間長、術后反應大和移植物的量有限等缺陷。且由于固有層結締組織對其被覆上皮的結構特異性起決定性作用[34],新形成角化組織的顏色、紋理較周圍不同,不利于美觀[35]。為了克服FGG在美學上的缺陷,Cortellini等[36]將釉牙骨質界到理想膜齦聯合線處的移植物表面的上皮保留,去除根方的上皮后將其縫合于半厚瓣和骨膜之間,稱之為部分上皮化游離齦移植。該方法產生的膜齦聯合線與周圍組織平齊,能在一定程度上提高術后美學效果。另有研究報告,在FGG術中使用氰基丙烯酸鹽粘合劑不僅可以減少移植物的收縮率還可有效減輕術區疼痛感[37]。需要注意的是當存在以下情況時,FGG的預后往往不佳:①受區制備不當;②移植物大小及厚度不足;③移植物對受區的適應性差;④移植物固位不佳[38-40]。
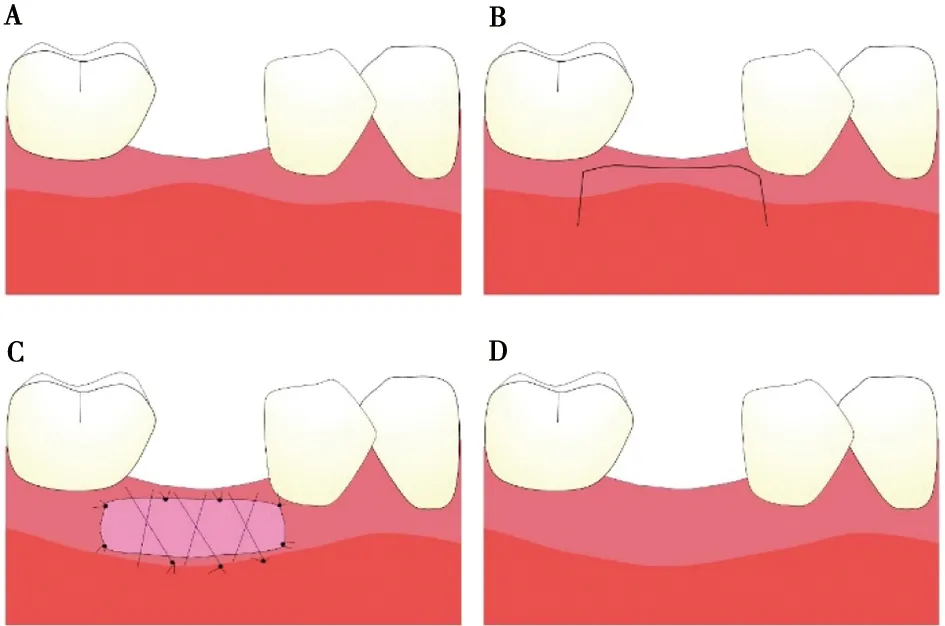
A:術前;B:手術切口;C:移植物固定縫合;D:愈后
4.2.2 結締組織移植術 上皮下結締組織移植物一般通過活門法、L法和信封法獲取,與游離齦移植物不同,上皮下結締組織移植物表面不帶有上皮結構。臨床上,CTG常與ARF和冠向復位瓣術(coronally advanced flap,CAF)聯合使用(圖3)。Tunkel等[41]在種植第二階段分別進行ARF和ARF+CTG,隨訪1年后發現ARF組的角化組織寬度平均增加4.63 mm,而ARF+CTG組平均增加4.10 mm,組間無統計學差異,但ARF+CTG較ARF能增加更多種植體頰側軟組織厚度。Cairo和Zucchelli等[42-43]則發現使用CTG+CAF能增加種植體頰側角化組織寬度。而Thoma等[44]的系統性綜述發現,對于種植體周角化組織增量病例,FGG依然是最佳選擇,CTG更適合用于種植體周軟組織增厚。

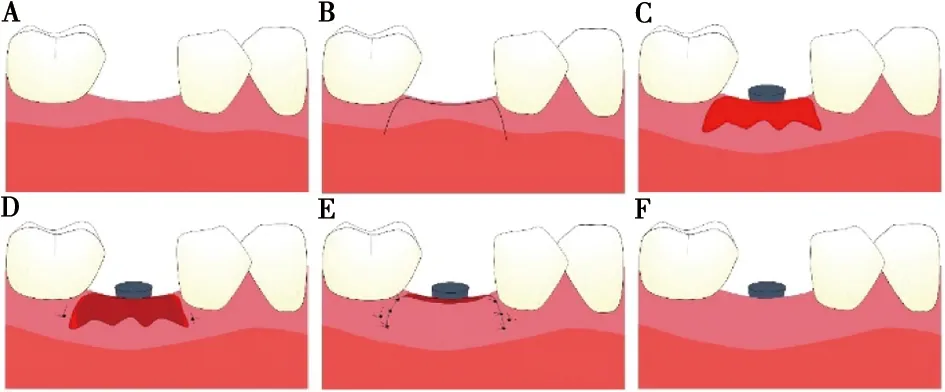
A:術前;B:手術切口;C:形成受植區;D:CTG放置并固定;E:縫合固定;F:愈后
4.2.4 自體血小板濃縮物 自體血小板濃縮物由靜脈血離心后制得,與FGG相比更容易獲得。目前為止,已經開發出三代APCs包括:富血小板血漿(platelet rich plasma,PRP)、富血小板纖維蛋白(platelet rich fibrin,PRF)、濃縮生長因子(concentrated growth factor,CGF)[46]。APCs中富含多種生長因子,如轉化生長因子-β1(transforming growth factor-β1,TGF-β1)、血管內皮細胞生長因子(vascular endothelial growth factor,VEGF)、胰島素樣生長因子(insulin-like growth factor-Ⅰ,IGF-Ⅰ)等[47],可以促進細胞的增殖、分化、趨化,利于創口愈合、組織再生。在一項半口隨機對照臨床實驗中,Temmerman等[48]分別使用FGG和富白細胞血小板纖維蛋白(leukocyte-and platelet-rich fibrin,L-PRF)對種植體周進行角化組織增寬。結果顯示兩組種植體頰側角化組織寬度均顯著增加,FGG組較L-PRF組平均多增加(1.3±0.9)mm。而使用L-PRF組,手術時間更短,患者的術后疼痛更少。Luo等[49]評估了PACs聯合CAF治療牙齦退縮的作用,Meta分析顯示使用APCs后,不僅能改善軟組織退縮和角化組織寬度等指標,還能加快術后軟組織的愈合。與此相反,Fabbro等[50]卻認為APCs在增加角化組織寬度方面的作用十分有限。不同學者在APCs對于增加角化組織寬度方面的作用持有不同觀點。且當前的研究多聚焦于APCs在根面覆蓋中的作用,關于APCs在增加種植體周角化組織方面的研究仍然較少。
4.3 異體組織移植
4.3.1 脫細胞真皮基質 為解決自體移植物需要開辟第二術區、美學效果不佳等問題,ADM等異體材料被開發用于牙周軟組織手術。ADM通過去除皮膚中的表皮和細胞制備而成,其主體結構為完整的基底膜復合物和主要成分為膠原束、彈性纖維的細胞外基質[51]。ADM最早在整形外科中,用于皮膚全層燒傷的治療。在過去的20多年里,ADM已廣泛應用于各種膜齦手術中,并取得了不錯的療效[52]。Park等[51]采用ARF聯合ADM治療種植體周角化組織不足,在隨訪6個月過程中,角化組織平均寬度從(0.8±0.6)mm增加到了(2.2±0.6)mm,mPI逐漸下降,但ADM的組織收縮率較高可達(50.7±9.2)%。在一項隨機對照研究中,Basegmez等[53]分別采用ADM和FGG用于種植體周角化組織寬度不足的治療,術后6個月對比發現ADM和FGG均能有效地增加角化組織,FGG平均增加2.57 mm,而ADM僅為1.58 mm。進一步對種植體周評估發現,ADM組的mPI和GI值均較FGG高。與FGG相比,ADM不需要制造額外切口,且術后美學效果更佳,可作為自體移植材料的替代品。但其較高的組織收縮率也不可忽視。
4.3.2 異種膠原基質 豬來源的膠原基質由Ⅰ型膠原和Ⅲ型膠原構成[54],它具有兩個功能面:上面較為致密利于細胞爬附;組織面疏松多孔,利于血凝塊的形成、細胞生長和組織整合[55]。XCM的三維支架結構,有助于成纖維細胞、血管及上皮細胞長入,最終形成新的角化組織[56-57]。XCM常用于根面覆蓋、天然牙或種植體周圍的角化組織增寬等。2009年,Sanz等[57]首次使用ARF+XCM增加種植體周角化組織寬度,隨訪6個月后ARF+XCM組和ARF+CTG組的角化組織寬度均顯著增加,兩組之間沒有統計學差異。與ARF+CTG相比,ARF+XCM能明顯縮短手術時間短,減輕患者術后疼痛。Schmitt等[58]對比使用前庭成形術+FGG和前庭成形術+XCM治療種植體周角化組織不足,評價其長期療效,結果顯示術后各組間角化組織寬度相當,無統計學差異,隨訪5年后發現前庭成形術+XCM組的角化組織喪失量可達52.89%,而前庭成形術+FGG組為40.65%,XCM的術后收縮率較FGG更大。在整個隨訪期內,前庭成形術+XCM組中的新生角化組織外觀與周圍一致。綜上,盡管XCM具有較高的組織收縮率,但其來源豐富、生物相容性佳,是目前較為理想的自體移植物替代體。
4.4 口腔黏膜組織工程
Izumi等[59]將自體口腔黏膜角化細胞接種于ADM支架表面,從而在體外形成全層口腔黏膜,并將其命名為體外口腔黏膜類似物(exvivoproduced oral mucosa equivalent,EVPOME)。組織學觀察顯示,通過該方法形成的全層口腔黏膜的上皮厚度較薄,但其仍具有與天然角化黏膜相似的結構[60]。與單純的ADM移植相比,EVPOME移植能加快組織愈合速度,減少軟組織收縮[59]。目前,EVPOME已在口腔頜面外科中用于軟組織缺損的修復,關于其在種植體周角化組織增寬方面的研究仍未見報道。
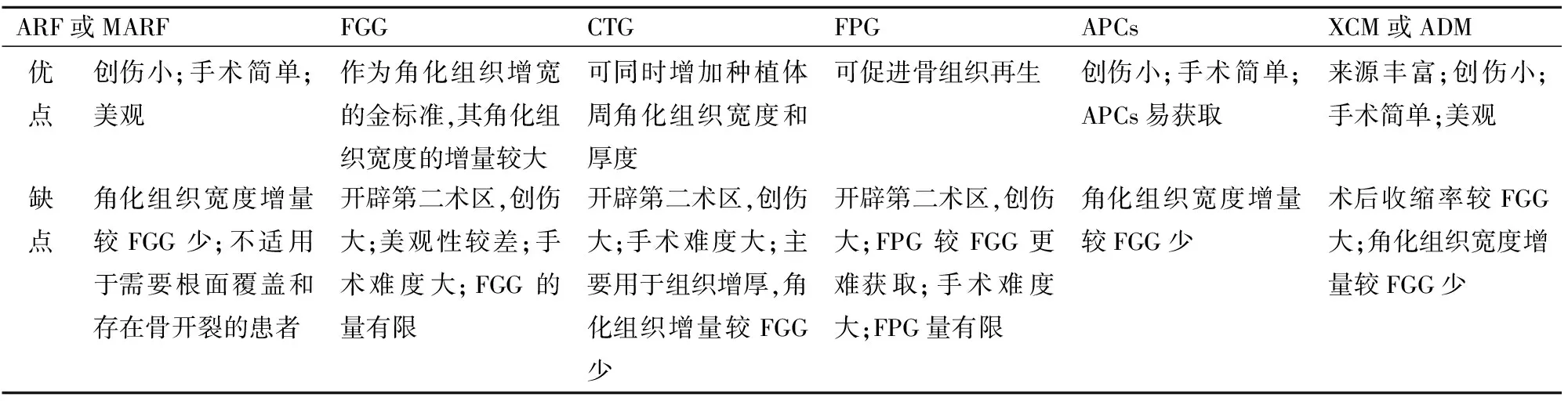
表1 不同術式的優缺點Tab.1 Advantages and disadvantages of different surgical methods
5 總結和展望
盡管種植體周角化組織寬度對于種植體的影響仍存在爭議,多數學者認為種植體周角化組織寬度不足,將引起刷牙不適,種植體周菌斑堆積,對軟硬組織造成不同程度的影響。因此,當種植體周角化組織寬度不足2 mm時,仍然建議使用角化組織增寬術。通過ARF聯合FGG治療種植體周角化組織不足,依然是目前角化組織增寬的金標準。隨著自體組織移植物替代體的不斷創新,ADM、XCM等材料相繼出現,可以有效提高術區的美觀程度,減少術后疼痛,降低操作敏感性及手術費用。然而,現有證據提示異體異種組織替代材料組織收縮率較大,其長期穩定性仍有待討論、研究。未來,對于新型自體移植物替代物的研發依然是該領域的主要方向。

