過硫酸鉀氧化4-氨基安替比林分光光度法測定地表水中揮發酚
葉開曉 童天喆 梁柳玲 洪 欣
(廣西壯族自治區生態環境監測中心,南寧 530028)
前言
酚在苯環或稠環上連接一個羥基則為一元酚,連接多個羥基則為多元酚,通常認為能與水蒸氣一起蒸出、沸點在230 ℃以下的一元酚為揮發酚[1]。揮發酚屬高毒物質,人體長期攝入被酚污染的水及水產品,可引起頭昏、瘙癢、出疹、貧血及各種神經系統癥狀。水中含高濃度酚類時,可造成魚類中毒死亡,用于灌溉農田,會使農作物枯死或減產[2]。
揮發酚是地表水環境質量標準的常規監測指標之一。揮發酚的測定方法很多,常用的主要有分光光度法[3]、流動注射分光光度法[4-5]、色譜法及色譜-質譜聯用法(GC、GC-MS、HPLC、HPLC-MS)[6-7]等。測定地表水揮發酚時,使用較為普遍的是4-氨基安替比林(4-AAP)分光光度法[8]。該方法的優點在于操作簡單、成本低、對操作人員要求不高、經蒸餾后的水體干擾少、適用范圍廣,但缺點是顯色劑4-氨基安替比林易氧化生成4-氨基安替比林紅,從而使試劑空白吸光度值明顯增高,嚴重影響方法檢出限和分析結果的準確度。解決辦法是對4-氨基安替比林進行提純,還有文獻提出更換氧化劑進行方法改進。有的采用硅鎂型吸附劑提純[8-9]、氯仿提純[10-12]、乙醇提純[3,9,11,13]等,有文獻以高碘酸鉀、碘、過硫酸銨[3,14-15]等代替鐵氰化鉀作為氧化劑測定揮發酚。標準方法[8]采用硅鎂型吸附劑提取,由于吸附劑是無選擇性吸附,在吸附雜質的同時也吸附4-AAP,導致溶液中4-AAP 實際濃度減少且難以確定減少量,氯仿萃取法受到的影響也與硅鎂型吸附劑類似。乙醇提取法可得到純度較高的固體試劑,但4-AAP 在乙醇中的溶解度大,導致4-AAP試劑損失也大。本研究利用4-AAP不溶于正己烷的特性,采用毒性較小的乙醇和正己烷(1+4)混合溶液提純固體4-AAP,可獲得純度高的固體4-AAP且損失比使用乙醇提純小,用無毒的過硫酸鉀代替有毒的鐵氰化鉀作氧化劑,有效降低了試劑空白的吸光度,取得了滿意的結果。
1 材料與方法
1.1 主要儀器與試劑
DR6000紫外可見光分光光度計(美國哈希公司);STEHDB-106-3 智能一體化蒸餾儀(濟南盛泰電子科技有限公司);Milli-Q Integral 10超純水儀(美國密理博);全玻璃抽濾裝置;氮吹儀(Turbo VAP Ⅱ)。
4-氨基安替比林(AR);鐵氰化鉀(AR);過硫酸鉀(Sigma);硫酸銅(AR);氨水(AR,0.90 g/mL);氯化銨(AR);無水乙醇(AR);正己烷(AR);三氯甲烷(AR);苯酚標準溶液(環境保護部標準樣品研究所,500 mg/L);揮發酚標準樣品(環境保護部標準樣品研究所)。
1.2 方法
1.2.1 試劑提純
將25 g 4-AAP置于全玻璃抽濾裝置中,分3~4次加入100 mL無水乙醇和正己烷(1+4)混合溶液進行洗滌,洗滌時用玻璃棒充分攪拌后抽濾,直至洗滌液呈無色或淡黃色,將洗至無色或淡黃色的4-AAP 用氮氣吹干1 h,待乙醇和正己烷揮發完全后,裝瓶,在干燥器內密封避光保存。使用時稱2.0 g 4-AAP 溶于純水中,并稀釋至100 mL,配制成20 g/L的4-AAP溶液。
1.2.2 樣品處理
取250 mL 水樣,置于500 mL全玻蒸餾瓶中,加25 mL 純水,及數滴甲基橙指示劑,用磷酸溶液(1+9)調至水樣由桔黃色變為橙色,加入數粒玻璃珠,加熱蒸餾,收集餾出液250 mL。
1.2.3 樣品測定
將水樣餾出液全部轉入250 mL分液漏斗中。另取8個分液漏斗,分別加入100 mL 純水,再加入0、0.20、0.50、1.00、3.00、5.00、7.00、10.00 mL苯酚標準使用溶液(1.00 μg/mL),補加純水至250 mL。向各分液漏斗內加入2.0 mL NH3-NH4Cl緩沖溶液(pH=10.7),混勻,加1.50 mL經提純的4-AAP溶液(20 g/L),混勻,再加入1.50 mL 過硫酸鉀溶液(20 g/L),充分混勻,密塞,放置10 min。向各分液漏斗中準確加入10.0 mL三氯甲烷,密塞,劇烈振搖2 min,倒置放氣,靜置分層。在分液漏斗頸管內塞一小團干脫脂棉,棄去最初濾出的數滴萃取液后,將三氯甲烷層通過干脫脂棉團直接放入光程30 mm 比色皿中,于460 nm 波長,以三氯甲烷為參比,測定吸光度值。
2 結果與討論
2.1 4-氨基安替比林提純條件優化
對未經提純的4-AAP和分別經50、100 mL無水乙醇+正己烷(1+4)洗滌提純的4-AAP進行空白樣品測定,由表1可以看出,經100 mL無水乙醇+正己烷(1+4)洗滌提純后的4-AAP的空白吸光度明顯降低且波動較小,RSD為4.1%,滿足實驗室空白要求(采測分離技術要求空白吸光度<0.080)[16]。
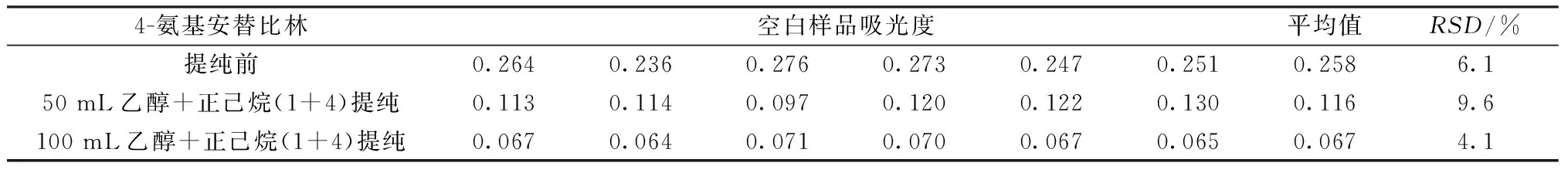
表1 4-氨基安替比林提純條件優化測定Table 1 Optimization of purification conditions for 4-AAP(n=6)
2.2 過硫酸鉀用量選擇
分別移取250 mL空白和苯酚(20.0 μg/L)水樣各6份,按樣品測定方法加入2 mL NH3-NH4Cl緩沖溶液(pH=10.7)和1.5 mL經提純的4-AAP溶液(20 g/L)后,分別加入濃度為20 g/L的過硫酸鉀溶液0.5~3.0 mL,搖勻,放置10 min 后,用10.0 mL三氯甲烷萃取后采用分光光度法測定。實驗結果表明,空白樣品和含苯酚水樣的吸光度值隨過硫酸鉀用量增加有所增大。在過硫酸鉀加入量2.0 mL時,空白吸光度接近0.080,用量大于2.0 mL后,空白吸光度大于0.080。含苯酚水樣的吸光度在過硫酸鉀加入量1.5 mL和2.0 mL時增幅不大,表明當加入1.5 mL過硫酸鉀溶液(20 g/L)時,水樣中酚已被完全氧化。所以,選擇1.5 mL過硫酸鉀溶液(20 g/L)為氧化劑的最佳加入量(圖1)。
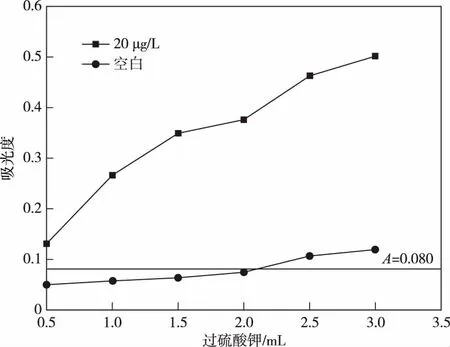
圖1 過硫酸鉀加入量對吸光度的影響Figure 1 Effect of potassium persulfate addition on absorbance.
2.3 顯色反應時間優化
在標準方法[8]中,以鐵氰化鉀作氧化劑,應在顯色后30 min內測定吸光度。當苯酚質量濃度為20.0 μg/L、加入2.0 mL NH3-NH4Cl緩沖溶液、1.5 mL 4-AAP 溶液、1.5 mL過硫酸鉀時,顯色反應時間對溶液吸光度的影響及萃取液穩定時間對吸光度的影響分別見圖2和圖3。由圖2、3可見,采用過硫酸鉀作氧化劑,顯色反應時間在10~90 min時,吸光度變化率小于5%;萃取后的萃取液在10~120 min時,吸光度變化率小于5%,表明顯色穩定性高,且顯色速率快。
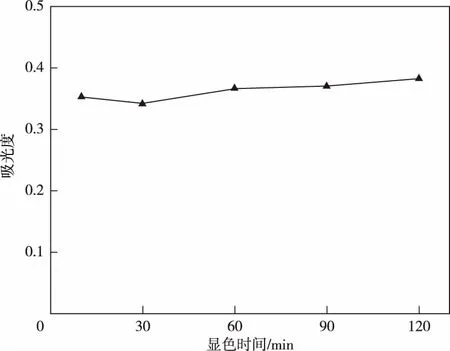
圖2 顯色反應時間對吸光度的影響Figure 2 Effect of reaction time on absorbance.
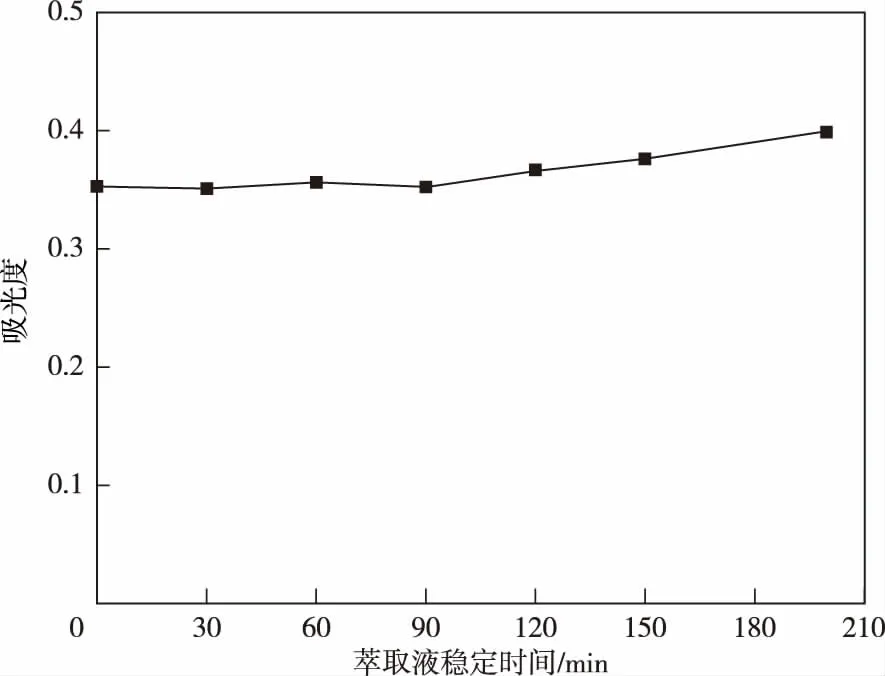
圖3 萃取液穩定時間對吸光度的影響Figure 3 Effect of extraction time on absorbance.
2.4 過硫酸鉀溶液的穩定性測定
將配制好的20 g/L的過硫酸鉀溶液置于4 ℃保存,分別在當天、7、15、30、45、60 d按測定方法測定空白樣品及苯酚濃度為20.0 μg/L的水樣,吸光度值分別為0.066、0.067、0.070、0.067、0.071、0.073和0.353、0.351、0.358、0.348、0.356、0.360,相對標準偏差分別為4.0%和1.3%。結果表明,過硫酸鉀溶液在兩個月內穩定性較好,避免了鐵氰化鉀溶液由于穩定性差,無法長期保存的問題。
2.5 標準曲線和檢出限
分別用鐵氰化鉀和過硫酸鉀作為氧化劑,按測定方法測定0~10 μg的苯酚標準系列溶液,繪制標準曲線,求得回歸方程分別為y=0.058 7x+0.008 6、y=0.054 6x+0.002 9,相關系數(r)分別為0.999 2、0.999 6,線性關系良好(見表2)。
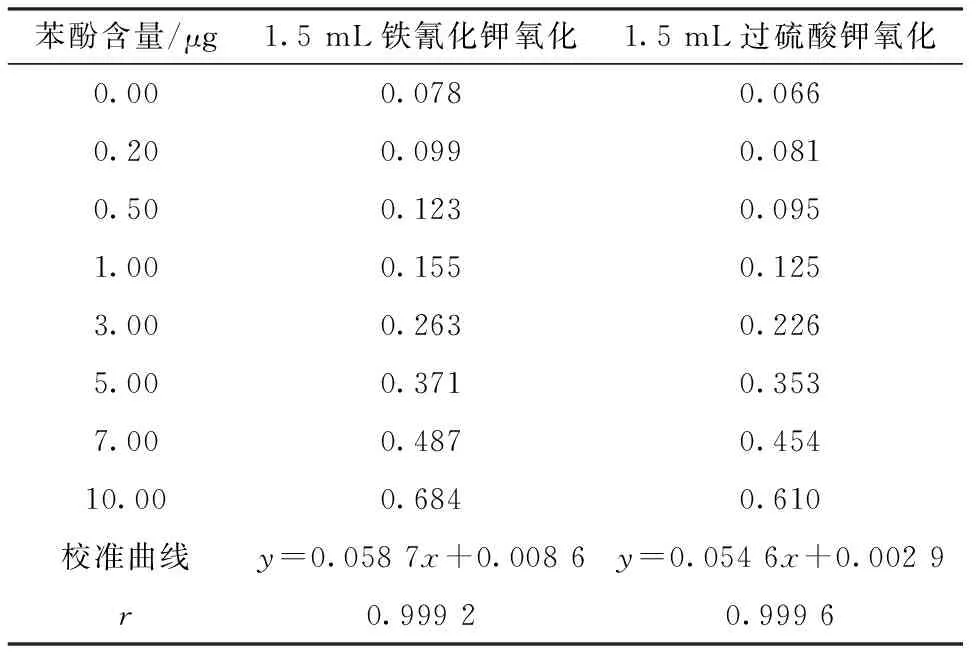
表2 揮發酚標準溶液的測定Table 2 Determination of volatile phenol standard solution
檢出限測試按照《環境監測 分析方法標準制修訂技術導則》(HJ 168—2010)附錄A.1.1 方法檢出限的一般確定方法進行。測定結果表明,方法的檢出限為0.3 μg/L,測定下限為1.0 μg/L,滿足HJ503—2009的要求(表3)。
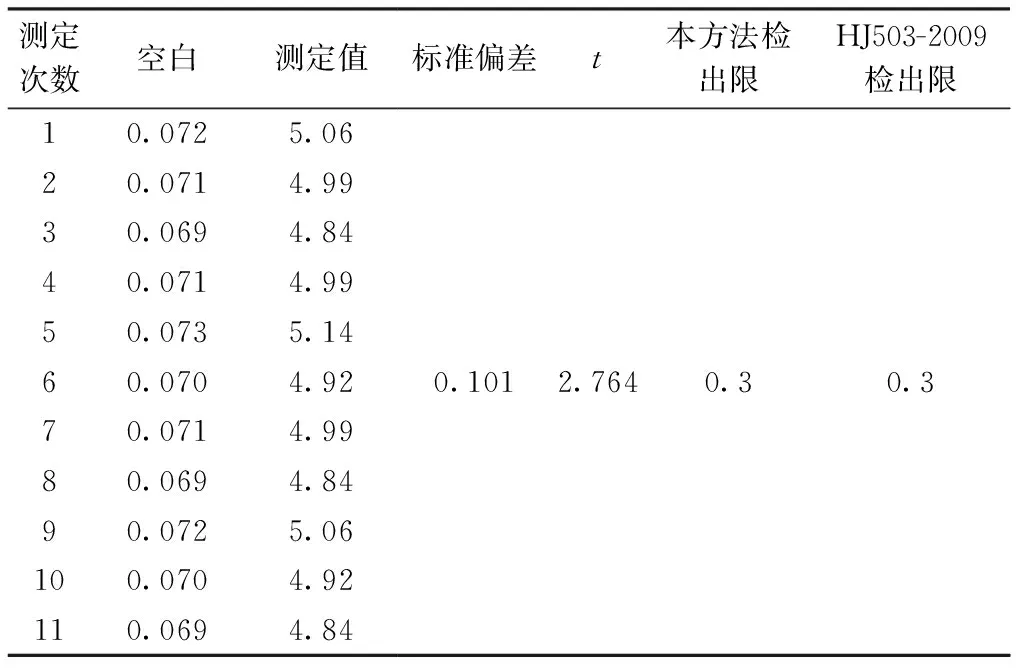
表3 檢出限測定Table 3 Determination of MDL(n=11) /(μg·L-1)
2.6 準確度測定
為了驗證方法的準確度,采用國家環保部標準品研究所的標準樣品進行驗證,結果表明,方法準確度在誤差允許范圍內(見表4)。

表4 標準樣品測定Table 4 Determination of standard samples(n=3)
在實際水樣中分別加入適量苯酚標準溶液,進行加標回收實驗,加標回收率見表5。由表5可見:鐵氰化鉀氧化方法所得平均回收率為94.2%,本方法平均加標回收率為96.0%,兩種方法所得的結果基本一致。
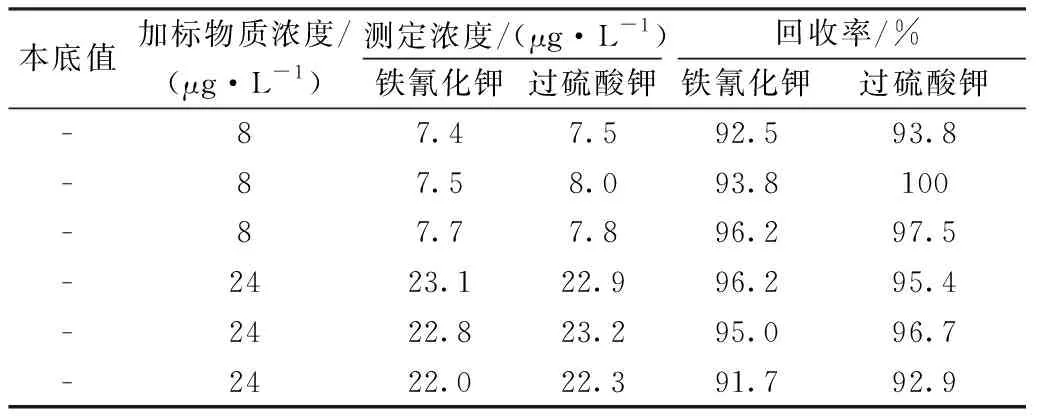
表5 加標回收率Table 5 The recoveries of volatile phenol(n=3)
3 結論
使用毒性小、中等極性、易揮發的乙醇和正己烷(1+4)混合溶液提純4-氨基安替比林,對操作人員損害較小、4-氨基安替比林損失小、易操作,可獲得高純度的4-氨基安替比林固體試劑。使用穩定、無色、無毒的過硫酸鉀溶液代替穩定性差、有毒的鐵氰化鉀溶液作氧化劑,有效降低了空白值,顯色穩定時間長,方法的檢出限、靈敏度和準確度均滿足標準分析方法的要求,適合地表水中揮發酚的測定。

