C反應(yīng)蛋白在預(yù)測食管癌患者放射性肺損傷中的作用
李敬霞,穆雙鋒,穆立祥,王曉宏
放射治療在食管惡性腫瘤的治療中得到了廣泛的應(yīng)用。超過70%的食管惡性腫瘤患者在治療過程中需接受放射治療[1],但在食管腫瘤的放射治療中,放射性肺損傷是常見的并發(fā)癥。放射性肺損傷的發(fā)生限制了靶區(qū)劑量的提高,并且使腫瘤局部控制率下降,同時嚴(yán)重影響了患者的生活質(zhì)量和生存期。目前放射性肺損傷的診斷主要依靠臨床及影像學(xué)表現(xiàn)來診斷,尚無理想的治療手段。基于以上原因,本研究從患者生物學(xué)因素、一般因素、物理學(xué)因素的角度對放療所致肺損傷機制進行了初步研究,希望早期預(yù)測放射性肺損傷發(fā)生,從而醫(yī)生可根據(jù)每個患者可能發(fā)生肺損傷風(fēng)險的大小來確定個性化治療方案。盡量在不增加放療并發(fā)癥的前提下調(diào)整治療計劃,既能達(dá)到治療腫瘤的最大增益,又可以提高患者的生活質(zhì)量。
曾有學(xué)者研究胸部放射治療中與放射性肺損傷相關(guān)的一些炎性細(xì)胞因子及相關(guān)劑量學(xué)參數(shù)[2-4]。但近年來,國內(nèi)外對放射性肺損傷新診斷策略的研究較少,也鮮有報道探討血清CRP水平與食管癌放射性肺損傷發(fā)生的關(guān)系。因此,本研究觀察了66例行三維適形放療的食管鱗癌患者,旨在觀察放射性肺損傷的預(yù)測因素,現(xiàn)報道如下。
1 材料和方法
1.1 樣本來源收集河南科技大學(xué)第一附屬醫(yī)院放療中心2013年11月至2014年12月接受三維適形放射治療(3DCRT)的原發(fā)食管癌患者66例。放療前完成常規(guī)采集病史、內(nèi)窺鏡、活檢、體格檢查、胸部CT、肺功能、血常規(guī)、生化全項檢測、血凝全項檢查、心電圖、彩超等檢查,根據(jù)患者主訴及查體可行骨掃描或其他檢查,并詳細(xì)記錄呼吸道癥狀及體征,定期行胸部CT復(fù)查。本研究通過醫(yī)院倫理委員會的審查,并在臨床試驗中心注冊。
1.2 病例選擇①入組標(biāo)準(zhǔn):所有患者均經(jīng)病理細(xì)胞學(xué)證實診斷為食管鱗癌;患者未行手術(shù)或化療;患者本人或家屬簽署了放射治療知情同意書并愿意參加此項研究,能配合醫(yī)生治療者;卡氏評分(KPS)≥70 分,年齡≤80 歲,無嚴(yán)重的心、肺、肝、腎功能障礙,無廣泛遠(yuǎn)處轉(zhuǎn)移;近0.5 a內(nèi)未患心肌梗死或腦梗死等重大疾病;患者放療劑量50~70 Gy;預(yù)期生存期>0.5 a。②排除標(biāo)準(zhǔn):有胸部放射治療或化療病史;有嚴(yán)重的肺功能障礙或肺纖維化病史;行全部或部分肺葉切除術(shù)者;一般情況差,不能耐受放療或放療中途放棄;有哮喘、嚴(yán)重的慢性支氣管炎、肺氣腫、嚴(yán)重肺部感染者或有其他嚴(yán)重疾病(如0.5 a內(nèi)發(fā)生過心肌梗死或腦梗死)。③治療前常規(guī)檢查:血常規(guī)、血凝全項、生化全項、肺功能檢查、胸部及上腹部CT、食管鋇餐片。
1.3 放療方法采用熱塑膜固定患者體位,在CT下行模擬定位,在瑞典醫(yī)科達(dá)公司Elekta XIO放療計劃系統(tǒng)(Radiotherapy Treatment Planning System)工作站上接受CT圖像后,行三維重建和調(diào)節(jié)CT的窗寬、窗位至最佳狀態(tài)后勾畫出靶區(qū)和危險器官。腫瘤靶區(qū)根據(jù)ICRU 50號和62號報告的概念勾畫大體腫瘤區(qū)域(gross tumor volume,GTV)、臨床靶區(qū)體積(clinical target volume,CTV)、計劃靶區(qū)體積(planning target volume,PTV)。一般分3~6個照射野,保證95%等劑量線覆蓋99%PTV、99%等劑量線覆蓋95%PTV,并避開脊髓等重要臟器。結(jié)合患者肺功能狀態(tài)和危及器官受量情況來確定治療計劃。由醫(yī)師勾畫照射靶區(qū),物理師設(shè)定治療計劃,由科主任或主任醫(yī)師審核確認(rèn)后方可執(zhí)行。物理學(xué)參數(shù)[V5、V10、V20、肺的平均劑量(mean lung doseMLD)]由計劃系統(tǒng)中的劑量體積直方圖(dose volume histogram, DVH)提供。放療處方劑量因人而異,一般50~70 Gy,平均62 Gy,每周5次,每次2 Gy,用醫(yī)科達(dá)PRICISE直線加速器完成。
1.4 細(xì)胞因子的測定用EDTA管收集同一患者放療前、放療中、放療結(jié)束時、放療結(jié)束后1個月及結(jié)束后3個月時的血液,室溫放置1 h內(nèi),3 000 r·min-1離心10 min后取血漿,分別留取凍存于-80 ℃冰箱中,采用全自動生化分析儀進行檢測,采用安徽大千生物工程有限公司的CRP測定試劑,依照說明書嚴(yán)格按步驟進行操作。
1.5 統(tǒng)計學(xué)分析數(shù)據(jù)采用SPSS 19.0 統(tǒng)計學(xué)軟件進行統(tǒng)計分析,單因素分析采用χ2檢驗,均數(shù)比較采用t檢驗。以P<0.05為有統(tǒng)計學(xué)意義。對多個樣本均數(shù)之間的差異采用重復(fù)測量方差分析。
2 結(jié)果
2.1 患者治療及隨訪情況全部患者隨訪時間>6個月,31.82%(21/66)的患者發(fā)生放射性肺損傷,其中≥2級 7.58%(5/66),<2級24.24%(16/66)。對于有癥狀的患者及2級以上的肺損傷患者行痰培養(yǎng)、吸氧、化痰、擴支氣管治療,根據(jù)患者情況適量甲強龍及抗生素治療,必要時行氧驅(qū)霧化吸入治療。經(jīng)過上述治療,有16例患者刺激性咳嗽及喘息癥狀消失,偶有干咳,復(fù)查CT提示:局部致密影吸收,或殘留少量斑片狀影,或局部肺紋理增多增粗。5例患者癥狀略有好轉(zhuǎn),但CT影像表現(xiàn)出與放射野相一致的條索狀影或網(wǎng)格樣改變。
2.2 臨床因素和放射性肺損傷的關(guān)系共有84例患者入組,其中1人因車禍死亡,3例未完成治療,未完成全部抽血3例,隨訪不足半年11例。最后入組患者66例(見表1)。統(tǒng)計學(xué)分析提示,年齡、性別、吸煙史、病灶位置與放射性肺損傷無明顯關(guān)系。紫杉類藥物應(yīng)用者更易發(fā)生放射性肺損傷(P=0.036)。在發(fā)生放射性肺損傷的21例患者中,5例處方劑量≤60 Gy,16例處方劑量>60 Gy,其中接受更高放射治療劑量的患者更有可能發(fā)生放射性肺損傷(P=0.016)。
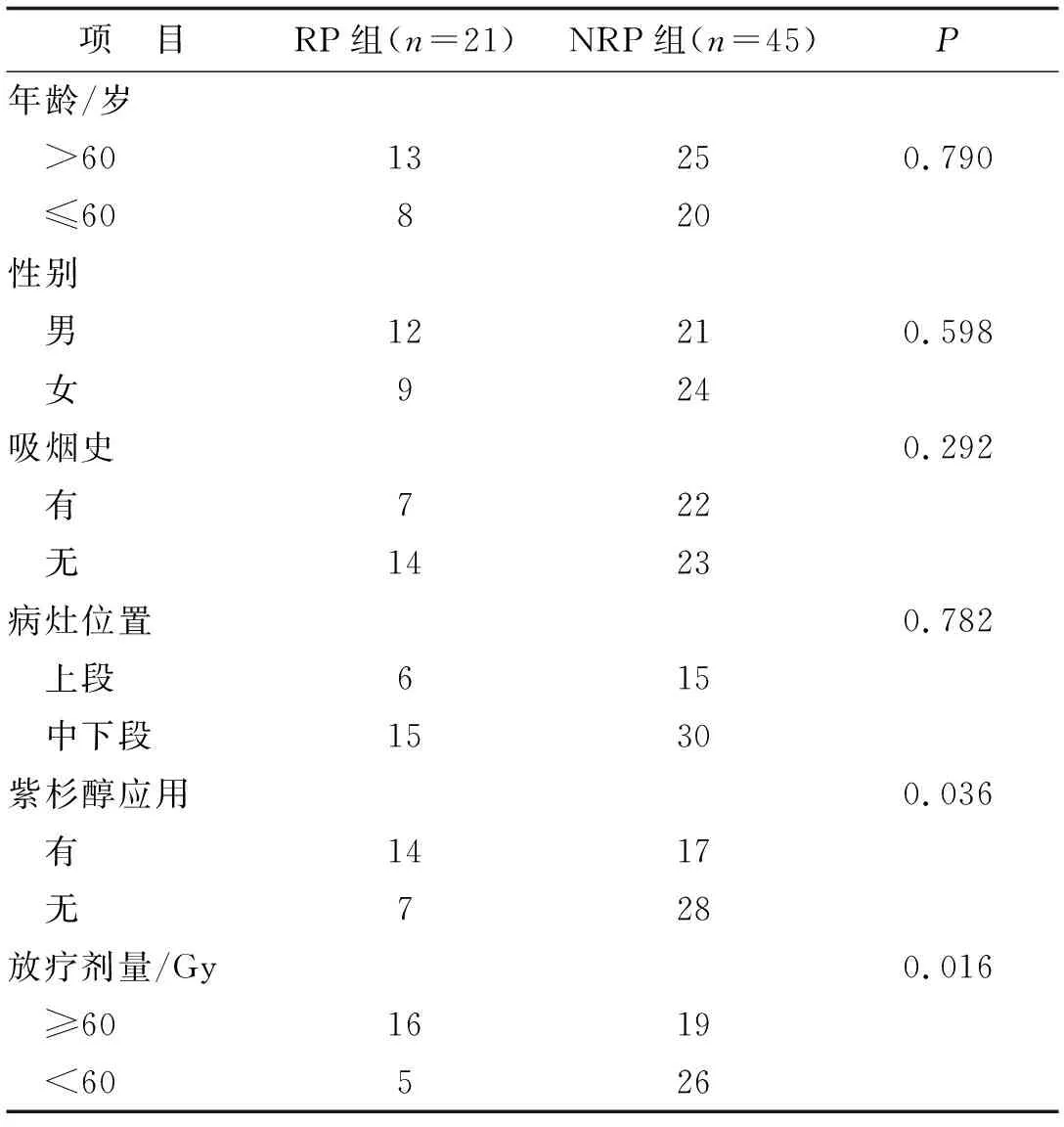
表1 患者臨床一般資料
2.3 物理學(xué)參數(shù)的情況應(yīng)用t檢驗進一步分析66例胸段食管癌患者的各項物理學(xué)指標(biāo)與放射性肺損傷的發(fā)生情況, 其中兩組全肺的V5、V10、V20、平均肺劑量及正常組織并發(fā)癥概率(normal tissue complication probability,NTCP)經(jīng)t檢驗差異無明顯統(tǒng)計學(xué)意義。見表2。
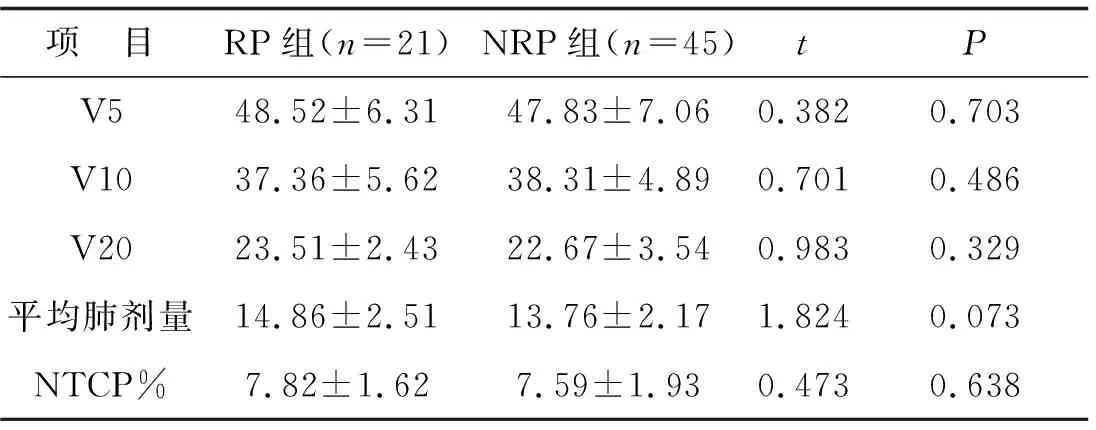
表2 物理學(xué)參數(shù)
2.4 放射性肺損傷組(RP)與無放射性肺損傷組(NRP)CRP在放療前后的變化可以看到在RP組患者血漿中CRP水平在放療過程中開始升高,放療結(jié)束3個月后緩慢降至正常水平,見表3。
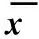
表3 放療前后血漿中CRP的變化(±s) pg·mL-1
本研究通過應(yīng)用全自動生化分析儀測量血漿CRP濃度(<9 mg·L-1為正常水平)來了解其與肺損傷發(fā)生的關(guān)聯(lián)。發(fā)現(xiàn)在放療前,RP組CRP水平為(1.79±0.75) mg·L-1,NRP組為(1.37±0.62) mg·L-1。RP組在放療中及放療后的各個時間點血漿濃度均高于NRP組,且兩組之間在放射治療劑量達(dá)40 Gy時,RP和NRP組開始差異有統(tǒng)計學(xué)意義。在RP組中,CRP水平持續(xù)上升,放療結(jié)束時達(dá)到最高水平。本研究進行了重復(fù)測量方差分析以了解血漿中CRP水平的時間變化規(guī)律,結(jié)果表明在整個時間過程中細(xì)胞因子水平變化和放射性肺損傷相關(guān)。
3 討論
放射治療是食管惡性腫瘤最重要的腫瘤局部治療方法之一,超過70%的食管惡性腫瘤患者在治療過程中需接受放射治療。Kong等調(diào)查發(fā)現(xiàn)每1 Gy高于常規(guī)處方劑量將提高3~5 a生存率約1%,降低死亡率3%[5]。國內(nèi)學(xué)者也發(fā)現(xiàn)食管癌同步放化療時放療劑量的提高有助于疾病的局部控制[6-8],但放射劑量的增加,隨之將提升放射治療相關(guān)并發(fā)癥的發(fā)生率和反應(yīng)強度。目前放療根治量的設(shè)置考慮將放療的并發(fā)癥限制在5%~15%之內(nèi)[5,9-11],也就是說,受限于少數(shù)(5%~15%)對于射線高度敏感的個體影響,85%~95%的患者沒有得到最佳的放射治療劑量。據(jù)此可以認(rèn)為絕大多數(shù)的食管癌患者沒有獲得最佳的生存率和治愈率。目前亟需將這些對放射線高度敏感的人群通過相應(yīng)的檢測篩選出來,從而在治療早期尚未出現(xiàn)嚴(yán)重不可逆損傷前,及時調(diào)整放射治療技術(shù)、計劃以及腫瘤處方劑量,達(dá)到針對不同患者的個體化放療。
放射性肺損傷的發(fā)生并非全是電離輻射所導(dǎo)致的直接損傷,而是與損傷后產(chǎn)生的炎性介質(zhì)所介導(dǎo)的急性免疫反應(yīng)密切相關(guān),一定劑量的電離輻射將導(dǎo)致肺泡巨噬細(xì)胞釋放出炎性細(xì)胞因子,激發(fā)炎性因子介導(dǎo)的急性自發(fā)性免疫反應(yīng)[12]。
放射性肺損傷發(fā)生發(fā)展過程中細(xì)胞因子的變化可以是導(dǎo)致?lián)p傷發(fā)生的原因或者啟動因素,也可以是損傷發(fā)生過程中的伴隨變化。檢測細(xì)胞因子的變化有望預(yù)測放射性肺損傷的發(fā)生或預(yù)測其發(fā)展過程,急性放射性肺損傷常發(fā)生在放療開始后的1~3個月,3個月后肺損傷將逐步轉(zhuǎn)為慢性肺損傷[13]。
細(xì)胞因子還可以作為放射性肺損傷的干預(yù)靶點,為放射性肺損傷的治療提供依據(jù)。C反應(yīng)蛋白屬于穿透素蛋白家族成員,是1930年被發(fā)現(xiàn)的急性時相反應(yīng)蛋白,主要由肝臟合成,并廣泛表達(dá)于全身各處,是由機體在應(yīng)激狀態(tài)下產(chǎn)生的一種蛋白,它是一種經(jīng)典的急性時相蛋白,具有反應(yīng)時間短、持續(xù)時間長的特點,在各種急性炎癥、組織損傷、心肌梗死等疾病時升高。CRP在許多炎癥過程中會升高,所以CRP篩查在是否存在炎癥以及跟蹤炎性疾病活動進展方面都占有重要地位[14]。 同時在肺部感染性疾病的診斷以及炎癥發(fā)生方面有較高的預(yù)測價值[15]。有研究發(fā)現(xiàn),CRP水平的變化貫穿于接受放療的肺癌患者的整個治療過程中,CRP可敏感反映體內(nèi)發(fā)生的病理生理變化,CRP的升高對早期預(yù)測放射性肺炎具有重要價值[16]。
本實驗數(shù)據(jù)顯示,在放射性肺損傷者血漿中CRP水平在放療中逐漸升高,在放療后1個月時達(dá)到最高值,后逐漸下降;非放射性肺損傷患者血漿中CRP水平相對平穩(wěn)。放療的各個時期和放療前無明顯差別。重復(fù)測量方差分析結(jié)果表明在整個過程中CRP水平變化和放射性肺損傷的發(fā)生相關(guān)。從本實驗的結(jié)果看,CRP可作為放射性肺損傷發(fā)生的預(yù)測因子,但是CRP達(dá)到多高的水平可提示有放射性肺損傷的發(fā)生,需要大樣本的臨床研究數(shù)據(jù)來進一步證實。
多種因素的影響導(dǎo)致放射性肺損傷的發(fā)生。放射物理學(xué)方面,本研究中放射性肺損傷組和無放射性損傷組全肺的V5、V10,V20、MLD、NTCP經(jīng)t檢驗無明顯統(tǒng)計學(xué)上的差異,表明DVH相關(guān)參數(shù)在兩組中是相同的。從患者的一般資料來看,本研究顯示紫杉類藥物的應(yīng)用、治療劑量和放射性肺損傷的發(fā)生有關(guān)。 在劑量學(xué)因素嚴(yán)格控制和化療方案嚴(yán)格篩選的前提下,CRP可作為放射性肺損傷發(fā)生的預(yù)測因子。
總之,放射性肺損傷的本質(zhì)是輻射原因引起的炎性細(xì)胞因子表達(dá)增加和信息的放大、傳遞。CRP在臨床預(yù)測、預(yù)防和治療放射性肺損傷中有深遠(yuǎn)的意義。另外,不可忽視間質(zhì)細(xì)胞和內(nèi)皮細(xì)胞的損傷在放射反應(yīng)中的作用。

