用KV-CBCT對(duì)食管癌不同固定體位動(dòng)態(tài)調(diào)強(qiáng)分次間擺位誤差的研究
徐曉捷,張瑞英,雷亞楠,侯 鵬,李敬霞
食管癌是我國(guó)常見(jiàn)的上消化道惡性腫瘤之一,放射治療是食管癌主要的治療手段,而調(diào)強(qiáng)放射治療是目前主流的放療技術(shù)。在放射治療過(guò)程中患者的體位重復(fù)性十分重要,用錐形束CT可以更好地保證放療體位的準(zhǔn)確性[1-2]。本研究通過(guò)對(duì)本院行錐形束CT(Cone Beam Computed Tomography, CBCT)位置驗(yàn)證的食管癌患者進(jìn)行研究,得到分次間的擺位數(shù)據(jù),分析不同體位固定下的擺位誤差,以指導(dǎo)臨床靶區(qū)(clinical target volume, CTV)到計(jì)劃靶區(qū)(planning target volume, PTV)的外擴(kuò)距離。
1 材料和方法
1.1 一般資料來(lái)自2019年5月至2020年1月在本院行動(dòng)態(tài)調(diào)強(qiáng)的胸段食管癌患者27例,其中體膜固定21例,頭頸肩膜固定6例;年齡46~85歲(中位年齡70歲),男15例,女12例。
1.2 設(shè)備Philips大孔徑16排CT模擬機(jī),瑞典醫(yī)科達(dá)Infinity加速器,計(jì)劃系統(tǒng)Monaco 5.11,深圳騰飛宇科技熱塑膜,頭頸肩膜規(guī)格605 mm×485 mm×2.4 mm,體膜規(guī)格560 mm×460 mm×2.4 mm。
1.3 定位及計(jì)劃設(shè)計(jì)患者均采用平靜呼吸狀態(tài)下仰臥位,體膜組(A組)雙臂上舉雙手交叉置于頭頂,頭頸肩組(B組)合適規(guī)格的聚氨酯頭枕雙臂平放置于體側(cè),均采用熱縮膜固定,配合碳纖維固定架和體位參考金標(biāo)固定。采用Philips16排大孔徑CT掃描,層厚均為0.5 cm。定位掃描的圖像傳到Pinnacle計(jì)劃系統(tǒng)。主管醫(yī)生在CT圖像上勾畫(huà)靶區(qū)GTV、CTV,物理師將畫(huà)好靶區(qū)的CT圖像傳至Monaco計(jì)劃系統(tǒng),在Monaco TPS上按照醫(yī)生的處方要求制作多個(gè)放射治療計(jì)劃。
1.4 治療計(jì)劃實(shí)施將審核通過(guò)的最優(yōu)治療計(jì)劃傳至加速器Mosaiq系統(tǒng)中執(zhí)行。首次治療按照患者體膜上的參考金標(biāo)及患者體表線進(jìn)行擺位,前3次及每周3次對(duì)患者行CBCT掃描,將得到的圖像與定位重建得到的DRR圖像進(jìn)行配準(zhǔn)。使用自動(dòng)配準(zhǔn)和人工微調(diào)相結(jié)合,直至結(jié)果滿意,記錄分次間的擺位誤差。
1.5 統(tǒng)計(jì)方法使用SPSS 23軟件進(jìn)行獨(dú)立樣本t檢驗(yàn),P<0.05為差異具有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 擺位誤差分析擺位誤差頻數(shù)分析:27例患者總共行CBCT掃描405次,平均每位患者掃描15次,得出平移誤差頻數(shù)數(shù)據(jù),可見(jiàn)y軸及患者頭腳方向>10 mm者高達(dá)8.4%。見(jiàn)表1。
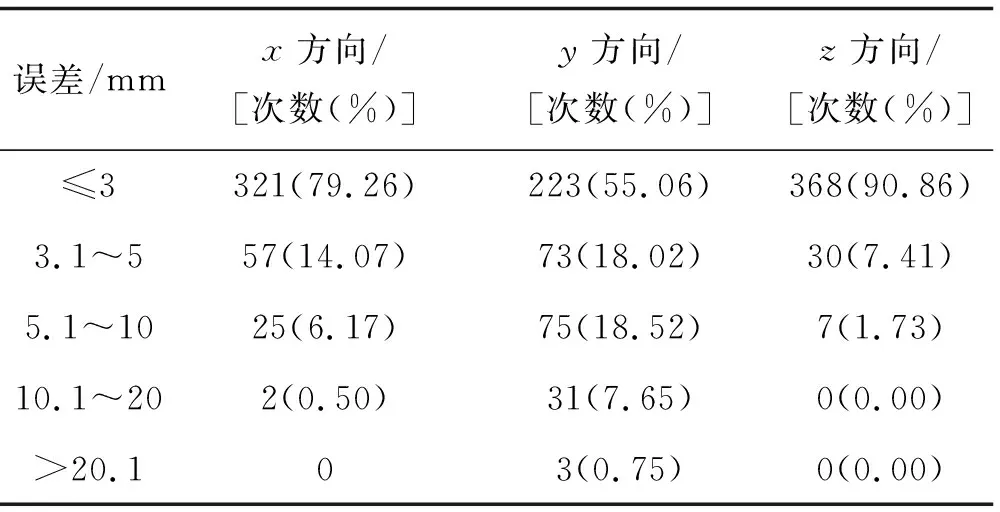
表1 27例405組擺位誤差數(shù)據(jù)頻數(shù)分析(n=405)
2.2 兩組擺位絕對(duì)誤差比較CBCT數(shù)據(jù)A組共有315人次,B組共有90人次,A組在x軸和z軸上絕對(duì)誤差小于B組,在y軸上大于B組,見(jiàn)表2。A組和B組的系統(tǒng)誤差和隨機(jī)誤差見(jiàn)表3-4。

表2 A組和B組三維方向的絕對(duì)擺位誤差比較(±s) mm

表3 A組和B組系統(tǒng)誤差Σ mm

表4 A組和B組隨機(jī)誤差δ mm
2.3 靶區(qū)外放邊界大小利用Van Herk等[3]提出的由CTV到PTV的外放公式M=2.5Σ+0.7δ(其中Σ表示系統(tǒng)誤差,δ表示隨機(jī)誤差)計(jì)算A組和B組單純考慮擺位誤差要外放的距離。見(jiàn)表5。

表5 兩種體位固定方式在位方向CTV到PTV的外放距離 mm
3 討論
我國(guó)放療行業(yè)已經(jīng)進(jìn)入三精治療時(shí)代,即精確定位、精確設(shè)計(jì)和精確治療[4]。圖像引導(dǎo)的放射治療(image guided radiation therapy, IGRT)是目前較精準(zhǔn)的放射治療技術(shù),能在保證靶區(qū)照射劑量的前提下降低周圍正常組織的放射損傷[5]。在多個(gè)研究和《腫瘤放射治療學(xué)》一書(shū)中均指出患者體位固定方式是影響體位三維精度的重要因素之一[6-8]。與頭頸部腫瘤相比,胸腹部的擺位誤差相對(duì)較大[9]。KV-CBCT能夠較清楚地顯示軟組織等結(jié)構(gòu),以及腫瘤和危及器官體積變化,是一種較精確的位置驗(yàn)證技術(shù)。Huddy等[10]的研究結(jié)果表明,CBCT測(cè)量擺位誤差較電子射野影像裝置(electronic protal imaging device, EPID)精確。食管癌調(diào)強(qiáng)放射治療在治療計(jì)劃上有靶區(qū)內(nèi)劑量分布均勻、靶區(qū)外劑量跌落相對(duì)較快的優(yōu)勢(shì),這樣的劑量分布特點(diǎn)對(duì)擺位精度的要求更高。擺位誤差可能導(dǎo)致靶區(qū)劑量不夠,而周邊的危及器官劑量變大或者超標(biāo),這將嚴(yán)重影響患者的生存時(shí)間和生存質(zhì)量,因此要盡量減小患者的擺位誤差,提高治療精度[11]。對(duì)食管癌擺位誤差相關(guān)因素進(jìn)行研究,對(duì)提高擺位精度,降低擺位誤差都有很好的臨床意義[12-14]。
本研究探討了食管癌不同固定體位的絕對(duì)擺位誤差以及CTV-PTV的靶區(qū)外擴(kuò)距離的影響。本研究結(jié)果顯示A組的絕對(duì)擺位誤差x、y、z軸分別為(1.911±1.641)、(4.386±4.206)、(1.342±1.072) mm,B組分別為(2.738±2.229)、(2.728±2.743)、(1.977±1.348) mm,且3個(gè)軸上均P<0.05,差異有統(tǒng)計(jì)學(xué)意義。
A組固定體位雙臂上舉雙手交叉放于頭頂可減少x軸和z軸的絕對(duì)擺位誤差,這是因?yàn)殡p手上舉,胸廓能較舒展地展現(xiàn)一個(gè)平滑的曲面,用體膜固定,體膜制作時(shí)又相對(duì)較緊,這樣對(duì)整個(gè)胸部有更好的固定作用,減小了患者左右方向和前后方向的擺位誤差。在y軸上頭頸肩膜固定可減少患者上下方向的絕對(duì)擺位誤差,因?yàn)轭^頸肩膜是從患者頭部開(kāi)始固定,頭腳方向頭部固定的準(zhǔn)確性相對(duì)胸部更精確,頭頸肩膜用乳膠枕固定了患者的頸部曲度,這樣頭腳方向固定得更準(zhǔn)確,所以頭頸肩膜固定的體位在y軸上下方向的絕對(duì)擺位誤差較小。體膜固定時(shí)上界一般在下頜下緣,患者上下的邊界依據(jù)是患者體表上的標(biāo)記線,由于患者體表皮膚活動(dòng)度大,導(dǎo)致上下邊界固定有誤差。頭頸肩固定患者左右位置活動(dòng)度較大,且頭頸肩膜對(duì)上胸廓的前后固定度較小,導(dǎo)致頭頸肩膜固定的左右和前后方向絕對(duì)誤差較大。這一結(jié)果與惠周光等[15]的研究結(jié)果一致,頭頸肩膜在減少上下方向擺位誤差有優(yōu)勢(shì),體膜在減少左右方向和前后方向擺位誤差有優(yōu)勢(shì)。
王丹等[16]對(duì)中上段食管癌調(diào)強(qiáng)放療進(jìn)行研究,結(jié)果表明在左右、頭腳以及前后3個(gè)方向的擺位誤差分別是(2.02±1.74)、(2.02±1.93)、(2.03±1.89) mm,上段食管癌由CTV到PTV的外放距離為左右4.7 mm、頭腳8.5 mm、前后5.6 mm;中段食管癌為左右5.0 mm、頭腳11.0 mm、前后6.2 mm。高超等[17]對(duì)42例食管癌行三維適形治療的擺位誤差進(jìn)行研究,結(jié)果表明在左右、前后、頭腳方向擺位系統(tǒng)誤差分別為-2.31、-0.55、-0.16 mm,隨機(jī)誤差分別為4.42、4.35、4.48 mm。擺位誤差使食管癌患者GTV 95%體積接受的劑量(D95)與原治療計(jì)劃相比降低了32 cGy,CTVD95降低了88 cGy。可見(jiàn)患者在治療中的擺位誤差對(duì)靶區(qū)劑量的影響明顯。因此,為了保證食管癌患者的精確治療,應(yīng)盡量保證患者體位有一個(gè)很好的重復(fù)性和準(zhǔn)確性[18-19]。
本研究表明,在x、y、z軸上A組和B組的系統(tǒng)誤差分別為0.346、-1.54。-0.616、-1.334;-0.685、-0.748 mm,A組和B組的隨機(jī)誤差分別為2.497、3.186,6.050、3.639,1.576、2.281 mm。系統(tǒng)誤差是相對(duì)誤差的平均值,反映了所有誤差的偏向性。本研究顯示,在本院Infinity加速器上治療的食管癌病人,y軸、z軸上誤差均偏向下和后方向。A組和B組在患者頭腳方向和前后方向均是負(fù)值,即分次間的擺位誤差更易偏向腳方向和后方向。本研究結(jié)果得出A組CTV到PTV的外擴(kuò)距離x、y、z軸分別為2.613、5.775、2.814 mm,B組CTV到PTV的外擴(kuò)距離x、y、z軸分別為6.080、5.882、3.467 mm。可見(jiàn)在左右方向和前后方向A組的外擴(kuò)距離均小于B組,在上下方向B組的外擴(kuò)距離小于A組,且用單因素方差分析3個(gè)軸向的P值均<0.05,有統(tǒng)計(jì)學(xué)意義,說(shuō)明體膜固定在x軸和z軸上有明顯優(yōu)勢(shì)。本研究結(jié)果可為本院食管癌患者在放射治療體位固定方面提供臨床參考。建議在本院Infinity加速器上做治療的、病變?cè)谛刂胁亢托叵虏康幕颊哌x擇體膜固定;而頭頸肩膜固定在z軸上有明顯優(yōu)勢(shì),建議胸上段的患者選擇頭頸肩膜固定。
本研究采集分析本科室現(xiàn)有的常規(guī)治療的數(shù)據(jù),并非隨機(jī)分組,兩組的樣本量不平均,分組中存在偏倚。在實(shí)際治療過(guò)程中,不可能對(duì)每位患者行自身配對(duì)研究,這也使得研究結(jié)果有一定的偏差。B組的數(shù)據(jù)量較A組少,這可能對(duì)研究結(jié)果存在一定的影響,但B組有90人次的樣本量有統(tǒng)計(jì)學(xué)意義。
食管癌由臨床靶區(qū)CTV外放到計(jì)劃靶區(qū)PTV時(shí),既要考慮呼吸運(yùn)動(dòng)引起靶區(qū)運(yùn)動(dòng),又要考慮放射治療時(shí)分次間擺位誤差,因此靶區(qū)的體積就會(huì)增大。隨著靶區(qū)體積的增大,正常組織肺和脊髓的受量也會(huì)相應(yīng)升高。每個(gè)單位均應(yīng)根據(jù)實(shí)際的測(cè)量數(shù)據(jù)測(cè)算出本單位具體的擺位誤差和系統(tǒng)誤差。本研究表明,雙臂上舉體膜固定和雙臂放于兩側(cè)兩種體位固定方式,對(duì)擺位誤差的影響各有優(yōu)劣,且誤差大小均在可控的范圍內(nèi),均具有較好的可重復(fù)性。對(duì)于胸上段食管等肺組織較少的病變部位建議選擇頭頸肩膜,對(duì)于胸中下段的病變部位涉及到肺組織建議選擇體膜固定。在臨床實(shí)踐中,可根據(jù)患者的具體情況選擇合適的體位固定方式。本研究結(jié)果可為不同的體位固定三維方向上CTV到PTV的外擴(kuò)距離提供臨床參考依據(jù),本院患者選擇頭頸肩膜固定的患者CTV到PTV的外擴(kuò)距離x、y、z軸分別為6.080、5.882、3.467 mm,選擇體膜固定的患者CTV到PTV的外擴(kuò)距離x、y、z軸分別為2.613、5.775、2.814 mm。個(gè)性化的外擴(kuò)距離既可以保證靶區(qū)有很高的劑量分布,又能減少正常組織受照劑量,對(duì)臨床靶區(qū)外擴(kuò)距離有一定的參考意義。

