一測多評法同時測定復明片中7種成分的含量
姚建華,趙博,王婧寧,趙志國,黃群*
1.遼寧中醫藥大學 附屬醫院,遼寧 沈陽 110032;2.遼寧大熊制藥有限公司 研究所,遼寧 本溪 117004
復明片由酒萸肉、車前子、決明子、枸杞子、地黃等24味中藥加工而成,臨床上主要用于肝腎陰虛所致的羞明畏光、視物模糊,青光眼初、中期白內障見上述證候的治療[1]。現代研究表明,復明片改善初發期老年性白內障患者[2]、糖尿病視網膜病變患者[3]的視力水平,治療玻璃體混濁[4]、原發性開角型青光眼視功能[5-6],改善中晚期青光眼術后眼底血液循環,提高視力[7]等臨床效果明顯。中藥及其制劑具有多組分、多靶點、整體調節的特點,單一組分控制模式難以全面評價其產品的內在質量,多指標控制模式近年來已逐步應用于中藥及其制劑的質量評價中。復明片現收載于《中華人民共和國藥典》(以下簡稱《中國藥典》)2015年版一部,現行標準和文獻報道中僅對復明片所含單一成分進行定量控制,尚未建立復明片多組分質量控制模式[8]。本實驗首次采用HPLC同時測定復明片中活性成分紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷含量,建立復明片多組分質量控制模式,同時以莫諾苷為內參物,建立其與其他6種成分的相對校正因子,實現一測多評法(QAMS)對復明片中7種活性成分含量的同時測定,有效地解決了傳統多指標成分控制模式部分對照品不易得、價格昂貴、檢驗成本過高的不足,為進一步完善復明片的質量標準和全面反映復明片的產品質量提供支持。
1 儀器與試藥
1.1 儀器
1100型高效液相色譜儀(美國Agilent公司);Prominence型高效液相色譜儀(日本Shimadzu公司);AB265-S型電子天平(瑞士Mettler-Toledo儀器有限公司)。
1.2 試藥
莫諾苷對照品(批號:111998-201703,CAS號:25406-64-8,純度:97.4%)、馬錢苷對照品(批號:111640-201808,CAS號:18524-94-2,純度:99.0%)、大車前苷對照品(批號:111914-201604,CAS號:104777-68-6,純度:90.2%)均來源于中國食品藥品檢定研究院;紅鐮霉素-6-O-β-龍膽二糖苷對照品(批號:CFS201701,CAS號:24577-90-0,純度:98.0%)、決明子苷對照品(批號:CFS201702,CAS號:123914-49-8,純度:98.0%)均來源于武漢天植生物技術有限公司;橙黃決明素-6-O-葡萄糖苷對照品(批號:PRF8062622,CAS號:129025-96-3,純度:99.5%)、山茱萸新苷對照品(批號:14082202,CAS號:131189-57-6,純度:97.8%)均來源于成都普思生物科技股份有限公司;乙腈為色譜純;其余試劑均為分析純。
復明片(規格:0.31 g/片,批號分別為PC218110591、PC219030101、PC219040171)來源于于西安碑林藥業股份有限公司。
2 方法與結果
2.1 溶液的制備
2.1.1對照品儲備液 分別精密稱取7種待測目標成分對照品適量,用60%甲醇溶液制成紅鐮霉素-6-O-β-龍膽二糖苷1.052 mg·mL-1、大車前苷0.176 mg·mL-1、莫諾苷1.126 mg·mL-1、決明子苷0.754 mg·mL-1、馬錢苷0.572 mg·mL-1、山茱萸新苷0.126 mg·mL-1、橙黃決明素-6-O-葡萄糖苷0.438 mg·mL-1的7種對照品儲備液。
2.1.2混合對照品溶液 精密吸取2.1.1項下7種對照品儲備液各2.5 mL,用60%甲醇制成紅鐮霉素-6-O-β-龍膽二糖苷52.6 μg·mL-1、大車前苷8.8 μg·mL-1、莫諾苷56.3 μg·mL-1、決明子苷37.7 μg·mL-1、馬錢苷28.6 μg·mL-1、山茱萸新苷6.3 μg·mL-1、橙黃決明素-6-O-葡萄糖苷21.9 μg·mL-1的混合對照品溶液。
2.1.3復明片供試品溶液 取復明片樣品(批號:PC218110591)適量,除去薄膜衣,研成細粉,取2.0 g,精密稱定,精密加入60%甲醇25 mL,加熱回流提取60 min,取出放冷,用60%甲醇補足減失質量,濾過,制成復明片供試品溶液。
2.1.4陰性樣品溶液 按《中國藥典》2015年版一部復明片質量標準項下的處方比例和制法,分別制備缺車前子、缺決明子、缺酒萸肉的3種陰性樣品,再按2.1.3項下方法制備陰性樣品溶液。
2.2 色譜條件及系統適用性試驗
色譜柱:Diamonsil C18(250 mm×4.6 mm,5 μm)柱;檢測波長分別為330 nm[9-11](0~17.0 min檢測大車前苷)、278 nm[12](17.0~36.0 min檢測紅鐮霉素-6-O-β-龍膽二糖苷、決明子苷、橙黃決明素-6-O-葡萄糖苷)和240 nm[13-15](36.0~65.0 min檢測莫諾苷、馬錢苷、山茱萸新苷);流動相:乙腈(A)-0.1%磷酸溶液(B),梯度洗脫(0~11.0 min,15.0%A;11.0~17.0 min,15.0%~19.0%A;17.0~36.0 min,19.0%~25.0%A;36.0~57.0 min,25.0%~41.0%A;57.0~65.0 min,41.0%~15.0%A);體積流量:1.0 mL·min-1;柱溫:30 ℃;進樣量:10 μL。精密吸取2.1.2~2.1.4項下制備的各溶液依法進樣檢測,記錄所檢測色譜圖,見圖1。結果顯示,所記錄色譜圖基線平穩,復明片中7種待測目標成分與其他雜質峰分離度均大于1.5,理論塔板數按各成分色譜峰計均不低于4500,陰性樣品對復明片中7種成分的同時測定無干擾。
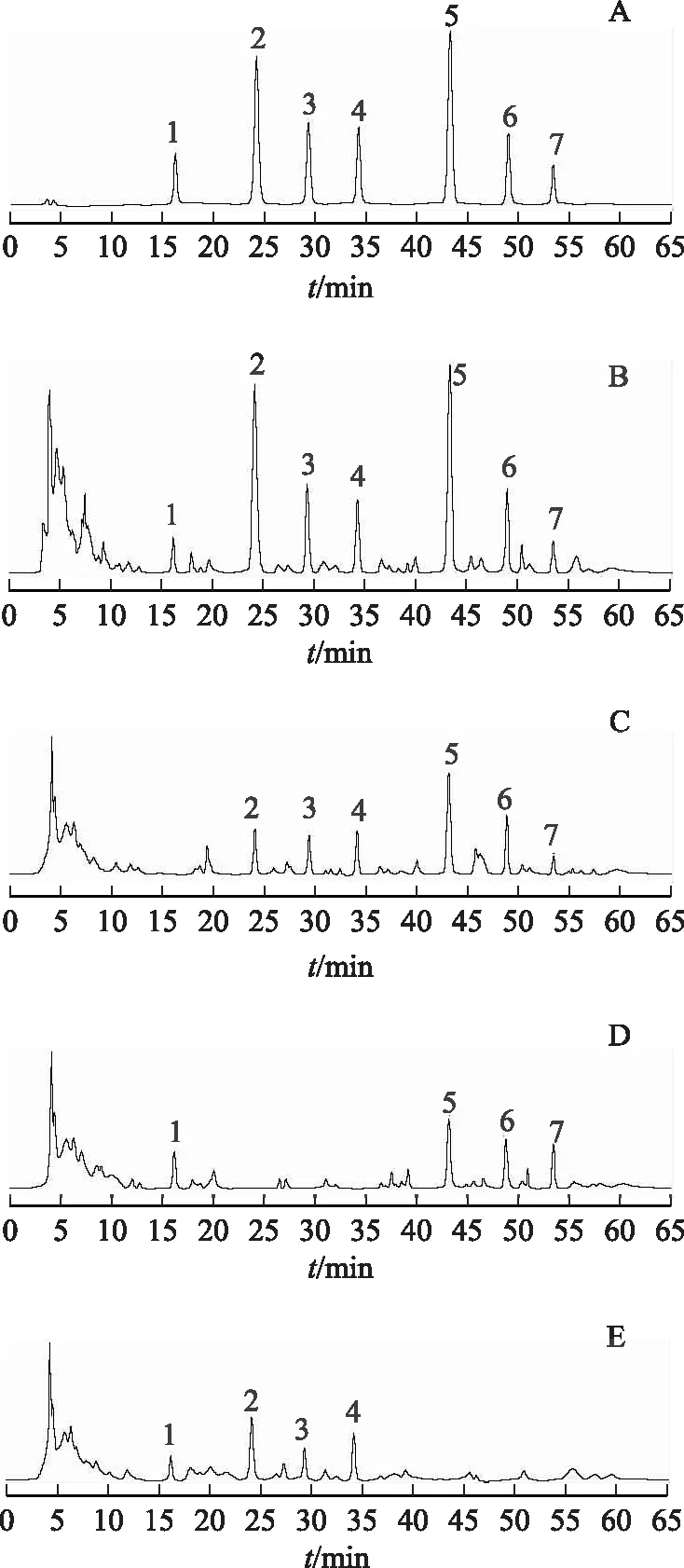
注:A.混合對照品;B.復明片;C.車前子陰性樣品;D.決明子陰性樣品;E.酒萸肉陰性樣品;1.大車前苷;2.紅鐮霉素-6-O-β-龍膽二糖苷;3.決明子苷;4.橙黃決明素-6-O-葡萄糖苷;5.莫諾苷;6.馬錢苷;7.山茱萸新苷。圖1 混合對照品及復明片的HPLC圖
2.3 線性關系考察
分別精密吸取2.1.1項下7種對照品儲備溶液適量,用60%甲醇溶液制成紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷25倍質量濃度差的6個混合對照品溶液,依法進樣檢測,記錄待測目標成分紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷峰面積,以質量濃度為橫坐標,峰面積為縱坐標,進行回歸,結果見表1。
2.4 精密度試驗
取2.1.2項下的混合對照品溶液重復進樣6次,測得復明片中紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷色譜峰峰面積的RSD分別為0.94%、1.28%、0.65%、1.03%、1.05%、1.36%和1.17%。
2.5 重復性試驗
按2.1.3項下方法平行制備同一批次復明片(批號:PC218110591)樣品6份供試品溶液,依法進樣檢測,記錄復明片中紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷色譜峰的峰面積,計算得7種待測成分含量的RSD分別為1.16%、1.71%、0.98%、0.35%、1.64%、0.87%和1.59%。
2.6 穩定性試驗
臨用新配1份復明片(批號:PC218110591)供試品溶液,于制備后0、2、4、8、12、24 h依法進樣檢測,記錄復明片中紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷色譜峰的峰面積,結果復明片供試品溶液24 h內穩定,各成分峰面積的RSD分別為1.01%、1.29%、0.62%、1.08%、0.98%、1.33%和1.15%。
2.7 加樣回收率試驗
取同一批次紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷含量已知的復明片(批號:PC218110591)樣品適量,除去薄膜衣,研細,取9份,每份1.0 g,精密稱定,隨機分成3組,依據《中國藥典》2015年版四部對加樣回收率試驗數據的要求,分別精密加入根據供試品溶液含量另行配制的混合對照品溶液(紅鐮霉素-6-O-β-龍膽二糖苷0.397 mg·mL-1、大車前苷0.049 mg·mL-1、莫諾苷0.435 mg·mL-1、決明子苷0.256 mg·mL-1、馬錢苷0.197 mg·mL-1、山茱萸新苷0.037 mg·mL-1、橙黃決明素-6-O-葡萄糖苷0.128 mg·mL-1)1.0、2.0、3.0 mL各1組,再按2.1.3項下方法制備加樣樣品溶液,依法進樣檢測,結果所測成分大車前苷、紅鐮霉素-6-O-β-龍膽二糖苷、決明子苷、橙黃決明素-6-O-葡萄糖苷、莫諾苷、馬錢苷和山茱萸新苷的平均加樣回收率及RSD分別為99.02%(1.21%)、97.43%(1.09%)、100.11%(0.64%)、98.49%(0.76%)、97.96%(1.19%)、96.98%(1.15%)和98.40%(1.51%)。
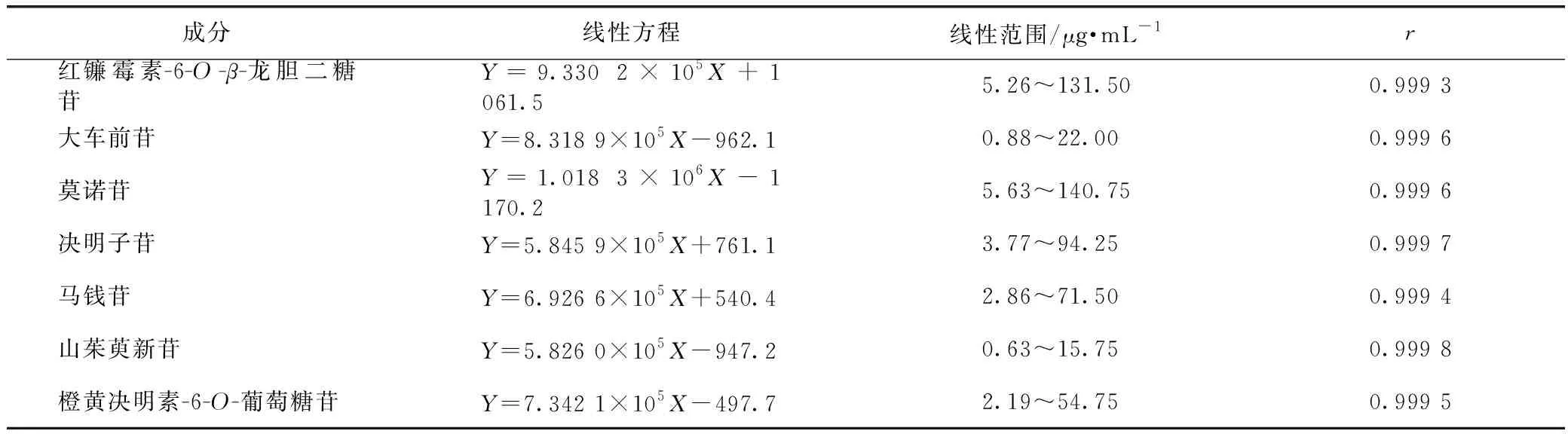
表1 復明片7種成分線性關系和范圍
2.8 相對校正因子的測定
精密吸取2.3項下6個混合對照品溶液適量,依法進樣測定復明片中紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷色譜峰的峰面積,以莫諾苷為內參物,按照公式(1)分別計算其他6種成分的相對校正因子,結果見表2。
fk/s=fk/fs=(Ck×As)/(Cs×Ak)
(1)
式中C代表質量濃度,A代表峰面積,k代表內參物,s代表其他目標成分。
2.9 相對校正因子耐用性考察
2.9.1不同儀器、色譜柱 取2.1.2項下制備的混合對照品溶液依法進樣測定復明片中紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷色譜峰的峰面積,對比考察Agilent 1100型、Shimadzu Prominence型2種品牌高效液相色譜儀和Diamonsil C18(250 mm×4.6 mm,5 μm)、Shimadzu wondasil C18-WR(250 mm×4.6 mm,5 μm)、Agilent TC-C18(250 mm×4.6 mm,5 μm)3種型號色譜柱對相對校正因子的影響,結果見表3。
2.9.2不同體積流量 取2.1.2項下制備的混合對照品溶液依法進樣,測定復明片中紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷色譜峰的峰面積,對比考察不同體積流量(0.8、0.9、1.0、1.1、1.2 mL·min-1)對相對校正因子的影響,結果見表4。
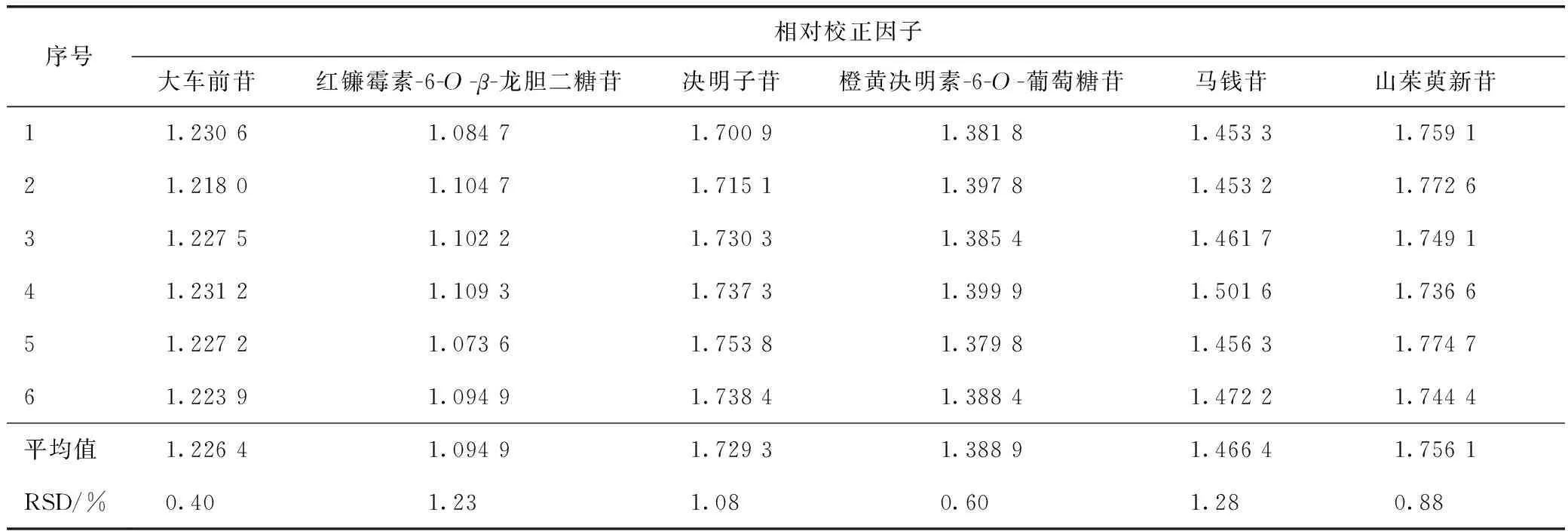
表2 以莫諾苷為內參物的相對校正因子
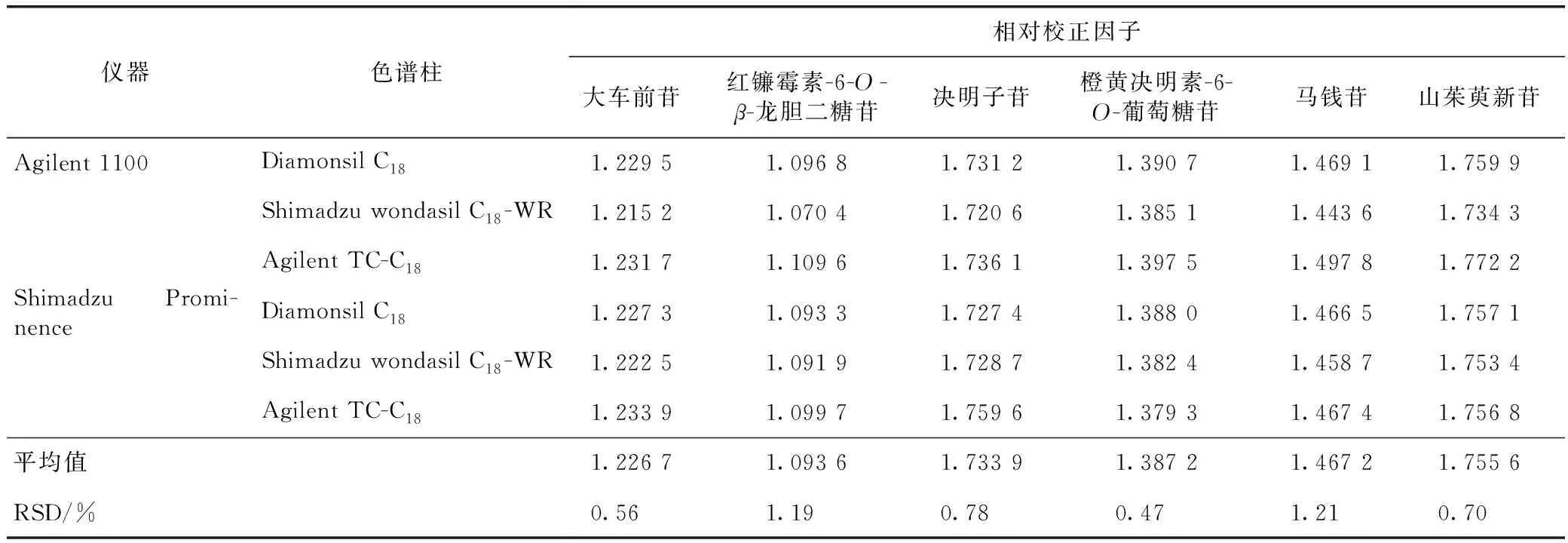
表3 不同儀器、不同色譜柱對相對校正因子的影響
2.9.3待測組分色譜峰的定位 以內參物莫諾苷色譜峰為基準峰,采用相對保留時間值法考察在不同儀器、不同色譜柱條件下其他待測6種成分與內參物莫諾苷的相對保留時間,結果見表5。
2.10 樣品含量測定
取3批復明片樣品(批號分別為:PC218110591、PC219030101、PC219040171)依法進樣測定,記錄復明片中待測目標成分紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷峰面積,分別采用外標法(ESM)和QAMS計算紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷的含量,結果見表6。
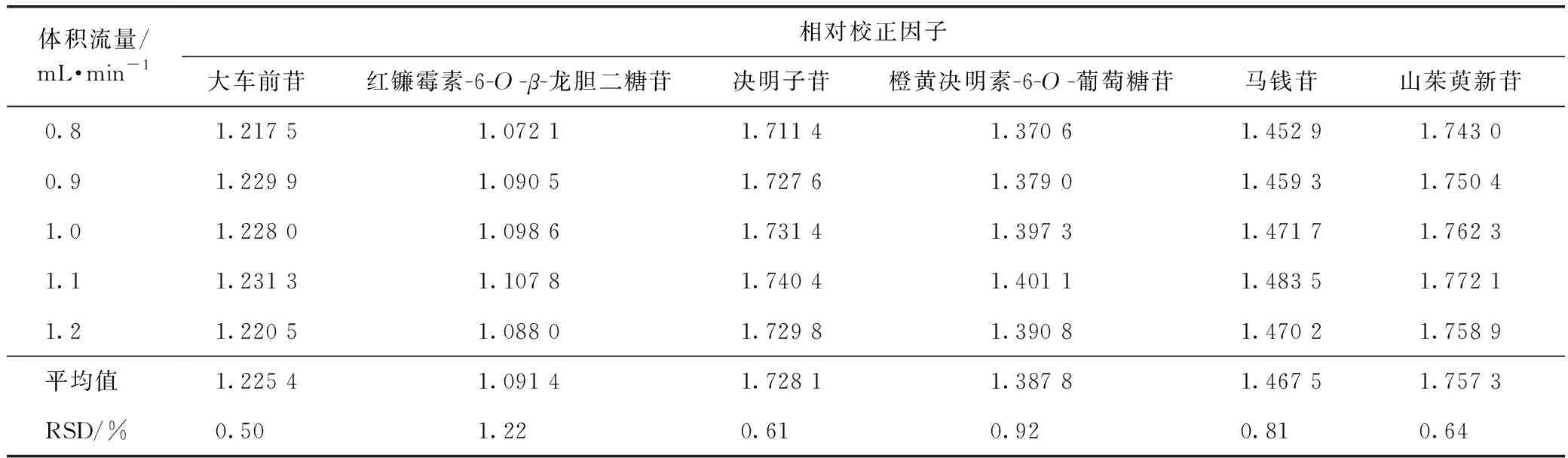
表4 不同體積流量對相對校正因子的影響
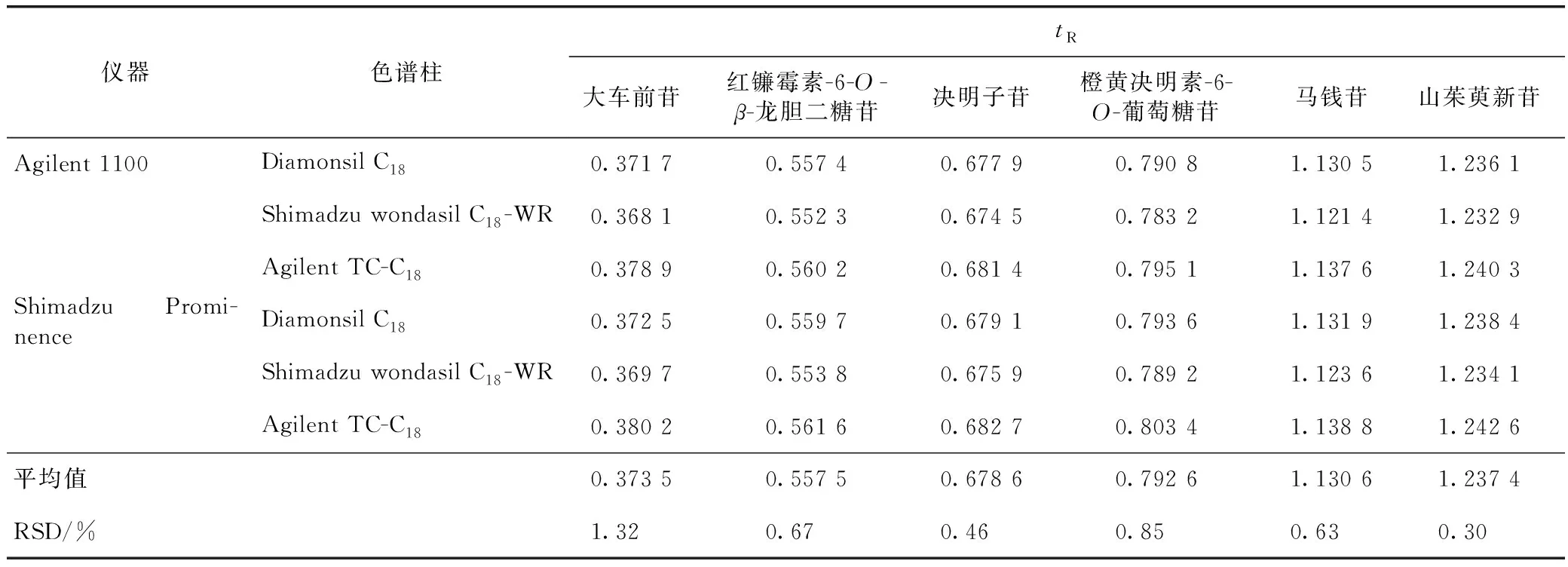
表5 不同儀器、不同色譜柱對相對保留時間的影響
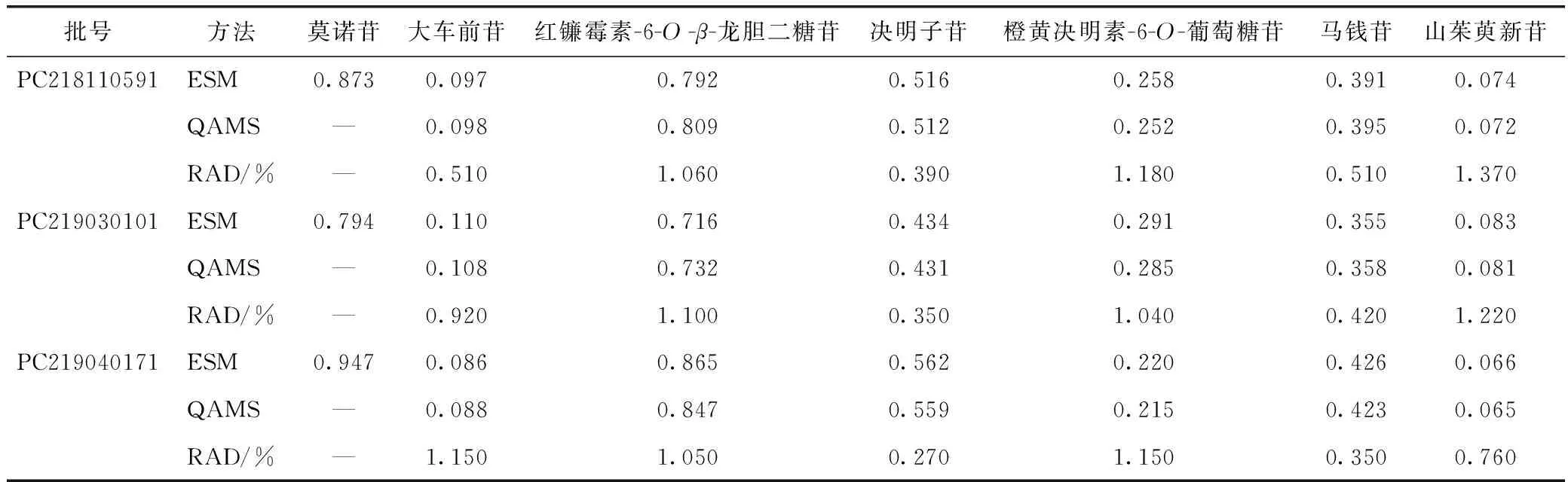
表6 復明片7種成分含量測定結果(n=3) mg·g-1
3 討論
3.1 指標性成分的確定
復明片由酒萸肉、車前子、決明子、枸杞子、地黃等24味中藥配伍而成,方中酒萸肉、枸杞子、菟絲子滋補肝腎、生精明目,女貞子、熟地黃、地黃補腎滋陰、益肝養血,石斛滋陰生津,合為君藥;附以決明子清熱明目,木賊、谷精草疏散風熱、明目退翳,黃連、夏枯草清肝瀉火、明目消腫,菊花平肝明目,牡丹皮清熱涼血,車前子清利濕熱,木通利尿通淋、清心除煩,羚羊角、蒺藜、石決明平肝潛陽、清熱開郁,澤瀉利濕泄熱,茯苓健脾滲濕,檳榔下氣行水,人參、山藥健脾補氣,諸藥共奏,以達滋補肝腎、養陰生津、清肝明目之功效。參考中藥質量標志物以君藥為首選,兼顧臣佐使藥的選定原則,選取復明片方中君藥酒萸肉所含主要活性成分莫諾苷、馬錢苷和山茱萸新苷,臣藥決明子所含特征成分紅鐮霉素-6-O-β-龍膽二糖苷、決明子苷和橙黃決明素-6-O-葡萄糖苷,佐藥車前子所含主要成分大車前苷為定量測定目標成分,為全面評價復明片的產品質量提供參考。
3.2 色譜條件流動相的確定
本實驗首先對流動相乙腈-水[8]、甲醇-水[14]進行考察,以復明片待測目標成分大車前苷、紅鐮霉素-6-O-β-龍膽二糖苷、決明子苷、橙黃決明素-6-O-葡萄糖苷、莫諾苷、馬錢苷和山茱萸新苷色譜峰的峰形、分離效果、色譜圖基線平穩情況及檢測時間等為考察指標,結果發現,乙腈-水為流動相時綜合效果較好,但鐮霉素-6-O-β-龍膽二糖苷、決明子苷、莫諾苷和馬錢苷色譜峰存在拖尾現象,遂以乙腈為有機相,對比考察了不同水相(0.1%磷酸溶液[13,15-16]、0.1%甲酸溶液[10-11])對考察指標的影響,同時對梯度洗脫比例不斷摸索,最終確定采用乙腈-0.1%磷酸溶液為流動相,按照正文中的流動相比例進行梯度洗脫,對復明片中7種指標性成分進行同時檢測。
4 結語
本實驗首次采用QAMS對復明片中紅鐮霉素-6-O-β-龍膽二糖苷、大車前苷、莫諾苷、決明子苷、馬錢苷、山茱萸新苷和橙黃決明素-6-O-葡萄糖苷含量進行同時測定,建立了復明片多指標成分質量控制模式,為全面評價復明片的產品質量提供了數據支持。

