液相色譜-串聯質譜法檢測類固醇激素在CAH篩查中的應用進展
金陳飛,崔夢竹,梁紅艷,姜曉峰
哈爾濱醫科大學附屬第四醫院檢驗科,黑龍江哈爾濱 150028
先天性腎上腺皮質增生癥(CAH)是一組由于類固醇激素合成代謝中某種酶缺乏導致皮質醇合成障礙為主要特征的常染色體隱性遺傳病,會導致腎上腺皮質生成類固醇激素的水平發生改變,并且根據疾病分型不同,激素水平變化有明顯差異。
類固醇激素又稱為甾體激素,是膽固醇經一系列酶催化而來的高效能物質,主要分為腎上腺皮質激素、性激素和維生素D。各種類固醇激素在體內水平極低,一般檢測水平在nmol/L或pmol/L數量級,因此尋找一種可靠、特異的分析方法成為臨床疾病診斷的首要任務。
目前類固醇激素的檢測手段主要包括放射免疫分析技術、化學發光免疫分析技術、酶聯免疫吸附測定、氣相色譜質譜分析法、液相色譜-串聯質譜法(LC-MS/MS)等[1-2]。免疫分析法具備操作簡單、快速的優點,然而RAUH[3]研究顯示,免疫分析法靈敏度較低,易引起交叉反應造成假陽性,無法同時檢測同一標本中的多種激素水平,無法實現類固醇代謝譜的高效、深入、準確的研究。WILSON等[4]研究表明,孕酮測定受不同類固醇(包括17α-羥孕酮、11-去氧皮質酮、20-二酮)所引發的高達10%的交叉反應影響,導致免疫檢測結果偏高。而LC-MS/MS憑借高通量、靈敏度高、特異度高、檢測標本多樣、檢測動態范圍寬等優勢在CAH臨床診斷中的地位越來越重要[5]。
1 CAH類固醇激素代謝通路及主要的CAH分類
CAH是腎上腺皮質功能減退較常見的原因之一。根據酶缺乏將CAH分為7型,具體各型詳見表1,不同酶缺陷時呈現不同的生化和臨床表現。腎上腺皮質類固醇激素合成代謝途徑見圖1。

表1 常見臨床CAH分型
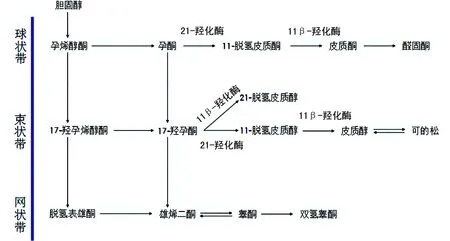
圖1 腎上腺皮質類固醇激素合成代謝途徑
21-OHD是CAH中最常見的類型,臨床可分為3型,分別為失鹽型、單純男性化型及非經典型。在腎上腺皮質類固醇激素合成代謝途徑中,21-羥化酶催化17-羥孕酮轉化為11-脫氧皮質醇和催化孕酮轉化為11-去氧皮質酮,兩者分別為皮質醇和醛固酮的前體。因此,CAH患者類型為21-OHD時皮質醇和醛固酮有不同程度的合成不足或完全缺乏,同時上游底物(17-羥孕酮和孕酮)水平因堆積而明顯升高,因此,17-羥孕酮水平顯著升高成為診斷21-OHD最有意義的指標,臨床通常根據17-羥孕酮水平的改變評估治療效果。因此,17-羥孕酮已被大多數國家納入新生兒篩查項目,這有助于快速檢測出21-OHD患兒。然而該項檢查受到較多因素干擾造成檢測結果假陽性高。由于臍帶血中17-羥孕酮水平很高,所以新生兒在出生1~2 d內17-羥孕酮往往高于臨界值,并逐漸下降。此外,早產兒和許多因其他疾病引起生理應激的足月嬰兒中,17-羥孕酮水平往往比實際水平高,篩查測試的陽性預測值在早產兒中僅為0.4%,而在足月兒中為30.1%[12-13],因此建議對所有17-羥孕酮水平升高的新生兒在1個月后進行第2次LC-MS/MS篩查。
11β-OHD的主要生化異常為低血鉀,但是嚴重度因基因突變類型而異,甚至可出現血鉀正常的情況。其他生化指標變化體現在血17-羥孕酮、雄烯二酮、脫氫表雄酮水平升高,血清皮質醇、醛固酮水平降低,血腎素活性減低。此外,該癥的特征性指標是血和尿11-脫氧皮質醇和去氧皮質酮水平升高,尿中二者的主要代謝產物四氫11-脫氧皮質醇及四氫去氧皮質酮水平升高,這是與21-OHD進行鑒別的關鍵指標。
2 LC-MS/MS法檢測類固醇激素方法學的建立
目前檢測類固醇激素的生物標本主要有血清、血漿、毛發[14]、尿液[15]、唾液[16]、子宮內膜[17]等。在方法開發建立的過程中可通過以下幾個步驟提高檢測性能。(1)標本處理:良好的標本前處理方法可以起到富集目標組分、消除或降低基質干擾、提高靈敏度的作用,反之則會容易引入誤差并延長分析時間。目前血液中類固醇激素的前處理方法有蛋白質沉淀、液液萃取和固相萃取,而多種前處理方法相結合具有低基質效應、回收率高、靈敏度高、自動及快速等優點,已逐漸受到臨床關注[18]。(2)檢測過程:要針對檢測項目的特點選擇合適的色譜柱、流動相流速、離子源和質量分析器,類固醇激素檢測通常與三重四級桿質量分析器或三重四級桿串聯線性離子阱質量分析器串聯,采用電噴霧離子源或大氣壓化學電離源,并利用多反應監測模式對靶向代謝組進行分析,按離子質荷比的大小順序進行收集和記錄,進而得到質譜圖用于結果分析。為了避免內源性或外源性基質物質的干擾,降低待測物信號的損失和信號波動,可在同一批分析中的所有標本中加入等體積的內標液,絕大部分待測物的信號波動和量的損失都可以得到校正。內標通常分為2型,即結構類似物內標和同位素標記內標,在類固醇激素檢測時常常選擇同位素標記內標[19]。新生兒篩查CAH時常常檢測的激素與相應內標檢測信息見表2。同時為確保準確度及批間或批內精密度,每次測量時均應準備質控品。(3)數據處理:合理的分析方式能為實驗研究提供更加精準的結果,保證結果的可靠性。質譜數據處理一般采用質譜儀對應的數據處理軟件,用空白提取液配制標準品做標準曲線,有效排除干擾因素,可以保證高通量、高準確性的數據處理。
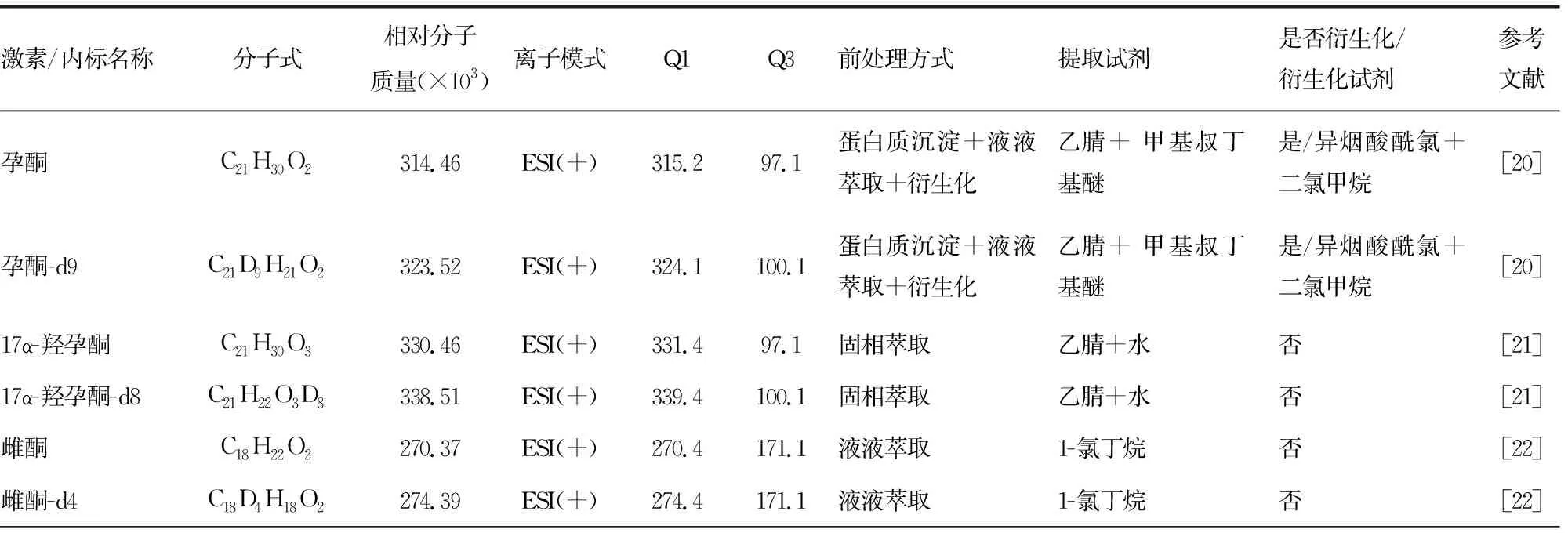
表2 新生兒篩查CAH時常檢測的激素與相應內標
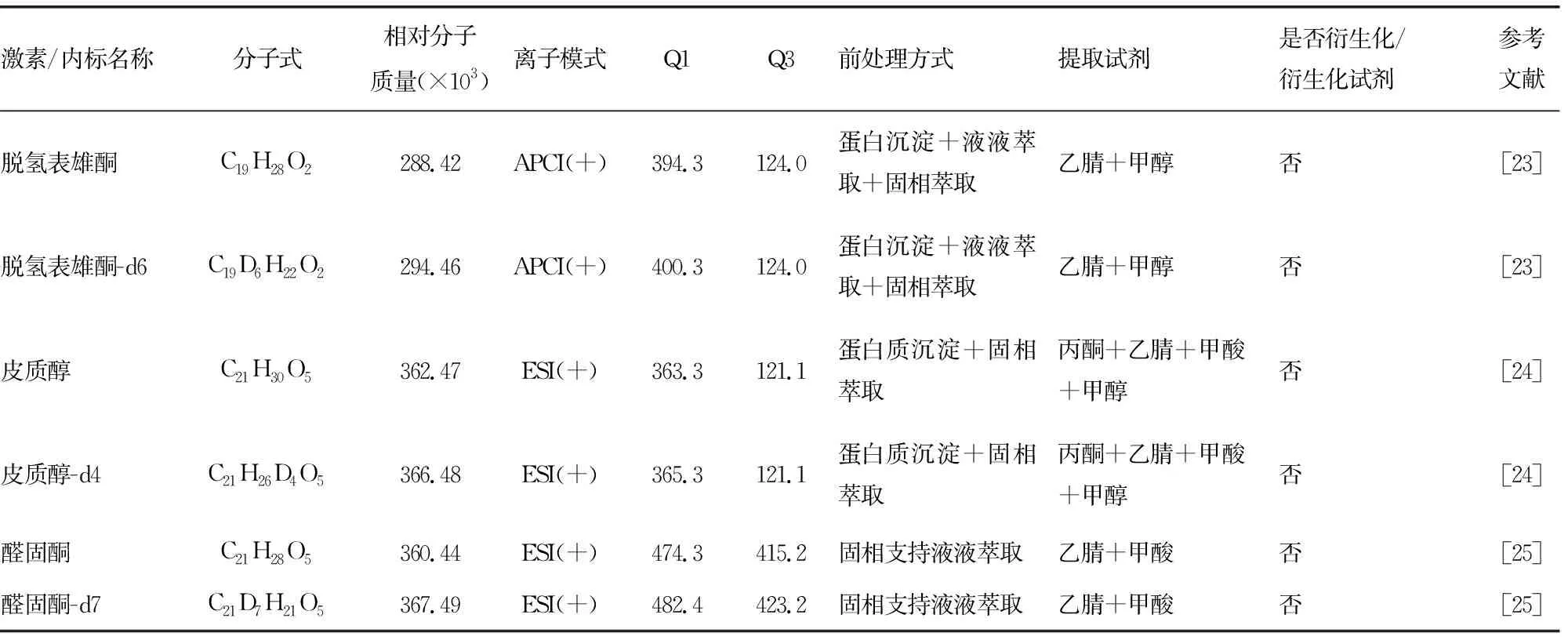
續表2 新生兒篩查CAH時常檢測的激素與相應內標
為了確保檢測結果準確可靠,需要對檢測方法進行性能評估,主要包括檢測下限與定量下限、精準度、線性關系、選擇性、穩定性、準確度、表觀回收率、基質效應等。TRAVERS等[26]建立了LC-MS/MS檢測血清中15種類固醇激素的方法,采用蛋白質沉淀和固相萃取相結合的方法提取血清甾體化合物和氘化內標物,回收率從21-脫氧皮質醇的64%到皮質醇的101%不等,并與免疫分析法比較,2種方法檢測皮質醇,脫氫表雄激素和睪酮的結果較一致,免疫分析法檢測醛固酮數值偏低,孕酮水平低于2 ng/mL的17-羥孕酮、雄烯二酮和11-脫氧皮質醇水平明顯偏高。分析這種差異產生的原因:(1)免疫分析法抗體特異性低導致的交叉反應,例如來自胎兒腎上腺區的類固醇單硫酸鹽,主要是17-羥基孕烯醇酮硫酸鹽導致免疫測定中17-羥孕酮水平錯誤升高[27];(2)LC-MS/MS在提取過程中加入了內標液,可以有效提升檢測特異性。
3 LC-MS/MS在CAH診斷中的應用現狀
新生兒篩查目的在于在癥狀出現之前盡早發現并準確診斷CAH等先天性疾病,而通常所用的免疫分析法(一級篩查)常常出現假陽性,增加了患者的心理負擔和經濟壓力。2018年由美國內分泌學會專家組發布的21-OHD臨床實踐指南(第二版)與2010年發布的第一版指南比較,新增新生兒篩查時推薦一級篩查采用常規方法檢測17-羥孕酮,并推薦了優先采用LC-MS/MS進行二級篩查,不推薦其他方法(如基因分型),以此提高CAH篩查的陽性預測值[28-29]。SCHWARZ等[30]發現CAH患病率和血清17-羥孕酮水平隨著新生兒體質量增加而降低,皮質醇的水平隨采樣時年齡不同而發生明顯變化,未觀察到17-羥孕酮或雄烯二酮與年齡有明顯相關性。值得注意的是雄烯二酮是較敏感的雄激素,并且其水平較17-羥孕酮穩定,且受皮質醇替代治療時給藥間隔時間的影響較少,也不受性別、疾病類型和抽血時間的影響,與17-羥孕酮有較好的相關性。在這項研究中作者證實(17-羥孕酮+雄烯二酮)/皮質醇是CAH的最佳判別方法,但若二者比值大于4時需注意是否在采樣之前使用了糖皮質激素類藥物,避免假陰性結果的發生。
2010年歐洲內分泌協會臨床指導委員會制訂的21-OHD臨床應用指南[28]指出經典型CAH患者17-羥孕酮水平通常高于300 nmol/L,非經典型CAH患者17-羥孕酮水平在6~300 nmol/L,當17-OHP<6 nmol/L時不支持CAH診斷。因此根據17-羥孕酮檢測水平對CAH疾病準確分型,進而輔助臨床精準治療具有重要意義。AMBROZIAK[31]等證明了與LC-MS/MS比較,免疫分析法檢測17-羥孕酮可能會增加非經典型CAH假陽性診斷的風險。由此可見,LC-MS/MS檢測17-羥孕酮在CAH診斷分型中具有重要意義。
目前,臨床多將17-羥孕酮水平是否升高作為新生兒篩查時判斷是否患21-OHD的首要指標,但表1中其他形式的CAH也可能導致檢測到17-羥孕酮水平升高[32]。由圖1可看出21-OHD患者缺乏21-羥化酶會使17-羥孕酮的下游產物11-脫氧皮質醇水平降低,21-脫氧皮質醇水平升高。因此,有研究者提出21-脫氧皮質醇作為21-OHD的另一標志物,那么21-脫氧皮質醇是否可以在一定程度上取代17-羥孕酮在21-OHD診斷中的地位有待研究。JANZEN等[33]建立的LC-MS/MS不僅避免了免疫分析法診斷CAH時的假陽性高的問題,還發現可以通過計算(17-羥孕酮+21-脫氧皮質醇)/皮質醇的數值進一步提高LC-MS/MS的靈敏度,在242 500例新生兒中,1 609例初篩試驗陽性,而通過計算確定了其中已確診的16例21-OHD患者,沒有誤報。由此可見,在二級篩查時可更多關注21-脫氧皮質醇的水平變化,并且選擇合適的計算公式來提高檢測方法的靈敏度,這也為CAH的診斷提供了新思路。
4 結 論
綜上所述,類固醇激素水平精準定量檢測對于CAH的診斷和確切分型具有重要意義。LC-MS/MS最主要的優勢就是高通量、靈敏度高、特異性強、檢測標本多樣、檢測動態范圍寬等,目前有望取代免疫分析法。但由于LC-MS/MS標本處理操作復雜,自動化程度較低,需要操作人員進行規范化培訓才可應用于臨床。因此,簡化標本處理操作流程、實現全自動化是目前面臨的挑戰,也是研究的焦點。

