模擬苯胺廢水的臭氧氧化過程初探
周 珉,羅西子
(上海化學工業區中法水務發展有限公司,上海 201507)
0 引言
苯胺是染料、樹脂、橡膠加工、醫藥化工等領域中的一種常見原料,易在生產過程中隨各類污水排放,一旦進入環境會對水體環境產生嚴重污染作用,甚至危害人體的免疫系統,神經系統等[1-2]。
苯胺廢水的處理方法有很多,常見的物理處理法包括溶劑萃取法、吸附法、液膜法等,化學處理法有濕式氧化法、芬頓氧化法、電化學氧化法等,生物法也常被應用于低濃度苯胺廢水的處理[3-4]。眾多方法中,臭氧工藝具有氧化性強,氧化速率快,殺菌效果好,無二次污染的特點,是一種有效的苯胺廢水處理工藝[4]。
現階段對于影響臭氧處理苯胺廢水的因素的研究有很多,研究方向多為不同初始工藝條件對苯胺去除的相關研究[5]。但從工程設計角度上,則更關注苯胺在去除過程中水質指標的變化趨勢。因此,本文通過對模擬苯胺廢水進行靜態臭氧氧化實驗,研究了廢水在反應過程中苯胺、色度、pH值、氨氮、COD、TOC等指標的變化,并探討和驗證了臭氧氧化苯胺廢水的反應機理,為工程設計提供相應的實驗數據和理論支撐。
1 實驗材料和測試方法
1.1 實驗材料
苯胺,AR(滬試),純度≥99.5%;碘化鉀,AR(滬試),純度≥99%;五水硫代硫酸鈉(Na2S2O3·5H2O),AR(滬試),純度≥99 %;異丙醇,HPLC(滬試),純度≥99.7%;淀粉;H2SO4;NaOH等。藥劑均采購于國藥集團化學試劑有限公司。
使用純水配置苯胺溶液,水質信息如表1所示。
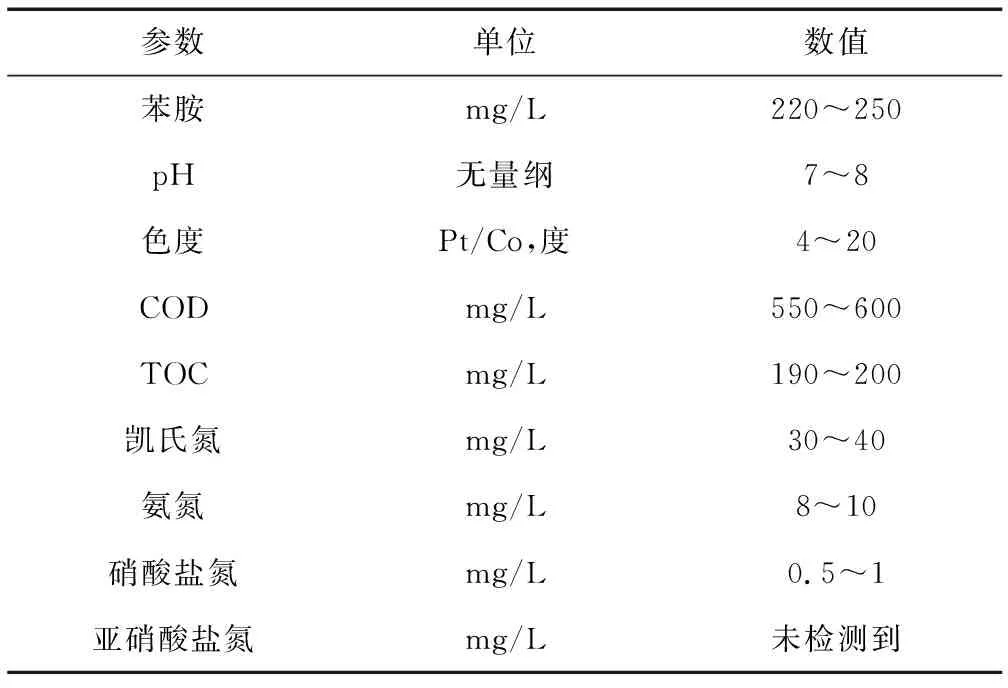
表1 苯胺廢水水質參數
苯胺和硝基苯采用GB/T 11889—1989《N-(1-萘基)乙二胺偶氮分光光度法》測定;pH值采用GB 6920—86《水質pH值的測定 玻璃電極法》測定;色度采用分光光度計測定;COD采用USEPA410.4《重鉻酸鉀消解后分光光度法》測定;TOC采用TOC儀測定,參考HJ 501—2009《水質 總有機碳的測定 燃燒氧化—非分散紅外吸收法》;氨氮和凱氏氮使用凱氏定氮儀測定,參考HJ537《水質 氨氮的測定 蒸餾-中和滴定法》;硝酸鹽氮采用HACH10020《變色酸法》測定;亞硝酸鹽氮采用GB/T 7493《水質 亞硝酸鹽氮的測定 分光光度法》測定;臭氧濃度采用碘量法測定,參考CJ/T 3028.2—94《臭氧發生器臭氧濃度、產量、電耗的測量》[6]。
1.2 實驗裝置
實驗在定制的帶有臭氧曝氣頭的4 L玻璃反應器中進行。選用奧宗尼亞LAB-2B臭氧發生器,以高純度氧氣為氣源,臭氧通過定制的曝氣頭通入反應器底部,隨后從反應器頂部逸出。反應后臭氧尾氣使用碘化鉀(KI)溶液吸收。實驗裝置如圖1所示。
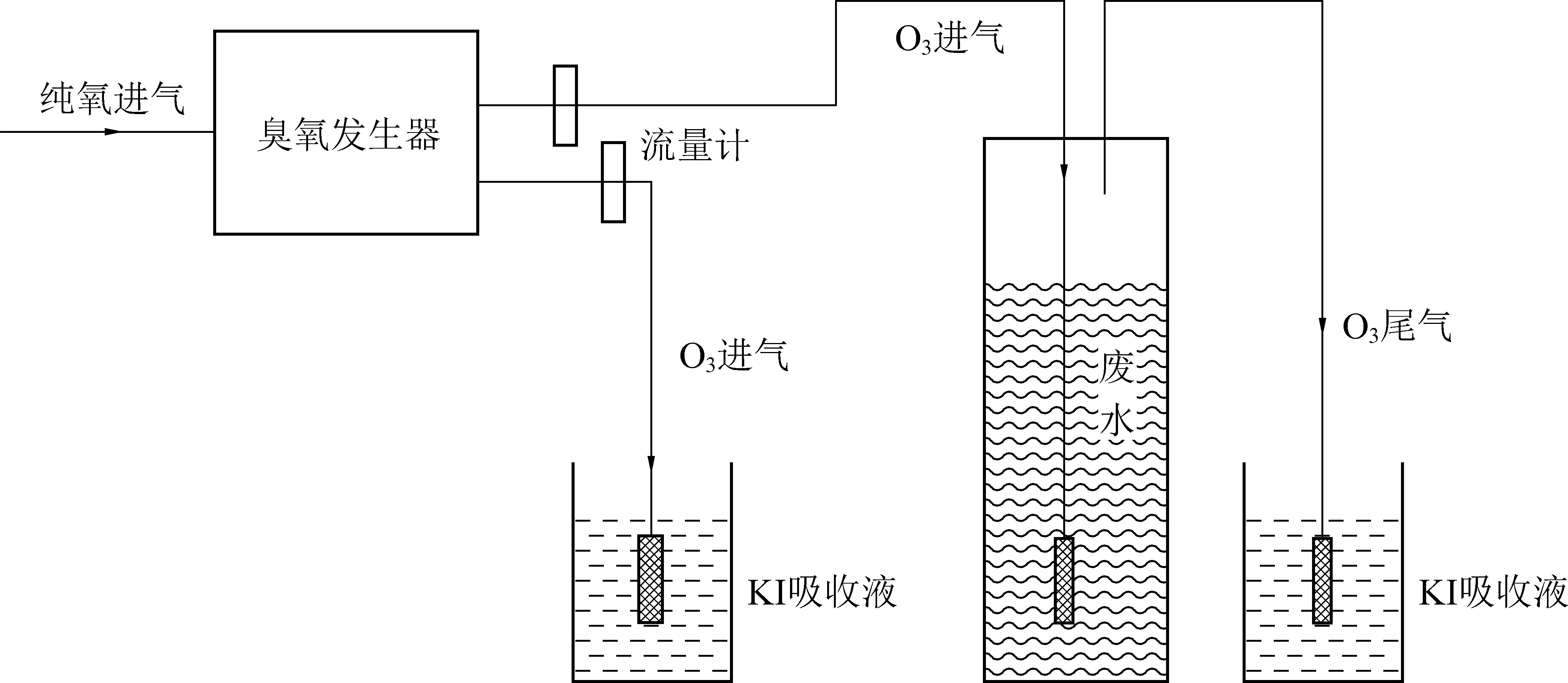
圖1 臭氧實驗裝置
1.3 實驗方法
所有反應均在室溫下進行。反應進行70 min,每10 min從反應器中部取樣,測定臭氧進、出氣濃度以及苯胺廢水相關水質指標,水質檢測參數包括苯胺、色度、pH值、氨氮、凱氏氮、硝酸鹽氮、亞硝酸鹽氮、硝基苯、TOC、COD。
2 結果與討論
2.1 反應過程中色度和苯胺濃度的變化
隨著反應的進行,觀察到廢水的顏色經歷了從無色到紅色再到無色的過程,廢水色度的變化和反應過程中苯胺的去除效果如圖2所示,苯胺初始濃度為227.6 mg/L,當臭氧消耗量達到60 mg/L時,廢水鉑鈷色度由4度上升至2 060度,隨后持續降低至50度以下,這可能是由于反應過程中生成了紅色的中間產物,隨后中間產物被進一步降解為無色化合物[7-8],色度再次被去除。與此同時,廢水中苯胺的濃度隨著臭氧的投加和消耗呈持續下降的趨勢,當臭氧消耗量達到116 mg/L時,苯胺去除率達到99.9%,色度47度。

圖2 臭氧對苯胺廢水苯胺及色度的去除效果
根據實驗結果可以看出,反應過程中廢水色度和苯胺的去除率并不同步。色度指標呈現先升后降的現象。因此在實際工程設計時,需通過實驗室小試確定合適的臭氧投加量以同時滿足色度和苯胺指標的相關要求。如果一味地按照苯胺的去除效果設計投加量,出水的色度可能較原水出現明顯的上升,對廢水排放情況造成風險;如果按照廢水色度的去除效果設計臭氧投加量,也可能存在過量投加的情況,造成浪費及運行成本上升。
2.2 反應過程中pH變化
與2.1相同的實驗條件下,隨著反應的進行,廢水pH值由初始的7.6逐漸降低至3.4,如圖3,主要是因為反應過程中苯胺逐漸被降解,生成并積累了酸性副產物[9]。
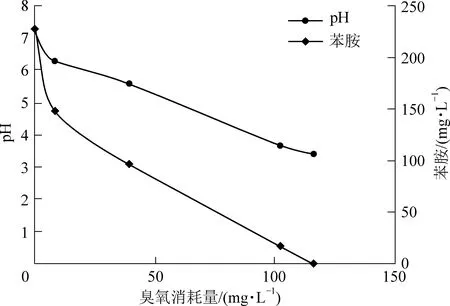
圖3 臭氧過程中pH的變化
為了考察pH對反應過程的影響,同時進行了另一組實驗,向初始pH值分別為3、5、7、9、11時的苯胺廢水中通入濃度為75 mg/L的臭氧,測得的苯胺去除效果如圖4,當初始反應pH值低于5時,苯胺的去除速率小于初始pH值高于7時;去除每毫克苯胺所消耗的臭氧量也更多。這可能是因為臭氧降解有機物的過程包括直接氧化和間接氧化,前者是臭氧分子直接與有機物發生反應,后者是指反應過程中,臭氧會誘發生成羥基自由基(·OH),由·OH與有機物發生反應[10-11],·OH是一種具有更高的電極電勢的氧化性物質,能提高臭氧的氧化效率,在堿性溶液中,臭氧能加速誘發·OH生成,在酸性條件下,·OH的生成會減緩,反應效率降低[12]。
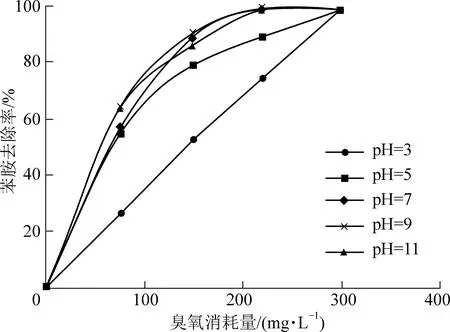
圖4 不同初始pH下苯胺去除率
根據圖3,當臭氧累計消耗量達到102 mg/L時,廢水pH值降低到了3.7,此時殘留苯胺濃度為17.1 mg/L,去除剩余苯胺時去除效率降低,所需的臭氧投加量較之前會大幅度增加。因此工程設計中,需考慮在臭氧氧化過程中pH的變化情況對構筑物、管道、設備腐蝕程度的影響以及通過實驗室小試選擇合適的pH反應條件。此外,由于pH在反應過程中持續降低,也可考慮在反應過程中通過酸堿自動投加系統控制整個反應過程中pH保持在合適條件下進行,以尋求最佳的臭氧投加量和臭氧利用率。
2.3 反應過程中氮類指標的變化
與2.1相同的實驗條件,反應過程中氮指標的變化如圖5。根據實驗結果,氨氮濃度逐漸升高(由7.65 mg/L升高至23.33 mg/L),總氮、亞硝酸鹽氮和硝酸鹽氮的濃度無明顯變化,這表明在臭氧過程中有機氮逐漸轉變為氨氮,但氨氮并沒有進一步被氧化為亞硝酸鹽氮或硝酸鹽氮。由圖6可知反應過程中也沒有明顯的硝基苯生成(濃度在0~1.3 mg/L之間)。這是因為反應過程中臭氧主要攻擊苯胺的苯環而非氨基[13]。臭氧對有機物的進攻是一種親電子攻擊,且臭氧易與C=C雙鍵發生反應,即攻擊苯環上電子云密度更高的區間[14];而苯胺所帶氨基的Π軌道會與苯環上的P軌道形成共軛體系,導致連接處的電子向氨基轉移,連接處電子云密度降低,則臭氧或羥基自由基會更容易攻擊氨基的鄰對位,破壞苯環結構[15]。
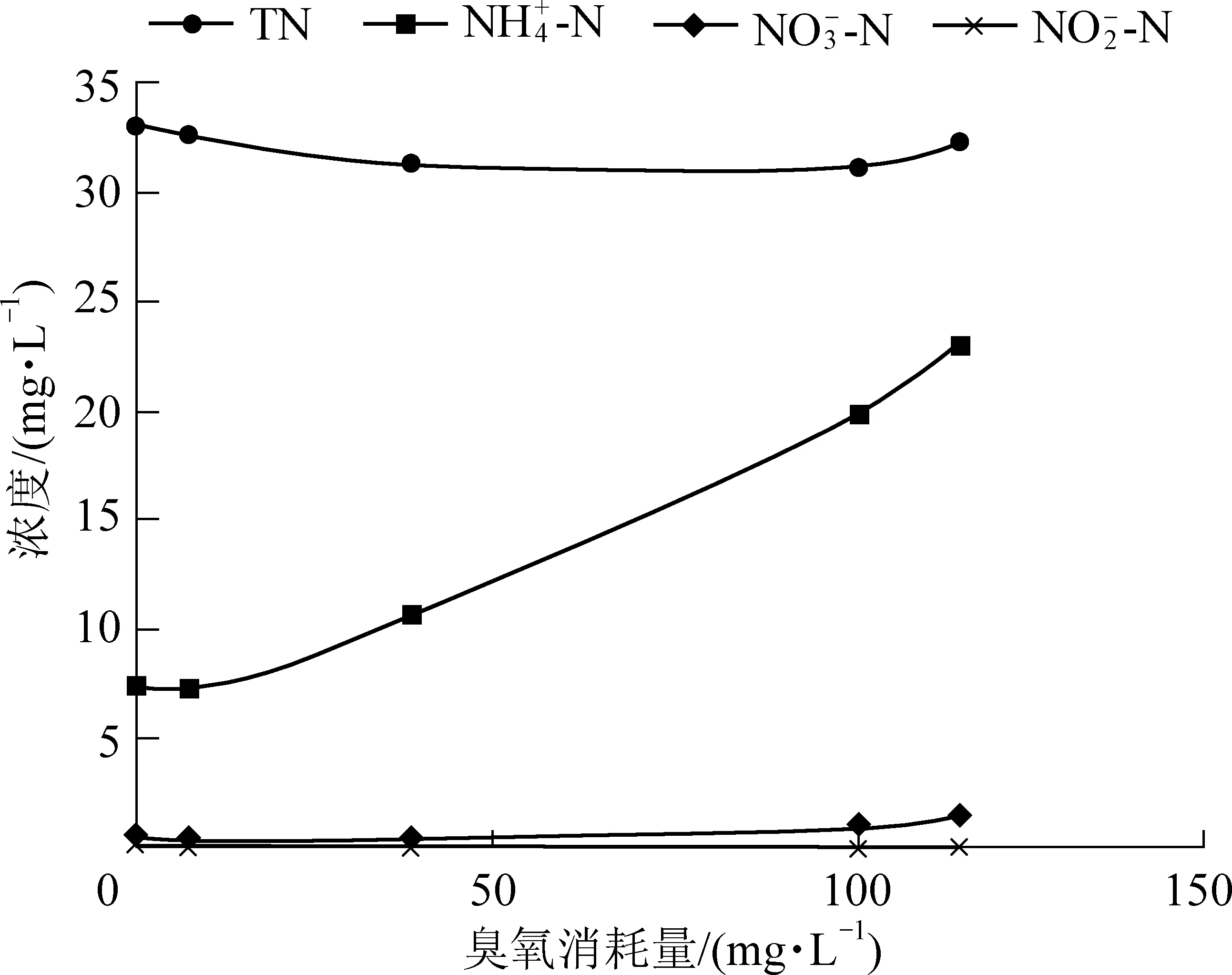
圖5 臭氧對苯胺廢水氮指標的去除效果
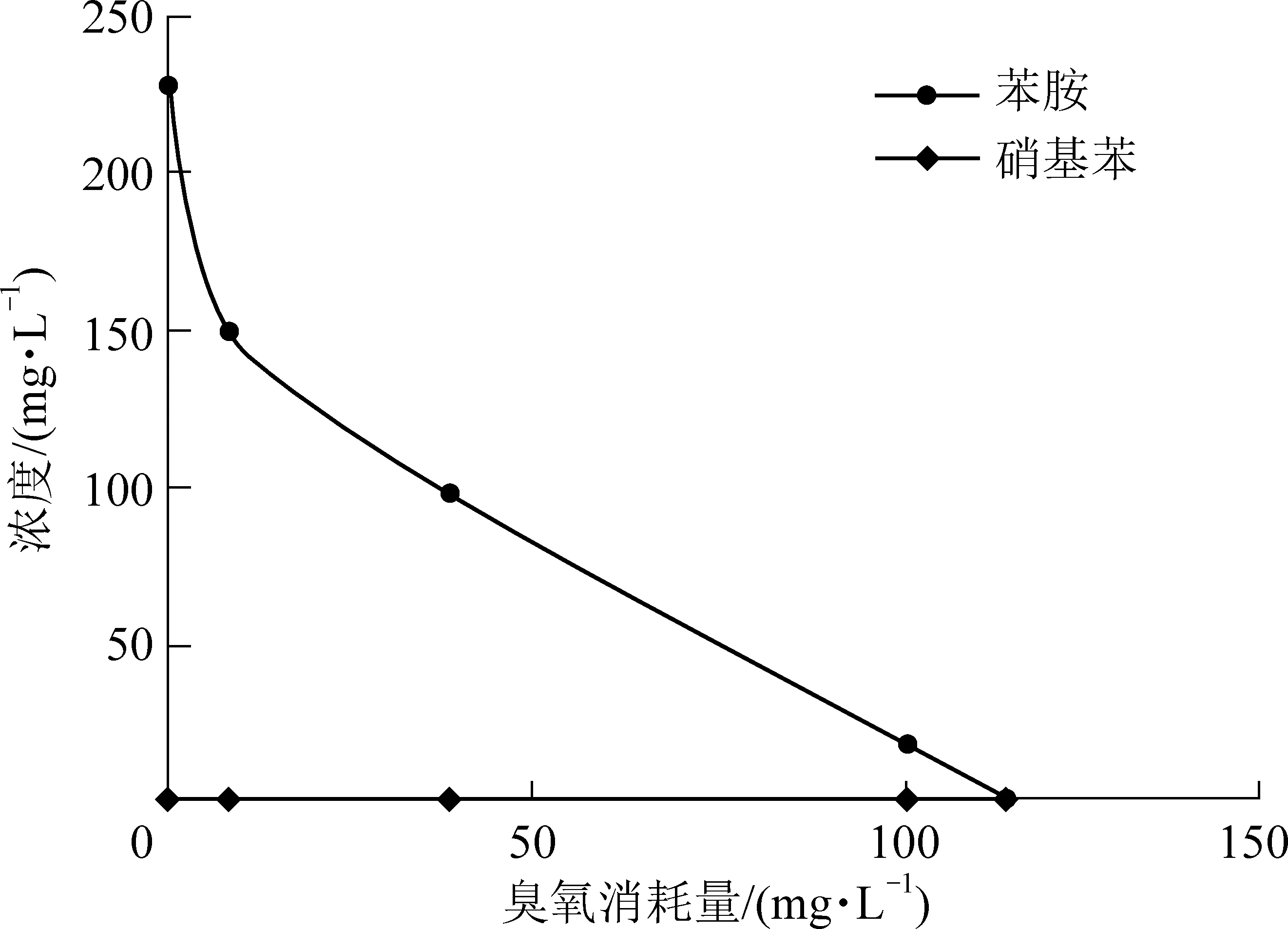
圖6 反應過程中苯胺和硝基苯的變化曲線
2.4 反應過程中TOC和COD的變化
與2.1相同的實驗條件,反應過程中的TOC和COD變化如圖7。當臭氧消耗量達到116 mg/L時,廢水的COD去除率達到64.5%(由初始605 mg/L降低至215 mg/L),TOC去除率僅為10.8%(由188.8 mg/L降低至168.5 mg/L)。這是因為苯胺及其中間產物在臭氧的作用下轉變為了其他小分子有機物,但并未完全被氧化為CO2和H2O[16],即苯胺物質通過臭氧氧化反應后礦化率不高、但有機物轉化率較高。
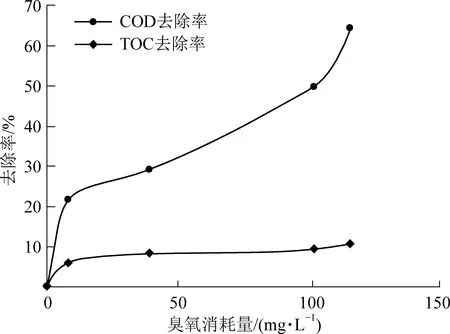
圖7 臭氧對苯胺廢水COD及TOC的去除效果
若需提高反應礦化率,需考慮采用臭氧耦合工藝,如臭氧-過氧化氫、臭氧-催化劑等方式進行實驗室小試或中試確定去除效果。但在實際工藝設計中,需盡可能羅列所有法律法律要求的水質指標,進行相應實驗并取得分析數據后決定工藝可行性。切忌不能僅由單一指標或部分指標進行工藝參數的確定。
3 機理探究
通過向臭氧反應器內投加羥基自由基猝滅劑,來考察臭氧氧化苯胺的過程是直接氧化還是間接氧化。實驗條件:溫度室溫;苯胺初始濃度196 mg/L;兩組實驗分別投加和不投加10 mg/L的異丙醇作為羥基自由基猝滅劑[17-18],得到的對比結果如圖8。投加異丙醇后苯胺的降解速率降低,但隨著臭氧投加量的增大,最終苯胺去除率仍能達到98%以上,這表明苯胺的氧化是臭氧直接氧化和間接氧化共同作用的過程,但臭氧直接氧化為主要過程。
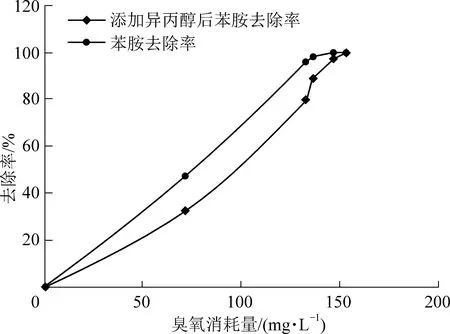
圖8 投加異丙醇后苯胺去除率變化曲線
羅雙[19]在其研究中指出,臭氧與苯胺發生反應后,苯胺首先會開環,苯醌開環后生成氨基苯酚和苯醌亞胺等物質,隨后,這兩種物質在臭氧的作用下聚合生成茚苯胺。與此同時,苯醌亞胺在臭氧作用下開環,開環產物在苯胺的存在下又會生成亞胺類物質,最終,這些中間產物都被臭氧氧化為馬來酸,草酸等小分子酸類[20-21],反應流程如圖9所示。這也解釋了實驗2.1至2.3的現象,即
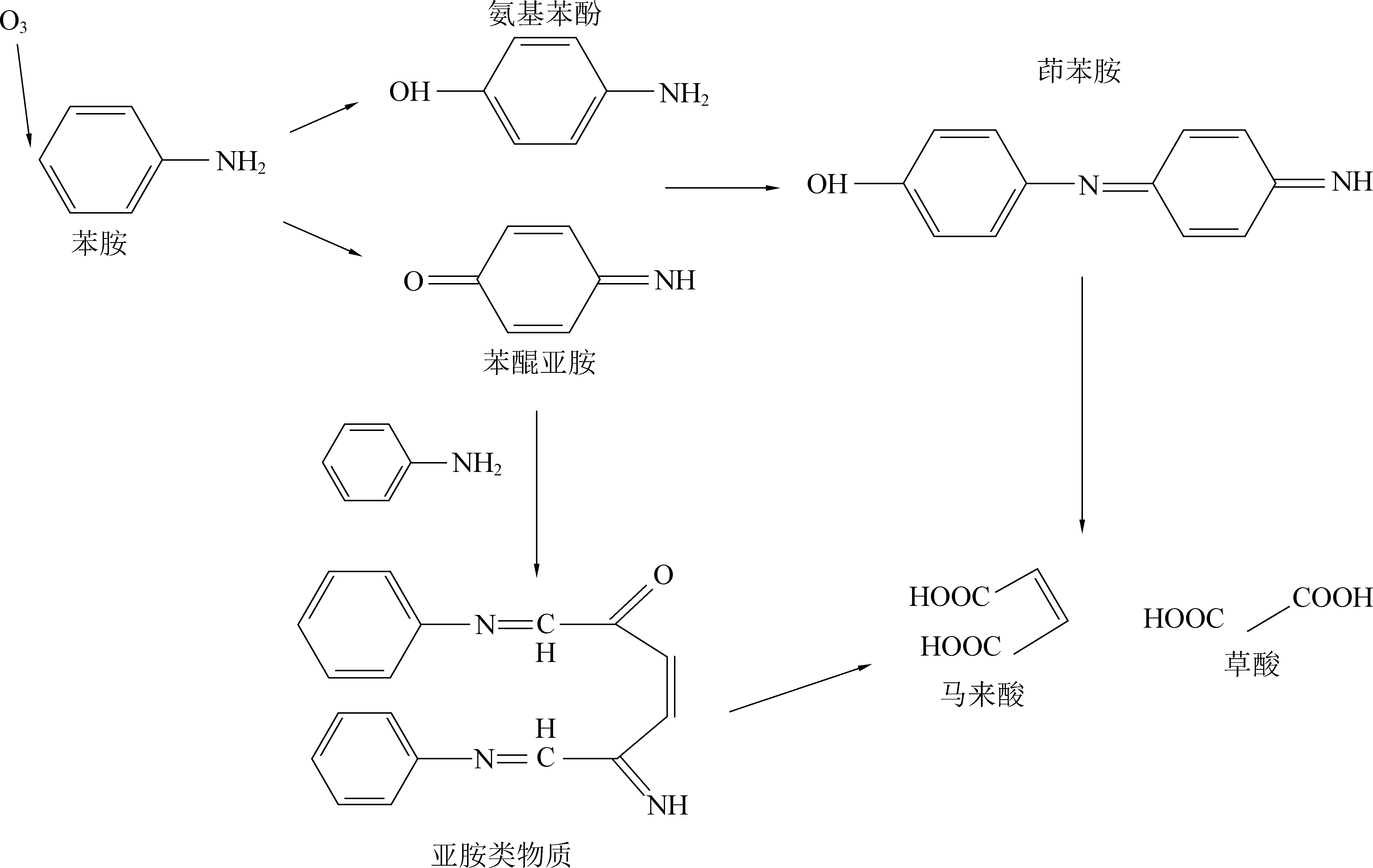
圖9 苯胺與臭氧反應機理
(1)反應過程中生成了紅色的醌類物質和紅棕色的亞胺類物質苯醌亞胺,隨后這類物質又被氧化為無色的小分子酸。因此,反應過程中的色度先上升,后下降。
(2)反應終點生成了馬來酸,草酸等,且這些小分子酸類逐漸積累,導致pH值下降;因此,反應過程中pH值持續降低。
(3)反應過程中氨基并非臭氧主要攻擊對象,苯胺反應過程中的副產物主要是醌類和亞胺類,并非硝基苯類物質;因此,反應后硝基苯物質濃度不高,且由于亞胺類物質的生成導致有機氮并非完全轉化為氨氮。
4 結論
本文利用模擬苯胺廢水進行靜態臭氧氧化小試實驗,得出了下述在工程設計中需考慮的內容,主要包括:
(1)臭氧氧化苯胺廢水的過程中,根據試驗結果,苯胺去除率隨臭氧投加量的增大而上升,當臭氧投加量達到116 mg/L時,苯胺去除率達到99.9%。反應過程中色度呈現先上升后下降趨勢,色度最大值達到2 060度;pH值從7.6下降至3.4;有機氮逐漸轉變為氨氮,但氨氮并沒有進一步被氧化為亞硝酸鹽氮或硝酸鹽氮,且反應過程中無明顯硝基苯生成;COD去除率達到64.5%,TOC去除率僅為10.8%。
(2)根據上述試驗結果,工程設計中需要關注多個關聯水質指標的變化,而不能僅關注單一指標。實驗結果表明,苯胺在氧化過程中pH、COD、TOC、苯胺、氮類、色度等相關指標均呈現不同的變化趨勢。若只關注其中一個指標,可能導致其余指標經反應后存在超標的風險。
(3)工程設計前需進行實驗室小試的驗證。工程設計不能完全依靠經驗或相似案例進行設計,需通過相關實驗預先積累相關數據后方能設計出經濟和技術層面均可行的工藝,滿足相關法律法規的要求。

