多模態超聲檢查對小肝癌的診斷價值及與病理分級的關系
于瑞娜,董 剛,張喜梅,李 燕,丁 璐
鄭州大學第一附屬醫院超聲科 鄭州 450052
肝癌是臨床常見的惡性腫瘤,具有較高的發病率和病死率[1]。調查[2]表明,我國新發肝癌人數和死亡人數均占全球總數的50%以上,肝癌對國民健康造成極大威脅。小肝癌是指早期肝癌或亞臨床肝癌,單個癌結節最大直徑≤3 cm或2~3個癌結節直徑之和≤3 cm,此類患者通常無明顯癥狀體征,具有較好的預后,及時診斷對于早期治療、降低病死率有重要意義[3]。病理學方法是診斷小肝癌的金標準,而術前診斷以無創影像學技術為主[4]。目前臨床診斷肝癌的影像學方式有CT、MRI、超聲等;CT、MRI因價格昂貴且有輻射,存在一定的局限性;超聲檢查以安全、無創、無輻射、分辨率高、可實施動態掃查等成為臨床首選[5]。近年來彈性成像、超聲造影、多普勒超聲技術的應用使超聲技術更加豐富,形成了多模態超聲模式,進一步提升了超聲的診斷能力。目前多模態超聲在惡性腫瘤中相關的研究[6]主要集中于乳腺癌、甲狀腺癌等,在小肝癌方面的研究較少,故作者進行如下研究,分析多模態超聲檢查對小肝癌的診斷效能及其與病理分級的關系,以期為小肝癌的早期診斷提供參考。
1 對象與方法
1.1臨床資料選取2017年5月至2019年5月在鄭州大學第一附屬醫院就診的疑似小肝癌且符合納排標準的92例患者。納入標準:①有慢性乙肝或丙肝病史。②初診患者,影像學檢查前未接受抗腫瘤相關治療。③實施多模態超聲檢查(彩色多普勒超聲、超聲造影、超聲彈性成像),單個占位病變直徑≤3 cm或2~3個病灶直徑之和≤3 cm。排除標準:①妊娠期、哺乳期女性。②合并其他部位惡性腫瘤。研究在實施前已獲得醫院倫理委員會批準(2017-XY-002),患者本人對研究內容均知情同意。92例患者中男58例,女24例;年齡23~80(48.4±12.3)歲;單發病灶68例,多發病灶24例;病灶直徑0.8~3.0(2.0±0.5) cm。
1.2超聲檢查方法和多模態超聲診斷標準使用日立HIVSION Preirus 彩色超聲檢查系統(凸陣探頭,頻率3~5 MHz;高頻線陣探頭,頻率5~10 MHz)。常規二維超聲掃查肝臟形態,觀察病變數量、形狀、大小、位置、邊界、內部回聲等。采用多普勒超聲模式觀察病灶血流信號并進行血流分級。啟動超聲彈性成像模式觀察病灶周圍肝組織的硬度,感興趣區域調節至病變大小的2~3倍,切面選擇避開肝內大血管和肝管,并進行彈性成像評分。超聲造影:以5 mL生理鹽水稀釋超聲造影劑(意大利BRACCO公司)原液后抽取2.4 mL經上肘靜脈團注法注射,連續觀察病灶5 min,強化過程分為動脈期(0~40 s)、門脈期(41~120 s)和實質期(120 s后),造影完成后回放觀察占位病變增強模式。
病灶血流分級標準[7]:0級為無血流信號;1級為1~2個點狀或絮狀血流信號;2級為3~4個點狀血流信號或1個長度超過病灶半徑的條狀信號;3級為≥5個點狀或≥2個長條血流信號。0~1級為良性;2~3級為惡性。
超聲造影[8]:依據病灶動脈期強化特征分為非特征性強化、不強化和強化,根據延遲期及門靜脈期的廓清特征分為非特征性廓清、不廓清和廓清,根據廓清與強化特征進行肝癌診斷:陽性、陰性及不確定診斷,未觀察到的病灶作為不強化、不廓清及陰性診斷。
彈性成像評分標準[9]:1分為病灶與周圍組織區域為均勻的綠色;2分為病灶區以綠色為主;3分為病灶區為藍綠相間或以藍色為主;4分為病灶全部為藍色;5分為病灶全部為藍色且病灶周圍組織存在少部分藍色。1~3分為良性;4~5分為惡性。
多模態超聲診斷:以各單個超聲技術診斷結果全部判斷為惡性,則為超聲多模態診斷惡性;否則為良性[10]。超聲多模態檢查結果由2名工作經驗≥5 a的超聲科醫生共同診斷,診斷結果不一致時經科室討論分析統一診斷意見。
1.3肝癌診斷及病理分級小肝癌診斷標準參照《原發性肝癌診療規范(2011年版)》[11],經穿刺活檢或手術切除組織經病理組織學和(或)細胞學檢查結果確診。小肝癌病理分級參照Edmondson-Steiner四級法[12]分為高分化(Ⅰ級)、中分化(Ⅱ級)、低分化(Ⅲ、Ⅳ級)。
1.4統計學處理采用SPSS 25.0進行數據分析,應用χ2檢驗或Fisher精確概率法分析良惡性結節多模態超聲征像和不同病理分級小肝癌的多模態超聲征像的差異,應用Kappa檢驗分析二維超聲、多普勒超聲、超聲彈性成像、超聲造影、多模態超聲對小肝癌診斷結果的一致性。檢驗水準α=0.05。
2 結果
2.1病理結果92例患者共發現結節102個,病理診斷為惡性結節75個(69例),良性(肝硬化)結節27個(23例)。75個惡性結節病理分級診斷為低分化35個(32例),高、中分化40個(37例)。
2.2良惡性結節多模態超聲征像對比見表1。惡性結節形狀不規則、邊界不清晰、內部回聲不均勻、后方回聲不變/增強、血流分級1~2級、超聲彈性評分4~5分、超聲造影增強方式快進快出占比高于良性結節。
2.3不同超聲技術對小肝癌的診斷結果見表2。多模態超聲診斷小肝癌特異性均高于二維超聲、多普勒超聲、超聲彈性成像、超聲造影,差異有統計學意義(χ2=25.729、15.600、13.886、5.283,P<0.05),且約登指數均高于二維超聲、多普勒超聲、超聲彈性成像、超聲造影。經Kappa一致性檢驗,多模態超聲診小肝癌與病理結果的一致性較好。
2.4不同病理分級小肝癌的多模態超聲征像對比見表3。惡性結節中低分化病灶形態不規則、邊界不清晰、內部回聲不均勻、后方回聲不變/增強、血流分級1~2級、超聲彈性成像評分4~5分、增強方式為快進快出占比高于高中分化。
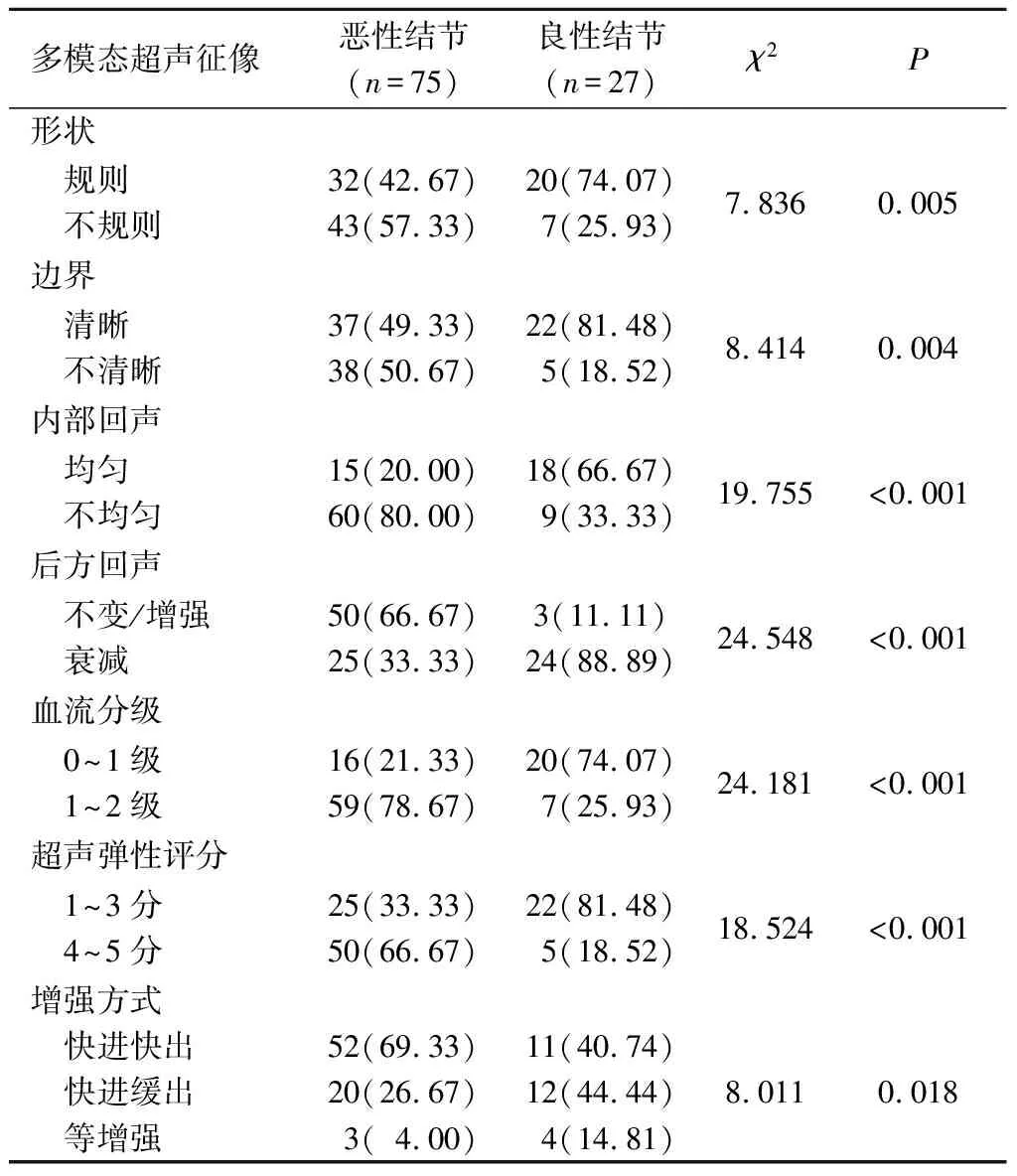
表1 良惡性結節多模態超聲征像對比 例(%)

表2 不同超聲技術對小肝癌的診斷結果
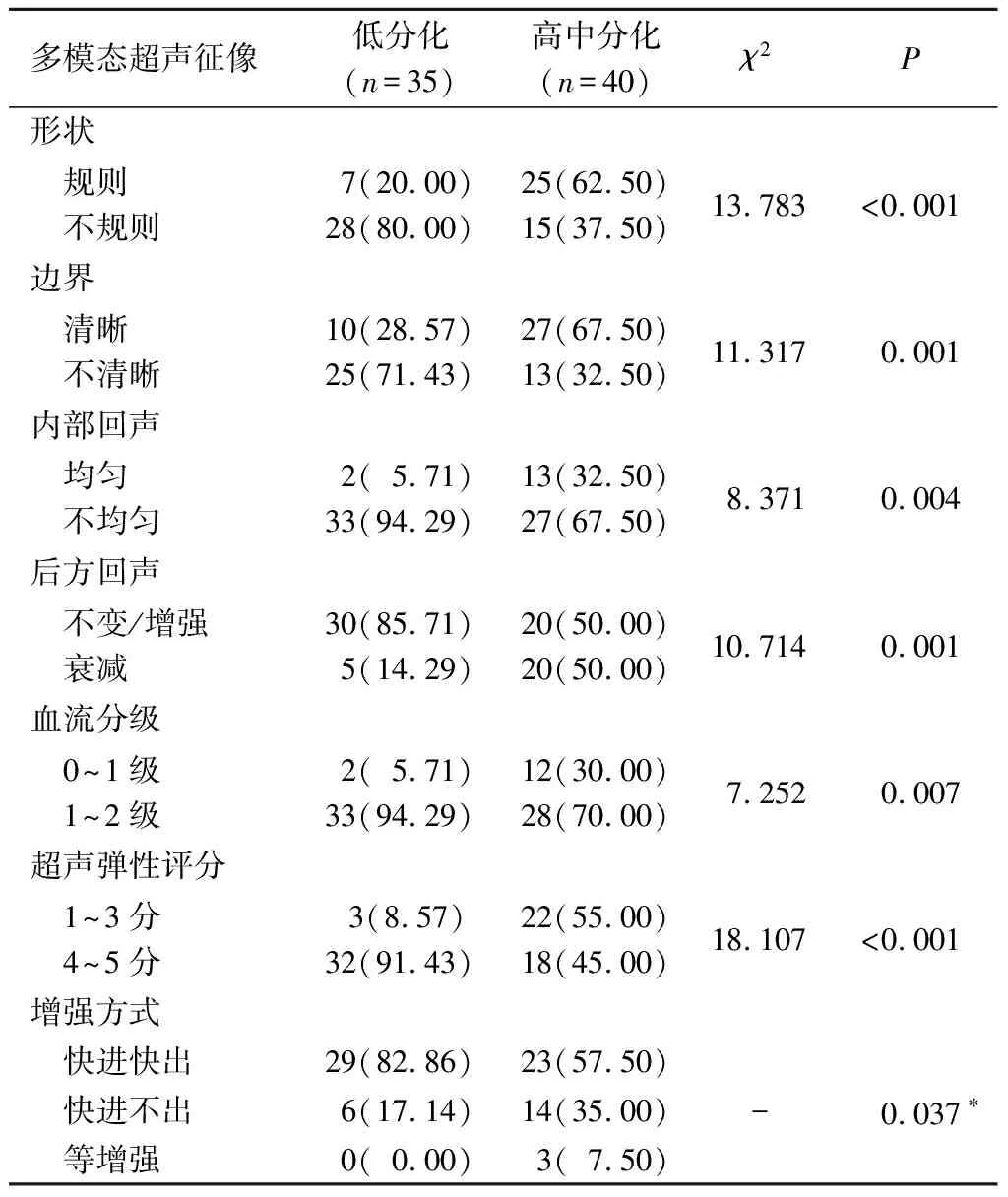
表3 不同病理分級小肝癌的多模態超聲征像對比 例(%)
3 討論
腹部超聲以圖像直觀、操作方便、安全無創和價格低廉的優勢成為肝臟檢查的首選,該方式可明確肝內有無占位性病變,判斷病變位置、性質及與肝內重要血管關系,對于指導臨床治療方式的選擇、手術方案的制定有重要價值[13]。雖然超聲輔助診斷肝癌具有多種優勢,但受病灶解剖部位、操作手法、操作者經驗、儀器設備等因素影響,其敏感性和準確定受到一定影響。隨著超聲影像學技術的發展,超聲診斷技術不斷豐富,形成了多模態超聲檢查,實現了各種單項技術的優勢互補,使超聲診斷能力大大提升,為惡性腫瘤的診療提供了幫助[14]。
本研究以病理診斷結果為金標準,多模態超聲征像中形狀不規則、邊界不清晰、內部回聲不均勻、后方回聲不變/增強、血流分級1~2級、超聲彈性評分4~5分、超聲造影增強方式快進快出在惡性結節中的檢出率高于良性結節;且多模態超聲診斷小肝癌的特異性、約登指數均高于二維超聲、多普勒超聲、超聲彈性成像、超聲造影。多模態超聲與病理結果具有較高的一致性,說明多模態超聲可提升小肝癌的術前診斷水平。
超聲檢查技術是利用超聲波特性及人體不同組織對超聲反射不同而產生的聲阻抗差異,從而對人體組織的形態、結構、物理特性及功能狀況作出判斷[15]。常規二維超聲組織分辨率高、重復性強,常用于胸腹部惡性腫瘤的早期篩查;多普勒超聲是在二維超聲的基礎上增加對檢查部位血流動力學信息的判斷,更利于對病灶性質的診斷[16];超聲彈性成像是對常規二維超聲的補充,主要以軟組織的彈性大小為參量反映病灶及組織的軟硬度,豐富了病灶形態特征和軟硬程度的信息[17];超聲造影是利用造影劑在血液循環中產生二次諧波信號成像,顯示病灶的循環灌注情況,并運用超聲造影動態圖像后處理分析,對病灶性質進行判斷[18]。小肝癌作為早期肝癌,其病灶聲學特征與周圍肝實質存在重疊,單純應用一項超聲技術診斷存在漏診或誤診可能。多模態超聲由二維超聲、多普勒超聲、彈性成像及超聲造影技術共同構成,結合了各項超聲技術的優勢,為病灶的判斷提供更多客觀依據,提升了超聲診斷能力,具有更好的診斷效能,此觀點在張明博等[10]研究中亦得到證實。
肝癌病理分級是評估預后的重要依據,肝癌由異型增生結節發展而來,分化程度越低其異型性越明顯。肝癌組織結構較為致密,存在肝竇結構消失,脂肪變性、組織成分均勻、細胞核密度大的特點。腫瘤細胞具有侵襲特性,其超聲征像表現為形態不規則、內部回聲不均勻[19]。腫瘤分化程度較低者,其細胞間橋不明顯,核異型性明顯,核分裂多伴壞死,與周組織組織粘連導致其活動度降低,超聲彈性成像顯示彈性小、硬度增加[20]。研究[21]表明,微血管密度與腫瘤的分化程度密切相關。高分化者因異型性低,病灶組織內存在部分小梁結構,新生血管滋養較少,動脈供血未發育完善,血流分級低;低分化者惡性程度高,血管內皮因子表達豐富,內部新生血管更多,血流分級更高。肝癌的主要供血動脈為肝動脈,造影后微泡可快速呈團狀增強,后快速退出,以快進快出為強化特征。惡性程度低的高分化癌細胞,由門靜脈和肝動脈雙重供血,造影微泡從門靜脈持續再注入,強化特點為快進慢出或等增強[22]。本研究結果中低分化結節中形態不規則、邊界不清晰、內部回聲不均勻、后方回聲不變/增強、血流分級1~2級、超聲彈性成像評分4~5分、增強方式為快進快出的檢出率均高于高中分化結節,說明小肝癌不同病理分級存在在超聲征像方面存在差異,超聲征象可為小肝癌的病理分級提供參考。
綜上所述,多模態超聲可為小肝癌的診斷提供更加豐富的信息,與病理診斷具有較高的一致性,且能對小肝癌的術前病理分級提供參考。

