Bispora sp. MEY-1來源的嗜酸海藻糖酶TreA酶學性質研究
蔣肖, 涂濤, 王坤, 彤麗格, 羅會穎
(中國農業科學院飼料研究所, 農業農村部飼料生物技術重點實驗室, 北京 100081)
海藻糖是一類非還原型二糖,由兩個α-D-葡萄糖通過α-1,1-糖苷鍵連接而成,通常以二水化合物的形式存在,是所有糖中化學性最不活躍的糖[1]。它廣泛存在于細菌、真菌、昆蟲、植物及藻類等生物體內,可以起到為生物體提供碳源,以及提高細胞耐受性的作用[2]。
海藻糖酶(trehalase,EC3.2.1.28)可以將海藻糖水解產生兩分子的葡萄糖。海藻糖酶廣泛存在于動物、植物和微生物體內,目前已經從多種生物體內分離出來了海藻糖酶基因。根據氨基酸序列相似性、結構相似性等特點,海藻糖酶在碳水化合物活性酶(carbohydrate-active enzymes, CAZy)數據庫中,被歸類到糖苷水解酶(glucoside hydrolase, GH)第15、37和65家族[3-4]。除了畢赤酵母通過海藻糖磷酸化酶分解海藻糖以外,其他真菌系統中都是通過海藻糖酶分解海藻糖,并且對海藻糖具有嚴格的底物專一性。基于海藻糖酶的催化特點,海藻糖酶可以廣泛應用于淀粉多糖制備、食品、臨床醫療和害蟲防治等生物工業中[2,5]。丁春磊[6]研究表明,在燃料乙醇生產過程中,添加海藻糖酶可有效提高乙醇的產率,改善酵母的健康狀態,降低生產成本。劉迎春等[7]對金龜子綠僵菌中的海藻糖酶ReATM1p進行酶學性質鑒定和基因敲除等研究,進一步證明了海藻糖酶在害蟲生物防治中的應用價值。韓雋等[8]研究表明,谷氨酸發酵生產的后期加入海藻糖酶可以提高糖酸轉化率的效果,進而提高谷氨酸的生產量。
根據海藻糖酶酶促反應的最適pH不同,可以將真菌海藻糖酶分為酸性海藻糖酶和中性海藻糖酶[9]。真菌中性海藻糖酶的最適pH為7.0,通常位于細胞胞質中,其酶活性受轉錄調控機制的影響;酸性海藻糖酶最適pH為3.5~6.0,是一種外分泌性糖蛋白,主要位于液泡、細胞壁或者分泌到胞外[9]。除此之外,還有一種源于嗜熱真菌的海藻糖酶,既具有酸性海藻糖酶最適pH反應條件的特點,又具備中性海藻糖酶可被Ca2+或Mn2+激活和被ATP抑制的特點[10-12]。目前,多種性質優良的糖苷水解酶基因資源被成功挖掘并報道,如最適pH為1.5的甘露聚糖酶[14]、最適pH為4.5的木聚糖酶[15]和最適pH為5.0的葡聚糖酶[16]等,人們研究最為清晰的是釀酒酵母中的酸性海藻糖酶。
Bisporasp. MEY-1菌株為本實驗室從酸礦中分離的一株嗜酸真菌,在pH 2.5~3.0的環境中生長情況最好[13]。本研究從嗜酸真菌Bisporasp. MEY-1中克隆了一個海藻糖酶基因TreA并在畢赤酵母GS115中成功實現了異源表達,通過對其酶學性質進行鑒定分析,以期獲得可以應用到工業生產的海藻糖酶,進而豐富海藻糖酶資源。
1 材料與方法
1.1 菌株、載體及試劑
Bisporasp. MEY-1菌株由本實驗室分離,保存在中國普通微生物菌種保藏管理中心(China General Microbiological Culture Collection, CGMCC),登記號為CGMCC250027。Bisporasp. MEY-1的活化和培養條件參照李燁青等[17]方法。基因克隆過程中間載體為pEASY-T3,克隆宿主為大腸桿菌感受態EscherichiacoliTrans-T1,均購自北京全式金生物技術有限公司。海藻糖酶基因TreA外源表達用的載體為pPIC9,表達宿主為畢赤酵母GS115,均為本實驗室保存。試驗中所用的總RNA提取試劑盒購自天根生化科技有限公司;反轉錄試劑盒購自東洋紡生物科技有限公司;細菌質粒提取試劑盒和DNA膠回收試劑盒購自天根生化科技有限公司;限制性核酸內切酶EcoRⅠ,NotⅠ購自TaKaRa有限公司;高保真DNA聚合酶Fast pfu DNA聚合酶購自北京全式金生物技術有限公司;其他試劑,如甲醇、乙醇和乙酸等試劑均購于國藥集團化學試劑有限公司。
1.2 培養基
試驗中所用到的培養基有馬鈴薯葡萄糖固體培養基(PDA)、馬鈴薯葡萄糖液體培養基(PDB)、LB液體培養基、LB固體培養基、MD培養基、YPD培養基、BMMY及BMGY培養基,其詳細配制參照李曉麗等[18]方法;海藻糖酶酶活性測定所用的DNS試劑配制參照李燁青等[17]方法。
1.3 海藻糖酶基因TreA序列分析
根據嗜酸菌株Bisporasp. MEY-1的全基因組序列測序結果,查找到一個新的海藻糖酶基因TreA,并對其進行生物信息學分析。首先,將序列提交給在線網站Softberry(http://linux1.softberry.com/berry.phtml)預測基因的內含子和外顯子,SignalP 4.1 Server (http://www.cbs.dtu.dk/services/SignalP/)預測編碼蛋白質信號肽的序列。然后利用Vector NTI Advance 10.0軟件將基因翻譯為氨基酸序列后,分析其氨基酸序列的長度、蛋白質理論分子質量。最后,將氨基酸序列提交到Expasy.PI(https://web.expasy.org/compute_pi/)預測新海藻糖酶TreA的等電點。
1.4 海藻糖酶基因TreA克隆與畢赤酵母重組載體構建
將嗜酸菌株Bisporasp. MEY-1在PDB培養基、30 ℃培養條件下活化48 h后,轉接到以海藻糖為唯一碳源的誘導培養基中,于30 ℃、210 r·min-1震蕩培養2~3 d,12 000 r·min-1離心10 min收集菌體。根據真菌總 RNA 提取試劑盒說明書提取菌體的總RNA,然后再利用反轉錄試劑盒Rever Tra Ace-a-TM kit將RNA反轉錄為cDNA。根據去除信號肽序列的全長基因設計引物(F: 5′-GCTGAATTCTACGTAGAATTCAAGA-TATATTCGACT-3′;R: 5′-CGAATTAATTCGC-CGGCGGCTCAAATAACCAAGG-3′)(橫線標注分別為限制性酶切位點EcoRⅠ和NotⅠ),然后以cDNA為模板進行PCR擴增。擴增產物經EcoRⅠ和NotⅠ雙酶切,利用T4 DNA連接酶將其連入載體pPIC9后熱擊轉化Trans-T1大腸桿菌感受態,挑取陽性克隆子送測序公司測序,測序正確的重組載體命名為pPIC9-TreA。
1.5 海藻糖酶TreA在畢赤酵母中的表達及純化
利用質粒小提試劑盒提取測序正確的pPIC9-TreA質粒,限制性內切酶BglⅡ將其線性化后,回收產物電擊轉化畢赤酵母GS115感受態細胞。然后將轉化子涂布于MD平板,在30 ℃培養箱中靜置培養48 h后挑取48個克隆子于含有3 mL BMGY培養基的離心管中震蕩培養(30 ℃,220 r·min-1);培養48 h后,4 500 r·min-1離心5 min,將菌體重懸于1 mL含有0.5%甲醇的BMMY培養基中誘導培養48 h。最后,通過酶活性測定獲得陽性克隆子進行搖瓶放大培養。
將篩選的陽性克隆子在YPD培養基中活化培養72 h,按1%的接種量接種于400 mL BMGY培養基震蕩培養48 h后,4 500 r·min-1離心5 min收集菌體轉入200 mL BMMY培養基中誘導培養48 h,每隔24 h補加0.5%甲醇。
誘導培養結束后,12 000 r·min-1離心5 min收集發酵液。將200 mL發酵液經10 kD膜包(Vivascience, Germany)濃縮至15 mL后,發酵液于pH 7.0、10 mmol·L-1檸檬酸-磷酸氫二鈉緩沖液中過夜透析。然后,將透析過的酶液通過陰離子純化柱(HiTrap Q HP)進行純化,收集不同濃度鹽離子洗脫下來的蛋白,并通過SDS-PAGE分析確定純化的單一條帶。
1.6 海藻糖酶TreA酶活性測定
海藻糖酶的酶活性測定采用3,5-二硝基水楊酸(3,5-dinitrosalicylic acid,DNS)法檢測還原糖生成量進行活性分析。具體方法如下:在pH 4.0、60 ℃條件下,1 mL的反應體系包括100 μL酶液和900 μL 1%的海藻糖底物,反應10 min,加入1.5mL DNS終止反應后沸水煮5 min,540 nm下測定OD值。對照組先加終止液,再加酶液。每組三個平行,一個對照。海藻糖酶活性單位定義:在pH 4.0、60 ℃條件下,每分鐘分解海藻糖生成1 μmol還原糖所需要的酶量為1個活性單位(U)。
1.7 海藻糖酶TreA酶學性質測定
測定海藻糖酶最適pH時,將純化的海藻糖酶TreA分別置于60 ℃,不同pH(1.0~12.0,其中pH 1.0~3.0是0.1 mol·L-1甘氨酸-HCl緩沖液;pH 3.0~9.0是0.1 mol·L-1磷酸氫二鈉-檸檬酸緩沖液;pH 9.0~12.0是0.1 mol·L-1NaOH-甘氨酸緩沖液)底物條件下進行酶促反應。測定海藻糖酶TreA的pH穩定性時,純海藻糖酶TreA酶液在不同pH 1.0~12.0緩沖液稀釋后置于37 ℃恒溫水浴鍋中處理1 h,然后在pH 4.0、60 ℃條件下測定其相對剩余酶活,未進行處理酶活為100%對照。
測定海藻糖酶的最適溫度時,純化的海藻糖酶TreA分別在20~90 ℃范圍內,pH 4.0條件下進行酶促反應。測定海藻糖酶TreA的熱穩定性時,純化的海藻糖酶TreA分別在60、65和70 ℃恒溫水浴鍋中分別處理0、2、5、10、15、20、30和60 min后,在pH 4.0、60 °C條件下測定其剩余酶活力,未進行處理的酶活為100%對照。
分別利用pH 4.0、0.1 mol·L-1磷酸氫二鈉-檸檬酸緩沖液配制不同濃度(0.5~10 mg·mL-1)的海藻糖作為反應底物。將純化的海藻糖酶TreA稀釋至合適的濃度分別在不同濃度的底物中反應5 min(pH 4.0、60 ℃),測定其酶活性。將測定的酶活數據利用GraphPad Prism 5.01軟件分析,獲得海藻糖酶TreA的Vmax和Km。
1.8 不同金屬離子或化學試劑對酶活力的影響
在海藻糖底物中分別添加NaCl、LiCl、KCl、AgNO3、HgCl2、MgCl2、MnCl2、Pb(CH3COO)2、NiCl2、ZnCl2、CoCl2、CuCl2、CaCl2、CrCl3、FeCl3、SDS、EDTA,和β-巰基乙醇共18種物質,使其終濃度為5和10 mmol·L-1。然后,在pH 4.0、60 ℃條件下分別測定海藻糖酶在不同底物中的剩余酶活力。以未添加任何物質的反應體系為對照組,計算處理后海藻糖酶TreA的相對剩余酶活,評估各種金屬離子和化學試劑對海藻糖酶TreA酶活力的影響,每組反應設計三個重復。
1.9 海藻糖酶TreA的蛋白酶抗性評估
在純化的海藻糖酶TreA中分別添加胰蛋白酶、蛋白酶K、膠原蛋白酶、糜蛋白酶、枯草蛋白酶和胃蛋白酶,使其終濃度為0.1 mg·mL-1,然后將其置于37 ℃恒溫水浴鍋中分別處理0、30和60 min。在pH 4.0、60 ℃條件下測定其相對剩余酶活,以未添加蛋白酶的反應體系為對照組,來評估海藻糖酶TreA的蛋白酶抗性。
1.10 數據分析
采用Excel 2018和Origin 2017對測定的數據進行處理、計算和差異性分析。
2 結果與分析
2.1 海藻糖酶基因TreA的克隆與序列分析
從嗜酸菌株Bisporasp. MEY-1的基因組中克隆海藻糖酶基因TreA,其cDNA全長序列為3 075 bp,可以翻譯編碼1 024個氨基酸。其編碼的氨基酸序列經在線網站進行信號肽預測,結果表明N端的前21個氨基酸為信號肽序列。TreA成熟蛋白的理論分子質量為109.6 kD,等電點為4.5,屬于糖苷水解酶32家族。海藻糖酶TreA的氨基酸序列經在線網站(http://www.cbs.dtu.dk/services/NetNGlyc/)預測,結果顯示其蛋白質表面共有7個潛在N-糖基化位點,分別為Asn117、Asn154、Asn177、Asn217、Asn274、Asn289和Asn564。在氨基酸組成方面,酸性氨基酸(天冬氨酸和谷氨酸)占9.28%;堿性氨基酸(賴氨酸和精氨酸)占4.88%;極性氨基酸(天冬酰胺、半胱氨酸、谷氨酰胺、絲氨酸、蘇氨酸和酪氨酸)占34.67%;疏水氨基酸(丙氨酸、異亮氨酸、亮氨酸、苯丙氨酸、色氨酸和纈氨酸)占34.47%。將TreA的氨基酸序列在NCBI數據庫中進行序列比對,該基因與Baudoiniapanamericana來源的海藻糖酶序列最為相似,序列一致性為68.9%,顯示了海藻糖酶基因TreA的新穎性。
2.2 海藻糖酶TreA重組載體的表達和純化結果
重組表達載體pPIC9-TreA在畢赤酵母GS1115中成功表達,將篩選的陽性克隆子進行搖瓶表達,獲得的發酵液進行后續的純化處理。粗酶液經濃縮、陰離子純化柱純化等一系列處理后,獲得單一純化峰,并將濃縮液、純化液及Endo H處理的純蛋白分別進行SDS-PAGE凝膠電泳分析。結果顯示,TreA的目的條帶大小為135 kD左右(圖1),經Endo H脫糖基處理后目的條帶降為110 kD左右,與理論分子質量一致。
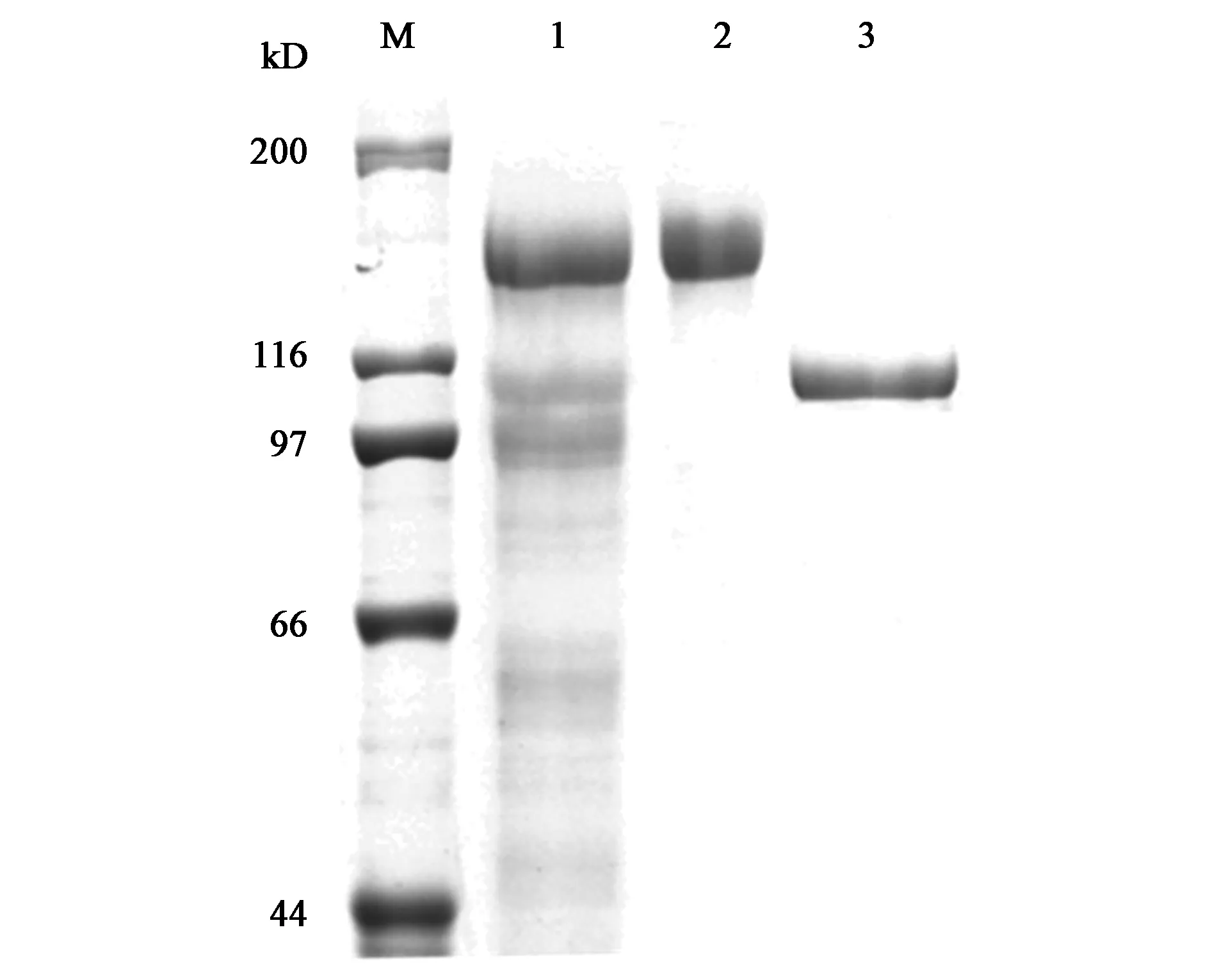
注:M—標準蛋白樣品的特定理論分子質量;1—濃縮后TreA; 2—純化后的TreA; 3—Endo H處理的TreA。Note:M— Molecular weight standard; 1—concentrated TreA with ultrafiltration membrane; 2—Purified TreA; 3—Purified TreA with Endo H.圖1 TreA的SDS-PAGE凝膠電泳分析Fig.1 SDS-PAGE analysis of purified recombinant TreA
2.3 海藻糖酶TreA的酶學性質分析
測定重組海藻糖酶TreA在不同pH緩沖液、50 ℃條件下的酶活性,結果表明,TreA的最適pH為4.0,在pH 2.2~5.0范圍內,該酶能夠維持其60%以上的酶活力,是一種酸性海藻糖酶(圖2A)。TreA在極酸條件下(pH 1.0~3.0)可維持100%的剩余酶活性,pH 4.0~7.0可維持100%的剩余酶活性,隨著pH條件向堿性方向移動,其穩定性逐漸減弱(圖2B)。TreA的最適溫度為60 ℃,在40~70 ℃之間都可以剩余50%以上的酶活力(圖2C),屬于中高溫酶。分析TreA的熱穩定性,在60和65 ℃下分別處理60 min,測定處理后酶液的剩余酶活分別為85%和70%,在70 ℃下處理30 min,依然能夠保持40%的酶活力(圖2D)。
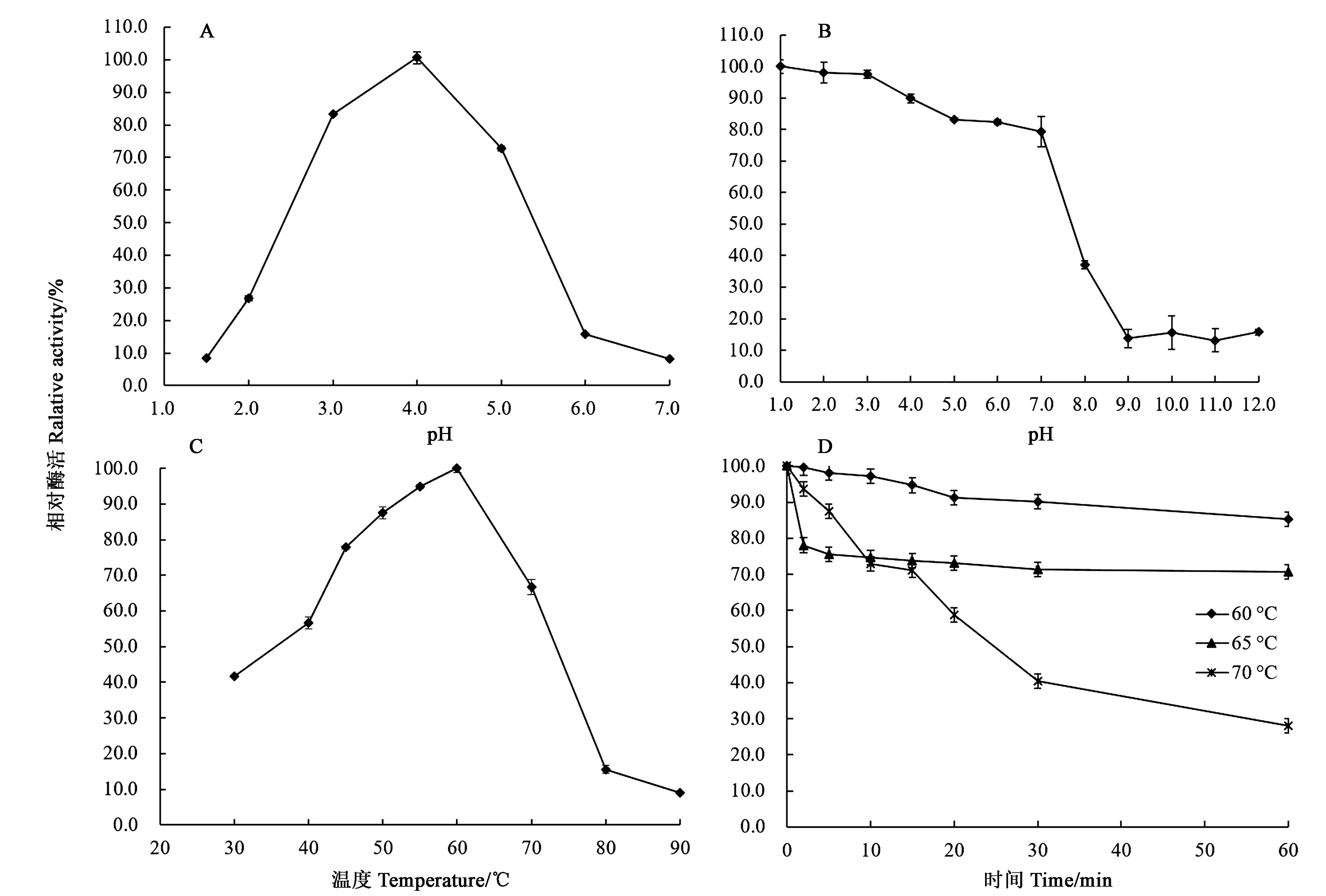
A:最適pH;B:pH穩定性;C:最適溫度;D:溫度穩定性A: Effect of pH on enzyme activities; B: pH stabilities; C: Effect of temperature on enzyme activities; D: Thermostability圖2 重組海藻糖酶TreA的基本酶學性質Fig.2 Characterization of purifird recombinant TreA
以1%海藻糖為底物,在最適條件(pH 4.0、60 ℃)下,重組海藻糖酶TreA的比活為1 913 U·mg-1,動力學參數Km和Vmax分別為0.67 mg·mL-1和119 μmol·min-1·mg-1。
2.4 金屬離子及化學試劑海藻糖酶TreA的影響
18種金屬離子和化學試劑對重組海藻糖酶TreA酶活性的影響如表1所示。當化學物質濃度為5 mmol·mL-1時,Fe3+、Mn2+、Pb2+和巰基乙醇對海藻糖酶起激活作用;SDS、Ag+和Hg2+對海藻糖酶具有抑制作用;Ag+、Na+、K+、Ca2+、SDS和Hg2+均對海藻糖酶TreA的酶活性具有抑制作用。濃度為10 mmol·mL-1時抑制效果較5 mmol·mL-1時更強,其中對海藻糖酶TreA酶活性影響最大的為Ag+,經5 mmol·mL-1離子處理后其相對剩余酶活性降為43.5%,經10 mmol·mL-1處理后幾乎沒有酶活性。Co2+、Fe3+和β-巰基乙醇可顯著提高海藻糖酶TreA的酶活性,Co2+、Fe3+濃度為5 mmol·mL-1時提高海藻糖酶TreA酶活性效果更加明顯,β-巰基乙醇濃度為10 mmol·mL-1時提高海藻糖酶TreA酶活性效果更加明顯。
2.5 海藻糖酶TreA對蛋白酶的抗性
測定純海藻糖酶TreA在含有0.1 mg·mL-1緩沖液中處理后的相對剩余酶活,如圖3所示,海藻糖酶TreA對胰蛋白酶、膠原蛋白酶和胃蛋白酶具有非常好的蛋白酶抗性,幾乎沒有酶活性的損失。然而,海藻糖酶TreA對蛋白酶K和糜蛋白酶的蛋白酶抗性較差,并且隨著在蛋白酶中處理的時間越長,酶活性損失越嚴重:海藻糖酶TreA在0.1 mg·mL-1蛋白酶K和糜蛋白酶中處理30 min后,相對剩余酶活分別為80%、40%;處理60 min后相對剩余酶活分別為60%、20%。另外,枯草蛋白酶對海藻糖酶TreA的酶活性也有輕微的抑制作用。

表1 不同金屬離子及化學試劑下純化重組海藻糖酶TreA活性Table 1 Activities of TreA under different concentration of metal ions and chemical reagents
3 討論
海藻糖酶作為一種常見的生物催化劑,在生物工業中的應用通常需要在酸性條件下進行,因此挖掘具有嗜酸特性的海藻糖酶基因具有重要意義。在本研究中,通過基因工程技術從嗜酸真菌Bisporasp.-MEY-1中成功克隆了一種酸性、耐中高溫的海藻糖酶TreA,其最適pH為4.0,在pH 2.2~5.0范圍內,可維持60%以上的剩余酶活力;在pH 1.0~9.0條件下處理1 h,可以維持79%以上的剩余酶活力,在最適pH和pH穩定性上具有明顯的優勢。目前已有多種真菌來源的酸性海藻糖酶基因被報道,劉迎春[7]利用RT-PCR、RACE等方法成功地克隆了金龜子綠僵菌的酸性海藻糖酶基因;釀酒酵母Saccharomycescerevisiae[19]、白色念珠菌Candidaalbicans[20]、構巢曲霉Aspergillusnidulans[21]中也分離鑒定出酸性海藻糖酶基因。此外,在NCBI數據庫中還報道了另外兩種絲狀真菌煙曲霉Aspergillusfumigatus和埃默森籃狀菌Talaromycesemrsonii來源的酸性海藻糖酶疑似基因序列[7],Bisporasp.-MEY-1來源的酸性海藻糖酶基因TreA與上述幾種來源的海藻糖酶基因的同源性在25%~50%之間。
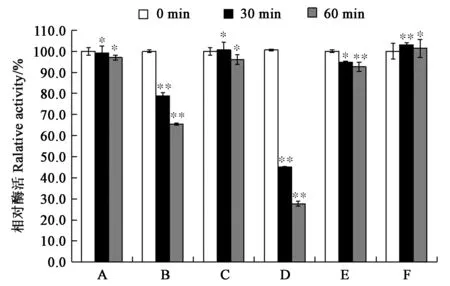
注:A—胰蛋白酶;B—蛋白酶K;C—膠原蛋白酶;D—糜蛋白酶;E—枯草蛋白酶;F—胃蛋白酶。 * 和**分別表示在P<0.05和P<0.01水平具有顯著性。Note:A—Trypsin; B—Proteinase K; C—Collagenase; D—Chymotrypsin; E—Subtilase; F—Pepsase. * and ** indicate significant difference at P<0.05 and P<0.01 levels, respectively.圖3 蛋白酶對純化重組海藻糖酶TreA的活性影響Fig.3 Effect of protease on enzyme activities of recombinant TreA
上述真菌來源的酸性海藻糖酶中,已有酶學性質報道的為來源于金龜子綠僵菌的海藻糖酶ReATM1p,NCBI登錄號為EF190950,與本研究中的酸性海藻糖酶TreA的序列一致性為47.8%。ReATM1p的最適pH為6.0,在pH 4.5~7.5范圍內具有較高的酶活力,但是當反應體系pH超過7.5時,酶活力迅速下降。與本研究中的酸性海藻糖酶TreA的最適pH和pH穩定性相比,ReATM1p的酸適應性明顯較差[7]。Enfert等[21]發現,為減少酸性條件下正電荷的積累,許多嗜酸蛋白表面進化出大量酸性氨基酸殘基。但是,已有晶體報道的海藻糖酶與本研究的酸性海藻糖酶TreA序列一致性最高的僅為22%,不滿足同源建模的條件,無法實現TreA三維結構的可視化分析。分析TreA和ReATM1p的一級結構時,發現TreA的氨基酸序列中酸性氨基酸(天冬氨酸Asp和谷氨酸Glu)占9.28%,ReATM1p的氨基酸序列中酸性氨基酸占8.4%。因此,推測可能是TreA中酸性氨基酸的比例明顯高于ReATM1p,導致TreA的酸適應性明顯高于ReATM1p。
酸性海藻糖酶在酵母中以一種單體形式發揮活性,在構巢曲霉A.nidulans中以二聚體形式發揮酶活性。酸性海藻糖酶Km的范圍為0.8~5 mg·mL-1[19],本研究中的酸性海藻酶TreA的Km為0.67 mg·mL-1,對海藻糖的底物特異性極強。酸性海藻糖酶另一特點是具有大量潛在的N-糖基化位點,這也解釋了TreA純化蛋白經EndoH脫糖基處理后在SDS凝膠條帶變小的原因[19-23]。此外,分析酸性海藻糖酶TreA的氨基酸序列,發現其N端1~18位的短肽為信號肽,這進一步驗證了酸性海藻糖酶可通過分泌途徑的靶向轉運,解釋了這類蛋白定位于細胞表面的原因[21]。
綜上所述,本研究成功獲得了一個新穎的酸性海藻糖酶基因TreA,并在畢赤酵母中實現了高效表達。該酸性海藻糖酶具有良好的酸適應性,同時對海藻糖有專一、較好的水解活力。這些特點表明酸性海藻糖酶TreA在生物工業中具有極大的應用價值。

