中晚期宮頸癌同步放化療聯合熱療增敏的效果觀察
徐小娟 朱玲
宮頸癌是常見婦科惡性腫瘤,發病率僅次于乳腺癌,居第二位[1]。我國每年宮頸癌新發病例數約為15 萬,死亡率在全身惡性腫瘤中居于第7 位 ,嚴重威脅女性生命安全和身心健康[2-3]。該病通常采用放療,也是II b 期以上中晚期宮頸癌患者治療的標準方案[4]。熱療是一種通過加熱阻礙腫瘤細胞生長的新技術,可致腫瘤細胞凋亡,可獨立應用,或與其它治療手段配合,以達增敏作用[5],熱療與放療配合可提高宮頸癌的放射敏感性和局部控制率[6],但查閱中國知網、萬方數據庫等平臺,未發現對其護理方案的深入研究,為此,本研究探討放化療聯合熱療增敏的中晚期宮頸癌患者的護理措施,旨在提高其臨床治效果和生存質量。
1 對象與方法
1.1 研究對象
選取2016 年6 月—2019 年6 月本院96 例中晚期宮頸癌患者為研究對象,納入條件:符合宮頸癌診斷標準且經病理實證[7];HGB ≥90 g/L 且卡氏評分[4]≥60 分;符合FIGO 分期Ⅱ~Ⅲ期[8]。排除條件:合并心、腦、腎重大器官疾病;存在認知功能障礙或精神病史;既往行放化療者;遠處轉移者。按照組間基線資料匹配的方法,將符合上述條件的96 例患者均分為對照組和觀察組。觀察組48 例,年齡30~66 歲,平均38.87±6.52 歲,臨床分期:Ⅱ期17 例,Ⅲa 期17 例,Ⅲb 期14 例;病理類型:腺癌11 例,鱗癌31 例,腺鱗癌6 例。對照組48 例,年齡32~65 歲,平均37.93±6.04 歲,臨床分期:Ⅱ期18 例,Ⅲa 期17 例,Ⅲb 期13 例;病理類型:腺癌10 例,鱗癌33 例,腺鱗癌5 例。兩組一般資料比較差異無統計學意義(P>0.05)。本研究經醫院倫理委員會批準進行,且全部患者均在自愿參與的前提下簽署知情同意書。
1.2 護理方法
1.2.1 對照組 采用直線加速器8MV 對患者全盆腔施行照射治療,每周照射5 次,每次劑量控制在0.8~2.0 Gy,行常規分割。外照射的總劑量45~50 Gy,實施全盆照射25~30 Gy 時,行中間擋鉛。擋鉛后給予腔內后裝治療,且加做當天不做外照射,每周1 次,每次劑量為6 Gy,A 點劑量控制為30 Gy。放療第1天開始進行化療,順鉑30 mg/m2,每周1 次,共6周期,治療同時給予常規護理干預。
1.2.2 觀察組 在對照組基礎上聯合熱療增敏,選用衡水非帛醫療設備銷售有限公司生產的威海眾恒ZD 型體外熱療機治療,頻率13.65 MHz,溫度40 ℃,每周于放療后或放療前1 h 治療2 次,每次60 min。護理措施如下:
(1)由于患者對于熱療缺乏認知,期間易出現恐懼、焦慮等不良情緒以及心率增快等不良反應,護理人員與患者及家屬及時溝通,宣講熱療在治療中的重要性,或者在其他患者同意的情況下參觀熱療治療環節,現場講解熱療的注意事項、必要的安全常識、飲食搭配,指導患者進食易消化、高蛋白質、低脂肪食物,提醒患者熱療前1 h 進少量流質或半流質,補充患者在熱療時所消耗的能量。
(2)熱療前,評估熱療部位皮膚情況,必要時備皮。指導患者穿柔軟棉質衣服,排盡尿液,采用醫用紙巾擦干尿道口殘留尿液與分泌物,避免治療時出現不適感。去除治療部位的金屬或磁性物品,防止高熱傳導造成局部燙傷。對于伴心血管代償功能不全或植入心臟起搏器患者以及出血性疾病、體濕調節障礙患者,禁止熱療。
(3)熱療中,患者完全暴露治療區域,切忌隨意改變體位。熱療8~10 min 后機器溫度上升較快,護理人員實時觀察患者溫度曲線,調節檢測點溫度,保證適宜溫度。期間密切觀察溫度變化,以不超過42 ℃為宜。皮下脂肪過厚患者熱耐受力較差,出現刺痛時,應在熱療部位增加隔熱墊,并停機查找原因,防止患者治療區域燙傷。囑患者禁止接觸儀器,提醒他人切勿接觸患者,避免造成燙傷。熱療時控制好輸出電壓與電流,實時觀察患者病情變化,出現不適感,應立即停止熱療,采取相應處理。
(4)熱療后,熱療護士幫助患者穿衣、站立,保持動作緩慢,適當保暖,多飲水。觀察皮膚是否有發紅、水泡等不良情況,熱療完成3 h 內禁沐浴。皮下脂肪厚度超過1.5 cm 會導致脂肪散熱性較差,因脂肪層吸收射頻波而產熱,造成皮下脂肪硬結,引發凝固壞死形成結節,此時應及時給患者講明緣由,可在1~2 周后自愈。依照放化療方案選擇治療時間,在放療前或放療后1 h 施行熱療,化療后需及時進行熱療,以達到增敏效果。
1.3 觀察指標
(1)治療結束1 個月內,根據兩組病灶情況判定治療效果,分為完全緩解(病灶瘤體完全消失且1 個月以上無新病灶)、部分緩解(病灶瘤體縮小≥30%且持續至少1 個月)、穩定(病灶瘤體縮小<30%且持續至少1 個月)、進展(病灶瘤體增大)4 個等級,有效=完全緩解+部分緩解[9]。
(2)隨訪1 年,觀察患者無瘤生存情況并計算其無瘤生存率。
1.4 統計學處理
采用SPSS 23.0 統計學軟件進行數據處理,計數資料組間率的比較行χ2 檢驗,等級資料組間比較采用兩獨立樣本的Wilcoxon 秩和檢驗。檢驗水準α=0.05,P<0.05 為差異具有統計學意義。
2 結果
2.1 兩組近期治療效果比較
觀察組近期治療有效率高于對照組,組間比較差異有統計學意義(P<0.05)。見表1。
2.2 兩組1 年無瘤生存率比較
觀察組1 年無瘤生存率高于對照組,組間比較差異有統計學意義(P<0.05)。見表2。
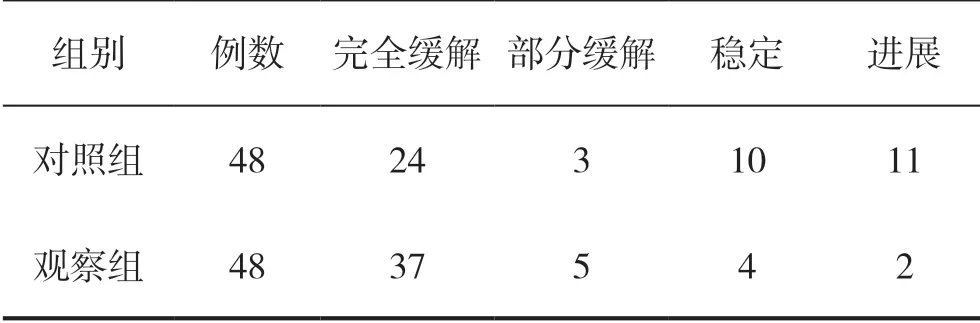
表1 兩組近期效果比較
3 討論
中晚期宮頸癌的病因病理較為復雜,為婦科典型的危險性病癥,其治療和康復受多種因素影響,生存質量明顯下降[10-11]。臨床多選用同步放化療方案治療中晚期宮頸癌,雖取得一定成效但存在諸多并發癥,遠期預后并不理想。因此,本研究在同步放化療基礎上聯合熱療增敏并給予全方位護理,通過維持40℃治療熱量,殺滅腫瘤細胞的同時,不損傷機體正常組織,還能夠減輕放化療副作用、提高機體免疫力[12]。
熱療作為治療腫瘤的主要手段,臨床應用越來越廣泛。熱療是應用電流經介質空氣為人體與電極間加熱,是將高頻電磁場作用于機體,電磁場能量在吸收后轉換成熱能,提高組織溫度,達到治療腫瘤目的[13]。其抗癌機理[9-11]:干擾并阻滯DNA、RNA 與蛋白質合成;激活溶酶體,損毀細胞;干擾癌細胞骨架排列,致其缺失以破壞細胞;刺激免疫系統;以熱量堆積,使癌細胞凋零。放療聯合加熱對癌細胞的殺滅作用高于單純應用加熱或放療,兩種方式在滅殺癌細胞群體中形成互補,且兩者之間存在協同增敏作用,加熱與部分放療藥物(順鉑)之間存在獨立與協同增敏作用。熱、放、化聯合作用優于熱放或熱化療法聯用,不單純是三因子單獨細胞毒作用相加,更是三因子療法中各因子之間協同增敏作用相加[14]。
宮頸癌早期無特異性表現,多數就診患者屬于中晚期,轉移率和局部未控制率較高,5 年內生存率不足50%[2]。分別從熱療前、熱療中、熱療后各環節給予全面、及時、科學的護理干預,從而提高治療依從性和生活質量。表1,2 顯示,采取放、化、熱聯合治療后1 個月,觀察組治療有效率高于對照組(P<0.05),與趙靚等[15]研究結果一致;隨訪1年,觀察組1 年無瘤生存率高于對照組(P<0.05),從數據上也證實了熱療相較于傳統治療安全可靠,可有效提高宮頸癌患者近、遠期效果。
總之,熱療增敏聯合同步放化療中晚期宮頸癌近期效果佳,可提高患者生存質量和1 年內無瘤生存率 。但本研究僅行1 年隨訪,遠期效果相關結果仍有待商榷,期待未來大樣本、長時間研究進一步深入探討。

