藥物輔助性犯罪中獸藥麻醉劑舒泰的UPLC-MRM-IDA-EPI-MS鑒定
吳小軍,董林沛,張云峰,趙 鵬,劉冰潔
(1.公安部物證鑒定中心,北京 100038;2.愛博才思亞太應用支持中心,北京 100015)
舒泰是一種寵物臨床常見的麻醉劑,它是由唑拉西泮和替來他明1∶1混合而成[1-3]。唑拉西泮是苯二氮卓類鎮靜劑,具有良好的肌肉松弛和抗驚厥作用;替來他明則是一種分離麻醉劑,止痛作用持久。這兩種藥物在藥物動力學上具有互補作用,常用于小動物的臨床麻醉。兩個藥物的代謝能力有一定差異,唑拉西泮在生物體內的穩定性要強于替來他明,實際檢驗過程中常常能檢測到唑拉西泮,而替來他明的濃度卻較低[4]。此藥物在動物身上應用廣泛,但近年來發現此類藥物在刑事犯罪領域的濫用現象時有發生,常見于藥物輔助性犯罪如迷奸、麻搶等[5-7]。目前對于唑拉西泮和替來他明的檢驗主要采用GC-MS法[1, 4],何思陽等[6]采用GC-QTOF鑒定藥物輔助性犯罪案件樣品中替來他明和唑拉西泮及其代謝物組分,取得良好的定性效果。氣質聯用法前處理較為繁瑣且靈敏度往往達不到要求。LC-MS法具有前處理簡單,靈敏度高等優勢,采用LC-MS法檢驗唑拉西泮和替來他明尚未見報道。由于基質的復雜性,有時候即使使用液質串聯四級桿MRM模式也難以避免假陽或假陰誤判。本研究在優化前處理的方式的基礎上建立了UPLC-MRM-IDA-EPI-MS同時定性、定量檢測唑拉西泮、替來他明的檢驗方法。該方法借助于信息依賴性獲取技術(IDA)能將多反應檢測(MRM)和增強子離子掃描模式(EPI)相結合[8-12]。不僅能保證在MRM基礎上獲得高靈敏度的定量結果,同時能借助于線性離子阱的增強子離子掃描技術,獲得二級質譜進行定性確證。值得指出的是EPI技術具有離子富集、信號增強的作用,即使在極低含量下也能獲得質量較高的二級全譜,為低濃度臨界值的定性提供參考。使用本方法對血液中唑拉西泮和替來他明進行定性和定量分析,簡便快速,并將定性和定量方法有機結合在一起,可以滿足復雜基質中目標物的準確定性和定量分析要求。
1 材料與方法
1.1 儀器、試劑、材料 超高效液相色譜-串聯四級桿復合線性離子阱質譜(島津LC-30AC- Scix5500-QTrap);高速離心機(Thermo-Fisher 臺式高速冷凍離心機);超純水機(Milli-Q Academic);高速振蕩器(CUTEMIXER CM-1000)
鹽酸唑拉西泮(cas:33754-49-3)、鹽酸替來他明(cas:14176-50-2)標準物質均購于天津阿爾塔科技有限公司;乙腈(色譜純Merck);甲醇(色譜純Merck);Prime HLB固相萃取小柱(Waters Oasis)
空白血液(購于北京市復興醫院醫院血庫);待測樣品:心血、尿液,來自某地公安機關送檢樣本。
1.2 標準溶液的配置 取唑拉西泮和替來他明標準物質各10 mg,精密稱定,用甲醇定容至10 mL,配置成1 mg/mL的混合標準品儲備液于4 ℃冰箱保存,再用甲醇稀釋至10 μg/mL作為混合標準品使用液。
1.3 樣品前處理 取血液(尿液)樣品0.5 mL于15 mL離心管中,加入2 mL乙腈,高速震蕩10 min,8000 r/min離心10 min,取上層清液過PRIME-HLB固相萃取小柱,收集洗脫液,過0.22 μm有機相濾膜,待測。若檢材中藥物濃度過高,可用乙腈稀釋至線性曲線范圍內測定。
1.4 超高效液相色譜條件 色譜柱phenomenex Kinetex F5(100×3.0 mm,2.6 μm);柱溫:40 ℃;流動相A相:乙腈,B相:含0.01%甲酸1 mM甲酸銨水。進樣體積3 μL。流速:0.45 mL/min。梯度洗脫程序:0~1 min,5%A相;1~1.1 min,20%A相;1.1~6 min,20%~95%A相;6~8 min,95%A相;8~8.1 min,5%A相;8.1~11 min,5%A相。
1.5 質譜條件 電噴霧離子源(ESI+);離子源溫度:500 ℃;噴霧電壓5500 V;氣簾氣壓力35 psi;噴霧器壓力50 psi;輔助加熱器壓力50 psi;掃描模式(MRM-IDA-EPI),MRM相關參數見表1。IDA采用動態背景扣除;掃描閾值100 cps;EPI源參數與MRM模式一致;碰撞能量CE(35±15eV);掃描范圍50~300 Da。

表1 唑拉西泮和替來他明的MRM質譜參數Tab 1 MRM parameters of zolazepam and tiletamine
2 結果與分析
2.1 離子對的獲取 采用針泵進樣方式,將100 ng/mL的唑拉西泮和替來他明標準品分別注入質譜中,分別采用正、負掃描模式對標準品進行掃描,結果表明在正離子模式下,唑拉西泮和替來他明均有較好的響應。在步進電壓為5的碰撞能量下分別對兩個化合物的子離子進行掃描,確定各個目標物的特征子離子,并進行去簇電壓和碰撞電壓的優化,得到一系列離子對,如表2所示。
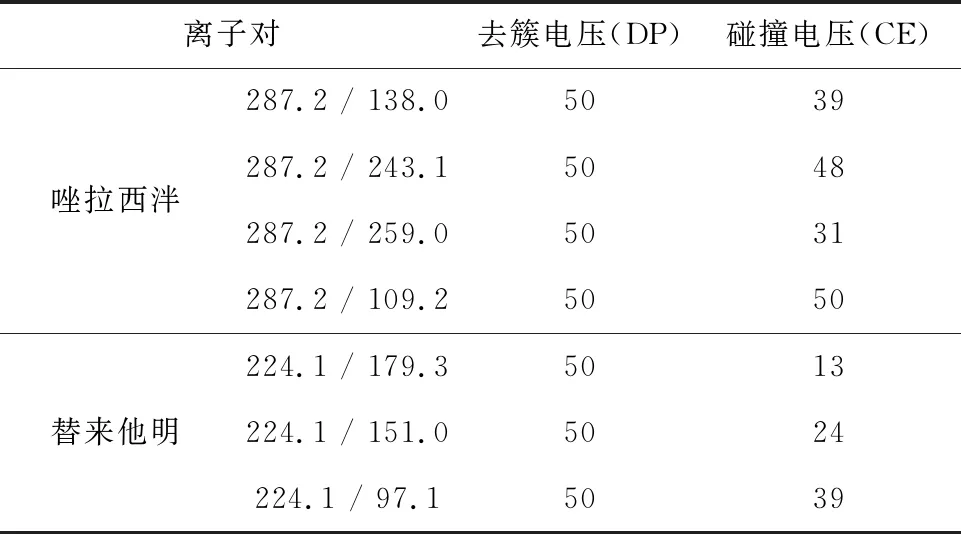
表2 唑拉西泮和替來他明優化后的備選離子對Tab 2 Alternative ion pairs optimized for zolazepam and tietamine
2.2 離子對的選擇及條件優化 離子對的選擇原則應該遵循無干擾、信噪比高等原則。采用液相色譜進樣,進樣濃度為100 ng/mL,使用MRM模式掃描監控各個離子對。如圖1中所示唑拉西泮和替來他明的備選離子對均不存在干擾,故選擇信噪比最高的離子對作為定量離子,信噪比次之的選作定性離子。篩選后的結果如表1所示。
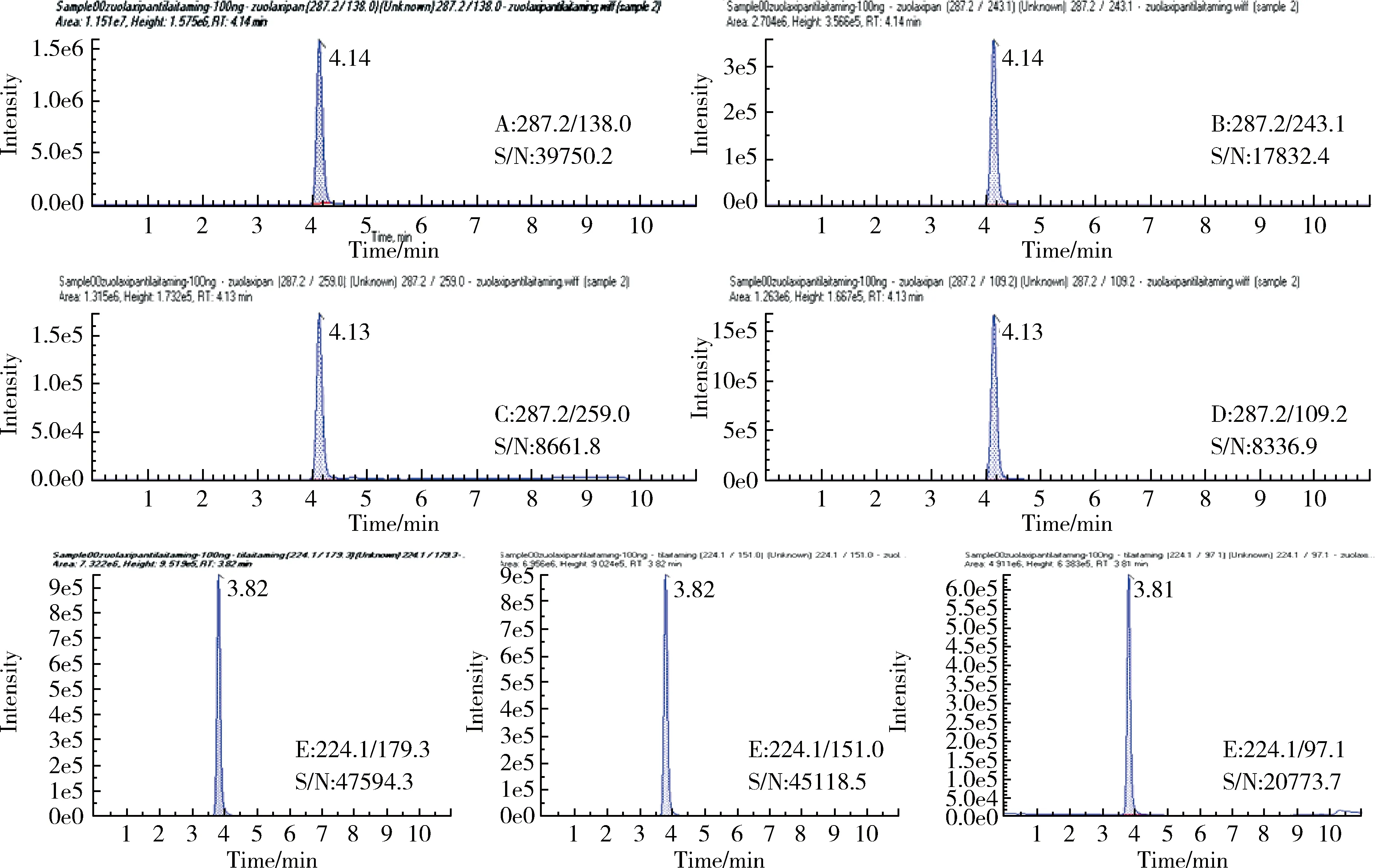
圖1 100 ng/mL 唑拉西泮和替來他明各個離子對的抗干擾及信噪比考察Fig 1 Investigation of anti-interference and signal-to-noise ratio of each ion pair of zolazepam and tiletamine at 100 ng/mL
2.3 基質工作曲線、靈敏度與精密度 采用外標標準曲線法定量。由于不同檢材的藥物含量差異較大,難以采用一致的內標濃度,需要根據不同的樣品設置內標,可操作性差;其次內標物質的選擇相對困難,氘代內標較為昂貴,故采用外標法定量分析。分別配置1、5、10、20、50、100 ng/mL的混合標準基質添加溶液,以定量離子對的峰面積(y)對目標物質的質量溶度(x)繪制標準曲線,結果表明兩目標物物線性關系良好(R2>0.995);以定量離子對的10倍信噪比作為方法的定量限(LOQ),以定性離子對3倍信噪比作為方法的檢出限(LOD)。將系列標準溶液中濃度為20 ng/mL的標準溶液,連續進樣6次,以峰面積的RSD值計算曲線點的精密度。結果如表3所示。兩種藥物的線性曲線相關性好,線性范圍完全能夠滿足日常辦案要求,對于高濃度藥物在檢驗過程中可以采用溶劑稀釋的方式,將藥物濃度稀釋至線性范圍內檢驗,不僅能滿足線性要求,對降低基質效應也有一定作用。

表3 方法的基質工作曲線、靈敏度與精密度Tab 3 calibration curves, sensitivity and precision of the method
2.4 方法的回收率與精密度 選擇同一批次的空白血,添加適量的混合標準溶液,配制成3個濃度水平(5、20、50 ng/mL)的待測樣品,每個水平3個平行樣,使用上述前處理方法處理后,使用基質外標曲線定量。結果如表4所示。各個水平的加標回收率均大于85%,方法穩定性符合要求。

表4 血液中唑拉西泮和替來他明的回收率和精密度Tab 4 Recovery rates and precision of zolazepam and tiletamine in the blood
2.5 EPI數據采集分析 運用MRM-IDA-EPI技術,分別采集了唑拉西泮、替來他明50 ng/mL基質添加的二級質譜圖,并將采集到的二級質譜圖導入數據庫中,用于定性檢索。如圖2所示,唑拉西泮的兩個子離子碎片138、243都是由母離子287碎裂產生,而替來他明的151、179則由母離子224碎裂產生,借助peakview軟件可以給兩物質的特征離子做碎片歸屬,進一步提高定性的準確性。
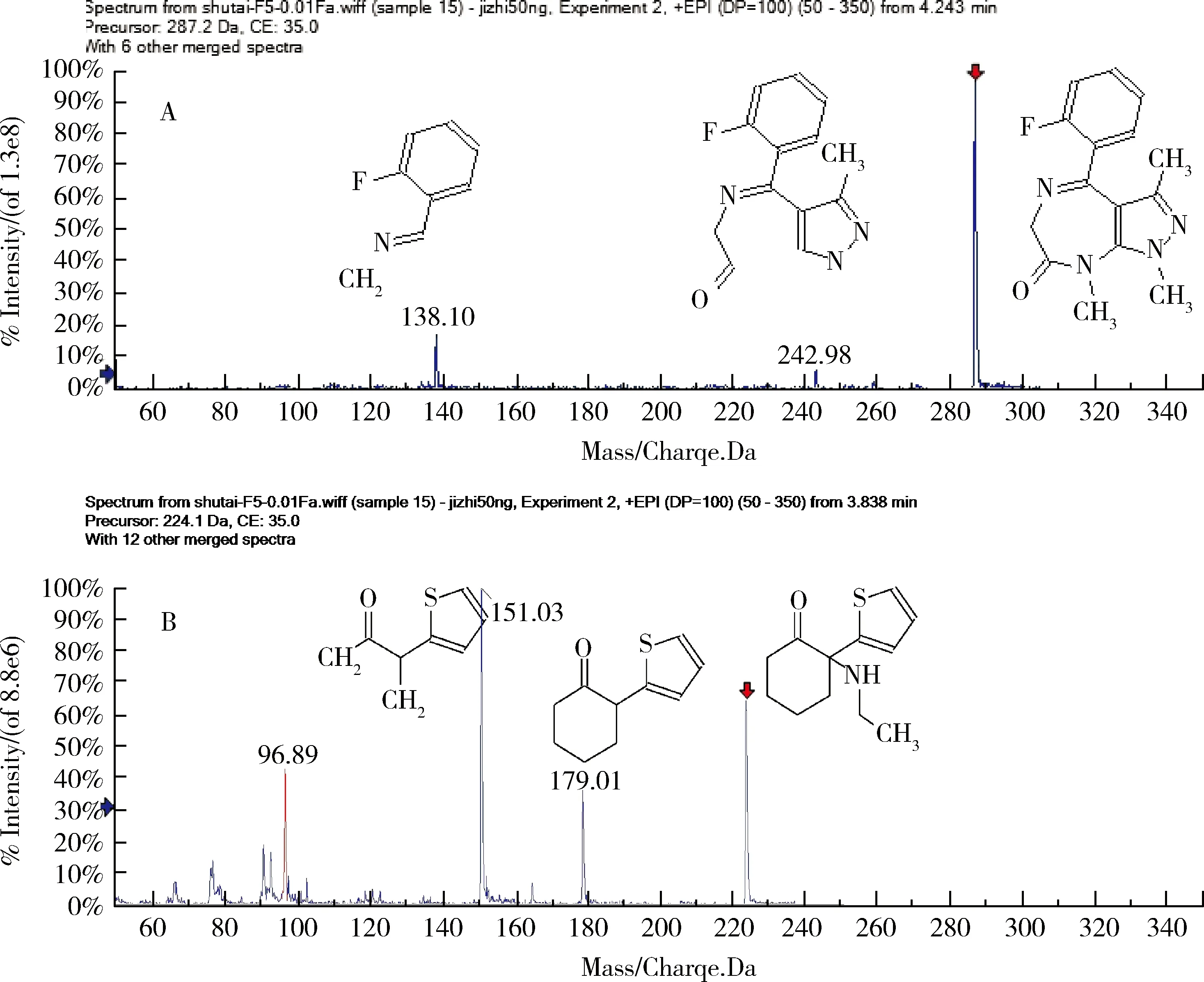
圖2 A-唑拉西泮和B-替來他明二級質譜圖Fig 2 Full spectrum of A-zolazepam and B-tiletamine
2.6 實際樣品檢測 2019年黑龍江某地發生一起命案,具嫌疑人供述,其將從獸藥店買來的麻醉劑注射進被害人體內,導致被害人死亡。當地公安機關立案偵查后,將檢材送至中心要求檢驗被害人血液和尿液中唑拉西泮和替來他明的含量。
運用上述建立的方法不僅能獲得高靈敏度的定量結果,還能借助EPI技術對樣本的目標物二級全譜與標準物質的二級全譜進行比對,獲得更加準確的定性結果。檢驗結果如圖3~圖5、表5所示。
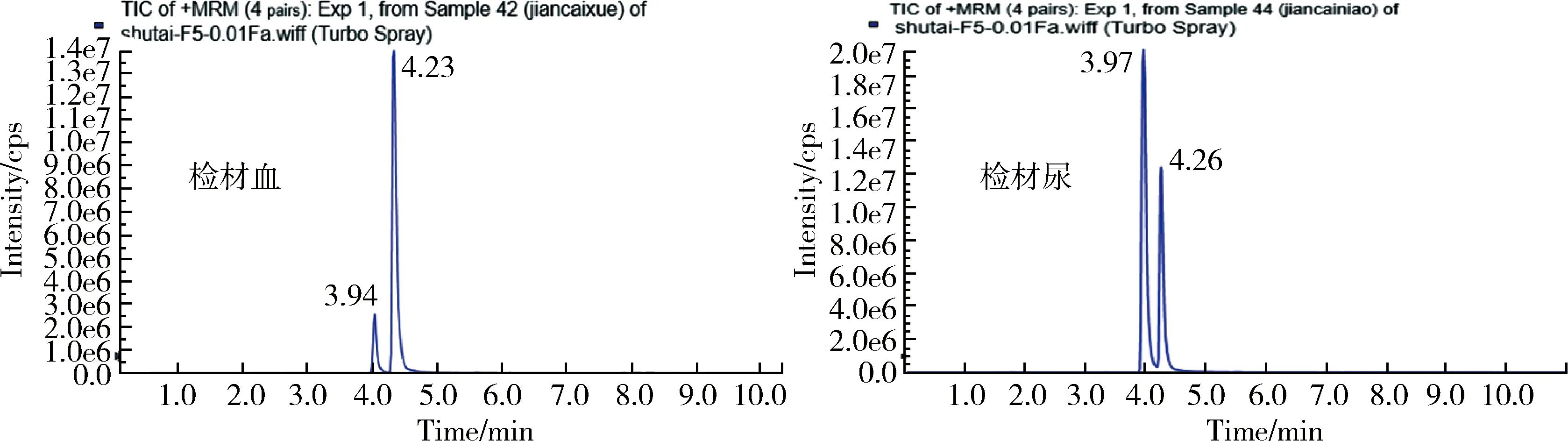
圖3 樣品總離子流色譜圖Fjg 3 Chromatogram of total ion flow of the sample
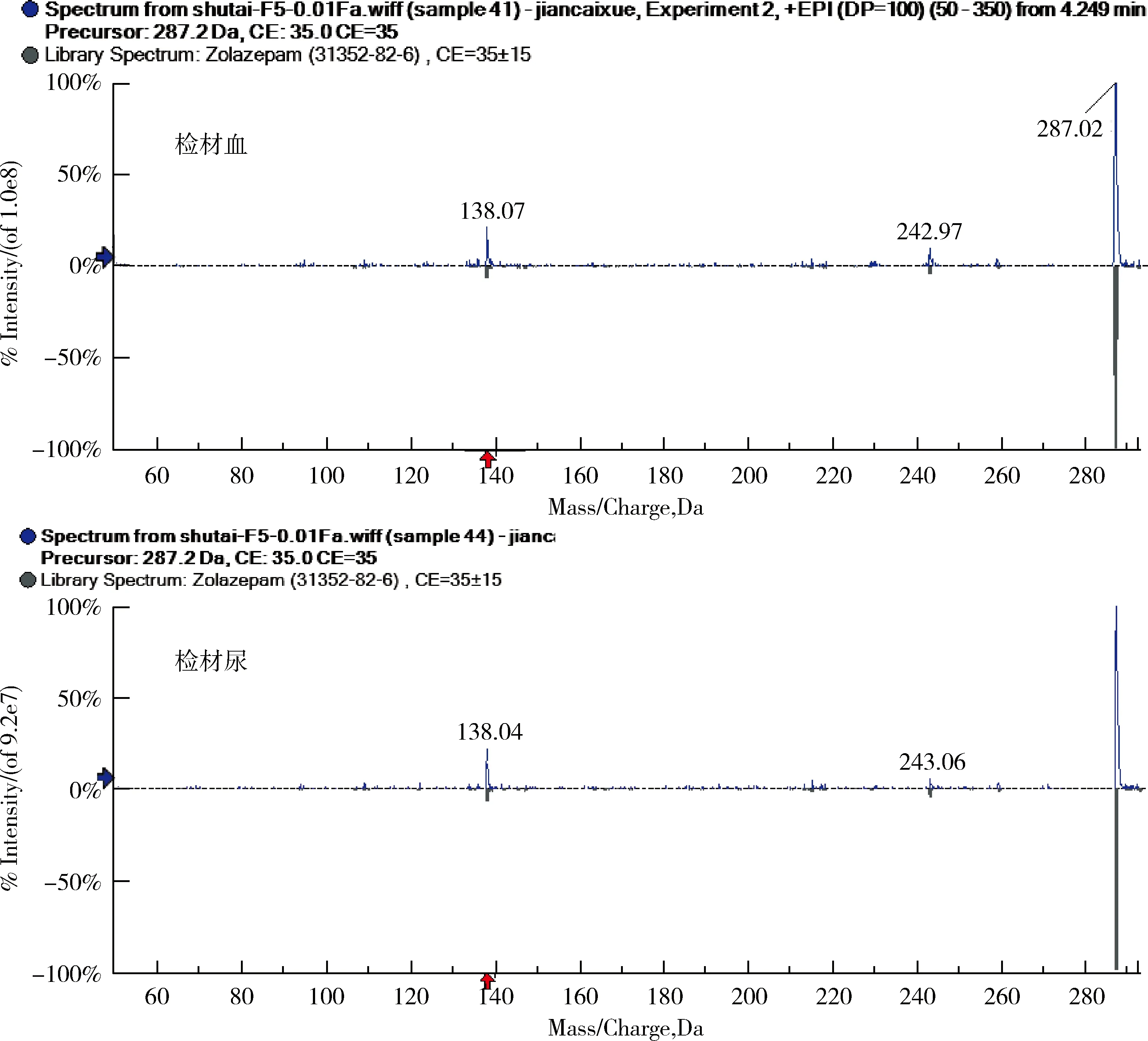
圖4 檢材血和檢材尿中唑拉西泮的EPI全譜與譜庫比對結果Fig 4 Comparison results of EPI full spectrum and spectrum library of zolazepam in blood and urine samples

圖5 檢材血和檢材尿中替來他明的EPI全譜與譜庫比對結果Fig 5 Comparison results of EPI full spectrum and library of tiletamine in blood and urine samples
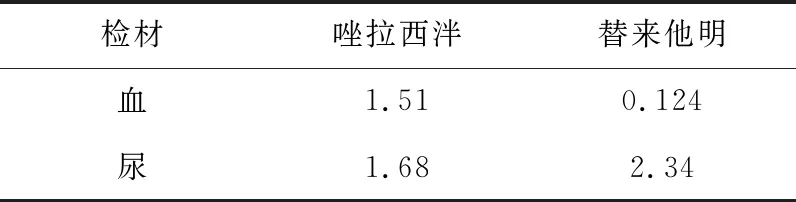
表5 樣品定量結果(μg/mL)Tab 5 Quantitative results of samples
3 討論與結論
3.1 色譜條件的選擇 本研究考察了phenomenex Kinetex F5(100×3.0 mm,2.6 μm);ACQUITY-UPLC-BEH C18(100×2.1 mm,1.7 μm)和ACQUITY-UPLC-HSS-T3(100×2.1 mm,1.8 μm)3種色譜柱,F5色譜柱為五氟苯基色譜柱,該柱對含鹵素含苯基及共軛基團的物質有較好的分離能力,而C18和T3色譜柱均為C18的鍵合相,區別在于T3色譜柱對極性化合物有更好的保留。研究結果表明phenomenex Kinetex F5(100×3.0 mm,2.6 μm)能夠將唑拉西泮和替來他明完全分離且信噪比高,另外兩種色譜柱均不能有效分離。根據藥物的結構,選擇酸性流動相有利于藥物電離,但過高的濃度的酸會使得基線噪音升高,研究過程中發現適當增加揮發性鹽可以改善峰形,經實驗后選擇0.01%的甲酸1 mM甲酸銨水-乙腈作為液相流動相。這兩種藥物出峰時間比較接近,采用梯度洗脫的方式使得兩物質更好分離。
3.2 基質效應考察 質譜分析過程中,樣品基質中的干擾組分會對目標待測物產生影響,從而產生基質增強或基質抑制效應。本研究中評價基質效應的方法是:基質效應=空白基質配制標準響應值/溶劑配制標準響應值×100%。當基質效應在80%~120%之間時,可用標準曲線定量。當基質效應<80%,為基質抑制效應,當基質效應>120%時,為基質增強效應,此時可考慮用基質標準曲線定量。在檢驗實踐中常通過三個途徑來減小基質效應的影響,一是對待測樣品的再凈化處理,常采用液液萃取或固相萃取的方式,去除樣品中的多肽、磷脂、無機鹽等干擾因素;二是改變液相分離條件,如改變洗脫強度、液相梯度或pH值等以提高分離度,避免待測組分與基質的共洗脫,使得在分離過程中能夠有效避開基質效應區間;三是減少進樣量或稀釋后進樣,基質效應一般伴隨著進樣載量增加而增加,只要靈敏度在許可的范圍內均可通過此途徑來減少基質效應的影響。綜合上述因素,本研究采用固相萃取的方式來減少基質效應對分析的影響。本研究考察了1、10、50 ng/mL三個濃度梯度的基質效應,固相萃取柱子選擇了Waters-PRIME- HLB,該萃取柱吸附劑可以吸附樣品中非極性干擾物而不影響目標物的回收率,特別是對于造成基質干擾的脂肪和磷脂,去除效率高達95%以上。研究發現唑拉西泮和替來他明的基質效應均介于90%~105%之間。在實際工作過程中為簡化實驗步驟可忽略基質效應的影響,采用溶劑標準曲線即可對二者準確定量,但本研究中為提高研究結果可靠性,故采用基質加標方式考察線性關系。
3.3 EPI定性方法的選擇 法醫毒物分析的檢材都是被害人的血、尿、胃內容物,基質比較復雜。使用MRM定性模式,當藥物濃度過低時,由于基質的干擾,經常會遇到離子對保留時間漂移、離子強度比例偏差大等問題,MRM定性準確性難以保證。本研究利用Q-TRAP線性離子阱技術,借助于數據依賴性獲取技術(IDA)能將多反應檢測(MRM)和子離子增強掃描模式(EPI)相結合,在采集MRM離子對時,根據設定好的采集條件能夠在相同的時間窗采集到關聯的增強子離子碎片全譜信息,為物質的準確定性增加了一個維度。線性離子阱技術具有離子富集的作用,借助于此技術即使在低濃度下,也能打出高質量的二級全譜信息。
法醫毒物關注的目標物絕大多數是臨床治療藥物、毒品及新精神活性物質,獸用麻醉劑在藥物輔助犯罪中并不多見,由于毒物種類非常多,獸用藥物很少進入法醫毒物分析工作者的視野,當遇到此類藥物時往往沒有現行有效的檢驗方法。在本案例所遇到的唑拉西泮和替來他明為獸用麻醉劑舒泰的主要成分,此類藥物用于人類麻醉在國內外文獻鮮有報道。在動物麻醉實驗中為監測其血藥濃度,多采用氣相色譜-質譜法,該方法定性、定量能力強,但操作繁瑣,靈敏度差。在偵辦迷奸、麻醉搶劫等案件中發現被害人往往后知后覺,侵害行為發生三五天后才報警,此時被害人體內的藥物濃度極低,氣相色譜-質譜法的靈敏度已遠遠達不到檢驗要求。
寵物用麻醉劑舒泰的主要成分為唑拉西泮和替來他明,二者通常為1∶1混合。從案例中可以看出替來他明的代謝速度比唑拉西泮快,故血中替來他明的濃度低于唑拉西泮,兩者都可經尿液排出,替來他明經尿液排泄的速率高于唑拉西泮。因這兩種藥物的代謝速率較快,在一些藥物輔助性犯罪案件的鑒定過程中常因被害人報警不及時,錯過最佳的檢驗時間窗口導致原藥在體內檢不出,后續研究可關注其代謝物。
本研究所建立的UPLC-MRM-IDA-EPI-MS法兼具定性和定量的功能。EPI增強子離子掃描技術,能夠增加定性維度,有效避免假陽性的發生;MRM選擇離子監控則使方法具備出色的靈敏度,此方法能夠滿足辦案的需求。

