年輕直腸癌5年死亡風險預測模型
——Nomogram
譚令 劉紫麟 馬驟 何洲 唐翎瀚 肖江衛
結直腸癌在全球癌癥發病率和死亡率中排名第三和第二[1]。在中國,2018年結直腸癌發病率排第二,并且中國結直腸癌的癌癥負擔迅速增加[2]。直腸癌腹腔鏡手術和新輔助治療的臨床運用,直腸癌的預后得到很大改善,直腸癌5年生存率明顯提高[3]。流行病學研究顯示,年輕結直腸癌(20~49歲)發病率不斷升高[3],而且年輕結直腸癌病人更容易發生于直腸[4]。目前臨床研究顯示,50歲以下的結直腸癌病人死亡率隨年齡增加[4],但年輕直腸癌病人死亡風險的研究相對較少,對于年輕直腸癌病人死亡風險因素尚不明確。為了研究年輕直腸癌病人死亡風險因素,我們運用SEER數據庫的直腸癌數據構建預測模型(SEER數據庫是美國大型癌癥數據庫之一[5]),預測年輕直腸癌病人5年內死亡的風險因素,并繪制Nomogram來預測年輕直腸癌病人5年內死亡的風險。Nomogram構建的預測模型整合多種危險因素,并量化評價相關危險因素所占風險概率[6-8],從而預測相關疾病的死亡風險概率。
對象與方法
一、對象
我們的研究對象來自SEER數據庫。我們使用SEERStat version 8.3.6軟件,從SEER數據庫(1975-2016年)中檢索出239594例病例數據。檢索準測:(1)按AJCC 6腫瘤疾病分類版本,組織學類型選擇直腸癌,并且限定組織學陽性診斷確保診斷正確;(2)診斷年齡>19歲;(3)生存時間限定完整生存時間的病例數據,并且限定隨訪必須為有效性隨訪;(4)排除來自于尸檢或死亡報告的病例數據;(5)排除隨訪時間為“unknown”的病例數據。提取數據:年齡、性別、婚姻狀態、Stage分期、T分期、N分期、M分期、放療、化療、腫瘤大小、淋巴結數量、生存時間、生存狀態等數據。對篩選出的239 594病例數據再次進行逐步篩選得到數據為5年內死亡的病例數和存活時間大于5年的病例數,篩選流程見圖1。
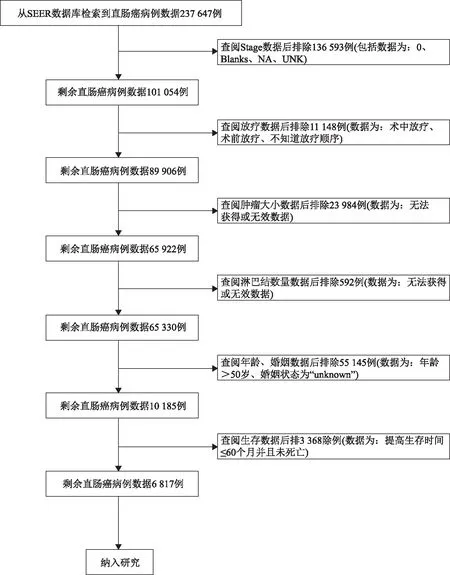
圖1 直腸癌病例篩選流程圖
二、方法
1.數據分析及構建Nomogram圖:納入病例數據首先采用χ2檢驗進行單因素分析,將單因素分析中有統計學意義的因素納入多因素Logistics回歸分析,多因素Logistics回歸分析有統計學意義的因素構建Nomogram預測模型。
2.評價Nomogram圖預測模型:繪制Nomogram預測模型ROC曲線評價準確性;隨機選取2 200例病人臨床數據進行內部驗證繪制Nomogram校準曲線,橫坐標是預測的年輕直腸癌病人死亡風險,縱坐標是實際年輕直腸癌病人死亡風險[9]。
三、統計學處理
所有統計分析采用SPSS 25.0軟件和R軟件3.6.1版本。P<0.05為差異有統計學意義。
結果
1.病人特征:我們通過逐步篩選后納入(2004~2015年)6817例直腸癌病人,存活時間≤5年的病例2 579例,存活時間>5年病例4 238例,所有病人的基本特征見表1。單因素分析顯示,年齡、性別、Stage分期、T分期、N分期、M分期、腫瘤大小、淋巴結數量、放療、化療、婚姻狀態是年輕直腸癌病人5年死亡風險因素(表1);多因素Logistics分析顯示,性別、Stage分期、T分期、N分期、放療、腫瘤大小、淋巴結數量、婚姻狀態是年輕直腸癌病人5年死亡風險因素(表2)。
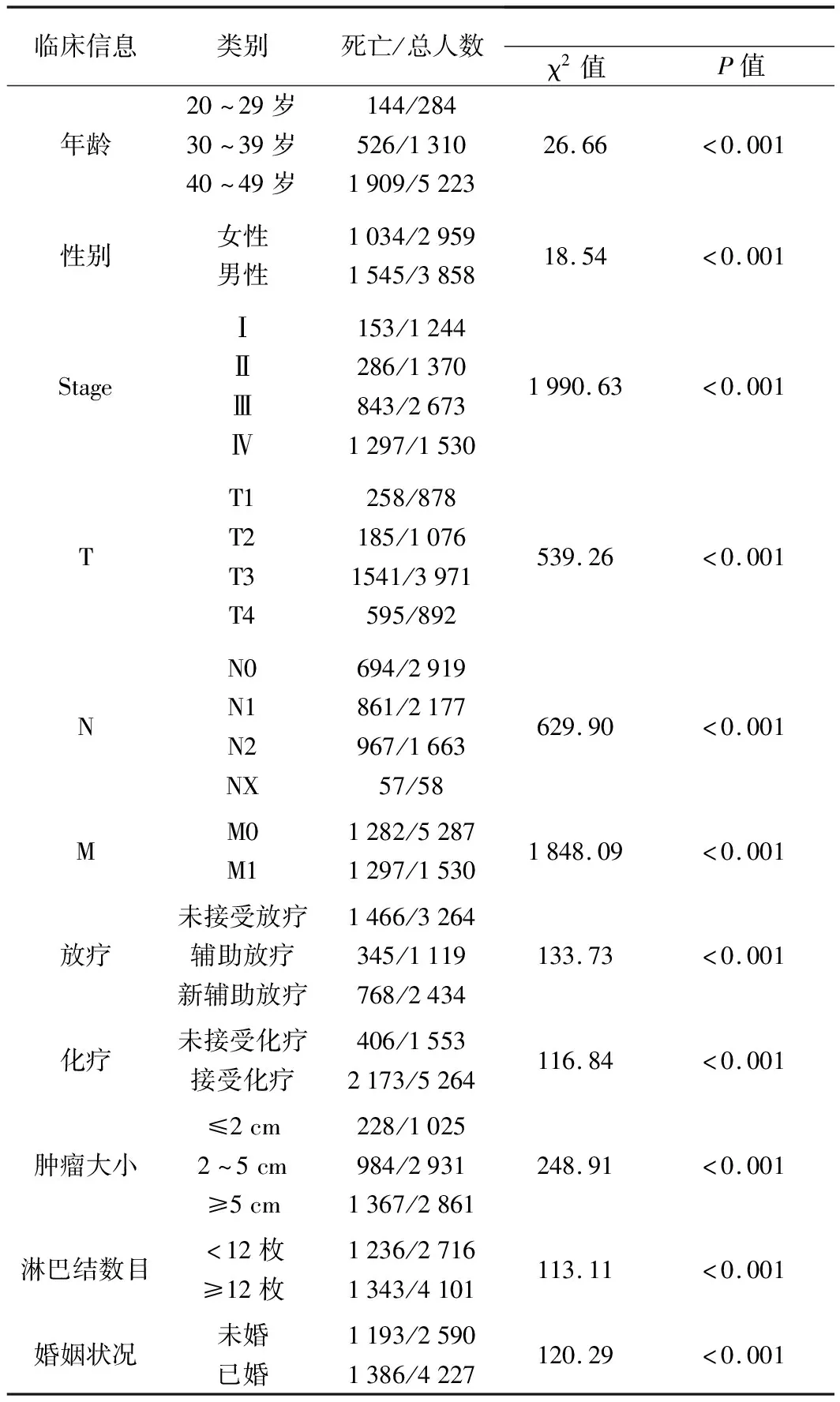
表1 年輕直腸癌病人的臨床信息及5年死亡風險單因素分析
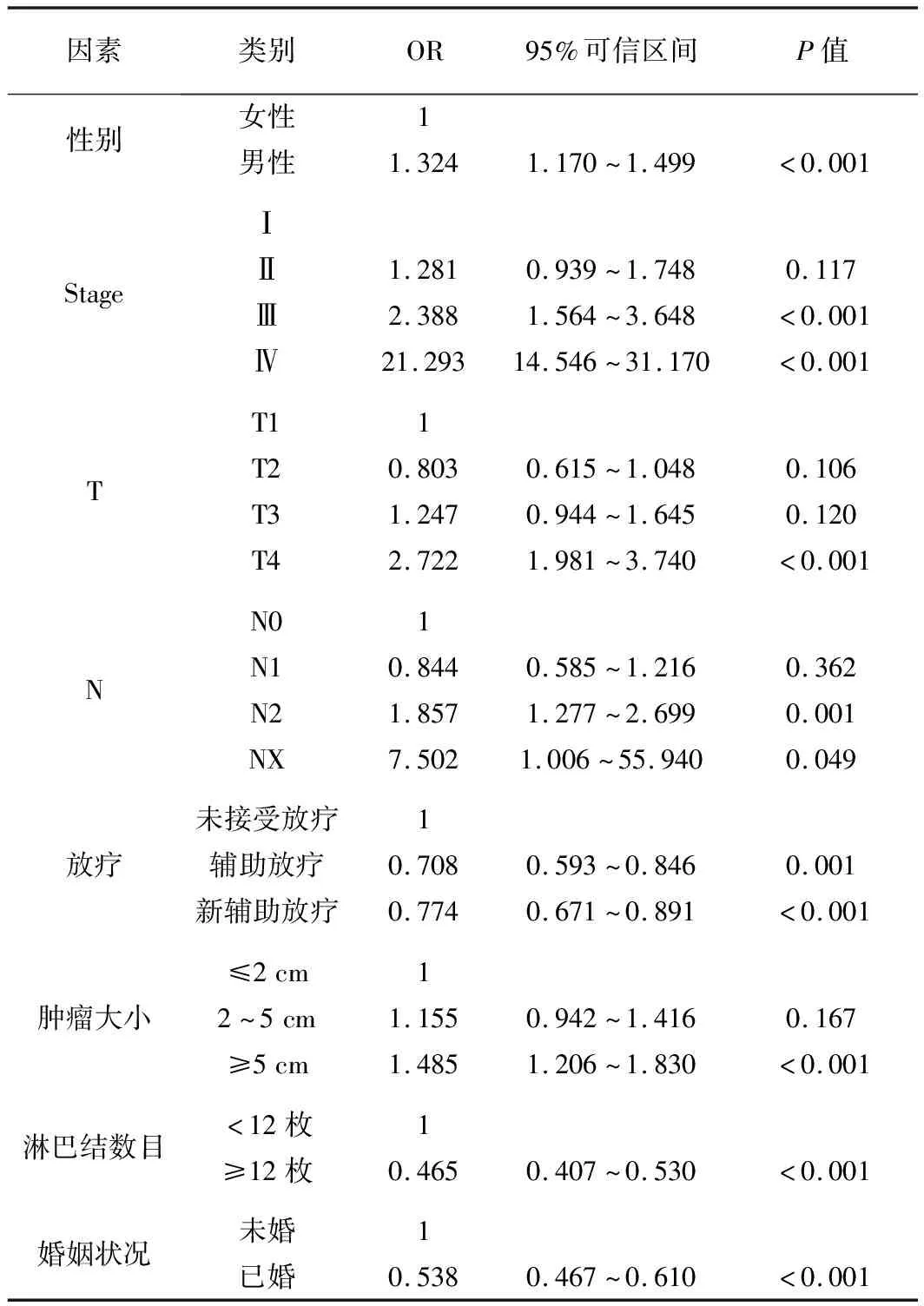
表2 年輕直腸癌5年死亡風險多因素分析
2.年輕直腸癌5年內死亡風險Nomogram:整合多因素分析結果中年輕直腸癌5年死亡風險因素,構建Nomogram模型(圖2)。Nomogram顯示,Stage分期對年輕直腸癌病人5年死亡風險影響最大,其次是N分期、T分期、淋巴結數量、放療,影響最小的是性別。Nomogram中每例病人的5年死亡風險是通過病人具備的每個因素在Nomogram中點尺度軸的得分相加得到一個總分,然后與總分標尺比對得出該病人5年死亡風險概率。例如一例病人:男性、Stage Ⅲ、T3、N2、未接受放療、化療、手術切除淋巴結少于12枚、未婚,這名病人的總分約為120.5分,總分標尺對應的5年死亡風險概率在0.5~0.6之間。
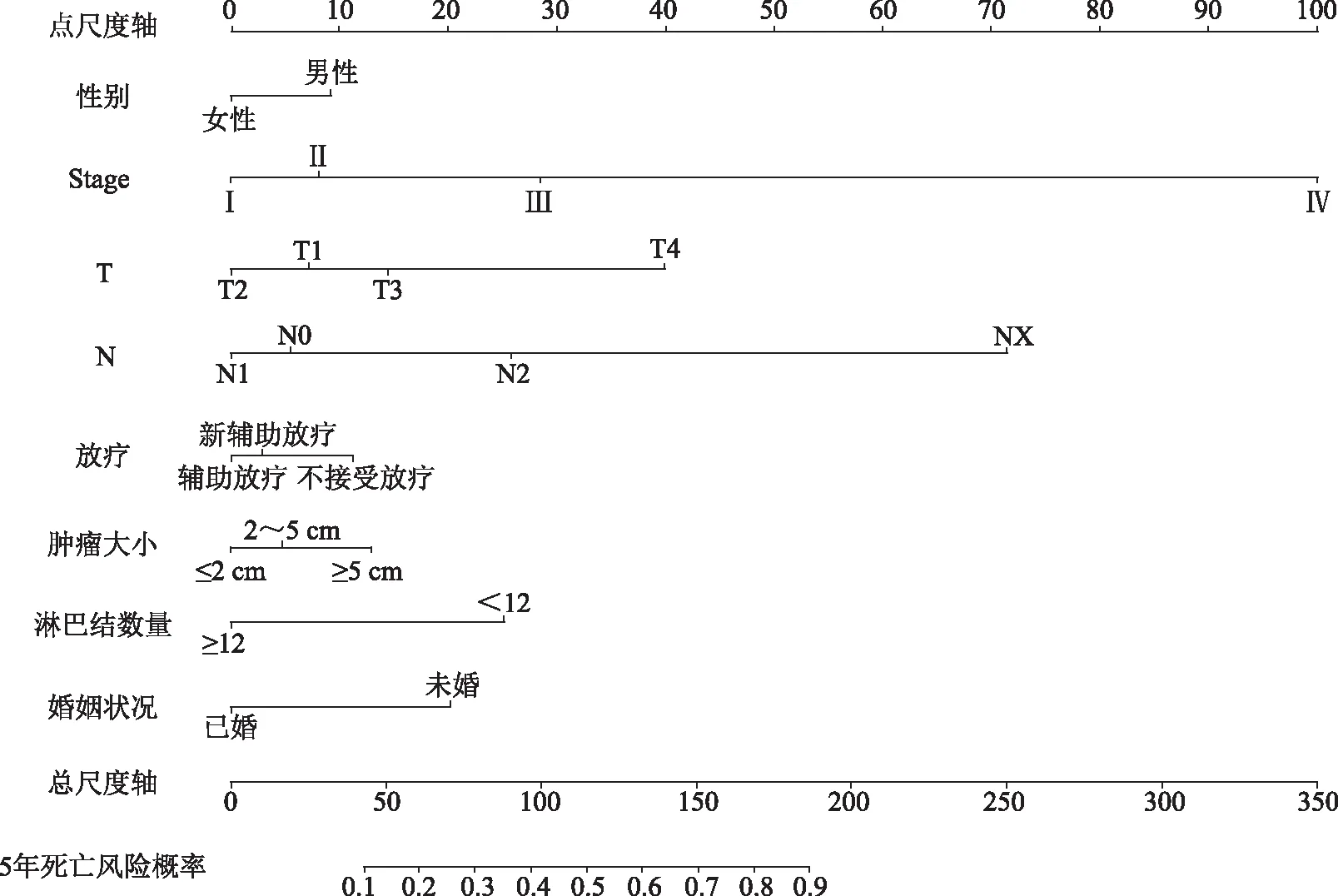
圖2 年輕直腸癌5年死亡風險Nomogram預測模型
3.評價Nomogram圖預測模型:繪制Nomogram預測模型的ROC曲線(圖3),ROC曲線下面積(0.833,95%CI 0.823~0.843,P<0.001);繪制Nomogram預測模型的校準曲線(calibration curve)(圖4)。校準曲線顯示,模型預測5年死亡風險概率與實際5年死亡風險概率相符。
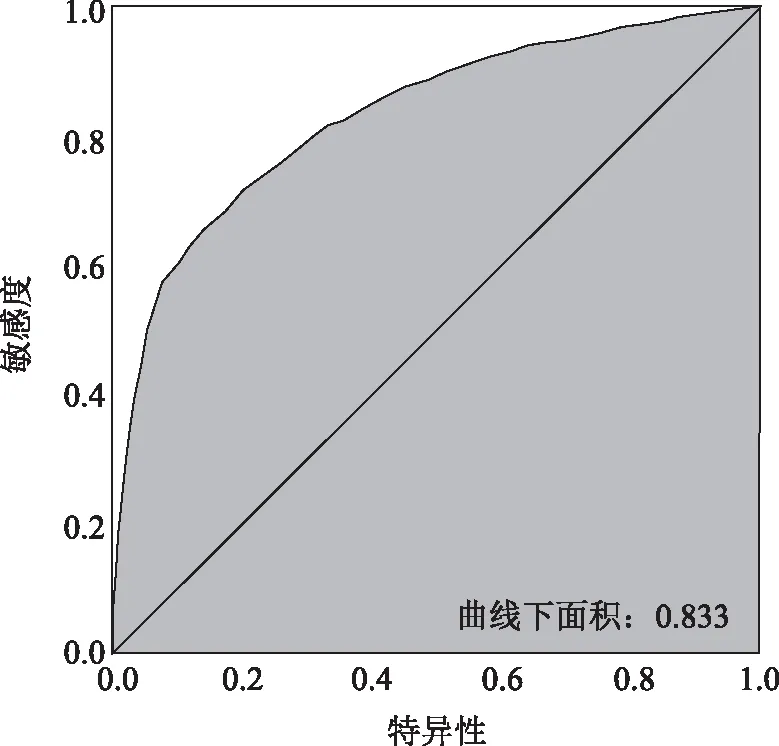
圖3 圖3 Nomogram預測模型的ROC曲線
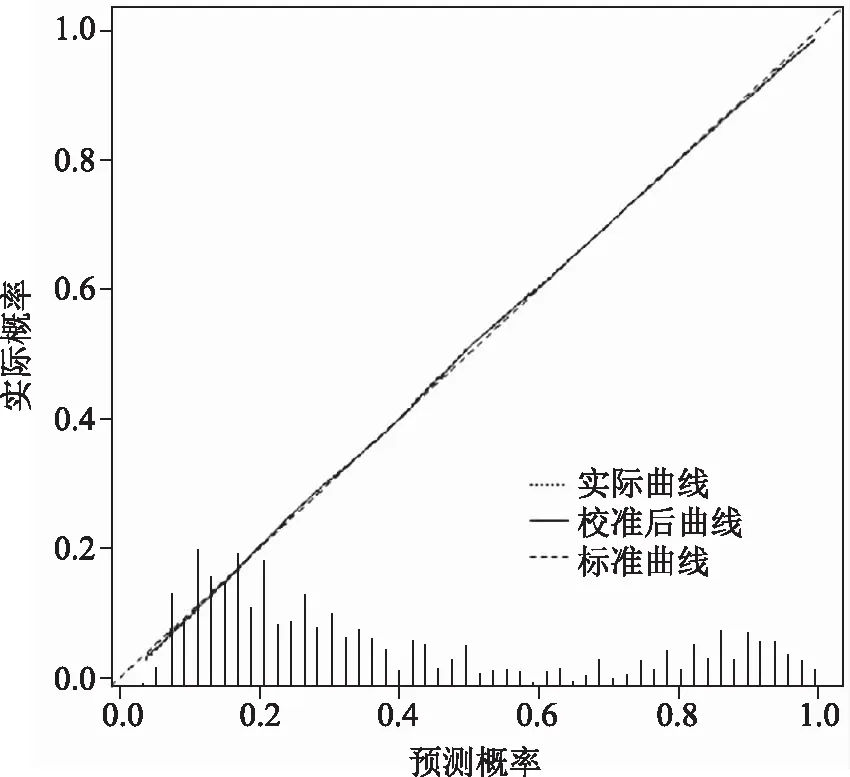
圖4 Nomogram預測模型的校準曲線
討論
目前,年輕直腸癌死亡風險尚不確切。有研究表明,吸煙、吻合口瘺、硝酸鹽、腫瘤浸潤腸壁外靜脈、手術清除淋巴結數目少于12枚是直腸癌的死亡風險因素[10-14]。本研究提出的Nomogram提示淋巴結數目小于12枚淋巴結的病人5年內死亡風險相對較大,這與上述研究手術清除淋巴結數目小于12枚增加死亡風險一致,同時,與目前AJCC和UICC推薦的直腸癌病人至少切除12枚淋巴結一致[15-16]。
我們的研究中,Stage分期對病人死亡風險的影響最大,其次是N分期、T分期、淋巴結數量、腫瘤大小,影響最小的是性別。目前的AJCC分期系統是預測病人生存和指導癌癥病人治療的重要工具,但AJCC分期系統里沒有包括病人的人口統計信息的影響。我們研究中包含了AJCC分期及人口統計信息,預測的準確性更高。
年輕直腸癌發病率逐年增加,而且發病率增加不僅僅是在西方國家,在一些亞洲國家也是一樣。韓國年輕直腸癌發病率明顯增加[17]。目前研究表明,對于年輕直腸癌發病率增加的危險因素包括久坐的生活方式、肥胖癥和糖尿病等因素[18-19]。但有研究表明,年輕直腸癌發病與運動和肥胖無關,而是與久坐不動的看電視等不活躍的生活方式相關[20]。年輕直腸癌病人腫瘤惡性程度高、診斷時分期晚、可切除性差及術后遠處復發風險高[21-23]。年輕病人直腸癌病理類型中,低分化、黏液腺癌和印戒細胞腺癌等高惡性程度類型占比明顯增加[24]。
我們研究表明,性別、Stage分期、T分期、N分期、淋巴結數量、放療、化療和婚姻狀態為年輕直腸癌5年死亡風險因素,并構建Nomogram顯示:Stage分期對年輕直腸癌病人5年死亡風險影響最大,其次是N分期、淋巴結數量、T分期等因素。我們是首次構建Nomogram來預測年輕直腸癌病人5年死亡因素的研究。而且研究表明,年輕直腸癌5年內死亡具有明顯差異,我們基于SEER數據庫構建Nomogram預測模型的準確性評價由ROC曲線和校準曲線驗證,ROC曲線及曲線下面積(0.833,95%CI 0.823~0.843,P<0.001)及校準曲線都顯示模型預測年輕直腸癌5年死亡風險的準確性。本研究是回顧性臨床數據分析研究,在一定程度上能準確的預測年輕直腸癌病人5年死亡風險概率,但仍需大樣本臨床隊列研究或隨機對照試驗驗證。
構建的Nomogram 能有效預測年輕直腸癌病人5年內死亡風險,對年輕直腸癌的預后干預具有臨床指導意義。

