對活化能相關模型的反思
鄒國華 童文昭 楊梓生


摘要:模型與建模在科學教育中具有重要地位,以活化能相關模型作為研究對象,發現活化能相關模型教學中存在未正確理解模型內涵,導致迷思概念以及固守已有模型形成思維定勢等問題。分析問題出現的原因,對活化能相關的模型教學進行反思,為科學模型教學提出相應的建議。
關鍵詞:科學模型;活化能;模型教學
文章編號:1005-6629(2021)05-0091-06 中圖分類號:G633.8 文獻標識碼:B
模型與建模的研究由來已久,其外顯的思想溝通和表達作用以及強大的解釋和預測功能,使其受到科學研究者的廣泛重視,而模型和建模對于科學研究的重要性在很大程度上決定了其在科學教育中的重要地位。科學家在科學研究中常通過科學建模來記錄、描述研究成果,以便更好地理解和運用成果;在教育領域,教育家也提出要通過科學模型和建模來提升教師和學生對科學本質的理解,提高他們對復雜問題的解決能力。王磊認為,科學模型是對于一個復雜系統的簡化和抽象表示,目的是用來解釋或者預測某些科學現象;科學建模指產生科學模型的過程,是一個動態的歷程,通常包括建構、應用、評估和修正四個方面。
《普通高中化學課程標準(2017年版)》首次將“模型認知”寫入其中,并將其歸為化學學科核心素養之一。此后,化學學科關于模型與建模的研究受到前所未有的重視,相關研究成果如雨后春筍般涌現。模型在科學認識中具有描述、解釋和預測等功能,是理論發展的一種重要方式,教學中模型的使用能促進學生對學科核心概念、科學本質的理解。從教學實踐來看,科學模型的教學方面還存在一些值得思考和改進的問題,下面以與活化能相關的幾個模型為例進行分析探討。
1活化能相關模型教學中存在的問題及討論
1.1未理解模型內涵,導致迷思概念
教學建模的目的之一是將科學知識、規律等內容深入淺出地進行表征,促進學生對科學本質的理解。正確理解教學中的模型,應先厘清各概念的內涵與外延,梳理概念與概念之間的聯系,否則,可能因未正確理解模型,導致迷思概念,對后續學習造成一定的困擾。
魯科版化學必修第二冊第2章第2節“化學反應與能量轉化”中,教材為了闡述反應過程中鍵能與能量變化的關系,呈現了如圖1所示的模型,并注釋“E1為破壞舊化學鍵吸收的能量,E2為形成新化學鍵釋放的能量”。人教版化學反應原理第二章第一節“化學反應速率”中,以圖2所示模型解釋反應物、生成物的能量與活化能的關系,文中解釋“E1表示反應的活化能,E2表示活化分子變成生成物分子放出的能量”,圖1和2是高中階段常見模型,在作業、試題中頻繁出現。表面上看,圖1和2基本相同,而E1在圖1代表破壞舊化學鍵吸收的能量,在圖2代表活化能。交談中發現,不少教師、學生由圖1和圖2總結出“破壞舊化學鍵吸收的能量等于活化能”“反應物的總鍵能等于活化能”等結論。那么,反應物的總鍵能是否等于活化能?鍵能與活化能之間有怎樣的聯系?為此,筆者開展了相應的科學模型教學的研究。
1.1.1正確理解活化能的科學模型
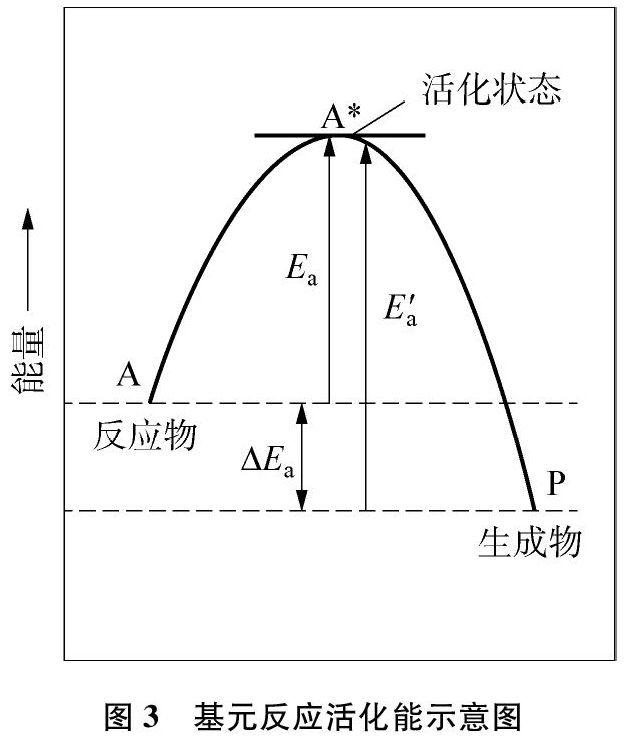
《普通高中化學課程標準(2017年版)》關于活化能內容要求為:知道化學反應是有歷程的,認識基元反應活化能對化學反應速率的影響。活化能具體內涵不屬于高中化學課程的要求,各版高中化學教材也未做深入介紹,而高中常出現與活化能相關的科學模型,學生容易因未正確理解而產生困惑。作為教師,應先理解活化能的科學模型,在學生存在困惑時深入淺出地進行解惑。
1.1.2厘清鍵能、活化能兩個模型間的關聯
高中階段將“101.3 kPa、298 K條件下,斷開1molAB(g)分子中的化學鍵,使其分別生成氣態A原子和氣態B原子所吸收的能量稱為A—B鍵的鍵能”,從定義可知,鍵能與活化能之間有區別,通過查閱資料發現,可通過鍵能粗略估算活化能。

