水提法提取香蕉皮淀粉的工藝研究
劉濤,張鐵鵬,劉寧,李昌虎,王璇
(哈爾濱商業大學食品科學與工程重點實驗室,哈爾濱 150076)
香蕉是熱帶、亞熱帶的特色水果,不僅營養價值豐富,而且香蕉產量很大,經濟價值也很高。數據顯示,2015年我國種植香蕉的總體面積達到了41.2萬公頃,每年生產的香蕉總量高達1246.7萬噸,平均單產達到了30.26 t/hm2。香蕉有穩定血壓、預防心血管疾病、防治動脈硬化和改善免疫系統等功效,還可以幫助減肥[1-4],所以香蕉的適用人群很廣,對香蕉的贊譽聲不絕于耳。但香蕉屬于呼吸活躍型的水果,因為運輸的過程路途較遠,香蕉會因呼吸而變質,且遠途的貯運保鮮非常困難,因此導致香蕉產量迅速增加,但是其銷售跟不上,使得香蕉采摘后損失特別大,嚴重損害了香蕉的經濟效益[5-8]。因此,香蕉產業所衍生出來的各種深加工行業紛紛發展起來。但是香蕉皮通常不被重視,作為廢棄物而被丟棄或者焚燒,給環境帶來不良的影響[9]。國外研究表明,香蕉皮提取有著很高的價值,是植物提取的最佳原料。香蕉皮里富含營養物質,如淀粉、果糖和多種人體所需的微量元素K、Ca、Mg、S、Fe、Zn等,通過香蕉皮提取得到的淀粉可以被當作脂肪的替代物,用于替代油脂和奶油,當被用于熟肉制品中時可以替代肉制品灌肉腸內50%的脂肪,也可被添加到面包、餅干等產品的配料中,都極大地降低了添加食品的脂肪含量,使食品更加健康,也可添加到膨化食品中,或作為香腸、冰淇淋等的凝固劑來改變食品的色澤和風味,所以香蕉皮可作為潛在的資源與原材料[10-11]。
目前,我國對于香蕉淀粉提取的研究很少。而我國的香蕉種植廣泛,產量大,主要是鮮吃,深加工少,運輸和保鮮技術也有待發展,造成大量的香蕉壞掉,經濟損失巨大[12],所以香蕉皮是可供淀粉提取的另一種資源。通過本試驗的開展,可使香蕉皮中的淀粉最大限度地被提取應用,同時也提供了一個香蕉皮深加工的新思路。
1 試驗部分
1.1 試驗材料、試劑與儀器
1.1.1 主要試驗儀器
V-1000可見分光光度計 翱藝儀器(上海)有限公司;HH.S11-2-S電熱恒溫水浴鍋 上海躍進醫療器械廠;DHG-9035A電熱恒溫鼓風干燥箱 上海一恒科技有限公司;TDL-80-2B離心機 上海安亭科學儀器廠;標準檢驗篩;分析天平等。
1.1.2 試驗試劑與材料
香蕉:市售;無水乙醇(AR)、碘(AR)、硝酸鈣(AR)、碘化鉀(AR)、可溶性淀粉等。
1.2 試驗方法
1.2.1 香蕉皮預處理及溶液配制
將待處理的香蕉皮里面的白色物質刮層后放入恒溫鼓風干燥箱中,先將溫度設定為80 ℃,對香蕉皮里面刮層后物質烘干直至恒重。將烘干后的原料用研缽研磨至粉末狀,分別使用20,40,60,80目篩篩選不同目數的香蕉皮粉末,收集粉末分裝到試劑瓶里,備用。
1.2.2 淀粉的提取以及性能測定1.2.2.1 淀粉的提取
在分析天平上準確稱量一定量處理好的香蕉皮粉末,把量取后的香蕉皮粉末置于研缽中,然后用5 mL的移液管準確移取5 mL一定體積分數的乙醇溶液,用研棒研磨1 min左右。轉到離心管中,在3000 r/min的轉速下離心10 min,取出后倒掉上層清液,用移液管準確移取5 mL蒸餾水于離心管中進行清洗,繼續在3000 r/min的條件下離心10 min后去除上層清液,然后準確移取5 mL一定濃度的硝酸鈣水溶液懸浮洗滌殘渣,把離心管1中的樣品轉入玻璃試管中,在已經加熱至沸騰的水浴鍋中加熱10 min,然后把試管中的樣品重新轉入離心管中在4000 r/min下離心4 min,最后將離心后的上清液放入容量為20 mL的瓶中,在此過程中提取2次殘渣,然后與提取的液體結合3次,再放入容量為20 mL的瓶中。
1.2.2.2 淀粉含量的測定
標準添加法測定:取3個比色皿,其中一個加入樣品液1 mL,在另一個比色皿中加同樣體積的樣品液和1 mL 100 μg/mL的淀粉標準溶液,然后用移液管稱量1 mL的蒸餾水加入第一個比色皿中補足2 mL,在第三個比色皿中用移液管準確稱量2 mL蒸餾水,最后用1 mL移液管準確移取0.1 mL NI2-KI分別加入3個比色皿中搖勻,用可見分光光度計在620 nm處測定吸光度,用公式(1)、(2)計算樣品中的淀粉含量及提取率。
1.2.2.3 淀粉總含量的測定及提取率的計算

(1)
式中:X為標準曲線上查到的樣品的淀粉濃度(μg/mL);Vt為樣品的總體積(mL);2為每支測定比色皿里樣品的總體積(mL);Vu為每支比色皿里的樣品原液體積(mL);W為樣品的質量(g);1000為將μg換算成為mg。

(2)
式中:X為稀釋至2 mL時的樣品濃度(μg/mL);Ax為樣品測定出來的顯色值;A50+X為加入標準淀粉使濃度提高之后的顯色值;50為加入標準淀粉使淀粉的濃度提高50 μg/mL。
計算出結果,再將解出來的X代入公式(1)中,可以得出樣品中淀粉的含量。
1.2.2.4 透明度的測定
準備50 mL 1%的淀粉乳,加熱攪拌15 min,冷卻至室溫。利用紫外分光光度計測定620 nm處淀粉糊的透光率,由公式(3)計算:
A=-lgT。
(3)
式中:A為吸光度值;T為透光率。
1.2.2.5 凍融穩定性的測定
準備8%淀粉懸浮液,加熱攪拌保持30 min,在振蕩水浴中將其降溫到50 ℃。稱量20 g淀粉糊置于已經稱重過的50 mL離心管m0,稱重m1,然后放入-20 ℃的冰箱中48 h。在室溫下4 h進行3個凍融循環,在3000 r/min離心15 min除去上層清液并稱重m2,用凍融析水率表示淀粉凍融穩定性,凍融析水率(ws)由公式(4)計算:
(4)
1.2.2.6 淀粉凝沉性和抗老化性的測定
準備1%淀粉乳,在100 ℃的磁力攪拌器中將其加熱至凝膠化,然后在室溫下冷卻,用1 cm比色皿測量650 nm處的透光率,并在靜置24 h后測定。
1.2.3 提取香蕉皮中淀粉的單因素試驗
1.2.3.1 不同體積分數的乙醇對香蕉皮中淀粉提取率的影響
準確稱量0.1 g處理好的相同目數過篩的香蕉皮粉末,各自采用體積分數20%、40%、60%、80%的乙醇5 mL,設置硝酸鈣濃度為80%,用不同體積分數的乙醇研磨0.1 g的香蕉皮粉末1 min左右,再把樣品加入離心機中采用3000 r/min的轉速離心10 min,倒掉上層清液,然后準確移取5 mL蒸餾水洗滌樣品,再次加入離心機中在3000 r/min的條件下離心10 min后棄去上層清液,然后加入相同體積分數80%的Ca(NO3)225 mL,將樣品放到試管中在沸水浴中加熱10 min,取上層的清液于容量瓶中,按此步驟再重復提取2次后定容。按公式(1)和公式(2)計算樣品中淀粉的提取率。
1.2.3.2 不同硝酸鈣濃度對香蕉皮中淀粉提取率的影響
準確稱取0.1 g處理好的相同目數過篩的香蕉皮粉末,在相同的乙醇體積分數60%條件下加入5 mL,設置不同的硝酸鈣濃度為75%、80%、85%、90%,用相同體積分數的乙醇60%分別研磨0.1 g香蕉皮粉約1 min,然后將樣品加入離心機中,用3000 r/min的速度離心10 min,然后丟棄上層的清液。取出5 mL蒸餾水,準確洗滌樣品,加入離心機中,以3000 r/min離心10 min,再次丟棄上層的清液,向樣品中加入相同濃度的Ca(NO3)225 mL,在沸水浴中加熱10 min。以4000 r/min的速度離心4 min后,將上清液轉移到容量瓶中,重復2次提取后設定體積。按公式(1)和公式(2)計算樣品中淀粉的提取率。
1.2.3.3 不同過篩目數對香蕉皮中淀粉效率的影響
準確稱取0.1 g處理好的20,40,60,80目的香蕉皮粉末,在相同的60%乙醇體積分數條件下加入5 mL,在相同的80%硝酸鈣濃度條件下,分別研磨不同目數的0.1 g香蕉皮粉末1 min左右,然后將樣品加入離心機中采用3000 r/min的轉速離心10 min后倒掉上層的清液,在準確移取5 mL蒸餾水洗滌樣品,加入離心機中用3000 r/min的轉速離心10 min后再次棄去上層的清液,分別加入與之前相同濃度的Ca(NO3)225 mL,將樣品放到試管中在沸水浴中加熱10 min,最后在4000 r/min轉速下離心4 min,取上層的清液于容量瓶中,按此步驟再重復提取2次后定容。按公式(1)和公式(2)計算樣品中淀粉的提取率。
1.2.4 響應面設計方案
在單因素試驗的基礎上,根據單因素試驗數據的分析研究,對乙醇體積分數、硝酸鈣濃度和香蕉皮粉篩數3個因素進行了響應面分析[13]。通過響應面法和響應面圖的試驗設計,優化了碘顯色法從香蕉皮中提取淀粉的工藝。以乙醇體積分數(A)、硝酸鈣濃度(B)、香蕉皮粉末過篩目數(C)3個因素為獨立變量,用+1,0和-1代表各因素的高、中、低水平。其中,-1,0和+1為自變量,即各因子的低、中、高水平。試驗因素的設計和編碼見表1。

表1 因素水平設計及編碼
2 結果與討論
2.1 單因素試驗
2.1.1 不同體積分數乙醇對淀粉提取率的影響
為了確保試驗中使用最佳的乙醇體積分數,分別配制不同體積分數的乙醇,進行單因素試驗。除了采用的乙醇體積分數不同外,對淀粉進行碘顯色法提取的其他條件都相同。乙醇的體積分數為20%、40%、60%、80%時,相應的淀粉提取率見圖1。
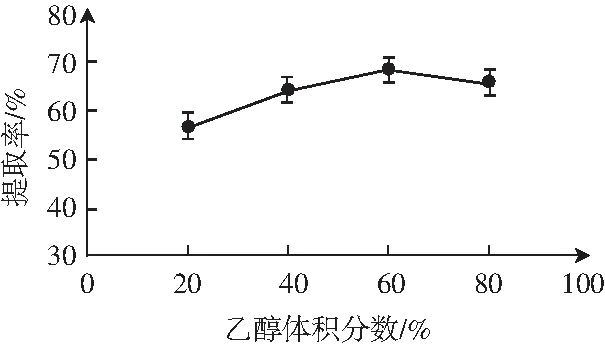
圖1 乙醇體積分數對淀粉提取率的影響
由圖1可知,當乙醇體積分數為20%、40%、60%時,乙醇對香蕉皮中淀粉的提取率會伴隨乙醇體積分數的變大而變大,當乙醇體積分數為60%時,乙醇對淀粉的提取率最高;而當乙醇體積分數大于60%時,乙醇對香蕉皮中淀粉的提取率會伴隨乙醇體積分數的變大而變小。這是由于如果乙醇體積分數過大,乙醇會揮發而對香蕉皮粉末研磨不充分,影響提取效率,而乙醇體積分數過小則對香蕉皮粉末的研磨和提取不充分[14],除此之外,因為研磨是用研缽人工進行,對香蕉皮粉末研磨的力度會有差異,從而影響了對淀粉的提取率,造成提取淀粉的準確性有誤差。綜合考慮,選擇40%、60%、80%的乙醇體積分數作為響應面水平。
2.1.2 Ca(NO3)2溶液濃度對淀粉提取率的影響
硝酸鈣濃度為75%、80%、85%、90%時,相應的淀粉提取率見圖2。
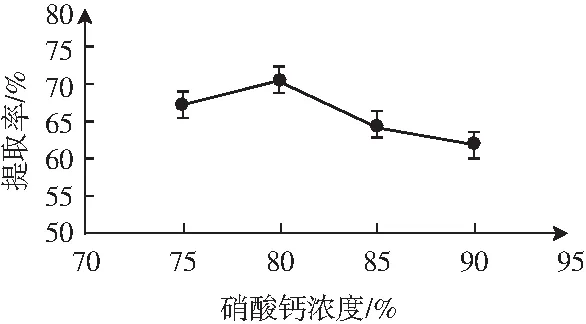
圖2 Ca(NO3)2溶液濃度對淀粉提取率的影響
由圖2可知,當硝酸鈣濃度小于80%時,硝酸鈣對淀粉的提取率會隨著硝酸鈣濃度的增大而增大,當硝酸鈣濃度為80%時,硝酸鈣濃度對淀粉的提取率最大;而當硝酸鈣濃度大于80%時,硝酸鈣對淀粉的提取率會隨著硝酸鈣濃度的增大而減小。這可能是因為硝酸鈣濃度增大會影響香蕉皮中雜質溶出的效果;也可能是由于當硝酸鈣濃度為80%時,其化學結構所擁有極性最適合于淀粉的大量溶出,所以當硝酸鈣濃度大于80%時淀粉的溶出量會減少,相應地硝酸鈣濃度對淀粉的提取率也會變低。綜合考慮試驗的結果與節約原料的要求,選擇硝酸鈣濃度為75%、80%、85%作為響應面水平。
2.1.3 香蕉皮粉末過篩目數對淀粉提率影響
當香蕉皮粉末過篩目數分別為20,40,60,80目時,相應的淀粉提取率見圖3。

圖3 香蕉皮粉末過篩目數對淀粉提取率的影響
由圖3可知,當篩孔數小于40目時,碘顯色法提取淀粉的速度隨篩孔數的增加而增加。當過篩目數為40目時,碘顯色法提取淀粉的速度最高。當過篩目數大于40目時,碘顯色法對淀粉的提取率則會隨著過篩目數的增加而減小。這可能是由于過篩目數為40目時,香蕉皮粉末在這個粒徑研磨比較充分,會與乙醇有一個良好的接觸,對淀粉的提取效率高。當過篩目數大于40目時,香蕉皮粉末會非常細膩,雖然會與乙醇的接觸更加充分,但是研磨起來只會隨著研棒的轉動粉末隨之轉動,對香蕉皮的粉末研磨不會特別充分。所以綜合考慮,選擇過篩目數20,40,60目作為響應面水平。
2.2 響應面結果與分析
為了優化通過單因素試驗確定的淀粉提取工藝條件,采用Box-Behnken對試驗方案進行設計[15],對淀粉提取工藝產生影響的主要因素進行優化試驗,選擇乙醇體積分數、硝酸鈣濃度、香蕉皮粉末過篩目數3個因素作為主要影響因素做顯著水平表,試驗結果見表2。

表2 響應面試驗方案設計和結果
將表2所得的所有試驗數據采用Design Expert 7.0.0統計軟件進行響應面分析[16],得到回歸模型的方差分析表,見表3。
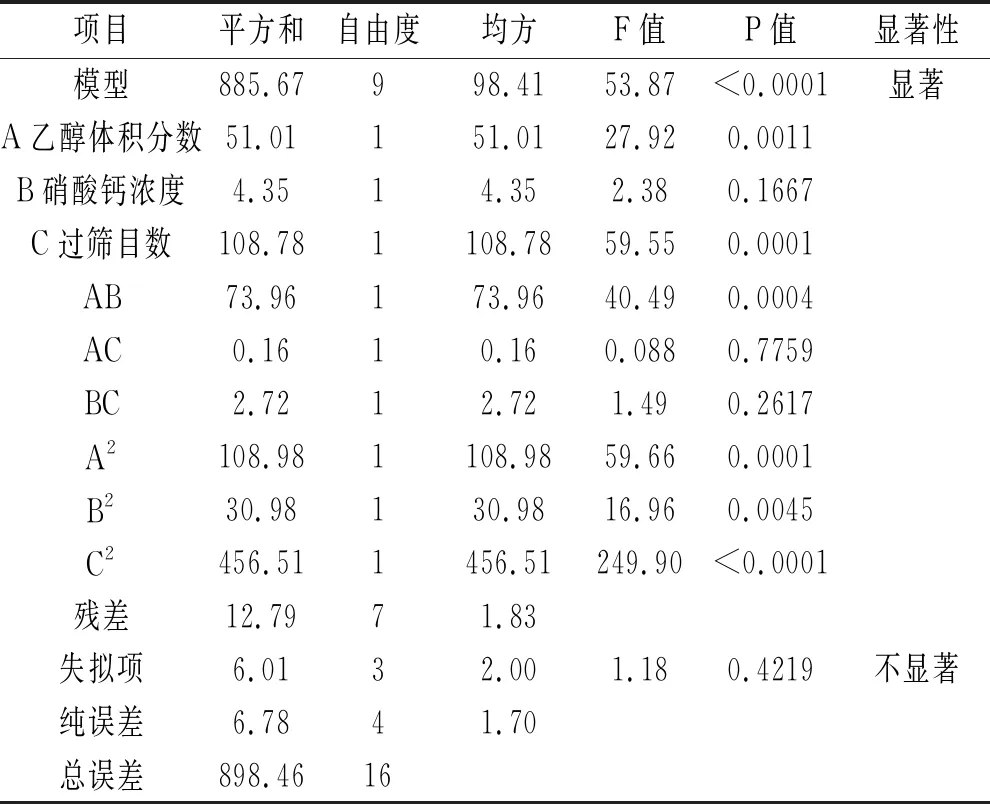
表3 二次項模型的線性系數及試驗結果的方差分析
利用Design-Expert 7.0.0軟件對17組試驗方案的試驗數據進行多重二次擬合,得到了乙醇體積分數(A)、硝酸鈣濃度(B)、香蕉皮粉末過篩目數(C)3個因素對淀粉提取率(Y)的回歸模型,試驗方案由4個水平組成,由單因素的方差分析確定。對淀粉提取率(Y)的回歸模型為:
Y=73.50+2.53A+0.74B+3.69C+4.30AB+0.20AC+0.83BC-5.09A2-2.71B2-10.41C2。
由表3可知,回歸模型極顯著(P<0.0001),失擬項不顯著(P=0.4219>0.05),回歸模型的決定系數R2=0.9858,說明可以用該模型對香蕉皮中淀粉的提取率進行較好的預測[17]。
由表3方差分析結果可知,在一次項A,B,C中,對香蕉皮中淀粉提取效果的影響極其顯著的因素為乙醇體積分數和香蕉皮粉末過篩目數,即A,C兩個因素,其P值接近0.0001,達到顯著水平;硝酸鈣濃度即因素B對香蕉皮中淀粉提取效果的影響較小;將3個因素對淀粉提取效果影響程度大小進行排序,依次為香蕉皮粉末過篩目數>乙醇體積分數>硝酸鈣濃度,即C>A>B。
在二次項A2、B2、C2中,乙醇體積分數、硝酸鈣濃度、香蕉皮粉末過篩目數中,對香蕉皮中淀粉提取率的影響達到極其顯著的是C2,其P值滿足P<0.0001;乙醇體積分數的二次項A2的P值接近0.0001,達到顯著水平,而硝酸鈣濃度的二次項B2對香蕉皮中淀粉提取率的影響不顯著。
在交互項AB、AC、BC中,乙醇體積分數與硝酸鈣濃度、乙醇體積分數與香蕉皮粉末過篩目數以及硝酸鈣濃度與香蕉皮粉末過篩目數之間的交互作用,AB這一組的交互作用對香蕉皮中淀粉的提取率產生了較顯著的影響,體現為P值接近0.0001;乙醇體積分數與香蕉皮粉末過篩目數和硝酸鈣濃度與香蕉皮粉末過篩目數即AC、BC這兩組的交互作用對香蕉皮中淀粉的提取率均不產生顯著影響。
由此對得出的回歸方程進行優化[18],剔除二次完全回歸方程中的不顯著因素B、AC、BC、B2,由此得到新的二次回歸方程為:
Y=73.50+2.53A+3.69C+4.30AB-5.09A2-10.41C2。
由上述回歸方程得出響應面分析圖和相應的等值線,見圖4~圖6。
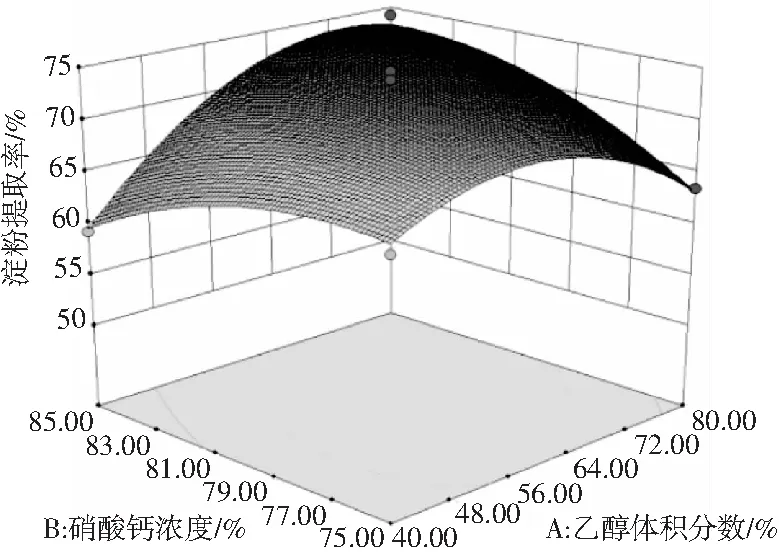
圖4 硝酸鈣濃度與乙醇體積分數交互作用影響淀粉提取率的曲面線圖

圖5 過篩目數與乙醇體積分數交互作用影響淀粉提取率的曲面線圖

圖6 過篩目數與硝酸鈣濃度交互作用影響淀粉提取率的曲面線圖
由圖4~圖6各因素的相互作用對香蕉皮淀粉提取效果的影響可以直觀地看出,若曲線的曲面越凹凸,表示該組因素的響應面值變化程度越大,代表其交互作用對香蕉皮中淀粉的提取效果影響越大。通過比較3組圖可知,乙醇體積分數與香蕉皮粉末過篩目數的交互作用,即AC這一組的交互作用對香蕉皮中淀粉的提取率影響較大,表現為響應面圖較陡,即響應面值的變化程度大;而乙醇體積分數與硝酸鈣濃度和香蕉皮粉末過篩目數以及硝酸鈣濃度的交互作用,即AB、BC這兩組的交互作用對香蕉皮中淀粉提取效果胡影響則不明顯,表現為響應面曲線比較平滑。綜上所述,可知響應面分析的結果和方差分析的結果完全相符。
采用優化的二次回歸模型對數據進行分析,得到了淀粉的最佳提取條件:乙醇體積分數為69.69%,硝酸鈣濃度為82.75%,香蕉皮粉末過篩目數為44.07目,此時香蕉皮中淀粉提取率的理論最大值為74.69%。為了便于實際操作量取、設置的準確,將香蕉皮中淀粉的最佳提取工藝修正為:乙醇體積分數為70%,硝酸鈣濃度為80%,香蕉皮粉末過篩目數為40目。按照得到的最佳提取工藝條件,對香蕉皮中的淀粉進行提取,且進行了3次平行驗證試驗,得到當處于最佳的提取工藝條件下時,淀粉的提取率平均值是73.8%,該值和模型的預測值基本相符,說明運用響應面法進行優化得到的香蕉皮中淀粉的提取工藝條件在實踐中是行之有效的。
2.3 香蕉皮淀粉性能檢測
2.3.1 透光率的測定
利用公式計算樣品的透光率,香蕉皮淀粉的透光率見表4。

表4 透光率性能測定
2.3.2 凝沉性和抗老化性的測定
香蕉皮淀粉的凝沉性和抗老化性的差異可以通過兩次測量之間的數據差異大小來表示,見表5。

表5 凝沉抗老化性測定
2.3.3 凍融穩定性的測定
利用公式計算香蕉皮淀粉的析水率,見表6。

表6 凍融穩定性的測定
3 結論
試驗以香蕉皮內部白色刮層烘干研磨后的粉末為原料,采用水法提取香蕉皮中的淀粉。對乙醇體積分數、硝酸鈣溶液濃度和香蕉皮粉篩數3個因素進行了單因素試驗。同時采用響應面法對試驗方案進行設計,優化了提取工藝,獲得最佳的提取條件。結果表明,采用水提取法對香蕉皮中淀粉進行提取的最佳工藝條件為:乙醇體積分數為70%,硝酸鈣濃度為80%,香蕉皮粉末過篩目數為40目,此條件下香蕉皮中淀粉的提取率為74.69%。根據此次試驗分析,可得出利用碘顯色法進行香蕉皮中淀粉提取具有操作簡便、提取率高、節能、省時等優點,且性能優異,有利于以后對香蕉皮中淀粉進行各項研究提供參考。

