“素養為本,情境引線”的探究式教學
——以《醛》的教學為例
張 剛
《普通高中化學課程標準(2017 年版)》中指出,要全面發展學生的化學學科核心素養,重視開展“素養為本”的教學,即倡導真實問題情境的創設,開展以化學實驗為主的多種探究活動,重視教學內容的結構化設計,激發學生學習化學的興趣,促進學生學習方式的轉變,培養他們的創新精神和實踐能力[1]。課標對化學教學提出了更高的要求,教師要結合教學內容精心設計教學環節,開展基于核心素養培養的教學活動。學生在習得知識、掌握技能的同時,形成和發展核心素養。筆者以人教版選修5 第三章第三節《醛》為例,通過創設情境、探究活動開展以學科核心素養為導向的課堂教學,以適應新課標的要求。具體教學設計如下:
一、教學設計思路
教學設計的整體思路如圖1
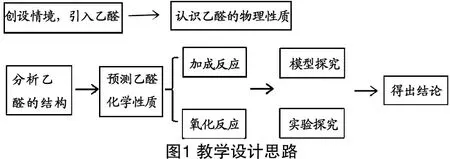
二、教學過程
1.環節一 創設情境,引入乙醛
同樣是喝酒,為什么有些人一喝酒臉就紅得像“關公”,而有些人卻越喝越白似“曹操”?
人的酒量大小與酒精在人體內的代謝有關。乙醇進入人體后,先經乙醇脫氫酶催化變成乙醛,接著乙醛又在乙醛脫氫酶的作用下變成乙酸,最后轉化為CO2和H2O。如果這兩種酶在人體內的含量都很大的話,酒精的代謝速度就很快。但如果這兩種酶的含量比較少,尤其是缺少乙醛脫氫酶的話,乙醛就會在體內大量積累,引起面部血管舒張而臉紅,同時作用于人的神經系統甚至出現醉酒現象。
過渡:喝酒臉紅的主要原因就是乙醛,它就是我們接下來要介紹的主角。
設計意圖:從生活走進化學,親切、自然,利用對生活現象的解釋,吸引學生的好奇心,激發學習熱情。通過對人體內乙醇的代謝過程,引導學生從化學視角看待實際問題。并讓學生學會關注自己的健康。
2.環節二 認識乙醛的物理性質
那么,乙醛是怎樣的一種物質呢? 下面我們來具體地認識一下。展示乙醛溶液,觀察顏色、狀態,并嗅一下氣味。
物理性質:無色、刺激性氣味、液體,密度比水小,沸點20.8℃,易揮發,能跟水、乙醇等互溶。
設計意圖:通過展示乙醛溶液,學生可以直觀感受并自主建構其物理性質,在此基礎上教師再做總結陳述。使學生掌握物質物理性質的學習方法,即一般從顏色、氣味、狀態、熔沸點、溶解性等角度分析。體現了“模型認知”核心素養。
3.環節三 乙醛的結構分析
展示乙醛的立體模型和核磁共振氫譜,讓學生根據原子的成鍵特點以及有機物的分類知識寫出乙醛的結構式,并指出其官能團。
設計意圖:通過立體模型的展示,學生可以直觀地了解乙醛的結構,將抽象的有機物結構具體化。學生通過回顧已學知識來完成結構式的書寫,溫故知新。展示核磁共振氫譜讓學生從氫原子的化學環境角度進一步了解乙醛的結構。由物理性質到物質結構,由表及里,由淺入深逐步認識乙醛。
4.環節四 預測乙醛的化學性質
請你從醛基的結構推測乙醛分子中化學鍵可能的斷裂方式,從而預測乙醛可能發生哪些反應?
學生預測:①醛基中C=O 雙鍵可能像C=C 雙鍵一樣能發生加成反應。
②醛基中C=O 雙鍵對C—H 鍵有活化作用,使C—H 鍵極性變強,可斷裂插入氧原子變為C-OH,被氧化,表現還原性。
設計意圖:分析乙醛的結構特點,用已有的價健和官能團的相關知識預測其可能的化學性質。培養學生的分析、判斷能力,并將“結構決定性質”這個“模型認知”潛移默化,使學生掌握學習有機物的一般方法。
5.環節五 對乙醛化學性質的探究
(1)對預測①進行模型探究
利用乙醛分子和氫氣分子的球棍模型分組拼插,探究乙醛的加成反應。引導學生參照碳碳雙鍵的加成原理寫出乙醛與氫氣加成的化學方程式。并播放乙醛與氫氣反應的模擬動畫。
書寫CH3CHO 與H2的加成反應:
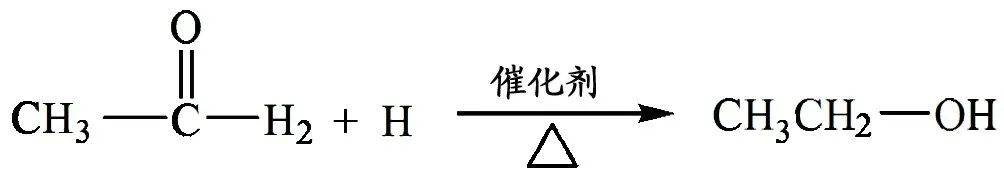
根據有機物的氧化、還原反應的定義判斷,乙醛的催化加氫也是什么反應? 體現了乙醛的什么性質?
回憶、思考:乙醛的催化加氫也是還原反應,說明乙醛有氧化性。

設計意圖:由醛基的不飽和性類比C=C 雙鍵引出加成反應,進而聯想到還原反應,培養學生嚴謹的邏輯思維。認識事物之間存在聯系,且一定條件下可以互相轉化,體現了“變化觀念”核心素養。
(2)對預測②進行實驗探究
你的預測②是否正確? 能通過實驗進行驗證嗎? 如能,請設計實驗方案。學生首先想到向乙醛溶液中滴加酸性高錳酸鉀溶液。
實驗探究1:取適量乙醛溶液于試管中,加入幾滴KMnO4酸性溶液,觀察實驗現象。
實驗現象:KMnO4酸性溶液褪色。
結論:乙醛能被KMnO4酸性溶液氧化,說明乙醛有還原性。
設計意圖:對猜想進行試驗探究,驗證猜想是否正確,體驗科學探究的一般過程,即“假設→設計方案→實驗→觀察現象→思考討論→得出結論”,培養學生的科學探究精神,發展核心素養。KMnO4酸性溶液是學生最容易想到的氧化劑,對乙醛被氧化更容易理解。
乙醛有還原性,還原性強弱如何? 能不能被弱氧化劑氧化呢?
實驗探究2:[與新制銀氨溶液反應]在潔凈的試管里加入1mL2%的AgNO3溶液,然后邊振蕩試管邊逐滴加入2%的稀氨水,至最初產生的沉淀恰好溶解為止,制得銀氨溶液。再滴入3 滴乙醛,振蕩后把試管放在熱水浴中溫熱。觀察并記錄實驗現象[2]。
注意事項:①試管內壁要潔凈。②不能用酒精燈直接加熱,要用水浴加熱。③加熱時不能振蕩或搖動試管。④配制銀氨溶液時,氨水不能過量(防止生成易爆物)。
設計意圖:以弱氧化劑銀氨溶液來探究乙醛的還原性強弱,掌握醛基的特征反應。分組實驗充分體現學生的主體地位,培養學生的實驗操作、觀察及分析能力。在實驗探究前要強調注意事項,加強實驗正確操作培訓,以提高實驗技能。
實驗現象:試管壁上出現閃亮的銀鏡。
討論分析,得出結論:Ag+被還原成Ag,乙醛被氧化,表現強還原性。
反應方程式:Ag+被還原成Ag,同時乙醛得到氧被氧化為乙酸,銀氨絡離子釋放出NH3,生成的乙酸在堿性環境中轉化為乙酸銨,而NH3極易溶于水難以放出氣體。整個反應可巧記為:乙醛和銀氨,生成乙酸銨,還有水、銀、氨,系數一、二、三。
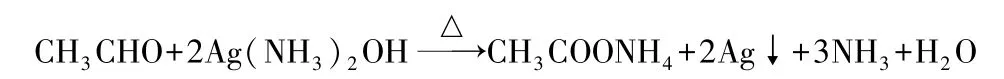
設計意圖:引導學生根據觀察到的實驗現象來判斷反應的產物并分析斷鍵原理,從而了解醛基的特性,并明確官能團對有機物化學性質的決定作用。培養學生的觀察、分析及推理能力,體現“證據推理”核心素養;訓練學生用化學符號表征反應的能力,并將產物口訣化,便于記憶,突破書寫難點。
應用:(1)檢驗醛基。(2)工業上制鏡或保溫瓶膽。
設計意圖:強化“性質決定用途”的觀念,介紹銀鏡反應的實際應用,使學生明白化學可以服務于生活,學有所用。
實驗探究3:[與新制 Cu(OH)2反應]在試管里加入10%的NaOH 的溶液2mL,滴入2%的CuSO4溶液4~6 滴,振蕩后加入乙醛溶液0.5mL 加熱到沸騰,觀察現象[2]。
通過閱讀,你覺得實驗應注意哪些事項:
①氫氧化銅懸濁液必須新制。
②反應發生的條件:堿性環境、直接加熱至沸騰。
設計意圖:以弱氧化劑新制氫氧化銅懸濁液來驗證乙醛的強還原性,進一步了解醛基的特征反應,進一步體驗實驗探究的基本過程,進一步掌握化學實驗的基本方法和技能,發展學生解決綜合實際問題的能力。同時,與生物課上菲林試劑用于葡萄糖的檢驗聯系起來,實現學科間的融合,引導學生從化學的角度來學習和理解生物知識,發展學生的科學素養。
實驗現象:試管內有紅色沉淀產生。
討論分析,得出結論:氫氧化銅跟乙醛反應變成氧化亞銅,銅的化合價降低,Cu 元素被還原,說明乙醛可被氫氧化銅氧化,表現還原性。反應可表示為:

設計意圖:引導學生通過對實驗現象的分析推測乙醛的還原性,培養學生基于證據的邏輯推理能力;回顧氧化還原反應的相關知識,從化合價變化角度分析判斷乙醛被氧化,實現知識遷移,并進一步鞏固學生采用化學符號表征具體反應的能力。
應用:檢驗醛基,醫院里用于尿糖的檢驗。
小結:引導學生小結乙醛的化學性質。乙醛可以被Ag(NH3)2OH、Cu(OH)2等弱氧化劑氧化,說明乙醛有強還原性。
歸納總結乙醛的性質:乙醛既有氧化性又有還原性,但氧化性較弱而還原性較強。
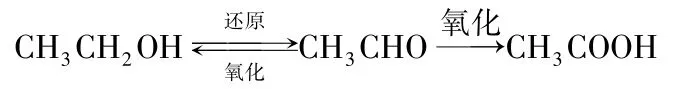
通過本節課的學習,你能解釋酒精在人體內代謝時都發生什么反應嗎?
設計意圖:讓學生自行歸納、總結,形成對所學知識的自我建構。明確醇、醛、羧酸之間是如何轉化的。呼應引入環節,引導學生學以致用,體現了從生活到化學,再從化學回歸生活的思想。
三、教學反思
本設計從熟悉的生活情境入手,更易激發學生的學習興趣,調動學生的主觀能動性。沿著“創設情境→分析結構→預測性質→實驗探究→觀察現象→分析推理→得出結論”這條主線進行探究式教學,環環相扣、層層遞進,激發學生的探究欲望,力求使所有的學生有效地全程參與各個環節。挖掘學生思考問題、解決問題的思維和潛能。逐步完成學生對乙醛知識的自主建構,掌握乙醛的加成反應及氧化反應的原理,形成對“物質結構、性質、用途”三者關系的規律性認知。在此過程中,學生的自主學習能力、觀察能力、和邏輯推理能力都得到了提升,培養了學生的科學探究精神,真正發展了學生的化學學科核心素養。

