NT-proBNP、hs-CRP、LAD與慢性心力衰竭合并心房顫動的相關性
趙美麗,肖立遠,劉 林,康 超,張秋香
(1.金鄉縣人民醫院 心內一科, 山東 濟寧 272200;2.濟寧市第一人民醫院 急診科,山東 濟寧 272000)
慢性心力衰竭(CHF)是多種因素導致的心肌收縮力減弱、心臟泵血功能降低而無法維持心排量的表現。該病常伴發心律失常,尤其以心房顫動最為常見,國外研究報道,在初診心力衰竭患者中,大約1/4的患者合并心房顫動,接近1/5的患者將來發展為心房顫動[1]。心房顫動可進一步影響心臟充盈與泵血功能,損害心功能,誘發嚴重并發癥,增加患者再住院率與死亡率[2-3]。因此,探討CHF患者發生心房顫動的危險因素,并給予適當干預,以維持竇性心律,對于改善CHF患者的預后至關重要。B型利鈉肽(BNP)是由心室肌細胞分泌的神經肽類激素,N末端B型利鈉肽原 (NT-proBNP)是BNP的前體,生物穩定性好,作為 心血管病的預測因子更具優勢。超敏C-反應蛋白(hs-CRP)是由肝臟合成的急性相反應蛋白,本研究分析了NT-proBNP、hs-CRP、左心房內徑(LAD)與CHF合并心房顫動的相關性,以期為該病的診斷與治療提供理論參考。
1 資料與方法
1.1病例選擇 2019年9月-2020年9月我院治療的CHF患者287例,納入標準:(1)符合《慢性心力衰竭診斷治療指南》[4]關于CHF診斷標準;(2)自愿參加研究。排除標準:(1)合并肺、肝、腎系統嚴重疾病;(2)合并血液系統疾病;(3)合并惡性腫瘤;(4)合并心臟瓣膜病、感染性心內膜炎、心包疾病、先天性心臟病、甲亢心臟病等。
1.2方法
1.2.1分組方法 按照是否合并心房顫動,將患者分為兩組,其中合并心房顫動患者91例為觀察組,未合并心房顫動患者196例為對照組。心房顫動診斷標準依據《2019心房顫動患者管理指南更新》[5]。
1.2.2資料收集 建立電子信息表,登記患者性別、年齡、體質量指數(BMI)、飲酒史、吸煙史、合并癥等。
1.2.3實驗室檢驗 采用日立全自動生化分析儀檢測空腹血糖(FBG)、總膽固醇(TC)、甘油三酯(TG)、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、尿酸(UA)、肌酐(Cr)。NT-proBNP采用萬孚免疫熒光飛特多通道檢測儀測定,檢測方法:抽取空腹靜脈全血2 ml,加入到EDTA 抗凝管,4 ℃下離心15 min,轉速3 000 r/min,抽取75 μl血漿,采用熒光免疫分析法行測定。hs-CRP采用德國西門子BN Prospec特種蛋白分析儀及其配套試劑盒,選用免疫散射比濁法檢測,嚴格按照說明書進行操作。
1.2.4影像學檢查 采用超聲心動圖測定左心室收縮末期內徑(LVESD)、左心室舒張末期內徑(LVED)、LAD、左室射血分數(LVEF),按Devereux 校正公式計算左心室質量指數(LVMI)。
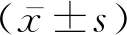
2 結 果
2.1基線資料比較 觀察組病程長于對照組,NYHA 分級為Ⅳ級的患者比例均高于對照組(P<0.01),見表1。
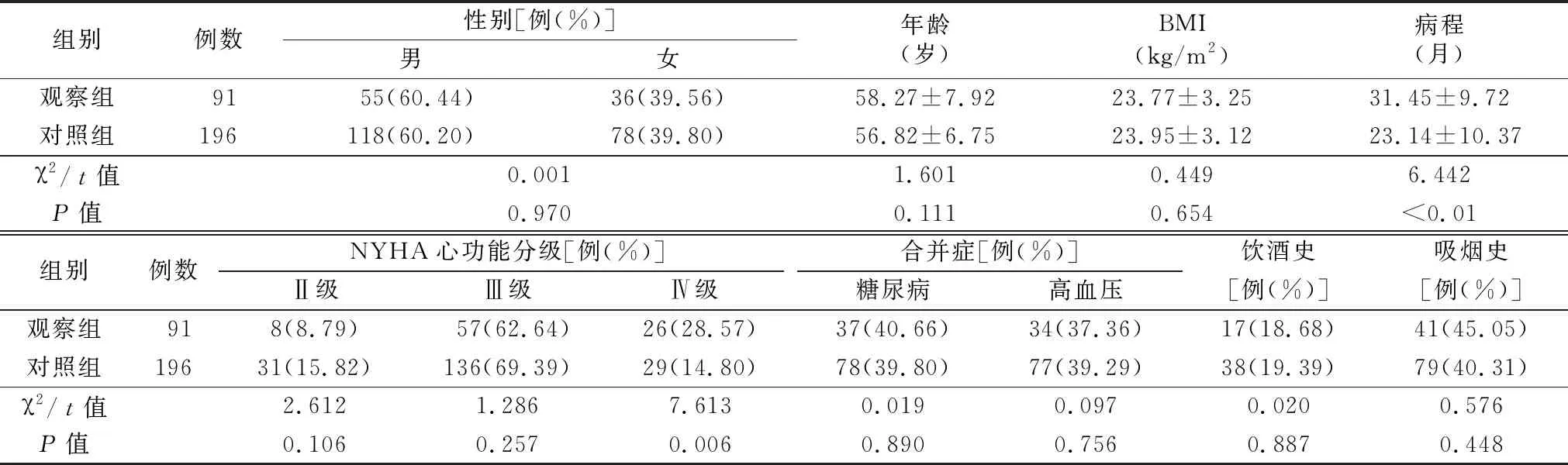
表1 兩組一般資料比較
2.2血糖、血脂、腎功能指標比較 觀察組UA、Cr高于對照組(P<0.01),兩組其他指標差異無統計學意義(P>0.05),見表2。
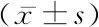
表2 兩組血糖、血脂、腎功能指標比較
2.3NT-proBNP與hs-CRP水平比較 觀察組NT-proBNP與hs-CRP水平高于對照組(P<0.01),見表3。
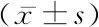
表3 兩組NT-proBNP與hs-CRP水平比較
2.4超聲心電圖指標比較 觀察組LAD大于對照組(P<0.01),兩組其他指標差異無統計學意義(P>0.05),見表4。
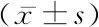
表4 兩組超聲心電圖指標比較
2.5回歸分析 Logistic回歸分析顯示,病程(OR=1.638)、NYHA分級(OR=2.242)、NT-proBNP(OR=2.863)、hs-CRP(OR=2.341)、LAD(OR=3.671)是導致CHF合并房顫的主要影響因素(P<0.05),見表5。
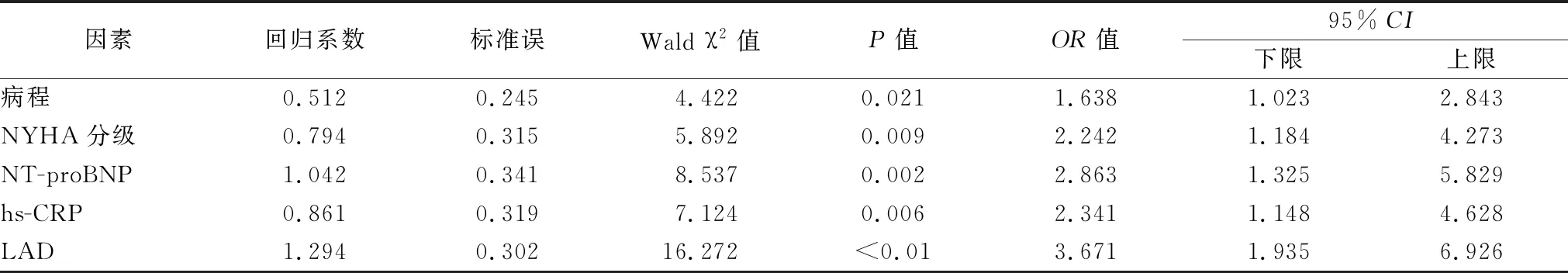
表5 CHF合并房顫影響因素的Logistic回歸分析
3 討 論
CHF是多種心臟病的最終結局,發病率較高。心臟結構與功能的異常改變是導致CHF的重要原因,同時也為心房顫動的發病提供重要病理基礎[6],因此大部分CHF患者伴有心房顫動。 研究資料表明,CHF合并心房顫動可加速病程進展,導致心功能急劇下降,誘發多種心血管并發癥,增加死亡風險[2-3]。在CHF的臨床治療中,預防心房顫動對于改善患者預后至關重要。
本研究結果顯示,病程、NYHA分級、NT-proBNP水平、hs-CRP水平以及LAD是導致CHF發生心房顫動的主要危險因素。隨著病程延長,神經激素、細胞因子的長期異常激活,離子通道調節紊亂,促進心臟重構,加重心肌損傷,導致心臟負荷不斷增加[7],心房顫動發病風險也隨之增加。國外研究對CHF患者進行長期隨訪,發現4.2年期間大約22%的CHF患者出現心房顫動并發癥,平均年發病率為5.4%,這表明患者病程與心房顫動發生率存在相關[1]。CHF患者心功能分級越高,心臟功能與結構損傷越嚴重,發生心房顫動的風險也越高。國外研究報道,NYHA分級為I級時心房顫動發生率大約為5%,NYHA分級為Ⅳ級時心房顫動發生率升高至50%[2]。本研究結果與上述結論存在一致性。
NT-proBNP主要由心室肌細胞分泌,其主要功能是抑制腎素-血管緊張素-醛固酮系統的過度激活,升高腎小球濾過率,促進血管舒張,減輕水、鈉潴留,從而減輕心臟負荷[8]。已有研究表明,當心功能不全時,NT-proBNP大量釋放進入循環系統,通過檢測血清NT-proBNP水平,可準確評估心力衰竭嚴重程度及治療預后[9-10]。隨著CHF病情加重,NT-proBNP逐漸升高,發生心房顫動的風險明顯增加[11]。炎癥因子是參與CHF發病過程的重要因素[12]。hs-CRP是一種急性相反應蛋白,當機體遭受病原體侵襲或組織創傷時,其濃度急劇升高,是評估多種疾病的活動性指標[13]。多項研究證實,hs-CRP可作為慢性炎癥導致心血管疾病的評估標準[14],hs-CRP水平與CHF的發生、發展密切相關[15-16]。hs-CRP可作用于心肌細胞膜相關受體,導致心房肌細胞損傷,是誘發心房顫動的獨立危險因子[17]。
已有研究表明,CHF患者心臟長期壓力負荷過重,心肌細胞的正常凋亡功能降低,心臟實質心肌細胞、間質膠原纖維的形態、數量及分布均發生病理性改變,打破正常的心肌間質與實質之間的比例平衡,導致心臟重構[18]。LAD增大是CHF患者左心房重構的結果。近年研究認為,心房重構是心房顫動發生與維持的中心環節[19]。隨著左心室內壓力及容積升高,左心房壓也隨之升高,引起左心房失代償性擴大,可促進心房顫動發生[20],這表明LAD增大是心房顫動的重要影響因素,與本研究結論一致。本研究中觀察組NYHA分級為Ⅳ級的患者比例、NT-proBNP水平均高于對照組,而觀察組LVEF小于對照組,但差異無統計學意義(P=0.066),這可能與疾病進展過程中,左心房的部分代償性作用有關,具體還有待進一步研究深入探討。
綜上所述,CHF合并心房顫動受多種因素影響,病程長、NYHA分級為Ⅳ級、NT-proBNP以及hs-CRP水平升高、LAD增大的CHF患者合并心房顫動的風險升高,對于存在上述危險因素的CHF患者應加強針對性干預,以減少心房顫動的發生。

