奧拉帕利靶向治療卵巢癌含鉑二線化療失敗的療效
王翠紅,范宇飛
(北京燕化醫院腫瘤科,北京 102500)
卵巢癌(ovarian cancer,OC)因臨床癥狀隱匿及篩查手段有限以至于早期不易被發現,70%以上患者確診時已為晚期,治療后70%多在1~2 年內復發,5 年生存率為30%~40%[1]。2015 年我國癌癥統計報告顯示[2],卵巢癌發病率高達52.1%,病死率居女性生殖道惡性腫瘤的首位。臨床上卵巢癌復發后鉑類耐藥患者采用脂質體阿霉素、吉西他濱、拓撲替康等單藥化療,鉑類敏感患者則選用鉑+紫杉醇等藥物聯合化療,盡量延長無鉑治療期,繼而再采用含鉑化療方案[3],但患者總生存期仍無顯著變化,未取得有效的臨床療效。奧拉帕利(Olaparib)是一種聚腺苷二磷酸-核糖聚合酶抑制劑,可阻斷DNA 堿基切除修復,并在同源重組修復缺陷的腫瘤中產生阻斷效應,目前在乳腺治療中已獲認可[4],2014 年分別被歐洲和美國用于化療后BRCA 突變鉑類敏感和晚期復發的卵巢癌的治療[5,6]。2018 年,我國國家藥監局也已批準奧拉帕利片劑在國內上市,并用于鉑類敏感復發性卵巢癌的維持治療。本研究選取2018 年10 月1 日~2019 年12 月31 日我院收治的44 例含鉑二線化療失敗的卵巢癌患者臨床資料,探討卵巢癌二線化療失敗后應用奧拉帕利靶向治療的療效,現報道如下。
1 資料與方法
1.1 一般資料 選取2018 年10 月1 日~2019 年12月31 日北京燕化醫院收治的含鉑二線化療間隔6個月以上進展的卵巢癌患者44 例,按照隨機數字表法分為觀察組與對照組,每組22 例。納入標準:①病理學確診為卵巢癌,臨床分期明確;②預期生存時間>3 個月,PS 評分0~2 分,血尿常規、肝腎功能、心電圖未見明顯異常;③經二線治療失敗后影像學或CA125 顯示疾病進展。排除標準:①嚴重心肺肝腎功能不全者;②精神障礙者;③依從性較差者。兩組年齡、病理類型、臨床分期比較,差異無統計學意義(P>0.05),具有可比性,見表1。本研究符合《赫爾辛基宣言》要求,患者知情同意并簽署知情同意書。
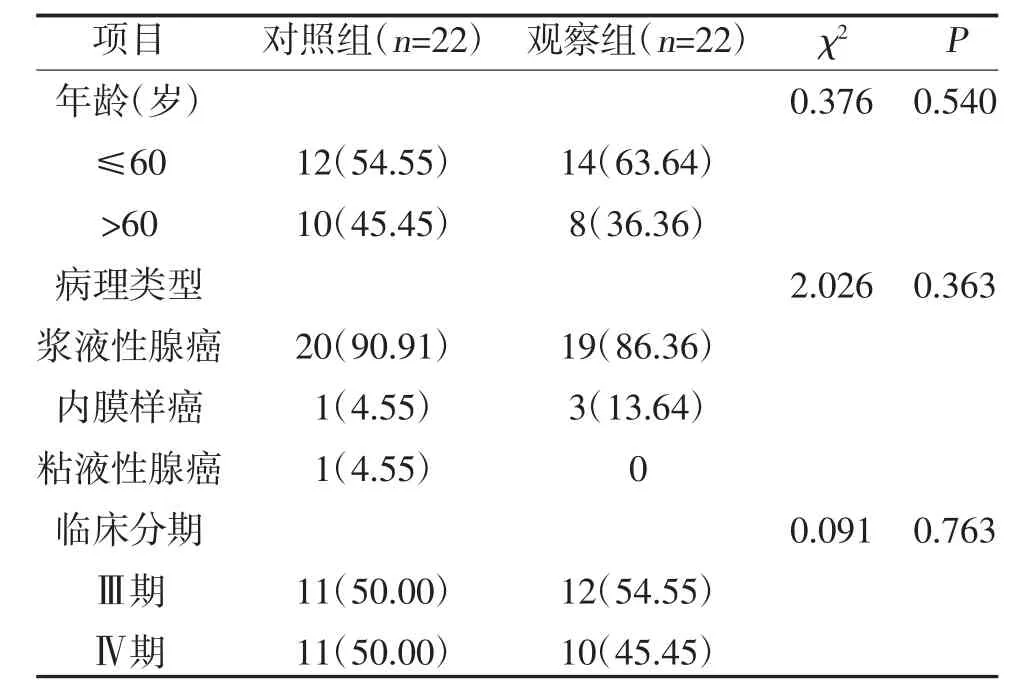
表1 兩組一般資料比較[n(%)]
1.2 方法 對照組予4 周期化療,方案根據前期治療選擇紫杉醇(辰欣藥業股份公司,國藥準字H20 057404;135~175 mg/m2,d1,Ⅳ,q3w)、紫杉醇(白蛋白結合型)(石藥集團歐意藥業,國藥準字H20 183044;260 mg/m2,d1,Ⅳ,q3w)、依托泊苷(江蘇恒瑞醫藥,國藥準字H3 205583;80 mg/m2,d1~d3,Ⅳ,q3w)、多柔比星脂質體(石藥集團歐意藥業,國藥準字H20 113320;30 mg/m2,d1,Ⅳ,q4w)±鉑類[順鉑(齊魯制藥,國藥準字H20 023461;75 mg/m2,d1,Ⅳ,q3w);卡鉑(齊魯制藥,國藥準字H20 020180;AUC=5,d1,Ⅳ,q3w)],每2、4 周期評估療效。觀察組予奧拉帕利(德國Abbvie Deutschland GmbH&Co.KG,批準文號H20180049)300 mg/次,2 次/d,口服,若出現Ⅲ度以上不良反應,將奧拉帕利從300 mg/次,2 次/d 減到150 mg/次,2 次/d,3 個月后復查。治療后觀察組每周查血常規1 次、每2 周查肝腎功能1 次;對照組每周查血常規2 次、肝腎功能1 次直至化療后第14 天。
1.3 觀察指標 比較兩組臨床療效、治療前后CA125水平及不良反應發生情況。
1.3.1 療效評價標準 根據實體瘤療效評價標準(RECIST 1.1)[7],將療效分為完全緩解:所有目標病灶消失;部分緩解:基線病灶長徑總和縮小≥30%;穩定:基線病灶長徑總和有縮小但未達到部分緩解或有增加但未達進展;進展:基線病灶長徑總和增加≥20%或出現新病灶。總有效率=(完全緩解+部分緩解)/總例數×100%。
1.3.2 CA125 水平 使用邁瑞試劑盒配套試劑檢測,采用化學發光免疫法檢測患者CA125 水平,正常范圍為0~35 U/ml。
1.3.3 不良反應 以美國國立癌癥研究所通用毒性標準3.0(NCI-CTC3.0)分級0~Ⅳ度進行評價,主要包括骨髓抑制(白細胞減少癥、血小板減少癥、貧血)、胃腸道反應(惡心、嘔吐)和神經毒性。
1.4 統計學方法 數據均采用SPSS 17.0 統計學軟件進行分析,正態分布的計量資料以()表示,組間比較采用t檢驗;計數資料以[n(%)]表示,采用χ2檢驗。以P<0.05 表示差異有統計學意義。
2 結果
2.1 兩組臨床療效比較 觀察組總有效率高于對照組,差異有統計學意義(P<0.05),見表2。

表2 兩組臨床療效比較[n(%)]
2.2 兩組糖類抗原CA125 比較 治療前,兩組CA125比較,差異無統計學意義(P>0.05);觀察組治療后CA125 低于對照組,差異有統計學意義(P<0.05),見表3。
表3 兩組治療前后CA125 比較(,U/ml)
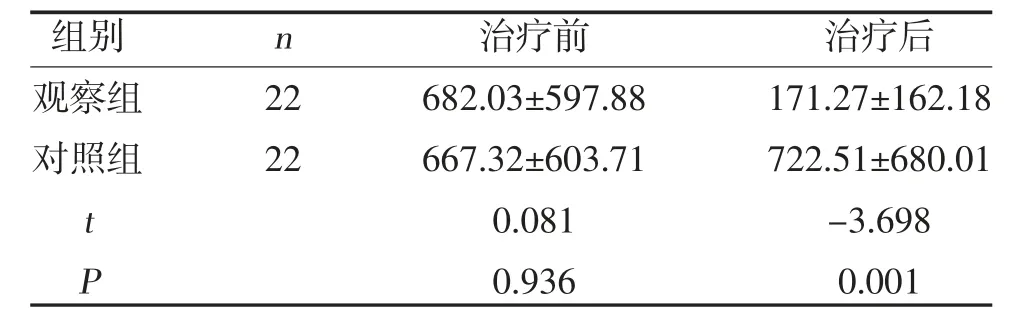
表3 兩組治療前后CA125 比較(,U/ml)
2.3 兩組不良反應比較兩組骨髓抑制、乏力、胃腸道反應發生率比較,差異無統計學意義(P>0.05);觀察組周圍神經病變發生率低于對照組,差異有統計學意義(P<0.05),見表4。
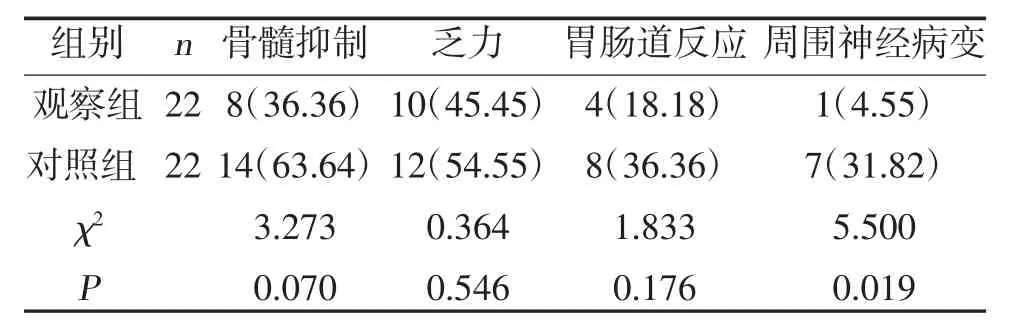
表4 兩組不良反應比較[n(%)]
3 討論
NCCN 指南推薦以鉑為基礎的化療方案作為卵巢癌初次化療的首選方案[8],治療模式常常是術后化療,停藥復查,復發后再治療,更短間期再次復發,再次治療,直至生命終結,治療過程中鉑類藥物成為多次備選藥,但其容易導致耐藥后疾病進展,也會出現患者無法耐受鉑類蓄積,進而出現骨髓抑制、消化道反應、腎功損害等毒副反應而終止治療。而PARP抑制劑有望打破卵巢癌近20 年內5 年總生存期無顯著改善的局面,即在一線或復發治療緩解后或者二線化療再進展后加PARP 抑制劑維持治療,以推遲疾病復發和緩解疾病進展時間,進而延長晚期卵巢癌患者的生存時間[9,10]。
人體內DNA 損傷有兩種主要修復過程,一種是PARP 參與的DNA 單鏈斷裂后的損傷修復,另一種是BRCA1/2 參與的同源重組修復,其中一種是修復障礙,而另一種是可代償。若兩者同時障礙,則可能促進細胞的凋亡,這即是PARP 抑制劑的作用機理-合成致死效應[11,12]。研究表明[13,14],鉑敏感復發卵巢癌患者應用奧拉帕利維持治療可長期臨床獲益。奧拉帕利通過作用于基因組不穩定和突變的腫瘤,使得腫瘤細胞選擇性凋亡,同時能增強免疫治療前的突變負荷[15]。卵巢癌的復發臨床上可表現為CA125升高、體檢發現腫塊、影像學檢查發現腫塊、出現胸腔或腹腔積液、出現不明原因的腸梗阻等癥狀,其中CA125 是最為常用的卵巢癌腫瘤標志物,尤其是漿液性卵巢癌的首選腫瘤標志物。CA125 的陽性率與腫瘤分期、組織學類型有關,晚期、漿液性癌患者的陽性率約84.10%、92.40%,在絕經后人群CA125 診斷卵巢癌的敏感度和特異度可達90.7%、89.8%[16]。本研究結果顯示,觀察組總有效率為54.55%,高于對照組的22.73%,差異有統計學意義(P<0.05),且觀察組治療后CA125 低于對照組,差異有統計學意義(P<0.05),這與奧拉帕利的靶向抑制和捕獲DNA損傷修復酶PARP,導致腫瘤細胞死亡相關。此外,本研究中兩組骨髓抑制、乏力、胃腸道反應發生率比較,差異無統計學意義(P>0.05);觀察組周圍神經病變發生率低于對照組,差異有統計學意義(P<0.05),雖然兩組骨髓抑制、乏力、胃腸道反應發生率無明顯差異,但觀察組總體數據低于對照組,且周圍神經病變不良反應發生率更低,與Pujade-Lauraine E 等[17]研究結果類似,其研究中1~2 級不良事件發生率為62%,≥3 級不良反應事件為36%,再次提示奧拉帕利靶向治療的患者耐受較好,不良反應較少。
綜上所述,針對卵巢癌含鉑二線化療復發的患者,奧拉帕利相比常規化療在近期療效及安全性方面均有優勢,可降低患者CA125 水平及不良反應發生幾率,對控制卵巢癌的進展具有良好效果。

