熱粘結復合纖維人造血管支架的制備及其性能
郭鳳云, 過子怡, 高 蕾, 鄭霖婧
(1. 浙江理工大學 紡織科學與工程學院, 浙江 杭州 310018;2. 浙江理工大學 先進紡織材料與制備技術教育部重點實驗室, 浙江 杭州 310018)
進入21世紀后,人類心血管疾病的發病率逐年增加,治療疾病的成本越來越高,這使得臨床人造血管支架的需求越來越大。現階段,內徑在6 mm以上的大口徑人造血管已經用于臨床,但內徑小于6 mm的小口徑人造血管常會植入失敗,因此,新型小口徑人造血管的研制和開發具有重要意義。自體或異體移植是臨床上進行小口徑血管重建的常用方法。但這些方法不可避免地會出現一些問題,如血液相容性差,力學強度較弱等[1]。目前,組織工程制備人造血管支架的方法主要有自組裝[2]、水凝膠[3]、溶劑澆鑄及浸出、熱致相分離、靜電紡絲等[4-5]。其中,由于靜電紡絲方法參數可控、經濟高效,作為具有代表性的制備纖維方法[6],能夠靈活有效地調控材料的組成、尺寸、結構和性能,所以近年來針對靜電紡絲人造血管支架的研究日益增加[7-9]。
聚乳酸-羥基乙酸共聚物(PLGA)、聚乳酸(PLA)、聚氨酯(PU)、聚己內酯(PCL)等生物可降解高分子,常被用作靜電紡制備人造血管支架材料[10-11],但由于各種各樣的缺陷以及組分單一的弱點,限制了其進一步應用。其中,力學性能作為血管支架使用最基本的先決條件,其研究對實際應用顯得尤為重要[12-13]。對人造血管支架的力學研究大都基于單向拉伸且強度較弱,沒有考慮到其在實際應用中的縱向拉伸及橫向伸縮擴張所需的力學差異性。除此之外,具有細胞無毒性、植入后耐穿刺不發生泄露、具備足夠的機械循環穩定性等也是人造血管支架所要滿足的功能需求。
由于血液相容性差,纖維力學強度較弱等,開發小口徑、力學性能持久且功能完整的人造血管支架具有一定的挑戰。從紡織材料學角度出發,使用生物相容性的合成材料通過紡織機械加工手段研制力學性能良好,盡可能滿足更多功能要求的人造血管支架,成為解決小口徑人造血管支架的一個有效方法。在此背景下,本文在前期調控靜電紡絲條件、血管材料的組成配比及纖維孔徑的工作基礎上[14-16],利用靜電紡絲技術結合浸泡脫管法,通過熱處理在保證適當孔隙率的情況下制備具有粘結結構的PCL/PU復合纖維小口徑人造血管支架,并對人造血管支架的微觀結構、雙向拉伸強度、細胞毒性和穿刺性等進行分析。
1 實驗部分
1.1 實驗材料與儀器
材料:聚氨酯(顆粒狀,相對分子質量為270 000)、聚己內酯(相對分子質量為 80 000)、膨體聚四氟乙烯管(e-PTFE)、羥乙基淀粉HES的生理鹽水溶液,國藥集團化學試劑有限公司;四氫呋喃(THF)、N, N-二甲基甲酰胺(DMF)、二甲基亞砜(DMSO)、胎牛血清(FBS),分析純,北京化工廠;含各種氨基酸和葡萄糖的培養基DMEM、小鼠成纖維細胞,中國科學院細胞庫。
儀器:靜電紡絲裝置(自制);AGS-X型萬能力學測試儀(日本島津公司);Quanta 250 FEG型掃描電子顯微鏡(美國賽默飛世爾科技(中國)有限公司);ELx800型酶聯免疫監測儀(美國寶特公司);BZF-50型真空烘箱(上海博訊公司)。
1.2 纖維膜和人造血管支架的制備
首先配制前驅體溶液:將聚氨酯(PU)和聚己內酯(PCL)溶于質量比為1∶1的四氫呋喃和N,N-二甲基甲酰胺混合溶液中,配制成質量分數為10%的PCL/PU混合溶液,其中PCL與PU質量比為1∶3。此外,將PVP溶于乙醇中,配制成質量分數為8%的PVP溶液,然后進行靜電紡絲,具體過程如圖1所示。
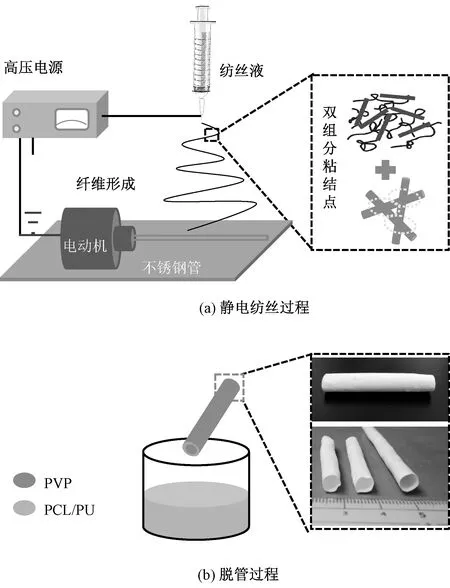
圖1 人造血管支架制備示意圖Fig.1 Preparation schematic of artificial blood vessel.(a) Electrospinning process; (b) Tubing-off process
將上述前驅體溶液裝入5 mL注射器中,調整合適的流速,設置電壓范圍為10~20 kV,靜電紡絲距離為20 cm。作為對比,PU、PCL/PU和PCL纖維膜靜電紡絲過程中直接用鋁箔接收。PCL/PU人造血管支架接收裝置為直徑2、3、5 mm的不銹鋼空心轉輥。PCL/PU人造血管支架紡絲過程主要包括靜電紡絲、溶解脫管和加熱粘結,具體為:第1步,紡制1層PVP纖維膜于轉輥上;第2步,在PVP纖維膜轉輥上繼續進行PCL/PU復合纖維的紡絲;第3步,將收集到的纖維和轉輥一起置于水中20 h,溶去內層PVP,脫去不銹鋼管轉輥,將得到的纖維管置入55 ℃干燥箱中熱處理,烘干,即可得到PCL/PU人造血管支架材料。
1.3 纖維膜和人造血管支架表面結構表征
將纖維膜剪裁成三角形,貼在樣品臺表面;將人造血管支架剪開,裁成方形片狀,內外表面和橫截面分別貼在樣品臺表面和側面。噴金處理后用掃描電子顯微鏡在真空環境觀察材料表面和截面形貌結構。
1.4 人造血管支架力學性能測試
選取直徑為5 mm的人造血管支架,剪切成小圓柱狀,長為15 mm,把樣品置于剪好的紙片框架上,空隙間距為5 mm,采用萬能力學測試儀進行力學拉伸測試。橫向拉伸方向為人造血管支架的圓周方向,縱向拉伸方向為人造血管支架的軸向方向。測試溫度為常溫,速度為10 mm/min。每個樣品至少測試5次,取平均值。根據測得的載荷位移繪制應力與應變曲線,計算樣品的斷裂強度和斷裂伸長率等力學參數。
拉伸力學穩定性測試通過固定拉伸強度為25 MPa和拉伸應變為200%,在儀器循環模式下進行實驗。
1.5 人造血管支架耐穿刺性能測試
作為對照,將人造血管支架和商用e-PTFE管分別連在2個封閉的注射器中間,管內填充人造血漿羥乙基淀粉HES的生理鹽水溶液,然后用同樣大小的注射器針頭進行穿刺實驗,觀察血漿滲出情況。
1.6 人造血管支架細胞毒性測試
首先對人造血管支架進行滅菌處理,然后置于96孔培養板中,添加細胞培養液和小鼠成纖細胞L929,每個孔內加入100 μL細胞懸液,分別培養1、3、5、7 d,加入DMSO、FBS和DMEM等營養基,在設定的時間內進行MTT實驗,用酶聯免疫檢測儀測定波長在490 nm處的吸光度A。每個樣品在每個時間點準備5個平行樣,取平均值。根據不同時間的空白組和實驗組吸光度差值之比,計算細胞的相對活性。
2 結果與討論
2.1 形貌結構分析
利用圖1所示裝置制備了不同口徑和長度的PCL/PU人造血管支架。PCL/PU人造血管支架呈現明顯的中空管狀結構,且結構完整可自支撐。通過懸掛重物承重測試發現,人造血管支架可承受416 g的重物。圖2示出PCL、PU、PCL/PU纖維膜和PCL/PU人造血管支架的掃描電鏡照片。

圖2 纖維膜和人造血管的掃描電鏡照片Fig.2 SEM images of fibrous film and artificial blood vessel. (a) PU fibrous film(×10 000); (b) PCL/PU fibrous film(×10 000); (c) PCL fibrous film(×10 000); (d) Inner layer of artificial blood vessel(×4 000); (e) Outer layer of artificial blood vessel(×4 000); (f) Cross-sectional of artificial blood vessel(×10 000)
由圖2(a)~(c)可以看出,靜電紡絲纖維表面光滑,結構完好,有明顯的粘結點,纖維呈無序均勻分布狀態。經統計纖維直徑平均為792 nm。由人造血管支架電鏡照片可以看出,其內外表面的纖維光滑無序,分布均勻,含有粘結點結構,截面纖維緊密交錯堆疊,該結構對人造血管支架力學性能的增強具有較大的促進作用。本文制備的人造血管支架具有由連續纖維交錯堆積形成的三維立體孔結構,具有一定的孔隙。根據質量、密度和體積,通過計算得出人造血管支架的孔隙率約為72%,這有利于細胞滲透、營養物質及代謝產物的輸送。
2.2 力學性能分析
為進一步了解材料的力學性能以滿足人造血管支架的應用要求,對PCL、PU、PCL/PU纖維膜和PCL/PU人造血管支架進行了拉伸測試,結果如圖3所示。研究發現,PCL/PU人造血管支架軸向拉伸強度高達68.6 MPa,較純PU纖維膜提高約7倍,且在25 MPa拉伸強度和200%的拉伸應變下,循環拉伸15次后材料力學性能仍然能夠保持,呈現出良好的拉伸循環穩定性。相比之下,PCL/PU人造血管支架的橫向拉伸性能較弱,平均強度為39.3 MPa。分析認為在縱向拉伸過程中,纖維之間形成了三維網絡結構,纖維間互相交錯相連;而在橫向拉伸時,纖維邊緣的缺口使得纖維間的滑移比較嚴重,所以縱向較橫向好。但二者均能滿足血管支架的力學要求,且這種各向異性的力學性能使其在臨床試驗中能得到很好的應用,更有利于人造血管支架的伸縮擴張。
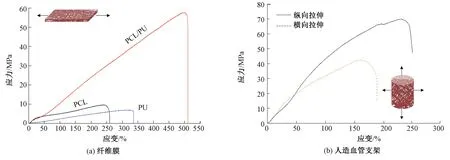
圖3 纖維膜和人造血管支架的力學性能Fig.3 Mechanical properties of fibrous film(a) and artificial blood vessel(b)
2.3 耐穿刺性能分析
血液透析或者抽血等過程往往需要對血管進行破壞性穿刺,因此,研究人造血管支架的耐穿刺性能具有重要意義。圖4示出本文制備的PCL/PU人造血管支架和商用e-PTFE人造血管支架的穿刺實驗對比圖。研究發現:PCL/PU在穿刺后10 h內液體不會流出,即不會滲血;而e-PTFE管則出現液體泄漏的現象,如圖中虛線標記區域所示。表明PCL/PU人造血管支架耐穿刺性較好,液體不會滲出。

圖4 人造血管支架穿刺實驗Fig.4 Vascular puncture experiment. (a) PCL/PU fibrous artificial blood vessel; (b) Commercial e-PTFE
2.4 細胞毒性分析
在實際的組織工程應用中,所用材料最基本的要求是要保證在一定范圍內具有血液相容性和細胞相容性。細胞相容性可由細胞生長狀況、形態變化和細胞活性來判斷。本文以小鼠成纖細胞L929為例,對人造血管支架材料進行了細胞毒性分析,并與e-PTFE和空白對照試驗進行對比,結果如圖5所示。

圖5 MTT法測試人造血管支架細胞毒性Fig.5 Cell viability according to a MTT assay
結果顯示隨著時間的增加,細胞相對活性最高達94%,且PCL/PU人造血管支架在第7天的細胞活性優于空白對照和e-PTFE支架,說明本文制備的PCL/PU人造血管支架基本無細胞毒性。
3 結 論
本文利用靜電紡絲技術結合浸泡脫管法制備了具有2、3、5 mm內徑的聚己內酯/聚氨酯(PCL/PU)人造血管支架。該復合人造血管支架的孔隙率為72%,其力學性能較純PU纖維膜提升7倍,且橫向和縱向均具有優異的拉伸力學性能;培養7 d后其細胞活性為94%,與商用的e-PTFE支架對比,該人造血管支架具有較好的耐穿刺性。本文制備的PCL/PU人造血管支架能滿足血管支架的基本要求,在人造血管組織工程領域具有潛在的應用前景。

