垃圾焚燒煙氣臭氧同時脫硝脫汞反應動力學研究
邵嘉銘,王智化,林法偉,唐海榮,許巖韋,何 勇,岑可法
(1.浙江大學 能源清潔利用國家重點實驗室,浙江 杭州 310027;2.天津大學 環境科學與工程學院,天津 300072;3.光大環保技術研究院(南京)有限公司,江蘇 南京 211102)
0 引 言
燃料燃燒會釋放大量污染物,如SO2、NOx、PM、Hg等,這些污染物經一系列的大氣化學反應,最終會形成酸雨、霧霾、光化學煙霧等自然災害,嚴重危害生態環境及人類健康[1-3]。近年來,由于能源結構的調整,傳統化石燃料燃燒的比重逐步減少,垃圾焚燒發電作為新能源板塊得到迅速發展[4]。針對垃圾焚燒煙氣,我國《生活垃圾焚燒污染控制標準》(GB 18485—2014)規定,垃圾焚燒電廠NOx和Hg的排放限值分別為250、0.05 mg/Nm3 [5-6]。2019年12月26日,生態環境部要求2020年1月2日起向社會公開各垃圾焚燒廠煙氣顆粒物、NOx、SO2、HCl、CO等常規污染物的日均值和爐膛溫度的自動監測數據。面對日益凸顯的環境問題,各城市對垃圾焚燒煙氣提出了更加嚴格的要求,排放限值也逐漸向超低排放標準靠近[6-7]。此外,關于煙氣排放中的重金屬Hg,2013年10月,我國簽署了全球首個汞限排國際公約《水俁公約》,對汞的排放和控制均提出了相關要求,汞的減排形勢也愈發嚴峻[8]。
目前,煙氣中的SO2可通過成熟的濕法脫硫技術高效脫除,而靜電除塵和布袋除塵技術可有效控制PM的排放[9-10]。對于NOx的脫除,選擇性催化還原技術(SCR)和選擇性非催化還原技術(SNCR)應用較廣[11]。煙氣中的Hg主要包含元素態(Hg0)、顆粒態(Hgp)和氧化態(Hg2+)3種形式,其中,Hgp可通過電廠現有除塵設備脫除,Hg2+可在濕法脫硫系統中脫除[12]。但Hg0由于易揮發、水溶性差、占比大,是煙氣Hg脫除的難題[13]。汞的脫除方法主要采用吸附技術,利用固定床反應器中的吸附劑對其進行捕集。現階段的污染物脫除技術僅針對某一種特定污染物,且設備復雜、占地面積大,不利于對現存電廠及空間緊湊的工業鍋爐改造。因此,開發一種多種污染物同時脫除的技術對于實際工業應用具有重大意義。
臭氧多種污染物一體化脫除技術,作為一種新興的低溫煙氣處理技術,近幾年成功應用于超低排放改造過程[14-15]。該技術的主要技術路線是向低溫煙氣中噴入臭氧,將NO氧化為NO2和N2O5、將Hg0氧化為Hg2+,利用其氧化產物的水溶性,借助濕法噴淋塔的噴淋吸收,最終實現NOx、Hg和SO2的一體化脫除[16]。該技術可適應復雜的煙氣條件和鍋爐負荷的變化,可處理低溫煙氣,對電廠現有設備的改造小,污染物脫除效率高,具有廣闊的發展前景。
臭氧對于垃圾焚燒煙氣中的有機污染物(如二噁英)也有降解作用,但由于煙氣中有機污染物種類多,反應機理復雜,因此,本文重點研究煙氣中無機污染物的氧化脫除。針對NOx的脫除,由于N2O5是硝酸的酸酐,在NO的氧化產物中溶解度最高,可被噴淋液高效吸收,提高NOx的脫除效率,故本文模擬選擇N2O5進行敏感性分析。本文建立了更全面的臭氧與多種無機煙氣污染物反應的均相反應機理,主要針對某垃圾焚燒廠煙氣成分,采用Chemkin Pro軟件對臭氧同時脫硝脫汞過程進行模擬計算,提出了NO和Hg氧化脫除的主要反應路徑,研究了反應溫度、O3/NO摩爾比、停留時間對脫除效率的影響,為臭氧多種污染物一體化脫除技術在垃圾焚燒電廠的實際應用提供了理論指導。
1 計算方法
計算采用Chemkin Pro軟件中封閉的均相反應模塊進行動力學模擬和敏感度分析。由于支鏈反應在不同反應條件下,反應速率存在差異,即不同的基元反應在不同反應條件下的反應權重不同,為了更準確地選擇基元反應以及動力學參數,對反應過程進行精確模擬,需明確各基元反應的重要程度。敏感度是指各影響因素對于反應的影響程度,包括反應速率敏感度、濃度敏感度、溫度敏感度等。

在前人研究結果[16-17]的基礎上,本文提出了更為全面的反應機理,該機理包含SO2、NO、NO2、O3、O2、Hg、H2O、HCl、HF等42種物質,由138個基元反應構成,基元反應動力學參數源于美國標準研究所NIST數據庫。通過拓展反應條件,利用該機理對O3與煙氣復雜成分中的NOx和Hg的氧化進行深入研究,垃圾焚燒電廠煙氣條件見表1。
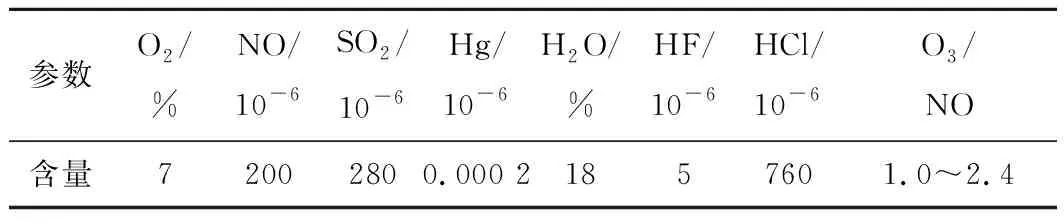
表1 計算采用的煙氣條件
2 計算結果與分析
2.1 反應路徑
為了探究臭氧深度氧化煙氣中NO的反應路徑,在煙氣溫度為110 ℃、O3/NO=1.5的條件下,對N2O5的生成進行敏感性分析,結果如圖1所示。可以看出,該反應體系內,影響N2O5生成的關鍵基元反應為R8、R9、R124、R126和R129。
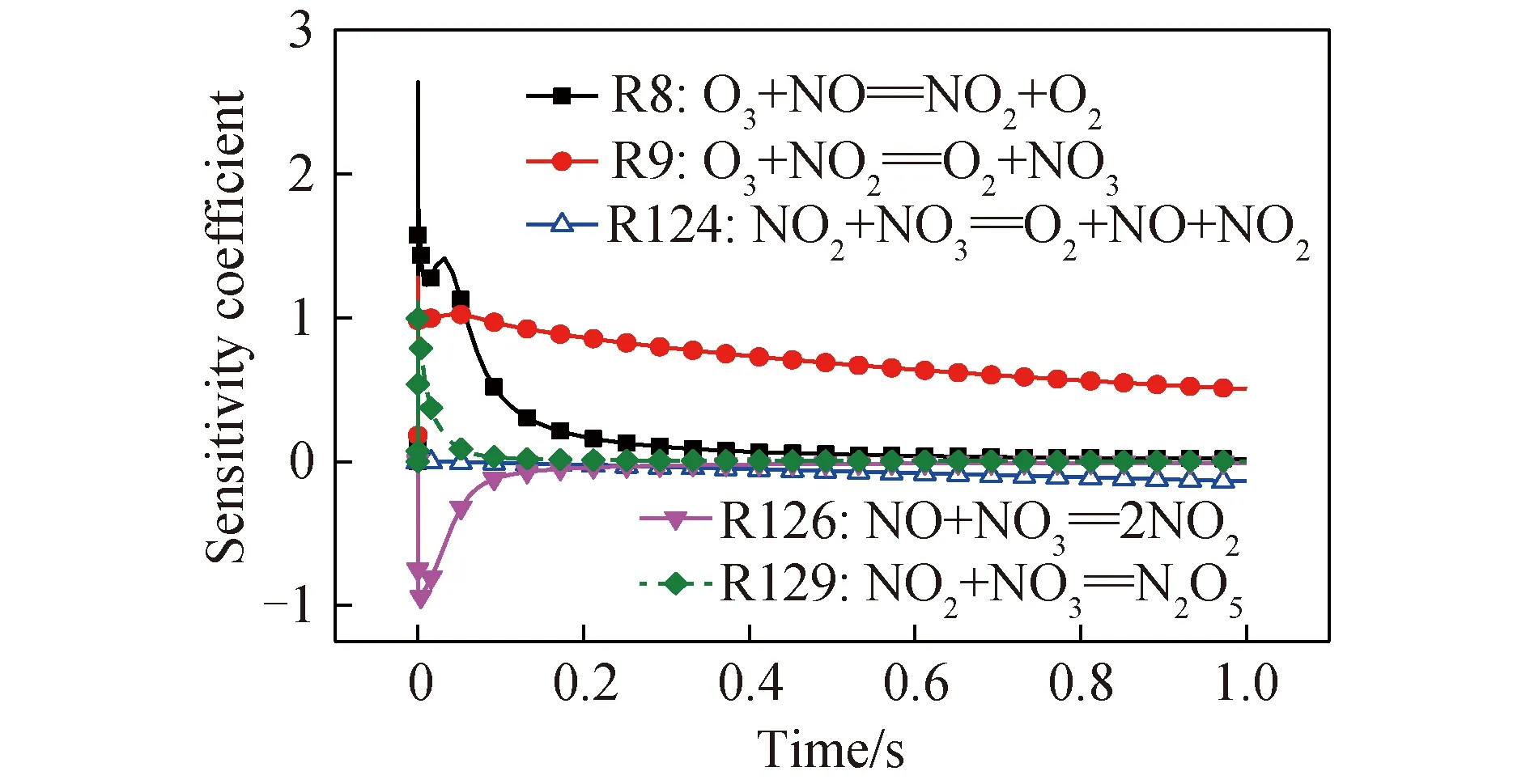
圖1 N2O5的無量綱敏感度系數Fig.1 Dimensionless sensitivity coefficient of N2O5

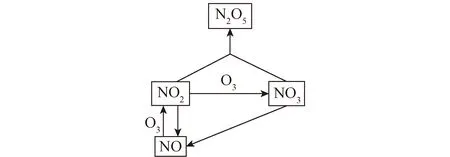
圖2 N2O5生成的主要反應路徑Fig.2 Main formation route of N2O5 formation
圖3為煙氣中Hg的無量綱敏感度系數模擬結果,可知,該反應體系下Hg氧化的關鍵基元反應為R9、R82、R89、R95、R96、R124和R133。可見反應體系中Hg的氧化路徑主要有:① Hg被NO3氧化為HgO;② Hg被Cl和Cl2氧化生成HgCl2,Hg的氧化路徑如圖4所示。HgO的生成主要依賴于NO的氧化產物NO3來實現,并非來自O3直接氧化Hg。實際鍋爐煙氣中,NO濃度遠大于重金屬Hg,因此在O3氧化NO的同時,微量NO3即可完成Hg的有效氧化。此外,垃圾焚燒煙氣中HCl的存在也有利于Hg的氧化。煙氣中的Hg0最終被氧化為HgO和HgCl2,由于Hg2+的水溶性,可實現在濕法洗滌塔中同時脫除NOx、SO2、Hg2+。

圖3 Hg的無量綱敏感度系數Fig.3 Dimensionless sensitivity coefficient of Hg
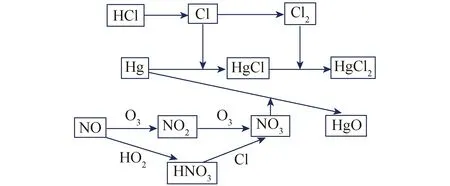
圖4 Hg的氧化反應路徑Fig.4 Main oxidation route of Hg
2.2 O3與NO反應的影響因素
根據垃圾焚燒廠的煙氣成分,在反應溫度為110 ℃、O3/NO摩爾比為1.5時,O3和NO反應后的產物濃度隨時間的變化如圖5所示。可以看出,O3將NO氧化為NO2的速率很快,在0.1 s內NO濃度迅速降為0,而NO2的濃度迅速升高至近200×10-6。因此,O3噴入煙道后,可很快將NO氧化為NO2。由于反應條件中O3/NO的摩爾比為1.5,過量的O3可將NO2深度氧化。由圖5可以看出,隨著反應時間延長,N2O5濃度增加緩慢,說明N2O5的生成需較長的反應時間。此外,反應體系中NO3濃度始終很低,說明NO3是一種極其不穩定的中間產物,無法長時間存在。由于N2O5是比NO2更易溶于水的高價態氮氧化物,故研究其生成過程中的影響因素,對提高氮氧化物的脫除效率、達到超低排放標準尤為重要。因此,本文進一步研究反應溫度、O3/NO摩爾比和反應時間對N2O5生成的影響,從而確定適合本文垃圾焚燒煙氣中N2O5的最佳生成條件。
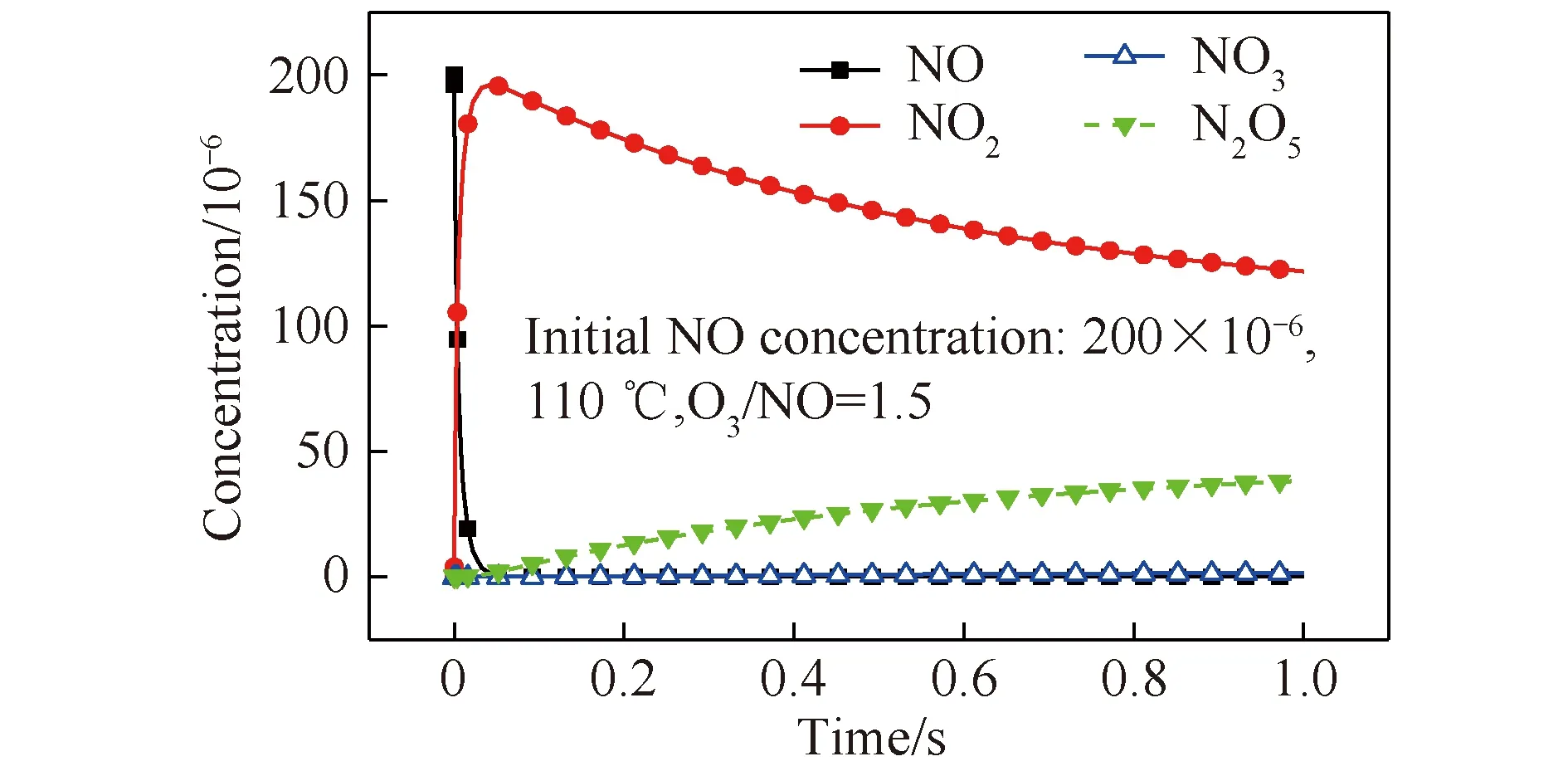
圖5 O3與NO的反應產物隨時間變化Fig.5 Reaction product of O3 and NO changes with time
圖6為反應溫度(60~150 ℃)對N2O5生成的影響。在NO初始濃度為200×10-6、O3/NO摩爾比為2.0條件下,N2O5的生成對反應溫度的變化較敏感。隨著溫度升高,N2O5生成量逐漸減小。60 ℃時,反應8 s時的N2O5生成量最大。溫度小于100 ℃時,反應后N2O5濃度可到達平衡狀態;但超過100 ℃,N2O5濃度到達峰值后,隨反應時間延長,N2O5濃度開始下降,說明溫度的升高在一定程度上會抑制N2O5的生成,其原因除了由于N2O5自身的分解反應隨溫度升高而加快外,關鍵中間產物NO3的分解速率也隨溫度的升高而加快。但溫度的升高也會加快N2O5濃度達到峰值所需的時間。在工業應用中,臭氧噴射裝置通常布置在脫硫塔前,由于煙氣流速較快,噴入后的O3和NO的反應時間也較短。因此,在有限的反應時間內,合理提高反應溫度,實現N2O5生成最大量,是提高NOx脫除效率的關鍵。
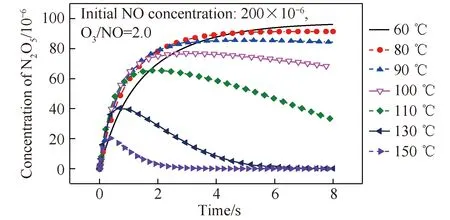
圖6 反應溫度對N2O5生成的影響Fig.6 Effect of temperature on N2O5 formation
由于本文垃圾焚燒電廠GGH換熱后的溫度在105~110 ℃,因此研究反應溫度110 ℃時O3/NO摩爾比對N2O5生成的影響,結果如圖7所示。可以看出,隨著O3/NO摩爾比增加,N2O5生成量增加,但增加速率相對減緩。O3/NO>2.0時,繼續增加O3的投入量,對N2O5生成的促進作用較小,且會增加運行成本及煙囪出口殘留的臭氧濃度。另外,溫度為110 ℃時,增加O3/NO摩爾比對N2O5濃度達到峰值的時間影響不大,需2 s左右。
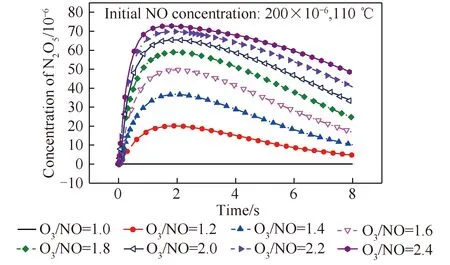
圖7 O3/NO摩爾比對N2O5生成的影響Fig.7 Effect of O3/NO molar ratio on N2O5 formation
2.3 O3與Hg反應的影響因素
反應溫度為110 ℃、O3/NO摩爾比為1.5時,Hg的氧化產物隨時間的變化如圖8所示。相較于NO氧化為NO2過程,Hg0的氧化需較長的反應時間,在5 s左右,氧化產物以HgO和HgCl2為主。由于該垃圾焚燒煙氣中含有較高濃度的HCl氣體,因此,反應體系中Hg0氧化產物中HgCl2的占比較大。
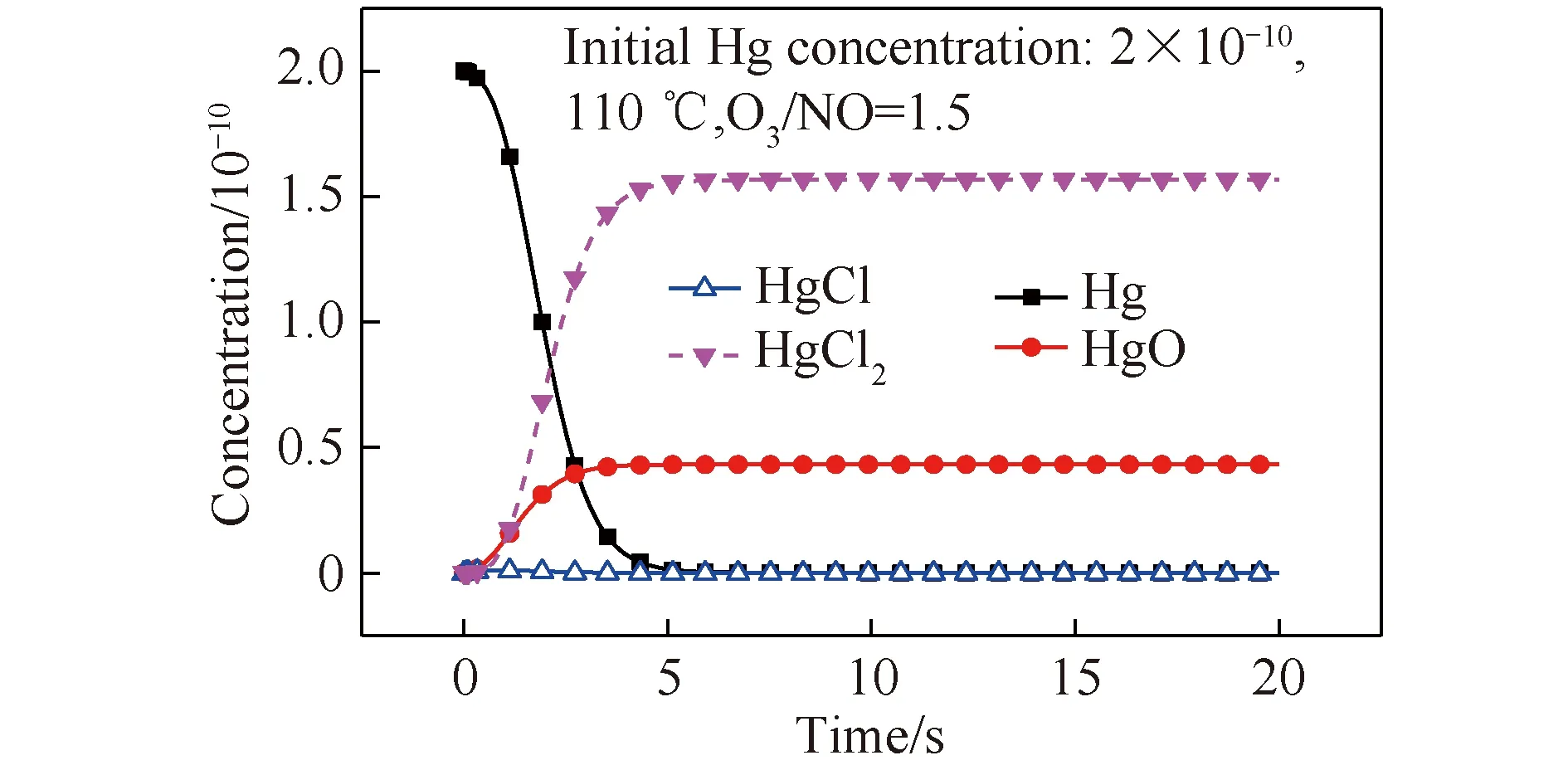
圖8 Hg的氧化產物隨時間的變化Fig.8 Oxidation production of Hg changes with time
由于煙氣中Hg濃度很低,采用O3/Hg摩爾比不易度量,因此,研究O3/NO摩爾比對Hg氧化的影響,模擬結果如圖9所示。可以看出,O3/NO摩爾比增加,可顯著提高Hg的氧化速率;O3/NO≥2.0時,在2~3 s內Hg0基本全部轉化為Hg2+;增大O3/NO 摩爾比,其對Hg脫除效率的促進作用逐漸減弱。考慮臭氧制備過程中的電耗,為了降低運行成本,在工業應用中O3/NO摩爾比取1.6時,即可完成Hg0向Hg2+的有效氧化,實現Hg的高效脫除。
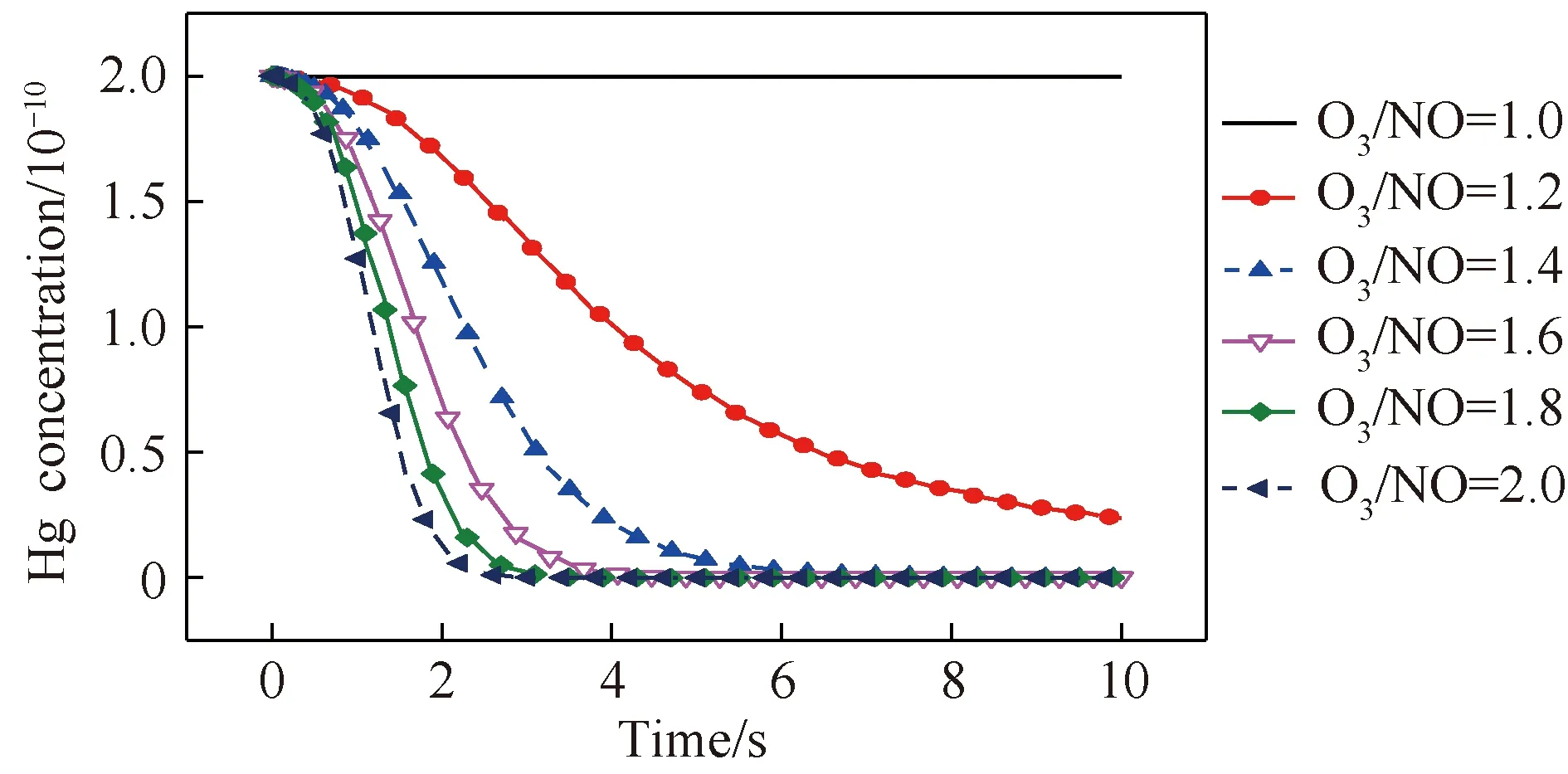
圖9 O3/NO摩爾比對Hg氧化的影響Fig.9 Effect of O3/NO molar ratio on Hg oxidation
圖10為反應溫度對于Hg氧化過程的影響。隨著反應溫度降低,Hg氧化達到平衡的時間逐漸延長。溫度小于110 ℃時,只要反應時間充足,Hg可完全轉化為Hg2+。但反應溫度超過110 ℃時,Hg的氧化效率隨溫度的升高逐漸減小,這主要是由于NO3分解速率隨溫度的升高而加快的緣故。根據模擬結果,煙氣中Hg氧化的理想反應溫度為110~130 ℃,反應時間為4~6 s。
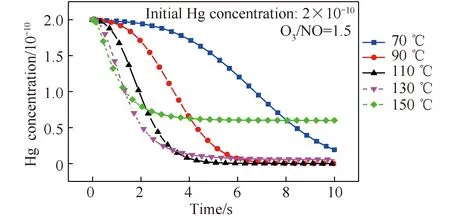
圖10 反應溫度對Hg氧化的影響Fig.10 Effect of reaction temperature on Hg oxidation
3 結 論
1)O3氧化NO為NO2的反應時間很快,在0.1 s內即可完成。但實現NO2向N2O5的深度氧化,需較長的反應時間。
2)NO3是N2O5生成過程的關鍵中間產物,由于其不穩定性,使N2O5的生成受溫度影響較大,升高溫度可加快反應達到平衡的時間,但同時也會降低氧化效率。N2O5的最佳生成溫度為60~80 ℃,反應時間為5 s以上。
3)Hg氧化的反應時間為4~6 s。垃圾焚燒煙氣中HCl的存在有利于Hg的氧化,O3對于Hg氧化也是通過NO氧化過程的中間產物NO3來實現,HgO和HgCl2是主要的氧化產物。
4)對于Hg的氧化脫除,O3/NO摩爾比增大、溫度升高均會加快氧化速率,在O3/NO>1.4,溫度小于110 ℃時,可使Hg0基本完全轉化為Hg2+,結合濕法脫硫系統可實現Hg的完全脫除。

