青霉烯類及碳青霉烯類抗生素的結構特點與分級管理建議
武明芬,趙志剛
(首都醫科大學附屬北京天壇醫院藥學部,北京 100070)
青霉烯類、碳青霉烯類藥物通常不會被大多數質粒和染色體介導的β-內酰胺酶所分解,因此具有抗菌譜廣、抗菌活性強的特點,近年來在臨床應用廣泛,特別是在多重耐藥菌感染、需氧菌與厭氧菌混合感染等治療中發揮著重要作用[1-3]。我國抗菌藥物分級管理制度對碳青霉烯類和青霉烯類藥物沒有細化分級管理,統一作為特殊使用級抗菌藥物管理,使其在臨床使用和管理中出現了一些不合理現象,如造成某些品種使用量逐年上升、G-桿菌對其耐藥越來越嚴重等[4]。因此,根據不同抗生素品種的結構特點和抗菌譜對其進行優化分級、加強管理十分必要。本文根據青霉烯類和碳青霉烯類藥物的結構特點,分析其不同品種抗菌譜、耐藥特點及藥動學特征的差異,進而提出分級優化管理建議,以促進抗菌藥物的合理使用,減少耐藥菌產生。
1 青霉烯類和碳青霉烯類藥物的結構與抗菌特性
1.1 青霉烯類和碳青霉烯類藥物的結構特點 青霉烯類和碳青霉烯類藥物屬于β-內酰胺類抗生素。青霉烯類藥物的結構由青霉烷與頭孢烯兩種母核組成(見圖1),將頭孢烯的雙鍵引入青霉烷的母核中,與2位羧基形成共軛雙鍵,便構成了青霉烯類的結構母核。將青霉烷4位的S換成C,即構成碳青霉烯類結構母核。這兩類抗生素的結構特點決定了其具有多重抗菌優勢,既具有類似于青霉素的強抗菌活性和頭霉菌素的廣泛抗菌譜,又對β-內酰胺酶具有高度穩定性。

圖1 青霉烯類與碳青霉烯類藥物的母核結構Figure 1 The nuclear structures of penems and carbapenems antibiotics
碳青霉烯類母核中的共軛雙鍵不僅提高了環的張力,還極大地提高了其抗菌活性,隨著4位的S換成C,鍵角由120°減小到108°,環的張力和抗菌活性都進一步增強。6位β-H與5位α-H呈反式構型,為青霉素結合蛋白提供了更佳的結合靶點,提高了藥物對β-內酰胺酶的穩定性,同時以α-羥乙基替換6位的酰胺側鏈,進一步提高了耐酶特性(見圖2)。
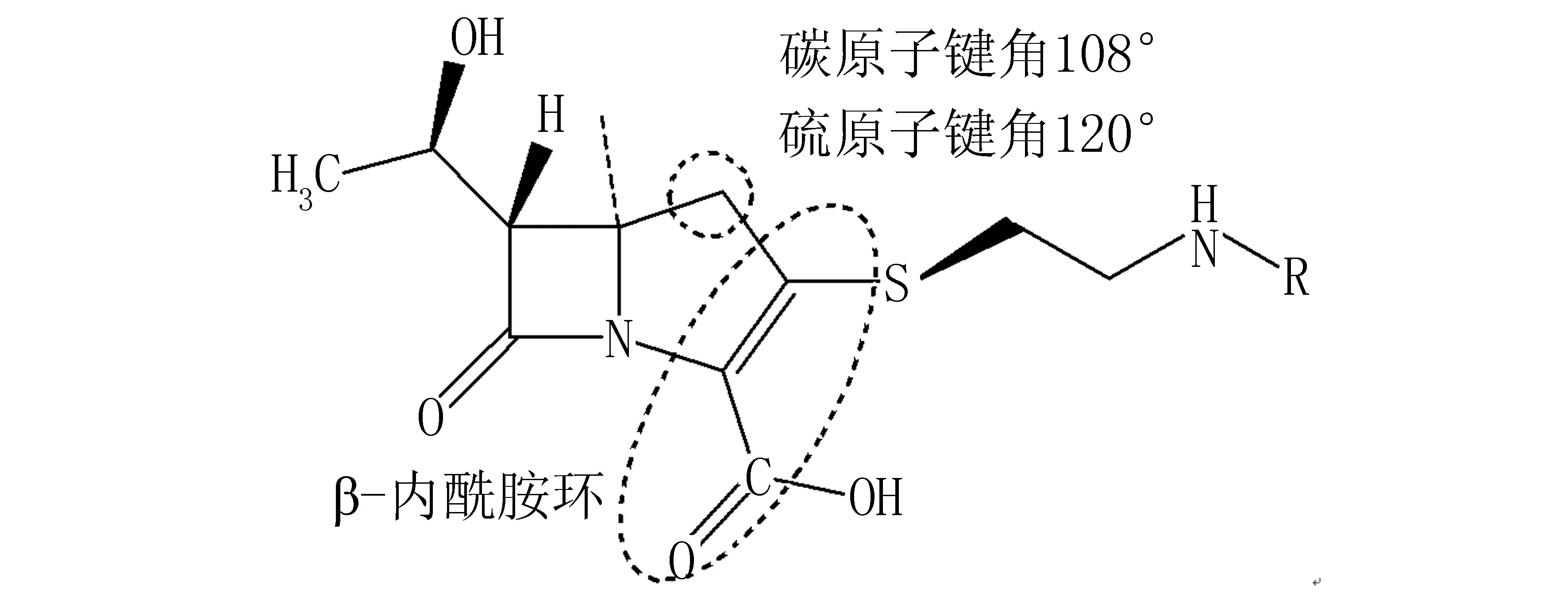
圖2 碳青霉烯的立體結構Figure 2 Stereoscopic structure of carbapenem
青霉烯類與碳青霉烯類抗生素有相似的共軛雙鍵,5、6位H呈反式構型, 6位具有耐β-內酰胺酶的α-羥乙基,其與碳青霉烯的主要差別是1位的堿性硫醚側鏈改為四氫呋喃,明顯降低了抗G-桿菌的作用,但仍具備對敏感菌較強的抗菌活性和對β-內酰胺酶的穩定性。法羅培南的結構見圖3。

圖3 法羅培南的分子結構Figure 3 Molecular structure of faropenem
1.2 碳青霉烯類抗生素的分類及抗菌活性 碳青霉烯類抗生素根據2位側鏈不同,可分為亞胺培南型和厄他培南型兩種類型。第一類是亞胺培南型,包括亞胺培南、帕尼培南、比阿培南和多尼培南(見圖4),在2位都具有堿性硫醚側鏈,具有很強的抗G-桿菌作用和廣泛抗菌特性,抗菌譜涵蓋需氧菌和厭氧菌,G+菌和G-菌,特別是對腸桿菌科和銅綠假單胞菌等非發酵菌具有廣譜作用,且對超廣譜β-內酰胺酶(ESBLs)和AmpC酶等都有高度的穩定性,但對糞腸球菌僅有抑菌作用,對屎腸球菌、耐甲氧西林金黃色葡萄球菌(MRSA)和嗜麥芽假單胞菌等均耐藥。

圖4 已上市的6種碳青霉烯類藥物的分子結構Figure 4 Molecular structures of six carbapenems on the market
亞胺培南和帕尼培南易被腎脫氫肽酶1(DHP-1)水解,所以加入西司他丁和倍他米隆制成復合制劑以防止水解和被腎小管重吸收以保護腎臟。美羅培南、比阿培南和多尼培南屬于1位甲基碳青霉烯,對DHP-1穩定,所以不需要制成復合制劑[5]。第一類碳青霉烯的半衰期約為1 h,需要一日兩次注射給藥。第二類是厄他培南型,只有厄他培南一個注射劑品種。厄他培南對DHP-1穩定,不需要制成復合制劑,是長效碳青霉烯,每日只需注射一次。
1.3 青霉烯類藥物的品種及抗菌活性 青霉烯類藥物目前僅有法羅培南一個口服品種上市。法羅培南對溶血性鏈球菌A群和B群具有較強的抗菌活性,對大多數厭氧菌和腸桿菌具有良好活性,對絕大多數β-內酰胺酶穩定,但對MRSA和屎腸球菌作用較差,對銅綠假單胞菌等非發酵菌活性差或無抗菌作用。
2 碳青霉烯類藥物的品種、專利情況、藥動學及臨床應用
2.1 品種及專利情況 國內已經上市的碳青霉烯類品種有亞胺培南、美羅培南、帕尼培南、厄他培南、比阿培南、多尼培南6種,已上市青霉烯類目前僅有法羅培南一個品種。已上市碳青霉烯類和青霉烯類的專利情況見表1,仿制企業、抗菌譜及適應證見表2。

表1 碳青霉烯類和青霉烯類藥物的專利情況匯總Table 1 Summary of the patents of carbapenems and penems
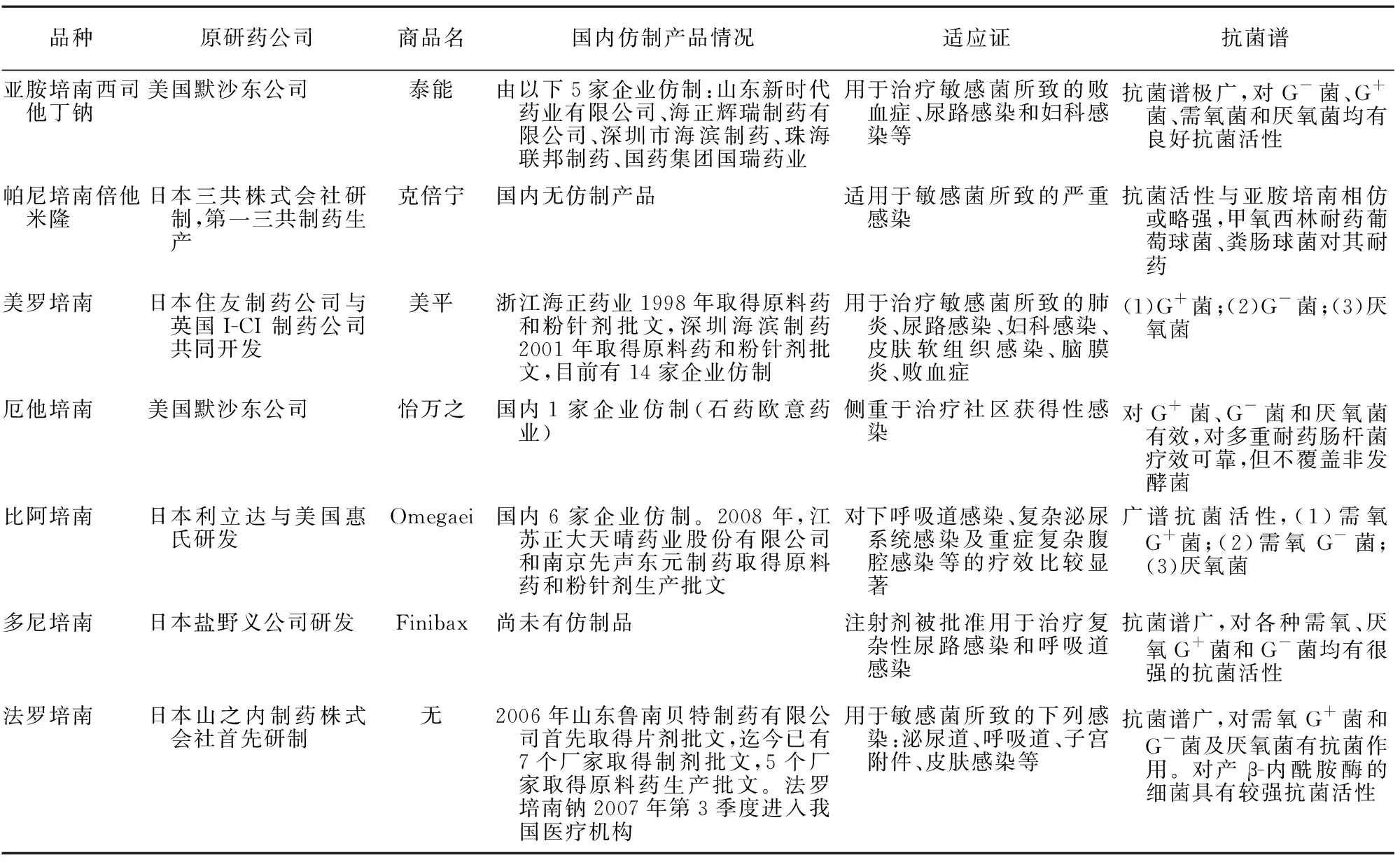
表2 已上市碳青霉烯類和青霉烯類藥物的仿制企業、抗菌譜及適應證Table 2 The generic companies,antibacterial spectra and indications of carbapenems and penems on the market
2.2 藥動學特征 已上市的碳青霉烯類抗生素均為水溶性藥物,一次給藥量為0.5或1 g可良好分布到肺組織、膽汁、膽囊、腹腔內等全身部位,但在腦脊液中的濃度較低,僅為血液中的8%~16%。血液和腦脊液中藥物的清除半衰期分別為1.0和7.4 h。美羅培南透過血腦屏障的能力相對較強,能很好地穿透進入細菌性腦膜炎患者的腦脊液;在化膿性腦膜炎急性期,血腦屏障對帕尼培南的通透性增加,在腦脊液中的濃度可超過大多數致病菌的最低抑菌濃度,所以美羅培南和帕尼培南可以用于中樞神經系統感染的治療[6]。大部分碳青霉烯類藥物的半衰期約為1 h,需每日2次或每日3次給藥。厄他培南半衰期約為4 h,每日給藥1次即可。該類藥物主要以原型從腎排泄,因此應根據腎功能調整給藥劑量。青霉烯類及碳青霉烯類的分類及藥動學特征見表3。

表3 碳青霉烯類及青霉烯類藥物的分類及藥動學特征Table 3 Classification and pharmacokinetics of carbapenems and penems
2.3 臨床應用 碳青霉烯類藥物的抗菌譜非常廣,曾被稱作對細菌的“最后一道防線”。臨床上主要用于重癥感染、多重耐藥菌感染、敗血癥等。常作為病原體明確前的經驗性治療的首選藥物,明確病原體后應及時“降階梯治療”。對于腎功能不全患者,所有碳青霉烯類藥物均應減量使用。
亞胺培南對敏感菌引起的敗血癥、尿路感染和婦科感染有效率在95%以上,對軟組織、骨關節和腹腔內感染的有效率超過90%,對下呼吸道感染的有效率為85%,細菌清除率為76%~92%[7]。亞胺培南西司他丁可能引起中樞神經系統(central nervous system,CNS)毒性,包括精神癥狀、休克、頭痛和癲發作等[8]。一篇薈萃(meta)分析納入了100多項比較亞胺培南與非碳青霉烯類抗菌藥物癲發作風險的研究,結果顯示,每1000例接受亞胺培南治療的患者中有4例出現癲發作[9]。亞胺培南的CNS毒性在有基礎CNS疾病或腎功能受損的患者中尤其明顯[10]。因此,亞胺培南不能用于治療腦膜炎,不能與阿昔洛韋聯用,給藥速度不宜過快。
美羅培南的抗菌譜與亞胺培南相似。對敗血癥、包括肺囊性纖維化合并感染在內的肺部感染、腹腔感染、腦膜炎等療效較好。但與亞胺培南不同,美羅培南對人DHP-1穩定,因此可以不聯合西司他丁使用。雖然美羅培南引起癲發作的風險略低于亞胺培南,但亞胺培南和美羅培南的頭對頭比較研究未發現兩者具有統計學差異[10]。
厄他培南對許多常見的需氧菌和厭氧菌均有良好的體外活性。但由于其對不動桿菌、腸球菌和銅綠假單胞菌的活性有限,不太適合晚發型院內感染。厄他培南的抗菌譜比亞胺培南或美羅培南窄,半衰期較長,可每日1次給藥。
帕尼培南與倍他米隆按照1∶1組方,以提高穩定性,適用于敏感菌引起的敗血癥、骨髓炎、肺部感染、膿胸、膽道感染、腹腔感染、腦膜炎等。臨床有效率和細菌學效果均達80%以上。給藥劑量0.5 g(按帕尼培南計),每日2次,最大劑量為2 g/d。
多尼培南是相對較新的碳青霉烯類藥物,有關其治療產ESBLs菌感染的臨床數據有限,但數據總體表明該藥與美羅培南或亞胺培南的療效相當[11]。多尼培南治療復雜性泌尿道感染和腹腔內感染的效果較好[12-13],抗菌譜與美羅培南相似,但對銅綠假單胞菌的體外抗菌活性似乎強于美羅培南[14]。
3 青霉烯類藥物的品種、藥動學及臨床應用
青霉烯類是唯一的一類對靜止期細菌有作用的β-內酰胺類抗生素,對β-內酰胺酶不僅穩定,而且還有抑制作用。但青霉烯類藥物的化學性質不穩定,而且在體內易代謝產生低分子硫化物,有惡臭。目前應用于臨床的僅有法羅培南一個品種,它是一個非典型的β-內酰胺類抗生素,屬于青霉烯類衍生物,通過阻斷細菌細胞壁的合成發揮殺菌作用,是唯一口服給藥的培南類藥物。與同類品種相比,法羅培南具有口服吸收好、無腎毒性、抗菌譜更廣和不易產生耐藥性的優勢。法羅培南專利情況見表1,抗菌譜及適應證見表2,藥動學特征見表3。
4 討 論
4.1 碳青霉烯類藥物的分級管理建議 我國抗菌藥物分級管理制度要求醫療機構按照非限制使用、限制使用和特殊使用的分級管理原則對抗菌藥物進行管理,各級醫師根據處方權限使用抗菌藥物[15]。特殊使用級抗菌藥物的使用應有嚴格的指征或確鑿依據,需經有關專家會診或本科室主任同意,其處方須由副主任醫師或主任醫師簽名方可使用,這類藥物應作為三線用藥。碳青霉烯類藥物在我國統一作為特殊使用級別管理,這樣會造成一些抗菌譜窄的藥物可及性差,醫療機構采購品種受限,必然造成某些碳青霉烯類藥物使用量過大,細菌耐藥率上升。另外,傳統的抗菌藥物如青霉素、頭孢菌素、喹諾酮類等通常與誘導多重耐藥G-菌相關,臨床需要能有效控制多重耐藥G-菌導致的嚴重感染、且不過度覆蓋非發酵菌的碳青霉烯類藥物。厄他培南抗菌譜包括需氧G+菌,非發酵菌以外的G-菌和厭氧菌,對產ESBLs腸桿菌科細菌發揮快速殺菌作用,但抗G-桿菌譜相對較窄,對銅綠假單胞菌和不動桿菌等不敏感,所以厄他培南恰能滿足以上臨床需求,用于治療多重耐藥的G-菌導致的嚴重社區獲得性感染。
厄他培南具有半衰期長、安全性好、不易產生耐藥性、日均費用低等優點,正確地使用可以在一定程度上遏制院內細菌耐藥發展,有效改善醫院耐藥環境。有研究顯示[16],醫院使用厄他培南后,包括亞胺培南在內的多種抗菌藥物的使用量下降,銅綠假單胞菌對亞胺培南的敏感性呈上升趨勢,厄他培南在臨床使用7年,對醫院的微生態環境產生了正面影響。2017年CHINET中國細菌耐藥性監測顯示,腸桿菌科細菌對厄他培南的敏感率高達92%。厄他培南還可用于直腸、結腸擇期手術的預防用藥,而其他碳青霉烯類抗菌藥物不可作為預防用藥。所以厄他培南在抗菌藥物臨床應用分級管理目錄中應該作為限制使用級抗菌藥物管理,放寬醫師的處方權限,這樣能提高厄他培南在臨床應用的可及性。在短時間內及時使用厄他培南,爭取最佳治療時機,可以減少患者感染機會,降低病死率。
4.2 青霉烯類藥物的分級管理建議 法羅培南具有抗菌譜廣(對需氧G+菌、需氧G-菌及厭氧菌均有廣泛抗菌作用),抗菌活性強(尤其是對G+菌),安全性高,耐藥性低等特點,逐漸成為對抗多重耐藥菌的一道防線。一項體外研究顯示[17],產ESBLs的大腸桿菌、肺炎克雷伯菌、銅綠假單胞菌等菌株對不同種類的抗生素具有共同耐藥性,但是對法羅培南和亞胺培南均敏感,且耐藥率最低。法羅培南口服給藥可以提高其在社區獲得性肺炎和慢性支氣管炎急性發作治療中的可及性。根據“能口服不肌注,能肌注不靜脈給藥”的給藥原則,法羅培南在給藥方式上具有自己獨特的優勢。而且法羅培南日均費用較低,抗菌譜較窄,作為特殊使用級抗菌藥物管理限制了其在社區的使用,作為非限制使用級管理又會造成抗菌藥物濫用。因此,綜合考慮法羅培南的結構特點、抗菌譜、藥動學特征,建議將其作為限制使用級抗菌藥物進行管理。
4.3 降級后如何避免濫用 將厄他培南、法羅培南作為限制使用級而非特殊使用級抗菌藥物管理,從一定程度上會增加使用量,容易造成抗菌藥物濫用。可以從以下三個方面加強管理,避免不合理使用。(1)醫保限制。我國2020年醫保目錄中厄他培南和法羅培南均為乙類報銷品種,厄他培南限用于多重耐藥的重癥感染,法羅培南限用于頭孢菌素耐藥或重癥感染患者,適應證和醫保的限制能夠控制兩種藥物濫用。(2)耐藥菌監測。醫療機構仍需進行持續的耐藥監測,細化臨床考核指標,防止厄他培南和法羅培南過量使用。(3)提倡耐藥菌感染抗菌治療的多樣化。針對目前細菌耐藥日益嚴峻的形式,應當提倡耐藥菌感染抗菌治療的多樣化,打破一遇到耐藥菌就使用最高級別抗菌藥物的慣性思維。對于一些輕中度的多重耐藥菌感染,宜選擇其他類別的抗菌藥物,如產ESBLs細菌所致的輕中度感染也可根據藥敏結果選用其他類別抗菌藥物,避免大量使用某一類藥物造成細菌對同類藥物交叉耐藥。

