基于偏最小二乘回歸法分析藥用紫草抗腫瘤譜效關系
廖梅
藥用紫草是我國傳統中藥,研究應用廣泛,主要指新疆紫草Arnebia euchroma
(Royle)Johnst(AE)、內蒙古紫草Arnebia guttata
Bunge(AG)及紫草Lithospermumerythrorhizon
Sieb.et Zucc(LE)的干燥根。實踐證明,紫草及其復方制劑可用于治療子宮絨毛膜上皮癌、胃癌、食道癌等疾病。作為紫草的主要有效成分,紫草素及其衍生物對人非小細胞肺癌細胞系(A549)顯示較好體內和體外抑制活性,其抗腫瘤作用機制可能與抑制細胞增殖、侵襲、遷移、上調p53基因(p53)、B淋巴細胞瘤-2基因相關X蛋白(Bax)、裂解半胱天冬酶-9(cleaved-caspase-9)、裂 解 半 胱 天 冬 酶-9(cleaved-caspase-3)和下調B淋巴細胞瘤-2基因(Bcl-2)的表達,激活細胞線粒體凋亡途徑,誘使受體相互作用蛋白激酶1(RIP1)和受體相互作用蛋白激酶3(RIP3)的增高導致細胞程序性壞死等途徑有關。本研究前期采用MTT法評價,結果顯示紫草甲醇提取物對A549表現出優異的細胞增殖抑制活性,其抑制作用呈現劑量依賴性,某些產地樣品的半數抑制濃度(IC值)與陽性藥紫杉醇相當。近年來,LC-MS/MS將液相色譜特別是超高效液相色譜與高靈敏度的質譜技術相結合,能夠獲得豐富的結構信息,從而建立快速、高效的分析方法。UHPLC-QTRAP-MS/MS(MRM)特征輪廓譜是在LC-MS/MS技術基礎上建立的能全面、特異性識別、表征和定量某一類結構性質相關化學成分的特殊指紋圖譜。由于MRM功能的高選擇性和靈敏性,根據樣品中每個MRM離子對表征的色譜峰面積可用于相對定量,在獲得單體化合物的標準品后可進行絕對定量。基于UHPLC-QTRAP-MS/MS(MRM)技術的紫草素類成分特征輪廓譜在定量的同時能實現化合物的定性需要,有效解決了大量譜效關系研究只篩選活性色譜峰而對其結構不明的問題。紫草素成分復雜,結構多樣,主要成分和微量成分的含量懸殊、分離純化困難,致使紫草素類成分與其抗腫瘤藥效關系仍不明確,影響其內在質量評價體系的建立。因此,筆者首先采用UHPLCQTRAP-MS/MS(MRM)特征輪廓譜技術建立不同產地紫草提取物的指紋圖譜,采用MTT法測定紫草甲醇提取物對A549細胞的抑制率作為藥效指標,然后通過偏最小二乘回歸法(PLSR)分析辨識與抗腫瘤活性具有重要影響的特征峰,最后對部分化合物進行活性驗證,為闡明藥用紫草的抗腫瘤藥效物質基礎提供科學依據。
1 儀器與材料
1.1 儀器
QTRAP4000質譜儀配備ESI離子源及Analyst 1.6.3,Peak View1.2數據處理系統(美國AB SCIEX公司),配備LC20ADXR高效液相色譜儀(日本Shimadzu公司);MS103DU電子分析天平(瑞士Mettler Toledo公司);Rt2100C型酶標檢測儀(深圳Rayto公司)。1.2 試藥
色譜純甲醇、乙腈(美國Fisher公司);分析純98%甲酸和甲酸銨(國藥集團化學試劑有限公司);雙氯芬酸鉀(中國食品藥品檢定研究院,批號100880);紫杉醇(Sigma公司,批號T1912);改良型RPMI-1640培養基(Hyclone,批號SH30809.01B);胎牛血清(杭州四季青生物工程材料有限公司,批號141215);胰酶(AMRESCO Inc,批號0457);MTT(AMRESCOInc,批號0793);DMSO(AMRESCOInc,批號0231)。藥用紫草飲片購買自安徽省亳州市百姓平價藥業有限責任公司,由嘉應學院張聲源副教授鑒定,樣品信息見表1。
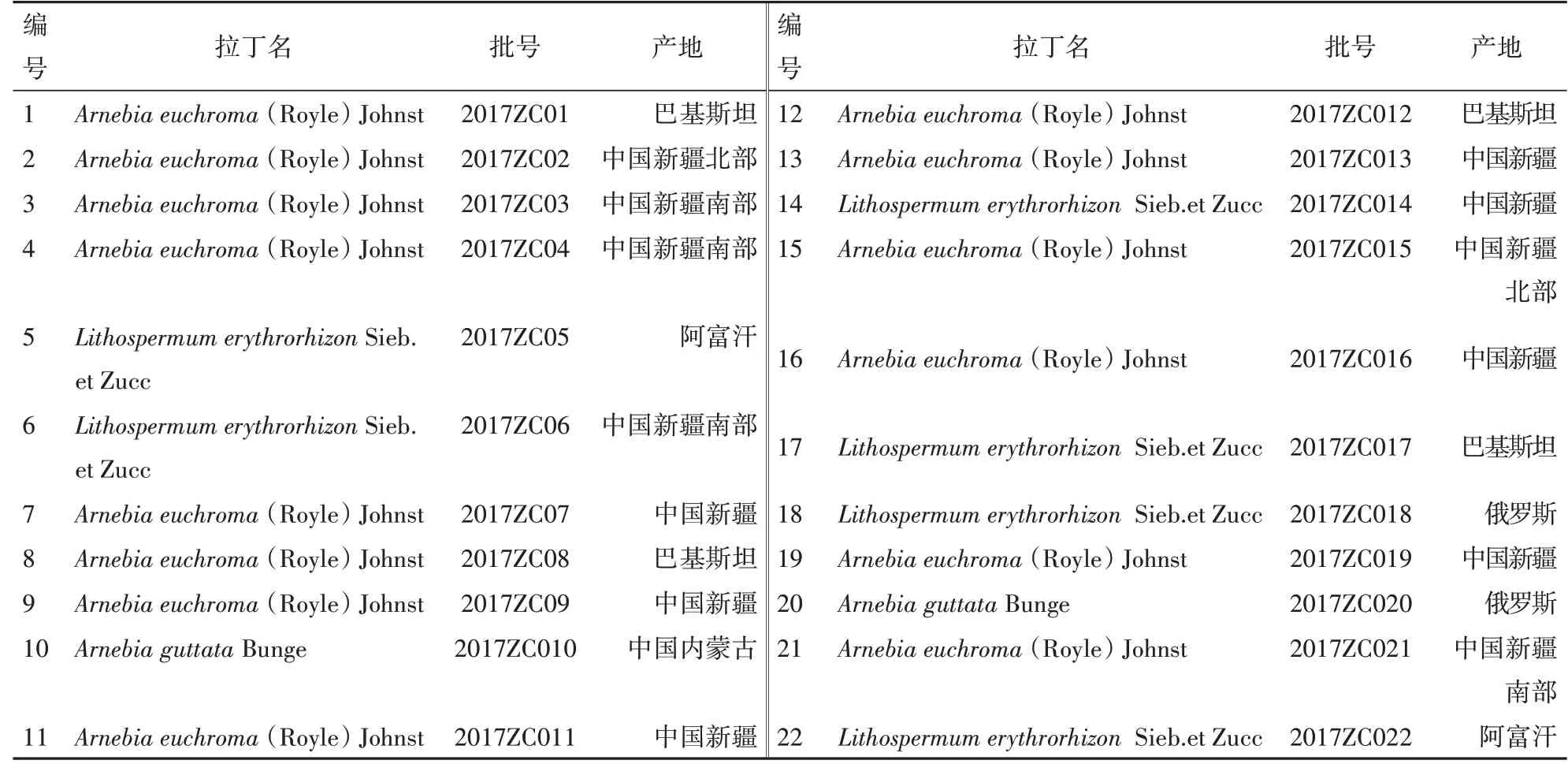
表1 紫草樣品信息
2 方法與結果
2.1 藥用紫草UHPLC-QTRAP-MS/MS(MRM)特征輪廓譜的建立
2.1.1 內標物溶液的制備
精密稱取雙氯芬酸鉀10 mg,加甲醇配成1 mg/mL的儲備液,吸取該溶液適量,甲醇稀釋至1μg/mL,作為內標物溶液,4°C下密封保存備用。2.1.2 供試品溶液的制備
各紫草樣品經適當粉碎后過40目篩,稱取1 g粉末,每個樣品重復制備3份。加20 mL甲醇搖勻,室溫超聲提取30 min,放冷至室溫,過濾要濾液;濾渣加10 mL甲醇重復提取2次,合并3次提取液。吸取提取液1 mL,10 000 r/min離心10 min,取上清液0.5 mL適量,甲醇稀釋10倍,即為供試品溶液。分別取各供試品溶液1 mL,渦旋混合2 min,即為質控樣品(QC)溶液。進樣前,精密吸取供試品溶液200μL,內標物溶液20μL,小心吹打混勻,進樣分析。2.1.3 分析條件
色譜柱為Welch Ultimate XB-C(100 mm×2.1 mm,1.8μm);5 mmol/L甲酸銨水溶液(含0.01%甲酸)為A相,乙腈為B相;洗脫條件為:0~0.1 min,20%B;0.1~10.0 min,20%~50%B;10.0~30.0 min,50%~60%B;30.0~35.0 min,60%~95%B;35.0~40.0 min,95%B;40.0~40.1 min,95%~20%B;40.1~45.0 min,20%B;柱溫40℃;進樣器溫度4℃;流速0.3 mL/min;進樣量10μL。ESI離子源,負離子電離模式。質譜參數為:CUR:30 psi,GS1:50 psi,GS2:50 psi,ISVF:-4.5 kV,TEM:500℃,DP:-60 V,CE:-30 eV,CES:15 v,MRM模式。
2.1.4 特征輪廓譜的建立
將22批紫草飲片按“2.1.2”項制得供試品溶液,按照“2.1.3”項下的測定條件進樣測定,并記錄各批次樣品色譜數據。為了考察儀器系統的穩定性和色譜峰的重現性,參考文獻方法設置QC進樣順序,采用MarkerView1.2.1軟件提取色譜峰數據。以雙氯芬酸鉀內標峰為參照執行保留時間(RT)校正和峰面積歸一化命令,最終相對定量57個特征峰(表2)。結果顯示各QC樣品中各特征峰的相對峰面積和RT值的RSD值分別在3.1%~8.6%和0.1%~2.5%。說明系統重現性良好,測定變量的差異是由樣品本身的差異引起。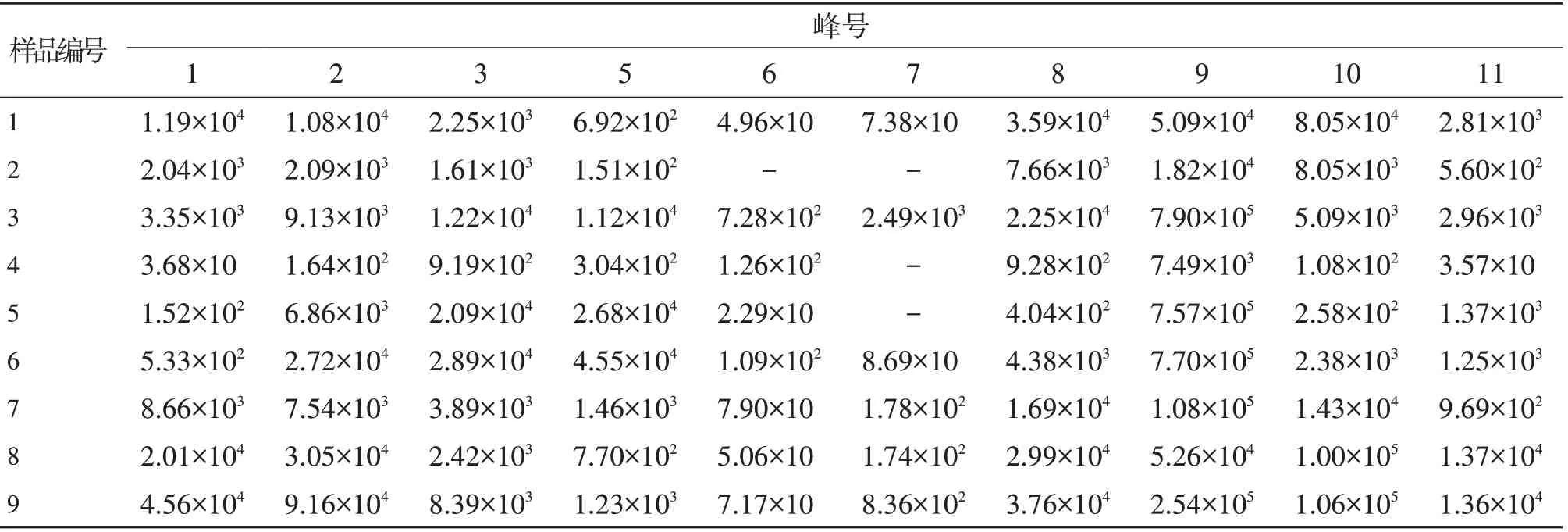
表2 22批紫草提取物中特征峰的相對峰面積
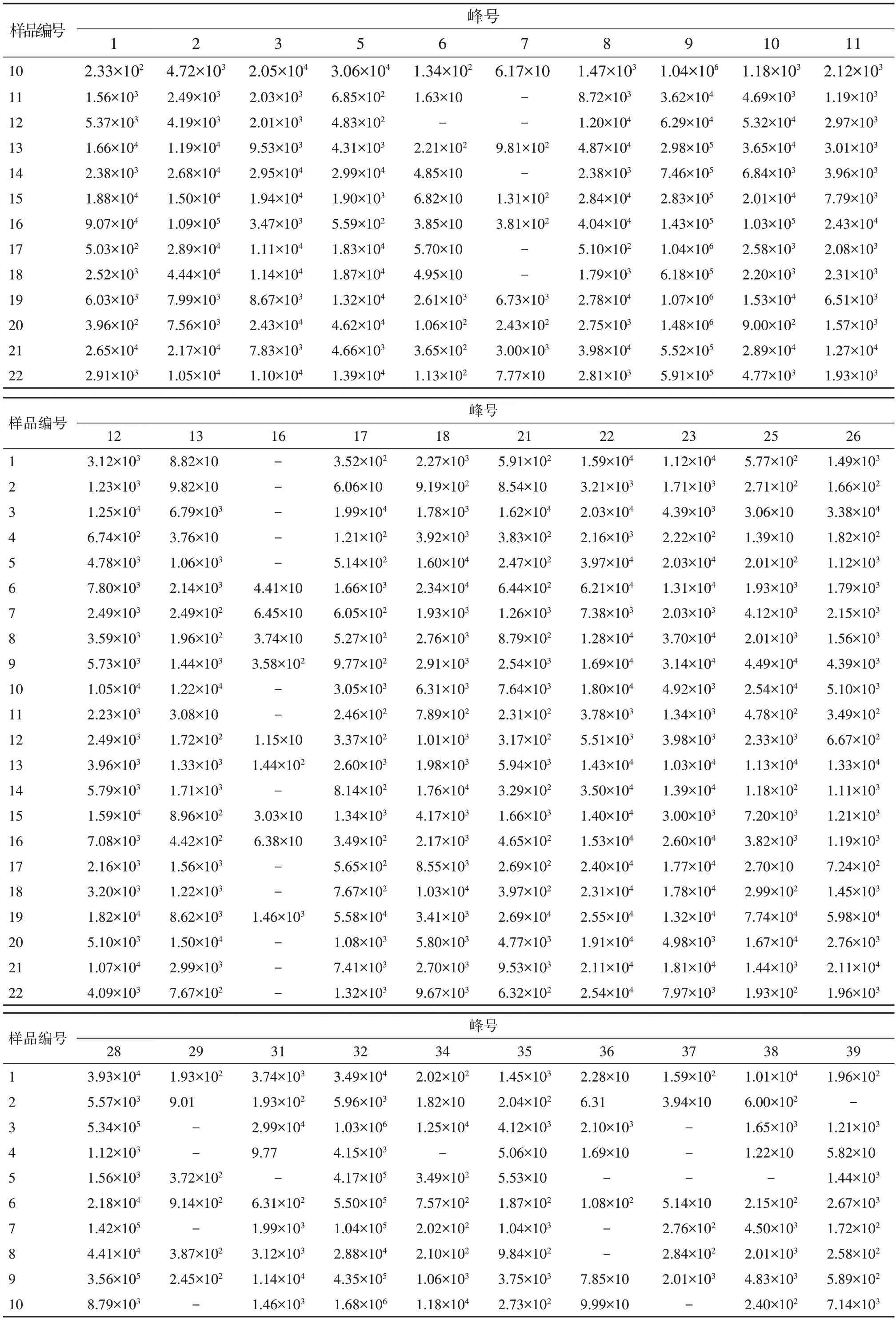
續表2 22批紫草提取物中特征峰的相對峰面積
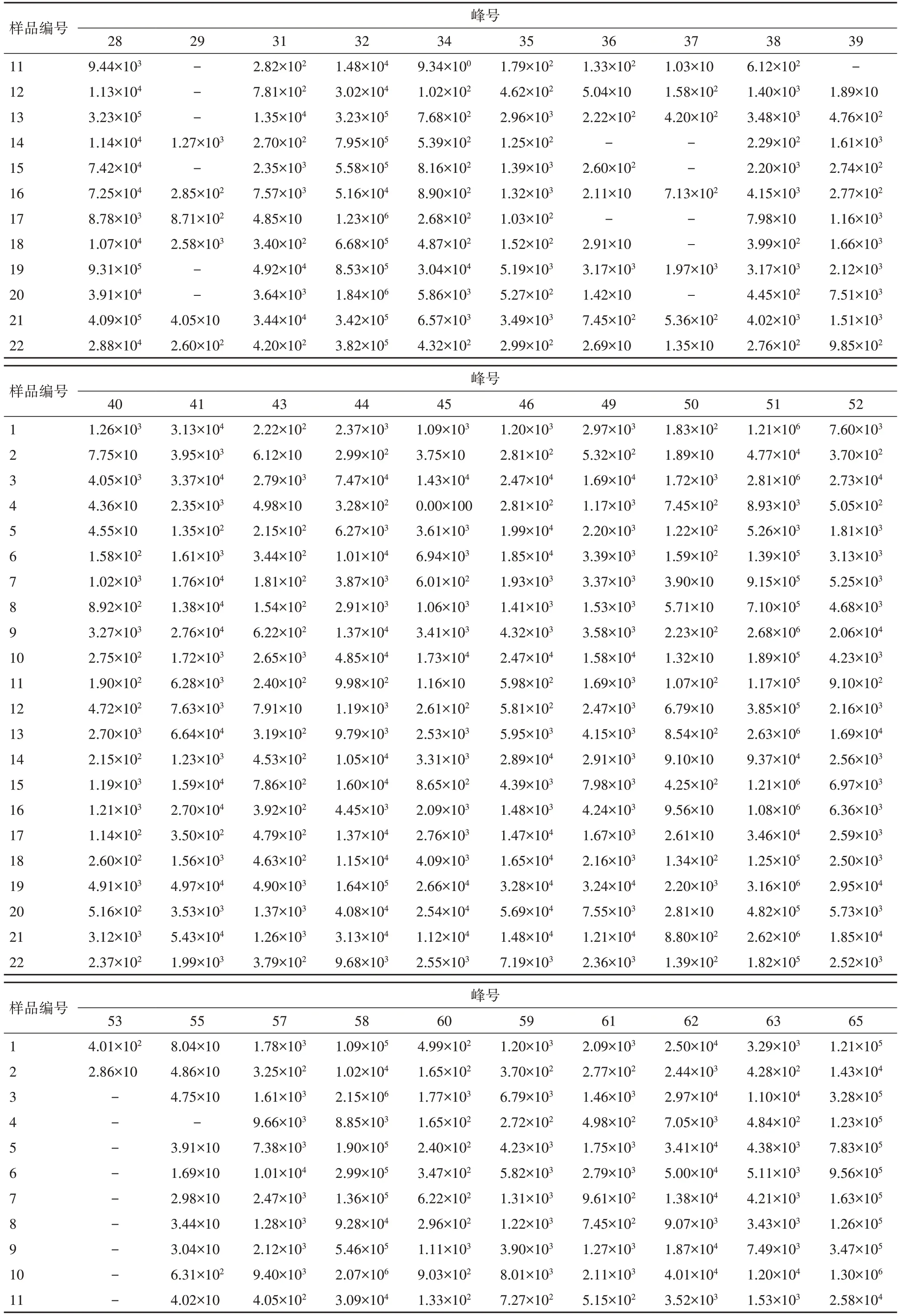
續表2 22批紫草提取物中特征峰的相對峰面積
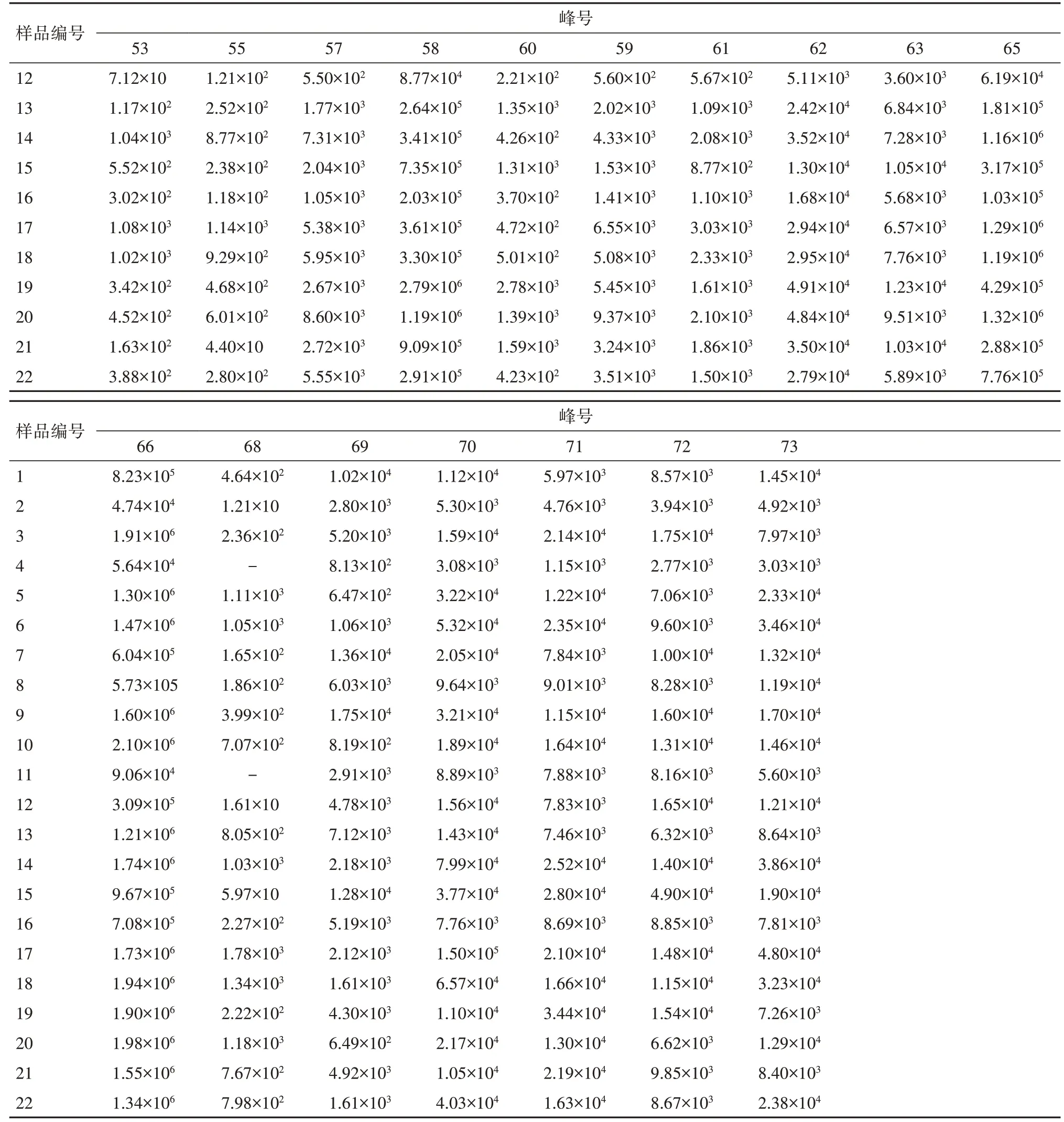
續表2 22批紫草提取物中特征峰的相對峰面積
2.2 紫草體外抗腫瘤藥效學實驗
2.2.1 樣品溶液的制備
分別取“2.1.2”項下的供試品溶液適量,10 000 r/min離心10 min,精密吸取上清液4 mL,氮氣吹干甲醇,加0.5 mL DMSO溶解配成工作儲備液,培養基稀釋1 000倍后配成生藥濃度為0.2 mg/mL的含藥培養基即為樣品溶液。最后取100μL含藥培養基加入100μL細胞液中,每個樣品設6個復孔。2.2.2 抗腫瘤活性的測定
取對數生長期A549細胞用RPMI 1640培養液調整細胞數為1×10個/mL的單細胞懸液,參考文獻測定各樣品的細胞抑制率(見表3)。結果顯示,在等生藥量濃度條件下,22批樣品的抑制率在0.182~0.989,可見不同來源紫草甲醇提取物對A549細胞的抑制作用存在較大差異,原因可能是不同紫草中所含紫草素類化合物含量存在差異,這種顯著性差異為譜效關系研究提供了良好的數據基礎。
表3 22批藥用紫草提取物的細胞抑制率(n=6)/±s
2.3 譜效關系辨識結果分析
PLSR集成了典型相關分析、主成分分析和多元線性回歸分析的基本功能,可以最大限度地利用數據信息,預測精度高,主要用于多因變量對多自變量的回歸建模,能較好地解決樣本量少于變量的問題,是一種模型擬合度好和預測能力強的數據處理方法,在譜效關系研究中被廣泛采用。本研究分別將22批次紫草的57個特征峰的相對峰面積作為自變量X,將A549細胞的抑制率作為因變量Y導入SIMCA-14.1軟件,采用PLSR模型將數據X和Y進行回歸分析,計算得到57個特征峰與抑制率的標準化回歸系數和變量投影重要性系數(VIP)值,見表4。VIP>1時,自變量在解釋因變量時差異有重要意義。由圖2可知,VIP均大于1且由大到小的順序為峰59、9、66、32、62、45、46、58、43、71、13、63、41、44、5、39、34、65、49、21、12、3、22和60,說明其對應的物質對A549細胞的抑制作用有重要影響。經過與對照品比對及質譜分析鑒定,確定了各峰代表的化合物(見表5)。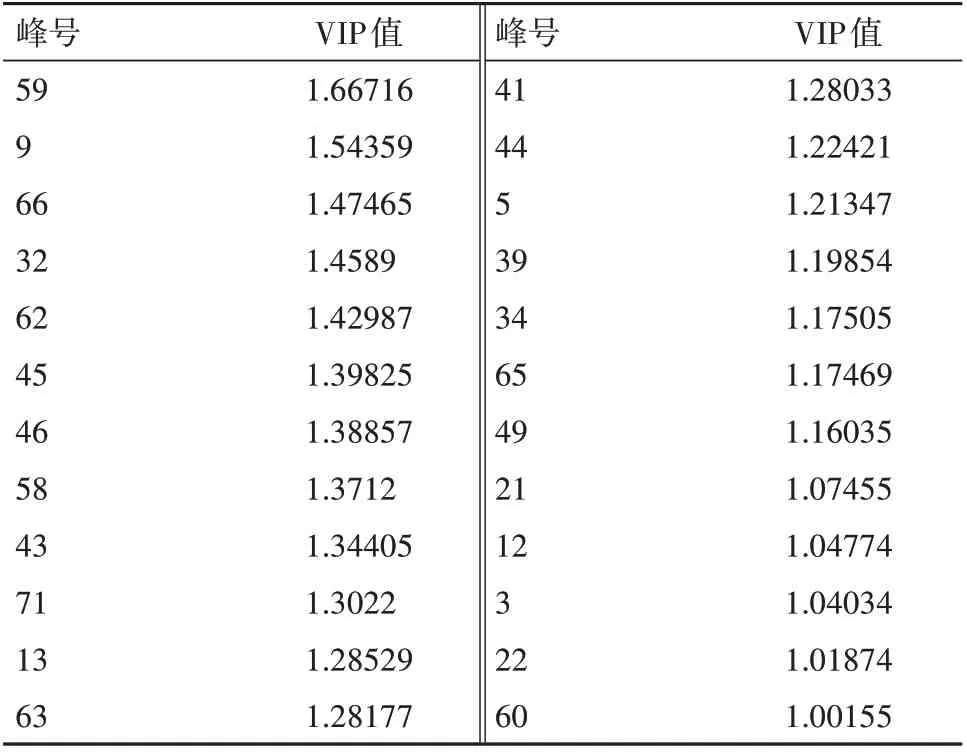
表4 各化合物對藥效的變量投影重要性系數(VIP)值

表5 經偏最小二乘回歸(PLSR)譜效關系辨識的化合物
2.4 體外抗腫瘤驗證試驗
對于有標準品的化合物,筆者采用MTT法驗證其對A549細胞的體外抑制活性,以紫杉醇為陽性對照。分別稱取各化合物適量,加DMSO溶解配成100 mmol/L的儲備液,臨用前培養基稀釋成0、0.1、0.5、1、5、10、25、50μmol/L的含藥培養基,最后取100μL含藥培養基加入100μL細胞液中,每個樣品設6個復孔。按“2.2.2”項下方法操作并計算化合物的IC值,結果見表6。結果顯示各化合物的IC值在0.74~22.60μmol/L之間,其細胞抑制率隨著濃度升高而增強,可能是紫草發揮體外抗腫瘤作用的重要成分。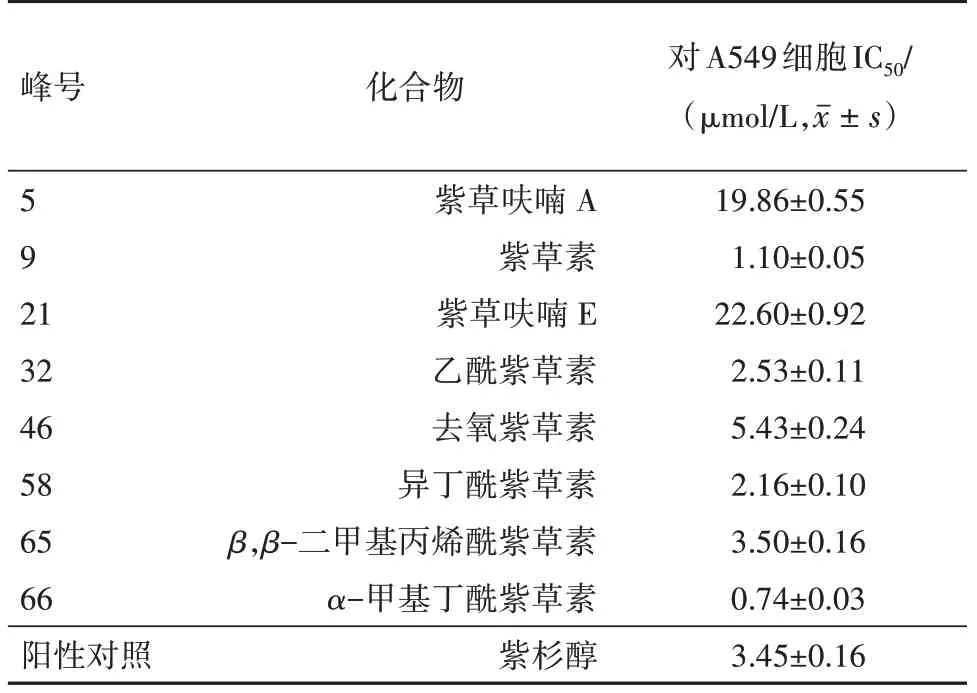
表6 化合物的體外抗腫瘤活性
3 討論
紫草中的紫草素類成分同分異構體多樣,由于幾個主要成分的干擾,其他微量成分根本無法在常規的紫外檢測器上顯示,色譜分離分析困難,目前關于如何有效建立紫草中的紫草素類成分指紋圖譜還未見文獻報導。本實驗采用UHPLC-QTRAPMS/MS(MRM)技術建立的紫草特征輪廓譜能同時對化合物進行定量和定性分析,有助于后期譜效關系研究對化合物的指認和鑒定。
目前,中藥譜效關系研究中多采用1個指標,或者將幾個藥效指標同時評價起到相互補充、相互佐證的作用,但有時卻會因幾個藥效指標同時評價得到相互矛盾的結果。因此,選擇有針對性、能代表藥物主要作用的指標至關重要。紫草素及其衍生物對A549細胞的抗腫瘤作用已有多篇文獻報導,藥效確切。課題組進一步通過MTT法確證了藥用紫草甲醇提取物也具有相當強的抗A549細胞活性;在相同生藥劑量時,不同來源紫草藥材對細胞的抑制率不同;相同來源的藥材其抑制率呈劑量依賴性。因此選擇對紫草提取物反應靈敏的A549細胞抑制率作為藥效指標對于評價紫草體外抗腫瘤活性是可行的。
目前譜效關系研究的數據處理方法眾多,具有各自的優勢和應用范圍。本研究采用PLSR法分析了紫草藥材樣品特征峰與其抗腫瘤作用的相關性。結果辨識出24種紫草素類成分與其抗腫瘤作用呈正相關,說明紫草的抗腫瘤效應是多種成分共同作用的結果。活性驗證結果顯示紫草呋喃A(5)、紫草素(9)、紫草呋喃E(21)、乙酰紫草素(32)、去氧紫草素(46)、異丁酰紫草素(58)、β,β-二甲基丙烯酰紫草素(65)和α-甲基丁酰紫草素(66)均對A549細胞有一定抑制作用,其IC值為0.74-22.60μmol/L,在一定程度上驗證了上述譜效關系研究結果。由于分離純化工作仍在進行,對于辨識出的其他化合物是否具有確切的藥效還有待課題組進一步深入探討。
綜上所述,本研究通過藥用紫草的譜效關系初步明確了與其抗腫瘤活性相關的物質,為紫草后續研究和開發提供了科學依據。

