有氧跑臺訓練對小鼠左右心肌特定miRNAs的影響
張海鵬,徐 琳,宋彥霖,徐盛嘉,楊 靖,馬繼政,鐘 勇
0 引 言
合理的體育活動是一種有效的干預措施,可以改善生活質量,并延長預期壽命。目前,廣泛認為有氧訓練可以誘發獨特的心臟保護表型,用來預防和治療心血管疾病。心血管系統反映出急性和長期運動的明顯改變。這些適應變化的核心涉及心血管系統內細胞和分子信號通路變化的協同整合,使組織能夠應答運動時人體的需求[1]。心臟肥大是機體對有氧運動主要適應之一,可以正常化室壁應力,減少氧氣消耗,并增加工作能力,使其存在明顯的機械優勢[1]。因此,認識運動性心肌肥大的適應過程,具有重要的生理意義。
當前,微小RNA分子(micro RNAs, miRNAs)已經成為潛在的生物標志物,可響應并參與運動中的適應性變化[2-3]。miRNAs是短的非編碼RNA,通過抑制蛋白質翻譯或增強信使RNA(mRNA)的降解,調節轉錄后基因的表達[2-3]。miRNAs參與正常的功能性心臟組織的發育,控制細胞的生長、分化、凋亡和增殖,并參與心血管病理生理變化的調控,例如肥大、纖維化和心肌細胞的損害[2]。
左右心室是相互依存的,嵌套在心包內,具有共同的隔膜,并被共同的心肌纖維包圍。研究表明耐力訓練后左室中發生的結構和功能適應,可能與右室存在不同。鑒于上述原因,本研究選擇肌肉組織高表達的肌組織特異miRNAs(miR-208a、miR-208b和miR-499)[2,3],以及其他的被認為在心肌中重要的miR-21、miR-17-3p[2-3],觀察長期的有氧練習左右心肌中這些miRNAs的變化,為有氧運動提供依據。
1 材料與方法
1.1 實驗動物取48只健康C57BL/6J雄性小鼠(8周齡),購自北京生命實驗動物技術有限公司(SPF級),小鼠置于光照/黑暗周期為12 h,溫度為(22±2)℃,濕度為45%~50%的屏障環境中,自由飲食。實驗程序經南京大學動物保護和使用委員會批準(IACUC-2006001)。將小鼠按體重隨機數字分組劃分為對照組和訓練組,每組24只。2組在第0周進行跑臺預適應及遞增負荷測試(incremental load test,ILT)后,運動組進行8周有氧跑臺訓練,對照組正常飼養不進行跑臺訓練。動物于下午1點至5點在明亮室內進行跑臺訓練或運動能力測試。
1.2 測試方法
1.2.1 ILT訓練組小鼠使用運動跑臺進行訓練(型號:ZH-PT,安徽正華),適應階段對照組與訓練組都以10 m/min的速度運動10 min,跑步機無傾斜角度,持續5 d[4]。48 h后進行ILT測試,測試方案為:小鼠以6 m/min的速度在跑步機上進行運動,每3分鐘增加3m/min的速度遞增直至小鼠力竭。當小鼠在1 min內觸碰跑步機末端5次及以上時,被定義為力竭。力竭速度計算公式為:
EV=V+(n/b)×a
其中V是最后一次完成階段的速度;n是未完成階段的保持的持續時間;b是每階段的持續時間;a是測試遞增速度[5]。
1.2.2 有氧訓練方案和表現評估本實驗中使用的有氧訓練方案參照文獻[4]進行。期間每周第6天定時記錄小鼠的體重變化情況。并在第0周適應性訓練、第4周和第8周有氧訓練結束后48 h對2組進行ILT測試,對小鼠的運動表現進行評估與記錄。
1.3 心肌樣本提取于第8周最后一次ILT測試結束48 h后,斷頸處死所有小鼠。在無菌無RNA酶的條件下,收集小鼠左、右心室心肌組織置于液氮中速凍,并存于-80°C中后續分析待測。
1.4 RNA的提取使用RNAiso Plus9(型號:9109,Takara)抽提試劑盒,將冷凍的左右心室心肌勻漿進行總RNA的提取。并進行定量聚合酶鏈式反應(RT-qPCR),所有樣品都是在一個批次內進行處理的。以探針法為基礎進行RT-qPCR,得到相應的cDNA產物。使用TaqMan PCR試劑盒(Thermo Fisher Scientific,美國)和Roche LightCycler?96 (Roche,瑞士)進行qPCR檢驗。qPCR條件為95℃預孵育5 min,95℃15 s、60℃60 s共 45個循環,最后37℃冷卻30 s。使用以下TaqMan?探針進行對應miRNA的檢測:snRNA U6 (ID: 001973)、hsa-miR-208a (ID: 000511)、hsa-miR-208b (ID: 002290)、mmu-miR-499 (ID: 001352)、hsa-miR-21 (ID: 000397)和mmu-miR-17-3p (ID: 002543)。所有反應進行3次技術重復。將心肌中miRNAs的相對snRNA U6歸一化表達,并使用2-ΔΔCt方法計算Ct值。
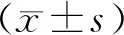
2 結 果
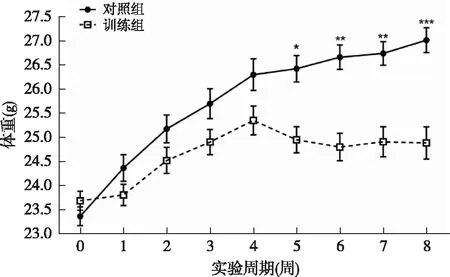
2.1 8周有氧訓練小鼠體重變化情況整個實驗周期間,對照組與訓練組在訓練后期產生體重變化上的差異,其中對照組于第5周、第6周、第7周和第8周的體重顯著高于訓練組(P<0.05;P<0.001;P<0.001;P<0.0001),見圖1。8周的跑步機有氧訓練方案結束時,對照組小鼠體重變化百分比(16.18±5.14)%與訓練組(5.30±6.15)%比較,差異有統計學意義(P<0.0001),見圖2。
*P<0.05、**P<0.001、***P<0.0001
*P<0.0001
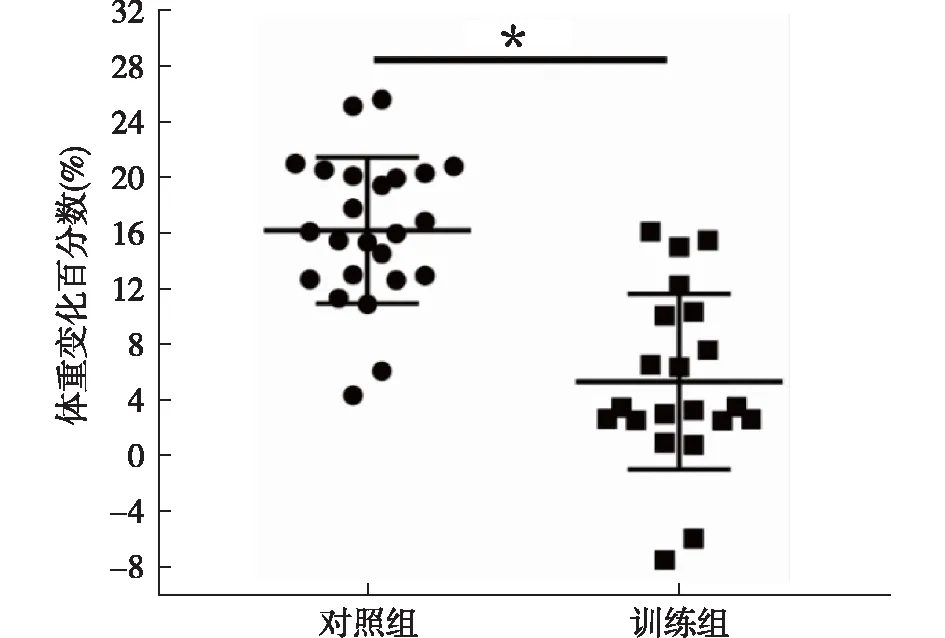
2.2 8周有氧訓練小鼠ILT測試結果第0周時對照組與訓練組的力竭速度差異無統計學意義(P>0.05);第4周訓練后訓練組力竭速度[(29.37±3.49)%]顯著高于對照組[(20.54±2.21)%,P<0.0001];第8周時測試結果表明,訓練組力竭速度[(35.71±4.53)%]仍顯著高于對照組[(21.28±5.47)%,P<0.0001];見圖3。此外,隨著有氧訓練方案的推行,訓練組小鼠的有氧運動能力不斷提升,與第0周力竭速度比較,第4周時提升40.79%(P<0.0001),第8周時提升71.15%(P<0.0001),第8周較第4周成績上升21.56%(P<0.0001)。
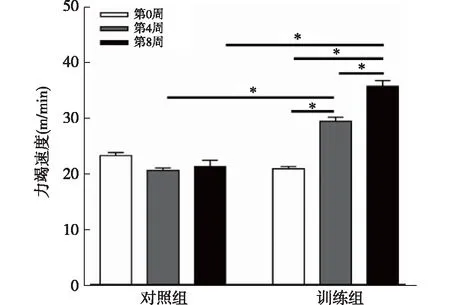
*P<0.0001
2.3 8周有氧訓練心肌組織中miRNAs的變化
2.3.1 左右心肌組織中肌組織特異miRNAs的變化與對照組比較,訓練組中左心室心肌miR-208b和miR-499的水平顯著下降(P<0.01;P<0.05),分別改變1.96倍與2.59倍,但在右室心肌中差異無統計學意義(P>0.05)。值得注意的是,miR-208a在小鼠左右心室的心肌中差異無統計學意義(P>0.05)。見圖4。
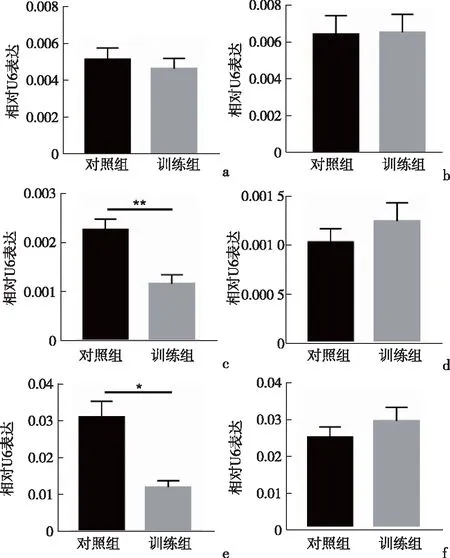
*P<0.05、**P<0.01
2.3.2 左右心肌組織中心肌其他miRNAs的變化與對照組比較,訓練組左心室心肌miR-21與miR-17-3p水平顯著減少(P<0.05;P<0.05),分別改變2.53倍和1.13倍。與左心室心肌的顯著改變不同的是,miR-21與miR-17-3p在右心室心肌中的水平差異無統計學意義(P>0.05)。見圖5。有氧訓練并不影響這些miRNAs在右心室心肌中的表達。
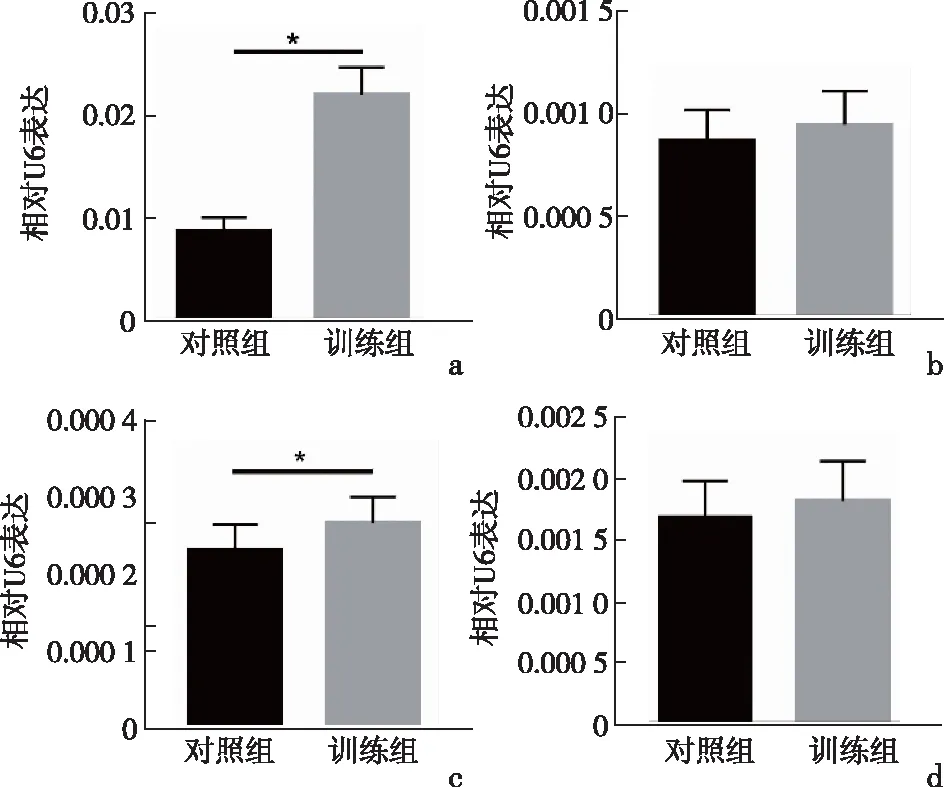
*P<0.05
3 討 論
長期有氧訓練會導致心臟超負荷,引起結構和功能發生適應變化,被稱為“運動員的心臟”。傳統上,認為這種心臟重塑的量在左右心腔之間是平衡的。但是,在劇烈運動期間,右心室會承受不成比例的后負荷和室壁應力,長期運動引起的變化可能更為明顯。本研究結果顯示心肌相關的miR-208b和miR-499水平僅在左心室心肌中下降,而miR-21與miR-17-3p僅在左心室心肌中增加。表明左、右心室心肌重構存在不同。
有氧運動引起的心臟肥大是一種生理反應,涉及對收縮和代謝成分的基因和蛋白質表達的精確編排。miRNAs參與這些生理過程的變化。前期研究發現,miR-208a、miR-208b和miR-499均由肌球蛋白基因編碼,因此也被稱為“肌相關microRNAs(MyomiRs)”,調節多個mRNA靶標,進而調節心肌肥大和代謝途徑[6]。研究表明,游泳訓練對miR-208a和miR-208b水平的表達存在抑制作用,會增加Med13、Purβ、Sox6、異染色質蛋白1β(Heterochromatin Protein 1β, HP1β)和特異性蛋白(specificity proteins,Sp)/Kruppel樣轉錄因子3(Kruppel-like transcription factor 3, SP3)蛋白的表達,調節代謝,收縮途徑和表觀遺傳控制,從而調節α-MHC/β-MHC比率并傳遞信號,誘發生理性的肌肉肥大。但miR-499未發生變化[6]。本研究結果顯示,8周有氧跑臺訓練可影響miR-208b和miR-499水平的變化,進一步表明這些MyomiRs參與調控心臟肥大。其出現差異的原因可能和有氧練習的方式有關[2-3]。另外,研究發現游泳訓練可增加miR-21水平[靶向磷脂酶和張力蛋白同源物(phosphataseandtensinhomolog, PTEN)和TSC-2],可激活心肌細胞PI3K/Akt/mTOR信號途徑[7];增加miR-17-3p的表達,可抑制PTEN(PI3K/Akt拮抗途徑),而PI3K/Akt是參與心肌肥大最重要的一個途徑[8];本研究同樣觀察到8周跑臺訓練后左室心肌miR-21和miR-17-3p水平增加,進一步支持體育活動的有益影響。但值得注意的是,在心血管疾病中,miR-21 的表達普遍升高[9]。
但在右心室的心肌中,未觀察到這些miRNAs的變化,表明左右心肌重構存在不同。與左心室相比,長期耐力運動右心室的擴大程度有所提高[10]。研究發現長期的有氧運動訓練主要是通過增加線粒體產生ATP的能力,增強右心室的代謝重塑[11]。因此,評定代謝相關miRNAs的變化,有助認識右心室的重構現象。運動過程中右心室承受的負荷和室壁壓力大于左心室[12]。在健康個體中,右心室具有足夠的心力儲備,以適應短期高強度運動期間肺動脈壓的升高[13]。但是,如果保持高強度運動數小時,則可能會影響右心室功能并導致心肌微損傷,最終導致心臟病理性改變[14]。認識運動性心肌肥大的適應過程,了解運動如何誘導心臟生長可能有助于確定新的治療靶標,以減輕對病理應激的不良心臟重塑。但這些途徑是否可以增強心臟有限的再生能力,從而幫助補償心肌細胞的損失,仍是未經證實的[15]。

