單孔加一孔腹腔鏡手術對右半結腸癌根治術患者療效的影響
張春雷,章社民,夏亞斌
(1.宣城市中心醫院普外科,安徽 宣城 242000;2.皖南醫學院附屬弋磯山醫院胃腸外科,安徽 蕪湖 241000)
結直腸癌是臨床常見的消化道惡性腫瘤,發病率逐年增高,嚴重威脅人類生命健康[1]。手術是目前唯一可能治愈結直腸癌的手段[2],其中腹腔鏡手術因創傷小、恢復快且療效確切,已得到廣泛普及;但傳統5孔腹腔鏡技術仍存Trocar孔多、手術切口大、切口疼痛明顯、切口欠美觀等局限。近年來,隨著微創外科技術的不斷進步,單孔腹腔鏡技術(single incision laparoscopic surgery,SILS)逐漸興起并成為熱點[3-4],但該技術對術者及器械要求極高,且缺乏“操作三角”,部分手術操作困難,限制了其使用[5]。而單孔加一(single-port plus one-port,SILS+1)腹腔鏡技術可形成倒三角手術平面,很大程度上降低了單孔手術的手術難度,減少了術中損傷,微創效果好,可操作性強,更易于推廣。本研究旨在探討SILS+1腹腔鏡手術對右半結腸癌根治術患者手術效果及炎性反應、免疫功能等的影響,為臨床手術方式的選擇提供參考。
1 資料與方法
1.1 一般資料
選取2016年1月至2020年12月宣城市中心醫院86例接受腹腔鏡右半結腸癌根治術的患者為研究對象,根據手術方式不同分為SILS+1組(n=40)與傳統腹腔鏡組(n=46)。兩組患者性別、年齡、體質指數、腫瘤直徑及位置、Dukes分期(A/B/C)等一般資料比較,差異無統計學意義(P>0.05)。見表1。
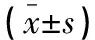
表1 兩組患者一般資料比較
納入標準:(1)術前經腸鏡及病理檢查證實為右半結腸癌;(2)腫瘤直徑≤6 cm,未侵犯周圍組織;(3)術前未行放化療等治療;(4)無手術禁忌癥;(5)美國麻醉醫師協會(ASA)分級為I~III級;(6)病例資料完整。排除標準:(1)局部晚期或有遠處轉移者;(2)伴其他惡性腫瘤者;(3)合并免疫系統疾病者;(4)嚴重心肝腎疾病者;(5)嚴重凝血功能障礙者;(6)嚴重肥胖,即體質指數>30 kg/m2者。
1.2 方法
1.2.1 手術方式 患者氣管插管全身麻醉后,取截石位,頭低腳高。SILS+1組采用SILS+1腹腔鏡手術:于患者臍下緣置入單孔器械,作為手術觀察孔、輔助操作孔及助手操作孔;左鎖骨中線肋緣下置入5 cm Trocar作為主操作孔;傳統腹腔鏡組采取傳統5孔法腹腔鏡手術:于臍下部1 cm 穿刺10 mm Trocar作為觀察孔,右髂前上棘內側約2 cm處穿刺12 mm Trocar作為主操作孔,右側腹直肌外側平臍穿刺10 mm Trocar、左側腹直肌外側平臍及左下腹各穿刺5 mm Trocar作為副操作孔。所有手術操作遵循全直腸系膜切除術(total mesorectal excision,TME)原則。
1.2.2 觀察指標 (1)圍手術期一般指標:包括手術切口長度、手術時間、術中出血量、引流量、淋巴結清掃數及術后首次下床時間、排氣時間、住院時間;(2)術后并發癥發生率:包括切口感染、皮下氣腫、腸梗阻、尿潴留等;(3)炎性應激及免疫功能指標:于術前1 d及術后3 d采集患者外周靜脈血5 mL,3 000 rpm 離心10 min分離血清,采用酶聯免疫吸附法(ELISA)檢查C反應蛋白(c-reactive protein,CRP)、白細胞介素-6(interleukin-6, IL-6)、降鈣素原(procalcitonin,PCT)水平,試劑盒購于上海酶聯生物科技有限公司操作按說明書進行;采用流式細胞儀測定CD3+、CD4+、CD8+及CD4+/CD8+水平。
1.3 統計學分析

2 結果
2.1 兩組患者圍手術期一般指標比較
與傳統腹腔鏡組相比,SILS+1組手術時間較長(P<0.05),術中出血量較少(P<0.05),切口長度較短(P<0.05),首次下床時間、排氣時間及術后住院時間提前(P<0.05);兩組患者術后引流量、淋巴結清掃數比較,差異無統計學意義(P>0.05)。見表2。
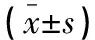
表2 兩組患者圍手術期一般指標比較
2.2 兩組患者術后并發癥發生率比較
術后兩組患者術后并發癥發生率比較,差異無統計學意義(P>0.05)。見表3。

表3 兩組患者術后并發癥發生率比較[n(%)]
2.3 兩組患者血清炎性應激指標比較
術前,兩組患者血清CRP、IL-6、PCT水平比較,差異無統計學意義(P>0.05);術后,兩組患者血清CRP、IL-6、PCT水平均升高(P<0.05),且傳統腹腔鏡組高于SILS+1組(P<0.05)。見表4。
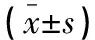
表4 兩組患者血清炎性應激指標比較
2.4 兩組患者免疫功能指標比較
術前,兩組患者血清免疫功能指標水平比較,差異無統計學意義(P>0.05)。術后,SILS+1組CD3+、CD4+及CD4+/CD8+水平與術前比較,差異無統計學意義(P>0.05);傳統腹腔鏡組CD3+、CD4+及CD4+/CD8+水平較術前降低(P<0.05),且低于SILS+1組(P<0.05)。見表5。
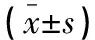
表5 兩組患者免疫功能指標比較
3 討論
單孔腹腔鏡技術是由傳統腹腔鏡發展而來,即通過單一小切口完成手術操作,具有腹壁破壞小、疼痛輕、切口美觀、術后恢復快等優點[6-7]。SILS+1是在單孔基礎上增加一個操作孔,由單孔操作的“小三角”轉變為“大三角”,保證了正確牽拉平面,極大降低了手術操作難度[8]。此外,新增的操作孔可直接用于術后引流管的放置,不增加額外的切口,使圍手術期更加安全。
SILS+1腹腔鏡技術是由傳統五孔法減孔而來,具有可操作性及微創美觀的優點,已在臨床得到廣泛應用。Omori等[9]首次報道了該技術在胃癌患者治療中的可靠療效,且微創性好。本研究結果顯示,與傳統腹腔鏡組相比,SILS+1組手術時間較長(P<0.05),但術中出血量較少(P<0.05),切口長度較短(P<0.05),首次下床時間、排氣時間及術后住院時間提前(P<0.05);而兩組術后引流量、淋巴結清掃數、并發癥發生率比較差異無統計學意義(P>0.05),與文獻報道一致[10-12],提示SILS+1腹腔鏡手術可獲得更好的療效,且不增加并發癥發生率,可能與手術切口小、疼痛輕、術后恢復快有關。SILS+1組手術時間較長,可能與該技術應用處于起步階段,手術醫師操作不熟練有關。
手術創傷應激引發的炎癥反應,易致切口感染而影響愈合,還可影響免疫功能,使術后恢復延遲[13-14]。CRP、IL-6及PCT均是重要的炎癥因子,能夠反映機體的炎癥應激反應程度[15];CD3+、CD4+、CD8+作為機體重要的免疫細胞,其水平變化能夠反映機體免疫功能狀況[16]。本研究結果顯示,兩組患者術后3 d的 CRP、IL-6及PCT水平均高于術前(P<0.05),且傳統腹腔鏡組高于SILS+1組(P<0.05),提示SILS+1腹腔鏡手術相比傳統腹腔鏡手術能夠減輕炎癥應激反應程度。術后3 d 的CD3+、CD4+及CD4+/CD8+水平均高于傳統腹腔鏡組,傳統腹腔鏡組術后3d的CD3+、CD4+及CD4+/CD8+水平相比術前降低(P<0.05),且低于SILS+1組(P<0.05),而SILS+1組較術前無明顯變化(P>0.05),提示SILS+1腹腔鏡手術對患者免疫的損傷小,有利于免疫功能恢復,可能是因為手術切口更小,術中出血更少,術后炎癥反應較輕。既往研究[17]也表明,切口數量的減少,不僅會減輕術后疼痛程度,還會減輕炎癥反應,更好地保護機體功能,從而有助于術后恢復。
綜上所述,與傳統腹腔鏡手術相比,SILS+1腹腔鏡手術更具微創效果,炎癥反應輕,且可保護免疫功能,促進術后恢復,近期療效較好,有望成為結腸癌手術方式的新選擇。

