超重和肥胖合并2型糖尿病微量白蛋白尿患者維生素D營養狀況臨床分析
曹 晉,拜 珂,安 欣,邵 英
(1.空軍第九八六醫院內分泌科,陜西 西安 710054;2.延安大學醫學院,陜西 延安 716000;3.西安工會醫院,陜西 西安 710100)
超重、肥胖癥和2型糖尿病發生、發展密切相關,有研究表明,在確診的2型糖尿病人群中,超重及肥胖者分別約占40%與23%[1],另一方面,在超重與肥胖的患者中糖尿病檢出率則分別為13% 和19%[2]。微量白蛋白尿(Microalbuminuria,MAU)是早期腎功能受損的特征性表現之一,有研究顯示,超重和肥胖的2型糖尿病患者中MAU發生率約為30%~45%左右,是患者發生心腦血管疾病和死亡風險的獨立預測因子之一[3]。維生素D屬于一種脂溶性必需營養素,在調節人體細胞分化和增殖、免疫功能、抑制炎癥反應、調節鈣磷代謝的作用已被臨床所證實[4]。維生素D營養狀況是否對超重和肥胖的2型糖尿病患者MAU造成影響目前國內鮮有報道。本研究旨在探討超重和肥胖的初診2型糖尿病合并MAU患者維生素D營養狀況,報告如下。
1 資料與方法
1.1 一般資料 選取2018年10月至2020年10月我院診治的超重和肥胖的初診2型糖尿病患者189例,病例納入標準:①年齡18~65歲,糖尿病診斷符合《中國2型糖尿病防治指南(2017年版)》[5]相關標準;②體重指數(BMI)>24 kg/m2,女性和男性的腰圍(WC)分別大于85 cm和90 cm;③腎小球濾過率(eGFR)>60 ml/(min·1.73m2)。排除標準:①納入前3個月內口服調脂或減肥類藥物者;②近3個月內接受過糖皮質激素或服用影響維生素D代謝的藥物者;③骨質疏松史、糖尿病急性并發癥、泌尿系統感染、痛風性腎病、慢性腎炎、高血壓腎病、嚴重的肝腎功能障礙、24 h尿白蛋白排泄率(24 hUAER)>300 mg/24 h、甲狀腺或甲狀旁腺疾病等。189例患者中男101例,女88例,年齡38~65歲,平均(55.45±8.93)歲。本研究經我院倫理委員會批準實施,納入的患者均簽署知情同意書。
1.2 研究方法
1.2.1 臨床資料的收集:收集項目包括性別、年齡、BMI、吸煙和飲酒史、收縮壓(SBP)、舒張壓(DBP)、空腹血糖(FPG)、餐后2 h血糖(2hPG)、糖化血紅蛋白(HbA1c)、胰島素抵抗指數(HOMA-IR)、總膽固醇(TC)、甘油三酯(TG)、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、血尿酸、同型半胱氨酸(Hcy)、24 hUAER、血清25-羥基維生素D[25(OH)D]。其中HbA1c采用高壓液相法測定;24 hUAER測定應用美國Coulter 貝克曼AU5421型全自動特定蛋白分析儀。血清25(OH)D測定采用電化學發光法(試劑盒購自羅氏公司)。
1.2.2 分組方法:①將納入的患者按照是否合并MAU分為兩組,分別為非MAU組[24 h尿白蛋白排泄率(24 hUAER) <30 mg/24 h,n=129]和MAU組(24 hUAER≥30 mg/24 h,n=60)。②參考《維生素D與成年人骨骼健康應用指南(2014年簡化版)》[6]中關于維生素D營養狀況評定標準:血清25(OH)D水平≥30 ng/ml為維生素D正常;25(OH)D水平<29 ng/ml為維生素D不足或缺乏。
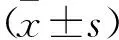
2 結 果
2.1 非MAU組和MAU組患者臨床資料比較 見表1。與非MAU組比較,MAU組收縮壓(SBP)、舒張壓(DBP)、糖化血紅蛋白(HbA1c)、胰島素抵抗指數(HOMA-IR)、甘油三酯(TG)、血尿酸、同型半胱氨酸(Hcy)水平、維生素D不足或缺乏比例較高,差異有統計學意義(均P<0.05),低密度脂蛋白膽固醇(HDL-C)、血清25-羥基維生素D[25(OH)D]水平較低,比較差異有統計學意義(均P<0.05)。

表1 非MAU組和MAU組患者臨床資料的比較

續 表
2.2 不同維生素D營養狀況分組相關血糖指標、24 hUAER比較 見表2。與維生素D正常組比較,維生素D不足或缺乏組HbA1c、HOMA-IR、24 hUAER水平較高,差異有統計學意義(均P<0.05)。
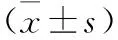
表2 不同維生素D營養狀況分組相關血糖指標、24 hUAER比較
2.3 24 hUAER與相關指標的Pearson相關性分析 見表3。Pearson相關性分析顯示24 hUAER與SBP、DBP、HbA1c、HOMA-IR、TG、血尿酸、Hcy呈正相關(均P<0.05),與HDL-C、25(OH)D呈負相關(P<0.05)。
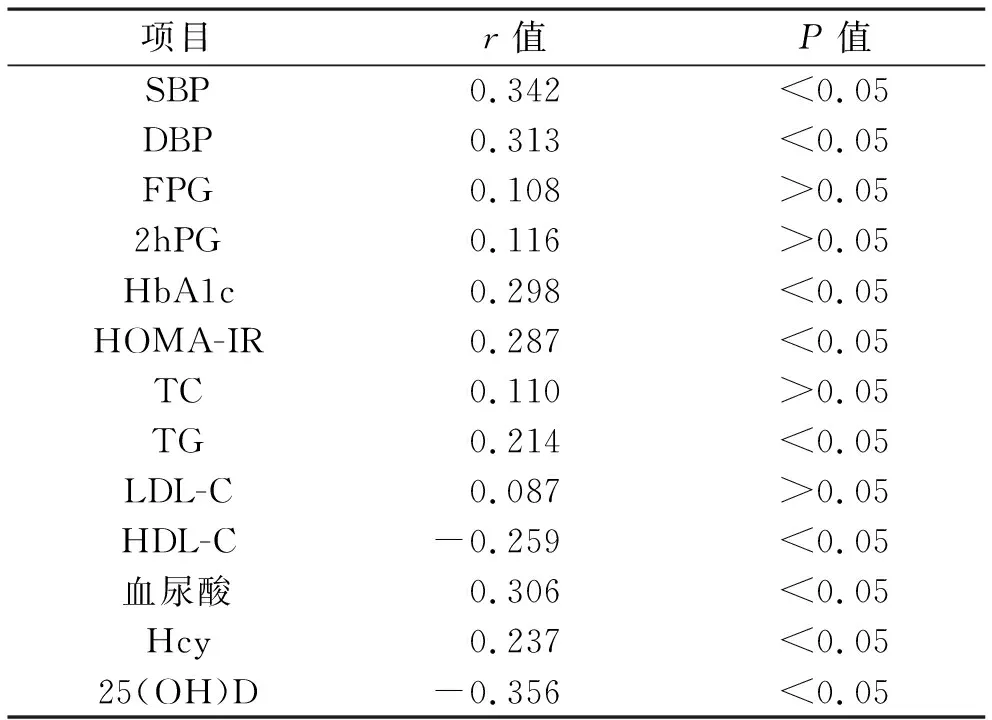
表3 24 hUAER與相關指標Pearson相關性分析
2.4 MAU發生因素的多因素Logistic回歸分析 見表4。以患者是否發生MAU為因變量,以表1中MAU組與非MAU組比較,差異有統計學意義的指標為自變量。多因素Logistic回歸方程顯示維生素D不足或缺乏是超重和肥胖的初診2型糖尿病合并MAU的獨立危險因素(P<0.05)。
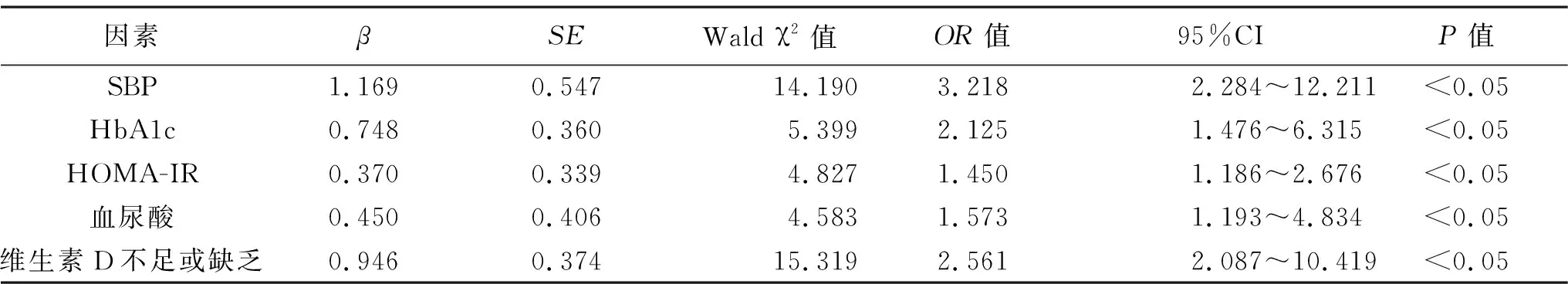
表4 MAU發生因素多因素Logistic回歸分析
3 討 論
本研究結果顯示,MAU組維生素D不足或缺乏比例高于非MAU組,且血清25(OH)D水平低于非MAU組,提示了超重和肥胖合并2型糖尿病MAU患者維生素D不足或缺乏檢出率偏高,且外周血維生素D含量不足,維生素D營養狀況較差。從另一個角度分析,按照維生素D不同水平分組比較提示,維生素D不足或缺乏組HbA1c、HOMA-IR、24 hUAER水平高于維生素D正常組,提示了在超重與肥胖的2型糖尿病患者中維生素D不足或缺乏者血糖控制水平較差,胰島素抵抗水平較高,發生MAU的幾率較高。本研究采用單因素Pearson相關性分析顯示24 hUAER與HbA1c、HOMA-IR呈正相關,與25(OH)D呈負相關,提示了微量白蛋白尿的發生與血糖控制水平、胰島素抵抗、維生素D營養狀況差有關聯,這與上述研究的結果相一致。為驗證MAU與維生素D營養狀況的關系,本研究在單因素的基礎上實施多因素Logistic回歸方程矯正混雜因素后顯示,維生素D不足或缺乏是超重和肥胖合并2型糖尿病MAU的獨立危險因素,則進一步揭示了超重和肥胖合并2型糖尿病MAU患者中維生素D營養狀況不佳,可能是MAU發生的獨立危險因素,對于此類患者可酌情考慮適量補充維生素D制劑,以降低MAU發生風險。
2型糖尿病發病較為隱匿,當患者初診時即可發生微量白蛋白尿,此類患者以典型的“腎小管損害”為主,一旦進展為大量蛋白尿期,則在后期演變為終末期腎病,顯著增加患者病死率[7-8]。糖尿病人群中多數可合并有超重或肥胖,而超重或肥胖的存在又可能加速微量白蛋白尿發生速率[9]。目前,糖尿病合并有MAU的發生機制尚不明確,可能與血糖異常升高、血糖波動、胰島素抵抗誘發的氧化應激和炎癥反應、血液黏稠度增加,血脂代謝異常等因素有關,上述因素導致腎臟血管粥樣硬化,血管內皮細胞受損,腎臟微循環障礙,最終引起腎小管損害而引發微量白蛋白尿[10-12]。
超重和肥胖的糖尿病患者中維生素D含量降低的機制為:①此類患者腹部脂肪增多增厚,機體內部分維生素D能夠溶解在肥厚的脂肪組織,導致外周血25(OH)D含量降低[13]。②超重和肥胖人群體積偏大,導致平均體質量分布的25(OH)D含量偏少,此類現象被稱為“稀釋現象”[14]。③超重或肥胖者日常的運動和戶外活動較少,日照量不足,導致皮膚合成的維生素D不足或缺乏[15]。
相關研究顯示,維生素D能夠提升胰島素敏感性,降低胰島素抵抗,改善胰島β細胞功能,對于控制血糖水平具有較好的療效[16];還能激活破壞甾醇調節元件結合蛋白,從而阻斷脂肪細胞合成脂蛋白,抑制脂肪蓄積,調節血脂代謝[17]。由此推測,維生素D的上述生理學效應在調節糖脂代謝,降低糖脂代謝毒物對腎臟血管內皮細胞的損害程度、降低微量白蛋白尿方面發揮了重要作用。另有研究表明,維生素D還能下調外周血腫瘤壞死因子(TNF)、白介素(IL)-6、C 反應蛋白(CRP)等炎性介質的表達,還能通過阻斷腎素- 血管緊張素- 醛固酮(RAAS)系統的活性,激活基質金屬蛋白酶(MMP),從而抑制甚至逆轉腎臟纖維化,降低腎臟重構,具有顯著腎臟保護作用[18]。維生素D還通過影響Wnt、Nephrin等細胞信號轉導通路,抑制腎臟足細胞損傷,發揮減輕蛋白尿的功效[19]。胰島素抵抗是超重和肥胖、糖尿病發生的共有病理生理基礎,而胰島素抵抗能夠誘發氧化應激,大量氧自由基,導致胰島組織的脂質過氧化損害。而維生素D能夠與靶細胞內的維生素D受體(VDR)結合后發揮調控炎癥、清除氧自由基的作用,從而起到抗炎抗氧化功效[20],有利于保護血管內皮,改善腎臟微循環,降低蛋白尿。
綜上所述,超重和肥胖合并2型糖尿病MAU患者中維生素D營養狀況不佳,維生素D不足或缺乏檢出率偏高,可能是MAU發生的獨立危險因素,值得臨床關注。

